|
|
Химия галогены(Ася). Галогены, как "рождающие соли"
Балашовский филиал
Государственное автономное образовательное учреждение
среднего профессионального образования Саратовской области
«Саратовский базовой медицинский»
Альбом
По теме: «Галогены, как "рождающие соли"»
Дисциплина: «Химия»
Специальность: 33.02.01.– «Фармация»
Преподаватель Белова Н. Л.
Утверждено на заседании ЦМК
фармацевтических дисциплин
Протокол № ___ от « »______2020 г.
Председатель ЦМК _____Тимофеева О.С.
Балашов 2020 г.
Содержание:
Введение 3
Открытие фтора 4
Открытие хлора 5
Открытие брома 6
Открытие йода 7
Открытие астата 9
Список используемой литературы 10
В ведение ведение
За таинственным для многих названием химических элементов из VII группы таблицы Менделеева кроются вполне известные и часто используемые в быту вещества: поваренная соль, обычный йод и активно рекламируемый компонент зубной пасты – фтор. Но это далеко не все интересные факты о галогенах. Это они делают морскую воду солёной, продлевают «жизнь» лампам накаливания и снижают температуру в холодильнике. Однако роль галогенов в истории человеческой цивилизации далеко не однозначна и до сих пор вызывает ожесточённые дискуссии.

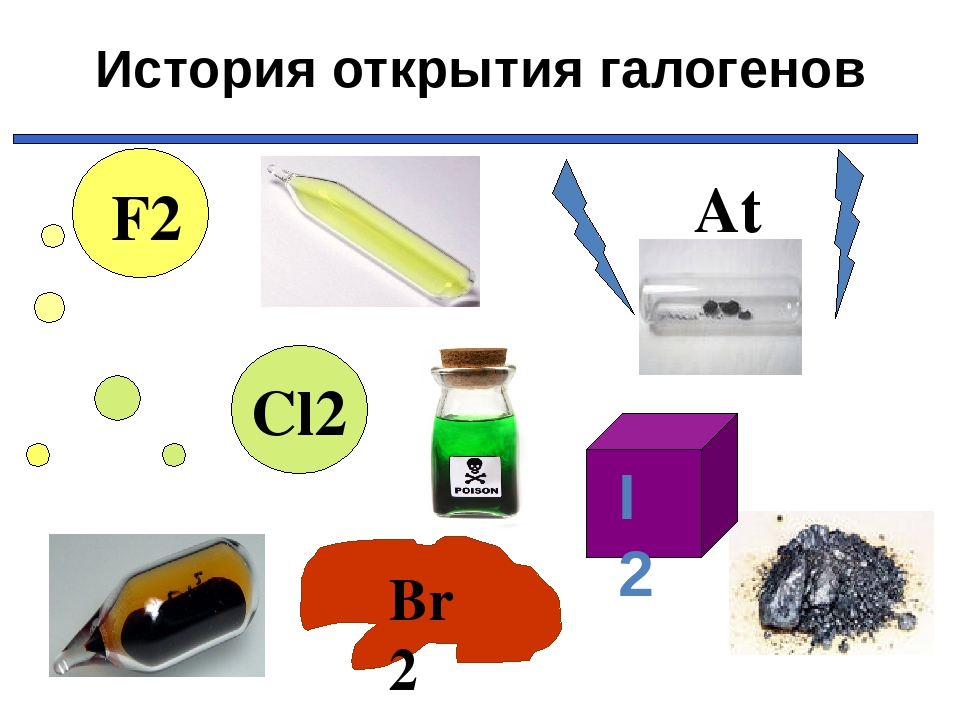
Открытие фтора
В ыделение газообразного фтора из фторсодержащих веществ оказалось одной из самых трудных экспериментальных задач. Фтор обладает исключительной реакционной способностью; причем часто его взаимодействие с другими веществами происходит с воспламенением и взрывом. ыделение газообразного фтора из фторсодержащих веществ оказалось одной из самых трудных экспериментальных задач. Фтор обладает исключительной реакционной способностью; причем часто его взаимодействие с другими веществами происходит с воспламенением и взрывом.
Первыми жертвами фтора были два члена Ирландской Академии наук братья Георг и Томас Нокс. Томас Нокс скончался от отравления фтороводородом, а Георг стал инвалидом. Следующей жертвой стал бельгийский химик П. Лайет. Мученическую смерть при проведении опытов по выделению фтора принял французский химик Джером Никлес. Отравились, надышавшись небольшими количествами фтороводорода, а также получили серьезные ожоги французские химики Жозеф Гей-Люссак, Луи Тенар и английский химик Гемфри Дэви. При попытках выделить фтор при помощи электролиза его соединений нанесли ущерб своему здоровью французский химик Эдмон Фреми и английский электрохимик Георг Гор. Только в 1886 году французскому химику Анри Муассану сравнительно безболезненно удалось получить фтор. Муассан случайно обнаружил, что при электролизе смеси жидкого безводного HF и гидродифторида калия (KHF2) в платиновом сосуде на аноде выделяется светло-желтый газ со специфическим резким запахом. Однако, когда Муассан докладывал Парижской академии наук о своем открытии, один глаз ученого был закрыт черной повязкой:
Нобелевская премия по химии была присуждена Муассану в 1906 г "в признание большого объема исследований - получения элемента фтора и введения в лабораторную и промышленную практику электрической печи, названной его именем".

Открытие хлора
П ервооткрывателем хлора оказался шведский аптекарь Карл Шееле, химическая интуиция которого была поистине поразительной, по словам французского химика Жана Батиста Дюма, Шееле "не мог прикоснуться к какому-либо телу без того, чтобы сделать открытие". В 32 года он был удостоен звания члена Стокгольмской академии наук, хотя был всего лишь аптекарским помощником, в том же году он получил место управляющего аптекой, принадлежавшей вдове Маргарите Соннеман, которая за два дня до смерти Шееле стала его женой. ервооткрывателем хлора оказался шведский аптекарь Карл Шееле, химическая интуиция которого была поистине поразительной, по словам французского химика Жана Батиста Дюма, Шееле "не мог прикоснуться к какому-либо телу без того, чтобы сделать открытие". В 32 года он был удостоен звания члена Стокгольмской академии наук, хотя был всего лишь аптекарским помощником, в том же году он получил место управляющего аптекой, принадлежавшей вдове Маргарите Соннеман, которая за два дня до смерти Шееле стала его женой.
Вот как описал Шееле свой опыт, выполненный в 1774 году: "Я поместил смесь черной магнезии с муриевой кислотой в реторту, к горлышку которой присоединил пузырь, лишенный воздуха, и поставил ее на песчаную баню. Пузырь наполнился газом, окрасившим его в желтый цвет: Газ имел желто-зеленый цвет, пронзительный запах":
Современное обозначение этой реакции таково:
MnO2 + 4HCl = Cl2 + MnCl2 + 2H2O.
В 1812 году французский химик Гей-Люссак дал этому газу современное название - хлор, что в переводе с греческого означает желто-зеленый.

Открытие брома
Б ром был открыт двадцатичетырехлетним лаборантом Антуаном-Жеромом Баларом. Балар изучал маточные рассолы южных соляных болот Франции. Во время одного из опытов, когда он подействовал на рассол хлором, он заметил появление весьма интенсивной желтой окраски, вызванной реакцией взаимодействия содержащегося в растворе бромида натрия с хлором. Через несколько лет напряженной работы Балар выделил необходимое количество темно-бурой жидкости, названной им муридом. В Парижской Академии наук Гей-Люссак и Тенар подтвердили открытие Баларом нового простого вещества, но нашли название неудачным и предложили свое - "бром", что в переводе с греческого означало зловонный. ром был открыт двадцатичетырехлетним лаборантом Антуаном-Жеромом Баларом. Балар изучал маточные рассолы южных соляных болот Франции. Во время одного из опытов, когда он подействовал на рассол хлором, он заметил появление весьма интенсивной желтой окраски, вызванной реакцией взаимодействия содержащегося в растворе бромида натрия с хлором. Через несколько лет напряженной работы Балар выделил необходимое количество темно-бурой жидкости, названной им муридом. В Парижской Академии наук Гей-Люссак и Тенар подтвердили открытие Баларом нового простого вещества, но нашли название неудачным и предложили свое - "бром", что в переводе с греческого означало зловонный.
Впоследствии французский химик Шарль Жерар, не получивший кафедру химии во Французском колледже, которую передали Балару, высоко оценив открытие им брома, не смог удержаться от резкого восклицания : "Это не Балар открыт бром, а бром открыл Балара!"

Открытие йода
В 1811 году французский химик-технолог и фармацевт Бернар Куртуа открыл йод. Друзья его рассказывают любопытные подробности этого открытия. У Куртуа был любимый кот, который во время обеда сидел обычно на плече своего хозяина. Куртуа часто обедал в лаборатории. В один из дней во время обеда кот, чего-то испугавшись, прыгнул на пол, но попал на бутылки, стоявшие около лабораторного стола. В одной бутылке Куртуа приготовил для опыта суспензию золы водорослей (содержащей иодид натрия) в этаноле, а в другой находилась концентрированная серная кислота. Бутылки разбились и жидкости смешались. С пола стали подниматься клубы сине-фиолетового пара, которые оседали на окружающих предметах в виде мельчайших черно-фиолетовых кристалликов с металлическим блеском и едким запахом. Это и был новый химический элемент йод. 1811 году французский химик-технолог и фармацевт Бернар Куртуа открыл йод. Друзья его рассказывают любопытные подробности этого открытия. У Куртуа был любимый кот, который во время обеда сидел обычно на плече своего хозяина. Куртуа часто обедал в лаборатории. В один из дней во время обеда кот, чего-то испугавшись, прыгнул на пол, но попал на бутылки, стоявшие около лабораторного стола. В одной бутылке Куртуа приготовил для опыта суспензию золы водорослей (содержащей иодид натрия) в этаноле, а в другой находилась концентрированная серная кислота. Бутылки разбились и жидкости смешались. С пола стали подниматься клубы сине-фиолетового пара, которые оседали на окружающих предметах в виде мельчайших черно-фиолетовых кристалликов с металлическим блеском и едким запахом. Это и был новый химический элемент йод.

Открытие астата
До своего открытия он был известен под именем, данным Менделеевым,- эка-иод (Eka-Iodum). Было очевидно, что элемент 85 должен обладать интересными про межуточными свойствами: с одной стороны, активностью галогенов, с другой - металлическими свойствами. Поэтому с конца XIX в. велись интенсивные поиски этого элемента в различных минералах. Несколько раз появлялись сообщения об его открытии, но эти сообщения не подтверждались. Авторы мнимых открытий давали элементу 85 разные названия: дакин (Dacinum - от названия древней страны даков, соплеменников готов, в средней Европе), гельвеций (Helvetium - от старинного названия Швейцарии, Гельвеция), англогельвеций (Anglohelvetium), лептин (от греч.- слабый, шаткий, обездоленный) и др.
В 1931 г. Аллисон с сотрудниками Политехнического института штата Алабама в США сообщил, что ему удалось обнаружить в растворе, извлеченном из монацитного песка с помощью магнетооптических методов, следы элемента 85, которому он дал название алабамий (Alaba mium); под этим названием элемент 85 фигурировал в учебниках и справочниках до 1947 г.
Реально, однако, один из изотопов элемента 85 (астат- 211) был получен лишь в 1940 г. Корсоном, Маккензи и Сегре в циклотроне, где производилась бомбардировка висмута быстрыми alfa-частицами. Период полураспада этого изотопа оказался всего 7,2 часа. Вскоре (1942 -- 1943) было установлено, что изотопы элемента 85 образуются во всех трех рядах радиоактивного распада. Элемент 85 получил свое название астат (Astatium) в 1947 г. в статье авторов открытия (Nature, 159, 24, 1947). Название произведено от греч.означающего "неустойчивый, шаткий", так как все изотопы астата оказались коротко- живущими. До недавнего времени в русской литературе элемент 85 называли астатин, что нельзя признать правильным, имея в виду слово, от которого образовано название.

Список используемой литературы
https://vivareit.ru/samye-interesnye-fakty-pro-galogeny/
https://xn--e1aahgrctjf9g.com/interesnye-fakty-o-galogenah/
http://www.chem.msu.su/rus/teaching/bogatova/fakt1.html
https://yandex.ru/images/search?text=%D0%BA%D0%B0%D1%80%D1%82%D0%B8%D0%BD%D0%BA%D0%B8%20%D1%85%D0%BB%D0%BE%D1%80%D0%B0%20%D0%BD%D0%B0%20%D0%B1%D0%B5%D0%BB%D0%BE%D0%BC%20%D1%84%D0%BE%D0%BD%D0%B5&from=tabbar
 |
|
|
 Скачать 0.94 Mb.
Скачать 0.94 Mb.

 ведение
ведение
 ыделение газообразного фтора из фторсодержащих веществ оказалось одной из самых трудных экспериментальных задач. Фтор обладает исключительной реакционной способностью; причем часто его взаимодействие с другими веществами происходит с воспламенением и взрывом.
ыделение газообразного фтора из фторсодержащих веществ оказалось одной из самых трудных экспериментальных задач. Фтор обладает исключительной реакционной способностью; причем часто его взаимодействие с другими веществами происходит с воспламенением и взрывом.
 ервооткрывателем хлора оказался шведский аптекарь Карл Шееле, химическая интуиция которого была поистине поразительной, по словам французского химика Жана Батиста Дюма, Шееле "не мог прикоснуться к какому-либо телу без того, чтобы сделать открытие". В 32 года он был удостоен звания члена Стокгольмской академии наук, хотя был всего лишь аптекарским помощником, в том же году он получил место управляющего аптекой,
ервооткрывателем хлора оказался шведский аптекарь Карл Шееле, химическая интуиция которого была поистине поразительной, по словам французского химика Жана Батиста Дюма, Шееле "не мог прикоснуться к какому-либо телу без того, чтобы сделать открытие". В 32 года он был удостоен звания члена Стокгольмской академии наук, хотя был всего лишь аптекарским помощником, в том же году он получил место управляющего аптекой, 
 ром был открыт двадцатичетырехлетним лаборантом Антуаном-Жеромом Баларом. Балар изучал маточные рассолы южных соляных болот Франции. Во время одного из опытов,
ром был открыт двадцатичетырехлетним лаборантом Антуаном-Жеромом Баларом. Балар изучал маточные рассолы южных соляных болот Франции. Во время одного из опытов, 
 1811 году французский химик-технолог и фармацевт Бернар Куртуа открыл йод. Друзья его рассказывают любопытные подробности этого открытия. У Куртуа был любимый кот, который во время обеда сидел обычно на плече своего хозяина. Куртуа часто обедал в лаборатории. В один из дней во время обеда кот, чего-то испугавшись, прыгнул на пол, но попал на бутылки, стоявшие около лабораторного стола. В одной бутылке Куртуа приготовил для опыта суспензию золы водорослей (содержащей иодид натрия) в этаноле, а в другой находилась концентрированная серная кислота. Бутылки разбились и жидкости смешались. С пола стали подниматься клубы сине-фиолетового пара, которые оседали на окружающих предметах в виде мельчайших черно-фиолетовых кристалликов с металлическим блеском и едким запахом. Это и был новый химический элемент йод.
1811 году французский химик-технолог и фармацевт Бернар Куртуа открыл йод. Друзья его рассказывают любопытные подробности этого открытия. У Куртуа был любимый кот, который во время обеда сидел обычно на плече своего хозяина. Куртуа часто обедал в лаборатории. В один из дней во время обеда кот, чего-то испугавшись, прыгнул на пол, но попал на бутылки, стоявшие около лабораторного стола. В одной бутылке Куртуа приготовил для опыта суспензию золы водорослей (содержащей иодид натрия) в этаноле, а в другой находилась концентрированная серная кислота. Бутылки разбились и жидкости смешались. С пола стали подниматься клубы сине-фиолетового пара, которые оседали на окружающих предметах в виде мельчайших черно-фиолетовых кристалликов с металлическим блеском и едким запахом. Это и был новый химический элемент йод.

