Гипопитуиаризм. Гипопитуитаризм( реферат). Гипопитуитаризм
 Скачать 409 Kb. Скачать 409 Kb.
|
|
Министерство образования и науки КР ОшГУ медицинский факультет РЕФЕРАТ Тема: Гипопитуитаризм Выполнила: Жумабай кызы Гүлжамал Группа: 6Лк7(а)-14 Проверила: Айтиева Айниса Ош 2020 2.1. АНАТОМИЯ И ФИЗИОЛОГИЯ ГИПОТАЛАМО-ГИПОФИЗАРНОЙ СИСТЕМЫ Гипофиз - железа внутренней секреции, расположенная в гипофизарной ямке турецкого седла клиновидной кости (рис. 2.1). Масса гипофиза составляет 0,5-0,7 г, размеры 1,3 *0,6 *1,0 см, но они могут меняться в зависимости от возраста и пола (у женщин он больше, чем у мужчин). В гипофизе различают две доли: переднюю (аденогипофиз) и заднюю (нейрогипофиз). Аденогипофиз состоит из трех 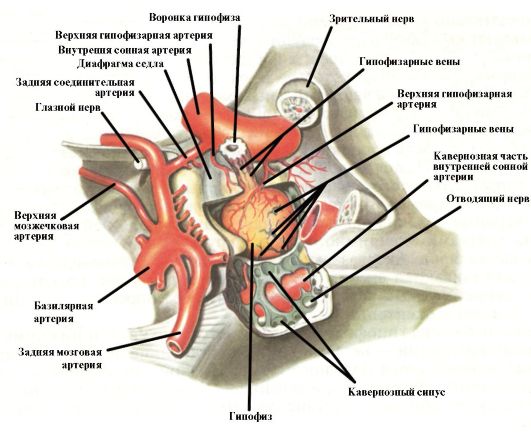 Рис. 2.1. Гипофиз (вид сверху) Рис. 2.1. Гипофиз (вид сверху)типов клеток: ацидофильных, базофильных, составляющих группу хромофилов, и хромофобов. Ацидофильные (эозинофильные) клетки вырабатывают гормон роста (ГР; соматотрофы) и пролактин (лактотрофы), базофильные клетки - тиреотропный гормон (ТТГ; тиреотрофы), адренокортикотропный гормон (АКТГ, кортикотрофы), а также гонадотропины (гонадотрофы): фолликулостимулирующий (ФСГ) и лютеинизирующий (ЛГ) гормоны. Хромофобные клетки рассматривают как источник, из которого дифференцируются хромофилы. В нейрогипофизе оканчиваются волокна гипоталамо-гипофизарного тракта, идущие от супраоптического и паравентрикулярных ядер гипоталамуса. Аксоны нейросекреторных клеток заканчиваются аксовазальными синапсами, по которым поступают секретируемые в ядрах гипоталамуса вазопрессин (антидиуретический гормон) и окситоцин. Аденогипофиз является ключевым регулятором эндокринной системы. Секретируемые им гормоны (ЛГ, ФСГ, ТТГ, АКТГ) регулируют функцию периферических эндокринных желез: щитовидной, коры надпочечников, гонад. Другие гормоны (ГР, пролактин) оказывают прямое действие на органы и ткани-мишени. Гипоталамус расположен на основании мозга и ограничен спереди перекрестом зрительных нервов, сзади мамиллярными телами, по бокам - зрительными нервами. Сверху в гипоталамическую область внедряется III желудочек мозга. Масса гипоталамуса взрослого человека составляет около 4 г. Проводящие пути тесно связывают гипоталамус с соседними структурами головного мозга. Взаимосвязь гипофиза и гипоталамуса осуществляется через портальную систему. Портальная система гипофиза включает первичную капиллярную сеть, которая контактирует с терминалями аксонов аркуатного, вентромедиального и паравентрикулярного ядер гипоталамуса. Капилляры первичного сплетения собираются в портальные вены, идущие вдоль гипофизарной ножки в переднюю долю гипофиза, где они распадаются на вторичную капиллярную сеть. Синусоиды вторичной капиллярной сети собираются в выносящие вены, по которым кровь, обогащенная гормонами передней доли гипофиза, поступает в системный кровоток. Известные в настоящее время гормоны гипоталамуса подразделяют на гормоны, усиливающие (рилизинг-гормоны, либерины) и тормозящие (статины) выделение соответствующих тропных гормонов, при этом их роль не сводится к схеме один либерин (статин) - один гормон гипофиза. Так, тиролиберин может сти- мулировать продукцию ТТГ и пролактина; гонадолиберин является общим рилизинг-гормоном для ЛГ и ФСГ; соматостатин подавляет секрецию ГР и АКТГ. Пролактин - белковый гормон, основной физиологической функцией которого является обеспечение лактации. Стимулирующее влияние на секрецию пролактина оказывает процесс кормления грудью. Основным ингибитором секреции пролактина является дофамин, синтезирующийся в гипоталамусе. Гормон роста (ГР, соматотропин) - полипептидный гормон эффекты которого на органы и ткани реализуются инсулиноподобным ростовым фактором-1 (ИРФ-1), синтезирующимися в печени под влиянием ГР. Основным эффектом ГР у детей и подростков является стимуляция продольного роста костей (преимущественно длинных трубчатых и в меньшей степени губчатых). Кроме того, ГР стимулирует синтез белка и задержку азота, оказывает липолитическое и антинатрийуретическое действие. Введение физиологических доз ГР дает кратковременный инсулиноподобный (снижение гликемии), а затем контринсулярный эффект. Синтез и секреция ГР контролируются двумя гипоталамическими нейропептидами - рилизинг-гормоном ГР (соматолиберин, ГР-РГ) и соматостатином. В течение дня уровень ГР в плазме сохраняется низким; пик содержания ГР отмечается после приема пищи, и его уровень прогрессивно увеличивается во время сна. У растущих детей интегральная суточная продукция ГР существенно выше, чем у взрослых. Лютеинизирующий гормон (ЛГ) в яичниках стимулирует овуляцию и синтез андрогенов клетками теки, а в яичках является регулятором продукции тестостерона клетками Лейдига. Фолликулостимулирующий гормоны (ФСГ) в яичниках стимулирует рост клеток гранулезы и секрецию эстрогенов; в яичках - вместе с тестостероном стимулирует сперматогенез (см. п. 5.1. и 6.1).
Адренокортикотропный гормон (АКТГ, кортикотропин) является стимулятором продукции кортизола и андрогенов в коре надпочечников (см. п. 4.1). Основной функцией тиреотропного гормона (ТТГ) является стимуляция синтеза и секреции гормонов щитовидной железы, а также трофическое воздействие на тиреоциты (см. п. 3.1). Самостоятельной и во многом автономной системой является нейрогипофиз, состоящий, как указывалось, из аксонов супраоптического и паравентрикулярного ядер гипоталамуса. Вазопрессин (аргинин-вазопрессин, антидиуретический гормон, АДГ) является белком, состоящим из 9 аминокислот. Рецепторы АДГ находятся в дистальных извитых канальцах нефрона; их активация приводит к усилению реабсорбции воды. В физиологических условиях секреция АДГ регулируется осморецепторами гипоталамуса: гиперосмолярность плазмы приводит к стимуляции секреции АДГ. Другими непрямыми стимуляторами секреции АДГ являются гиповолемия и артериальная гипотензия. Окситоцин так же, как и вазопрессин, состоит из 9 аминокислот, но отличается от него двумя аминокислотными остатками. Окситоцин, воздействуя на мускулатуру матки, увеличивает силу ее сокращений, обеспечивая таким образом родовую деятельность и послеродовое сокращение матки. Стимулируя сокращение миоэпителиальных клеток альвеол молочных желез, окситоцин способствует поступлению молока в млечные протоки. Физиологическими стимуляторами секреции окситоцина являются растяжение половых путей женщины и кормление грудью. МЕТОДЫ ОБСЛЕДОВАНИЯ ПАЦИЕНТОВ С ГИПОТАЛАМО-ГИПОФИЗАРНОЙ ПАТОЛОГИЕЙ 2.2.1. Физикальные методы Клиническая картина гипоталамо-гипофизарной патологии отличается значительным разнообразием, поэтому какие-либо специфические физикальные методы для обследования пациентов с патологией гипофиза отсутствуют. Тем не менее, вопреки бытующим представлениям, именно данные клинической картины имеют наибольший удельный вес для постановки диагноза.
2.2.2. Лабораторные методы Для диагностики нарушения продукции гипофизарных гормонов чаще всего используется определение базального уровня гормонов, реже различные функциональные пробы (табл. 2.1). Исследование уровня гипоталамических гормонов клинического значения в настоящее время не имеет. Табл. 2.1. Лабораторная диагностика гипоталамо-гипофизарных заболеваний 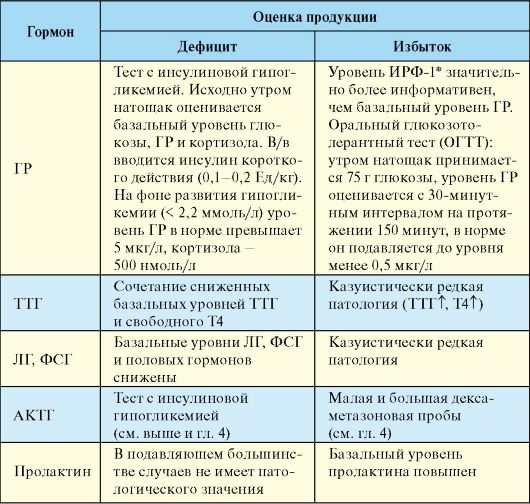 * *ИРФ-1 - инсулиноподобный ростовой фактор. 2.2.3. Инструментальные методы К инструментальным методам, которые используются для визуализации гипоталамо-гипофизарной области, относятся рентгенокраниография, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). Среди дополнительных методов следует указать на определение полей зрения (периметрия), которое показано пациентам с макроаденомами гипофиза, а также после перенесенных нейрохирургических вмешательств, которые могут осложниться спаечным процессом с нарушением зрительной функции. Рентгенодиагностика интраселлярных опухолей гипофиза основывается на определении размеров турецкого седла. В норме размеры турецкого седла составляют: сагиттальный - 12-15 мм, вертикальный - 8-9 мм (рис. 2.2). 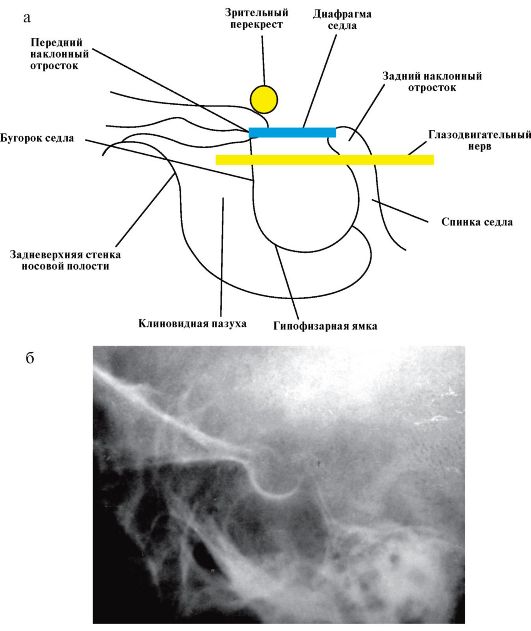 Рис. 2.2. Рентгенокраниография: Рис. 2.2. Рентгенокраниография:а - рентгенографические ориентиры турецкого седла; б - рентгенограмма турецкого седла в норме Большие аденомы гипофиза вызывают значительное увеличение размеров, расширение входа в турецкое седло, истончение и укорочение клиновидных отростков, углубление дна, выпрямление, разрушение спинки седла, двухконтурность (нечеткое очертание одного или двух контуров) седла, как правило, не представляют диагностических трудностей (рис. 2.3). При микроаденомах гипофиза, которые не выходят за пределы турецкого седла, какие-либо изменения на рентгенограммах чаще всего отсутствуют.
Более информативным и относительно недорогим методом визуализации гипофиза является КТ. Тем не менее факторами, существенно ограничивающими его использование, являются плоскостной характер изображение, помехи от костных структур, невозможность дифференцировать небольшие патологические образования, рентгенологическая плотность которых близка к плотности цереброспинальной жидкости или нормальной мозговой ткани. Методом выбора визуализации гипофиза и гипоталамуса, а также методом выбора топической диагностики новообразований гипоталамо-гипофизарной области является МРТ (рис. 2.4). Она позволяет различить малейшие изменения структуры гипофиза, наличие кистозного компонента опухоли, кисты, кровоизлияния и проч. Костная ткань и различные обызвествления на МРТ не дифференцируются. 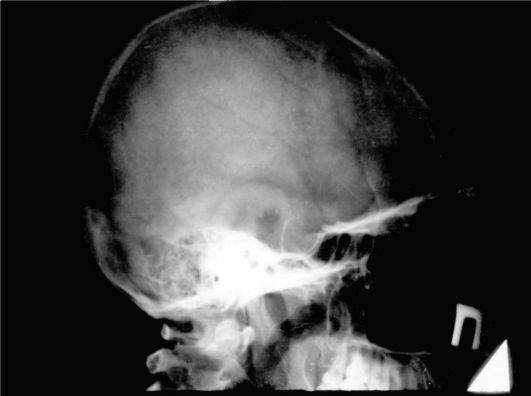 Рис. 2.3. Рентгенограмма черепа при макроаденоме гипофиза Рис. 2.3. Рентгенограмма черепа при макроаденоме гипофиза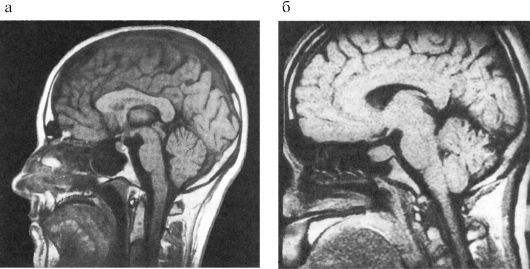 Рис. 2.4. Магнитно-резонансная томография гипоталамо-гипофизарной области: Рис. 2.4. Магнитно-резонансная томография гипоталамо-гипофизарной области:а - норма (сагиттальная проекция); б - макроаденома гипофиза (сагиттальная проекция) Использование контрастных веществ значительно увеличивает диагностические возможности МРТ. Важным преимуществом МРТ является отсутствие лучевой нагрузки и, таким образом, возможность многократного динамического обследования пациента МЕТОДЫ ОБСЛЕДОВАНИЯ ПАЦИЕНТОВ С ГИПОТАЛАМО-ГИПОФИЗАРНОЙ ПАТОЛОГИЕЙ 2.2.1. Физикальные методы Клиническая картина гипоталамо-гипофизарной патологии отличается значительным разнообразием, поэтому какие-либо специфические физикальные методы для обследования пациентов с патологией гипофиза отсутствуют. Тем не менее, вопреки бытующим представлениям, именно данные клинической картины имеют наибольший удельный вес для постановки диагноза.
2.2.2. Лабораторные методы Для диагностики нарушения продукции гипофизарных гормонов чаще всего используется определение базального уровня гормонов, реже различные функциональные пробы (табл. 2.1). Исследование уровня гипоталамических гормонов клинического значения в настоящее время не имеет. Табл. 2.1. Лабораторная диагностика гипоталамо-гипофизарных заболеваний  *ИРФ-1 - инсулиноподобный ростовой фактор. *ИРФ-1 - инсулиноподобный ростовой фактор.2.2.3. Инструментальные методы К инструментальным методам, которые используются для визуализации гипоталамо-гипофизарной области, относятся рентгенокраниография, компьютерная томография (КТ) и магнитно-резонансная томография (МРТ). Среди дополнительных методов следует указать на определение полей зрения (периметрия), которое показано пациентам с макроаденомами гипофиза, а также после перенесенных нейрохирургических вмешательств, которые могут осложниться спаечным процессом с нарушением зрительной функции. Рентгенодиагностика интраселлярных опухолей гипофиза основывается на определении размеров турецкого седла. В норме размеры турецкого седла составляют: сагиттальный - 12-15 мм, вертикальный - 8-9 мм (рис. 2.2).  Рис. 2.2. Рентгенокраниография: Рис. 2.2. Рентгенокраниография:а - рентгенографические ориентиры турецкого седла; б - рентгенограмма турецкого седла в норме Большие аденомы гипофиза вызывают значительное увеличение размеров, расширение входа в турецкое седло, истончение и укорочение клиновидных отростков, углубление дна, выпрямление, разрушение спинки седла, двухконтурность (нечеткое очертание одного или двух контуров) седла, как правило, не представляют диагностических трудностей (рис. 2.3). При микроаденомах гипофиза, которые не выходят за пределы турецкого седла, какие-либо изменения на рентгенограммах чаще всего отсутствуют.
Более информативным и относительно недорогим методом визуализации гипофиза является КТ. Тем не менее факторами, существенно ограничивающими его использование, являются плоскостной характер изображение, помехи от костных структур, невозможность дифференцировать небольшие патологические образования, рентгенологическая плотность которых близка к плотности цереброспинальной жидкости или нормальной мозговой ткани. Методом выбора визуализации гипофиза и гипоталамуса, а также методом выбора топической диагностики новообразований гипоталамо-гипофизарной области является МРТ (рис. 2.4). Она позволяет различить малейшие изменения структуры гипофиза, наличие кистозного компонента опухоли, кисты, кровоизлияния и проч. Костная ткань и различные обызвествления на МРТ не дифференцируются.  Рис. 2.3. Рентгенограмма черепа при макроаденоме гипофиза Рис. 2.3. Рентгенограмма черепа при макроаденоме гипофиза Рис. 2.4. Магнитно-резонансная томография гипоталамо-гипофизарной области: Рис. 2.4. Магнитно-резонансная томография гипоталамо-гипофизарной области:а - норма (сагиттальная проекция); б - макроаденома гипофиза (сагиттальная проекция) Использование контрастных веществ значительно увеличивает диагностические возможности МРТ. Важным преимуществом МРТ является отсутствие лучевой нагрузки и, таким образом, возможность многократного динамического обследования пациента. Гипоталамо-гипофизарная недостаточность (гипопитуитаризм) - клинический синдром, развивающийся в результате деструкции аденогипофиза с последующим снижением продукции тропных гормонов и нарушением деятельности периферических эндокринных желез (табл. 2.6). Табл. 2.6. Гипоталамо-гипофизарная недостаточность 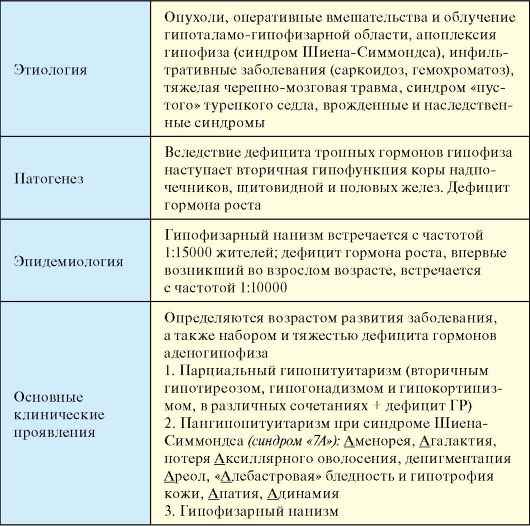 Окончание табл. 2.6 Окончание табл. 2.6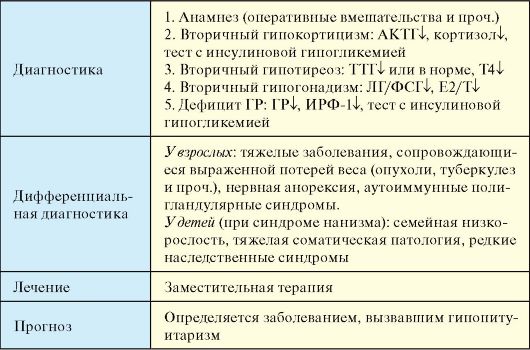 Выделяют пангипопитуитаризм - дефицит всех гормонов аденогипофиза и встречающийся значительно чаще парциальный гипопитуитаризм. Выделяют пангипопитуитаризм - дефицит всех гормонов аденогипофиза и встречающийся значительно чаще парциальный гипопитуитаризм.Этиология Опухоли гипофиза, приводящие к его деструкции с выпадением продукции тропных гормонов. Окологипофизарные опухоли (краниофарингиома, менингиома, метастазы различных опухолей и проч.). Оперативные вмешательства в гипоталамо-гипофизарной области, облучение гипофиза. Апоплексия гипофиза (септико-эмболический или ишемический инфаркт) или синдром Шиена-Симмондса (СШС). Классический СШС описан у женщин после родов, осложненных сепсисом, тромбоэмболиями и массивной кровопотерей. Гипертрофия передней доли гипофиза во время беременности, сменяющаяся ее инволюцией после родов, способствует тому, что все перечисленные осложнения ведут к нарушению кровообращения в гипофизе, ангиоспазмам, гипоксии и некрозу. В последние годы встречается редко. Синдром аналогичный СШС описан при кровопотерях другого генеза, в том числе и у мужчин. Инфильтративные заболевания (саркоидоз, лимфоцитарный гипофизит, гемохроматоз, гистиоцитоз). Тяжелая черепно-мозговая травма Синдром «пустого» турецкого седла (см. п. 2.8). Как правило, легкий парциальный гипопитуитаризм, часто в сочетании с гиперпролактинемией, обнаруживается не более чем у 10 % пациентов. Врожденные и наследственные синдромы: - наследственный дефицит гормона роста и ряда тропных гормонов (мутация гена гормона роста, генов Pit-1 и Prop-1);
- дефекты развития гипоталамо-гипофизарной системы (голопрозэнцефалия, септооптическая дисплазия, врожденная аплазия и гипоплазия гипофиза и др.); - идиопатический дефицит ГР и тропных гормонов гипофиза. Патогенез В основе патогенеза пангипопитуитаризма лежит дефицит тропных гормонов и гормона роста (ГР). В зависимости от локализации, обширности и интенсивности деструктивного процесса выпадение или снижение гормонообразования в гипофизе может быть равномерным и полным (пангипопитуитаризм) или частичным, при котором сохраняется продукция одного или нескольких гормонов. Хотя некротические процессы в гипофизе отмечены в 1,1-8,8 % всех аутопсий, частичная гормональная недостаточность развивается при поражении 60-70 % передней доли, а пангипопитуитаризм - при поражении 90 % и более. В результате наступает вторичная гипофункция коры надпочечников, щитовидной и половых желез. В редких случаях одновременного вовлечения в патологический процесс задней доли или ножки гипофиза возможно снижение уровня вазопрессина с развитием несахарного диабета. Одновременное снижение содержания АКТГ и кортикостероидов, антагонистичных вазопрессину в отношении водного обмена, может нивелировать, смягчать клинические проявления недостаточности вазопрессина. Выпадение продукции пролактина приводит к агалактии. При парциальном гипопитуитаризме наиболее часто страдают гонадотропная и соматотропная функции, значительно реже нарушается продукция АКТГ и ТТГ. У взрослых снижение продукции ГР с его универсальным влиянием на белковый синтез приводит к прогрессирующей атрофии гладкой и скелетной мускулатуры и внутренних органов. Врожденный дефицит ГР в наиболее манифестной форме проявляется синдромом нанизма (от лат. nanos - карлик), который харак-
теризуется резким отставанием в росте и физическом развитии. Гипофизарный нанизм, не является однородным по этиологии и патогенезу состоянием: у большинства больных возникает патология регуляции и секреции других гипофизарных гормонов, как правило, имеются нарушения секреции ФСГ, ЛГ, ТТГ, что сопровождается различными сочетаниями эндокринных и обменных нарушений (пангипопитуитарный нанизм). Наследственные варианты недостаточности ГР, сочетающейся с дефицитом других тропных гормонов, чаще всего связаны с дефицитом фактора Ргор-1 или фактора Pit-1. Фактор Pit- 1 уже в ранних стадиях эмбриогенеза присутствует в соматотрофах, лактотрофах и тиротрофах, где играет важную роль в инициации экспресии генов, ответственных за синтез гормонов этими клетками аденогипофиза. Фактор Prop-1 (prophert, предвестник Pit1) определяет первоначальную закладку сомато-, пролакто- и тиреотрофов, дифференциация которых происходит при участии активатора транскрипции Pit-1. Мутации в указанных генах вызывают комбинированный дефицит ГР, пролактина и ТТГ. Большинство случаев гипофизарного нанизма приходятся на идиопатический дефицит ГР. Эпидемиология Точные данные о распространенности различных форм гипопитуитаризма отсутствуют. СШС в настоящее время следует рассматривать, как весьма редкое заболевание; в большинстве случаев он описывается у женщин в возрасте 20-40 лет. Гипофизарный нанизм встречается с частотой 1:15 000 жителей; разница в заболеваемости у мужчин и женщин отсутствует. Дефицит гормона роста, впервые возникший во взрослом возрасте, встречается с частотой 1:10 000. Клинические проявления Парциальный гипопитуитаризм клинически проявляется вторичным гипотиреозом, гипогонадизмом и гипокортицизмом в различных сочетаниях, а также весьма неспецифической симптоматикой дефицита ГР (табл. 2.7).
Пангипопитуитаризм при классическом течении синдрома Шиена-Симмондса (СШС) в большинстве случаев развивается медленно, в течение нескольких лет. Характерна неуклонно нарастающая потеря массы тела, при тяжелом течении достигающая 25-30 кг. Истощение обычно равномерное, мышцы атрофируются, внутренние органы уменьшаются в объеме. Характерны изменения кожных покровов: истончение и сухость придают коже вид папиросной бумаги, Табл. 2.7. Клиническая картина гипопитуитаризма 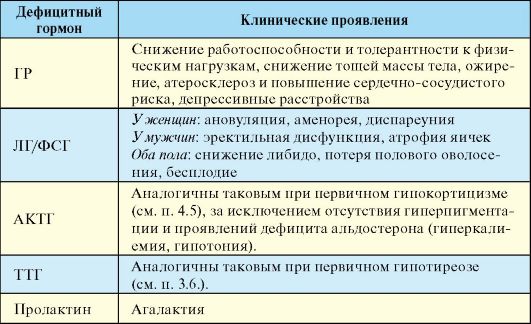 отмечаются сморщивание, шелушение в сочетании с бледно-желтушной, восковидной окраской. Исчезают волосы в подмышечных впадинах и на лобке, депигментируются соски и кожа в области промежности. Характерны аменорея, снижение либидо, эректильная дисфункция, постепенная атрофия половых органов и молочных желез. При развитии заболевания после родов характерны агалактия. В типичном случае обнаруживается синдром «7А» (Аменорея, Агалактия, потеря Аксиллярного оволосения, депигментация Ареол, «Алебастровая» бледность и гипотрофия кожи, Апатия, Адинамия). Для поздних стадий характерна резкая общая слабость, апатия, адинамия, вплоть до полной обездвиженности, гипотермия, ортостатический коллапс и коматозное состояние, которые без лечения приводят к гибели больного. Острая аденогипофизарная недостаточность (гипофизарная кома) представляет собой сочетание острой надпочечниковой недостаточности и гипотиреоидной комы. отмечаются сморщивание, шелушение в сочетании с бледно-желтушной, восковидной окраской. Исчезают волосы в подмышечных впадинах и на лобке, депигментируются соски и кожа в области промежности. Характерны аменорея, снижение либидо, эректильная дисфункция, постепенная атрофия половых органов и молочных желез. При развитии заболевания после родов характерны агалактия. В типичном случае обнаруживается синдром «7А» (Аменорея, Агалактия, потеря Аксиллярного оволосения, депигментация Ареол, «Алебастровая» бледность и гипотрофия кожи, Апатия, Адинамия). Для поздних стадий характерна резкая общая слабость, апатия, адинамия, вплоть до полной обездвиженности, гипотермия, ортостатический коллапс и коматозное состояние, которые без лечения приводят к гибели больного. Острая аденогипофизарная недостаточность (гипофизарная кома) представляет собой сочетание острой надпочечниковой недостаточности и гипотиреоидной комы.Гипофизарный нанизм проявляется резким отставанием в росте и физическом развитии. К людям карликового роста относят мужчин, имеющих рост ниже 130 см, и женщин - ниже 120 см. Наименьший описанный рост карлика составил 38 см. Дети с классической соматотропной недостаточностью чаще рождаются с нормальной массой
и длиной тела, и начинают заметно отставать в развитии с 2-4-летнего возраста. Для детей с органическим генезом дефицита ГР (краниофарингиома, черепно-мозговая травма и т.п.) характерны более поздние сроки проявления дефицита роста, после 5-6-летнего возраста. При идиопатическом гипофизарном нанизме на фоне отставания в росте отмечаются нормальные пропорции тела ребенка. У нелеченных взрослых отмечаются детские пропорции тела. Черты лица мелкие («кукольное лицо»), переносица западает. Кожа бледная, с желтоватым оттенком, сухая, иногда наблюдаются цианоз, мраморность кожи. У нелеченных больных рано появляются «старообразность», истончение и морщинистость кожи (геродерма), что связано с недостаточностью анаболического действия ГР и замедленной сменой клеточных генераций. Распределение подкожной жировой клетчатки колеблется от истощения до ожирения с преимущественно верхним, или «кушингоидным» (висцеральным) отложением. Волосы могут быть как нормальными, так и сухими, тонкими, ломкими. Вторичное оволосение чаще отсутствует. Мышечная система развита слабо. У мальчиков, как правило, имеется микропенис. Половое развитие задержано и наступает в сроки, когда костный возраст ребенка достигает пубертатного уровня. Значительная доля детей с дефицитом ГР имеет сопутствующий дефицит гонадотропинов. Диагностика Для диагностики гипопитуитаризма у взрослых важнейшее значение имеют данные анамнеза (операции и облучение гипофиза, осложненные массивным кровотечением роды и т.д.). При гормональном исследовании определяется сочетание низких уровней гормонов периферических эндокринных желез (Т4, тестостерон, эстрадиол, кортизол) со сниженными или низкими уровнями тропных гормонов и ГР. В большинстве случаев необходимо подтверждение дефицита тропных гормонов и ГР в стимуляционных пробах (см. табл. 2.1). Всем пациентам показано проведение МРТ головного мозга.
Основными методами клинической диагностики гипофизарного нанизма являются антропометрия и сопоставление ее результатов с перцентильными таблицами. Для исключения различных скелетных дисплазий (ахондроплазия, гипохондроплазия) оцениваются пропорции тела. При рентгенографии кистей и лучезапястных суставов определяется костный (рентгенологический) возраст, при этом для гипофизарного нанизма характерна значительная задержка окос- тенения. Дефицит ГР необходимо подтвердить пробой с инсулиновой гипогликемией (табл. 2.1). Весьма ценным исследованием в диагностике дефицита ГР является определение уровня ИРФ-1. Дифференциальная диагностика У взрослых гипоталамо-гипофизарную недостаточность необходимо дифференцировать с целым рядом заболеваний, приводящим к похудению (злокачественные опухоли, туберкулез, энтероколиты, спру и спруподобные синдромы, порфириновая болезнь и др.), в том числе от нервной анорексии (см. п. 11.4). Сочетание недостаточности нескольких эндокринных желез встречается в рамках аутоиммунных полигландулярных синдромов (см. п. 9.1). Идиопатический гипофизарный нанизм дифференцируют от других форм низкорослости: при врожденном гипотиреозе, раннем половом созревании, врожденной дисфункции коры надпочечников, сахарном диабете (синдром Мориака, Нобекур), на фоне тяжелых соматических заболеваний, при генетических остеоартропатиях, а также с так называемой семейной низкорослостью (конституциональная задержка роста). В последнем случае, как правило, удается выявить аналогичные случаи низкорослости у одного из родителей. Гипофизарный нанизм необходимо дифференцировать от ряда редких генетических синдромов, таких как прогерия (синдром Гетчинсона-Гилфорда), синдром Ларона (периферическая нечувствительность к ГР в результате дефекта гена его рецептора), синдром Рассела-Сильвера (внутриутробная задержка роста с асимметрией туловища), синдром Секкеля (птицеголовые карлики), синдром Прадера-Вилли (задержка роста с рождения, ожирение, крипторхизм, гипоспадия, олигофрения), синдром Лоуренса-Муна-Барде-Бидля (низкорослость, пигментная дегенерации сетчатки, атрофии дисков зрительных нервов, гипогонадизм, задержка умственного развития), ахондроплазия (задержка роста за счет диспропорционального укорочения конечностей).
Лечение При возможности устранение причины заболевания (удаление опухоли гипофиза или гипоталамуса). Заместительную гормонотерапию начинают с компенсации вторичного гипокортицизма препаратами кортикостероидов (см. п. 4.5). Назначение тиреоидных гормонов до компенсации гипокортицизма может привести к развитию острой надпочечниковой недостаточ- ности. Недостаточность половых желез компенсируется с помощью эстрогенов, прогестинов и препаратов тестостерона. Гипотиреоз компенсируется препаратами левотироксина. В основе патогенетической терапии гипофизарного нанизма лежит заместительная терапия препаратами генно-инженерного человеческого ГР (0,07-0,1 ЕД/кг массы тела ежедневно подкожно в 20.00-22.00 часа). Для лечения дефицита ГР у взрослых рекомендуемые дозы препарата составляют 0,125-0,25 ЕД/кг). Лечение при гипопитуитарной коме аналогично таковому при острой надпочечниковой недостаточности (см. п. 4.5.3). Прогноз Определяется конкретным заболеванием, при котором развился гипопитуитаризм. При крупных аденомах гипофиза, по поводу которых предпринималось оперативное вмешательство, а также при инфильтративных заболеваниях процесс обычно необратим. При гипофизарном нанизме вовремя начатая заместительная терапия ГР позволяет достичь пациенту приемлемого для социальной адаптации роста. |
