гормоны. Гормоны это органические вещества, которые образуются в тканях одного типа (эндокринные железы, или железы внутренней секреции), поступают в кровь, переносятся по кровяному руслу в ткани другого типа (тканимишени), где оказывают своё биологическое действие (т е.
 Скачать 216.79 Kb. Скачать 216.79 Kb.
|
|
ГОРМОНЫ КОРЫ НАДПОЧЕЧНИКОВ В коре надпочечников образуются из холестерина стероидные гормоны: кортикостероиды (глюкокортикоиды и минералокортикоиды) и половые гомоны (женские и мужские). Биохимические особенности коры надпочечников В расчете на 1 грамм ткани кора надпочечников занимает второе место в организме после головного мозга по содержанию холестерина и первое место - по содержанию аскорбиновой кислоты (витамина С), необходимой для превращения холестерина в стероидные гормоны. Распад стероидных гормонов Обезвреживание стероидных гормонов происходит в печени двумя путями. 1)Около 90 % стероидных гормонов сначала восстанавливается, затем конъюгирует с глюкуроновой кислотой и легко экскретируется смочой. 2)У 10 % глюкокортикоидов, минералокортикоидов и мужских (но не женских) половых гормонов происходит отщепление боковой цепи у 17-го углеродного атома и его окисление с образованием кетогруппы, в результате чего образуются 17-кетостероиды (17-КС), которые также выделяются с мочой в связанном с глюкуроновой кислотой виде. Таким образом, 17-КС – это не гормоны, а продукты 24 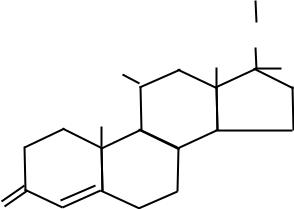 распада гормонов: глюкокортикоидов, минералокортикоидов и мужских (но не женских) половых гормонов. ГЛЮКОКОРТИКОИДЫ Представителями глюкокортикоидов являются гидрокортизон (кортизол, рис. 10), кортизон и кортикостерон. CH2OH C
Рис. 10. Строение кортизола O Ткани-мишени для этой группы гормонов: печень, мышцы, жировая, лимфоидная и соединительная ткани. Причем в печени глюкокортикоиды повышают проницаемость мембран для транспорта веществ в клетку и активируют анаболические процессы (то есть синтез веществ), а в остальных тканях – понижают проницаемость мембран и стимулируют катаболизм (то есть распад веществ). Действие глюкокортикоидов на метаболизм Углеводный обмен. Во всех тканях-мишенях глюкокортикоиды тормозят гликолиз. В печени гормоны усиливают глюконеогенез и синтез гликогена, в остальных тканях – уменьшают транспорт глюкозы в клетку, в мышцах – снижают синтез гликогена. При избытке глюкокортикоидов (применение их для лечения в больших дозах или длительно, а также повышенное образование глюкокортикоидов в организме) развивается гипергликемия вследствие активации глюконеогенеза в печени и понижения утилизации глюкозы в периферических тканях. Длительная гипергликемия может привести к срыву инсулярного аппарата поджелудочной железы и развитию стероидного диабета. 25 Липидный обмен. В печени глюкокортикоиды повышают синтез триглицеридов, липопротеинов очень низкой плотности (ЛПОНП) и кетоновых тел. В жировой ткани гормоны увеличивают распад жира на конечностях, но усиливают отложение жира на туловище и лице. Поэтому при избытке глюкокортикоидов наблюдается так называемое паукообразное ожирение и повышение уровня кетоновых тел в крови. Белковый обмен. В печени глюкокортикоиды увеличивают синтез белка, в остальных тканях – снижают синтез и стимулируют распад тканевых белков. В связи с этим при избытке глюкокортикоидов наблюдаются замедление заживления ран, атрофия и слабость мышц, в костях – остеопороз (разрежение кости, что сопровождается легко возникающими переломами, например, компрессионными переломами позвонков и длинных костей уже при минимальной травме). В лимфоидной ткани избыток глюкокортикоидов приводит к угнетению синтеза антител и уменьшению образования лимфоцитов, поэтому при стрессе (когда вырабатывается много глюкокортикоидов) снижается иммунная защита организма и повышается восприимчивость к инфекционным заболеваниям. Указанный механизм действия глюкокортикоидов на лимфоидную ткань лежит в основе их применения при лечении аллергии и при трансплантации для подавления реакции отторжения пересаженного органа. Системное действие глюкокортикоидов 1)Глюкокортикоиды усиливают секрецию HCl в желудке. Механизм их действия обусловлен тем, что глюкокортикоиды тормозят синтез простагландинов, которые снижают секрецию HCl, поэтому при избытке глюкокортикоидов в организме могут развиваться стероидные язвы желудка. 2)Глюкокортикоиды обладают противовоспалительным действием. Они воздействуют на все стадии воспалительного процесса, но особенно сильно снижают проницаемость мембран и ингибируют синтез простагландинов, которые являются тканевыми факторами воспаления, поэтому применение глюкокортикоидов возможно для лечения воспалений. 26 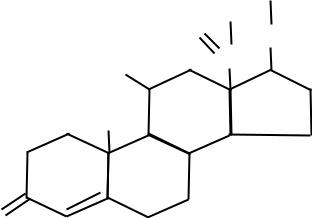 3)Глюкокортикоиды снижают повышенную реактивность организма, т.е. гиперчувствительность, поэтому используются при лечении аллергии, и, в частности, анафилактического шока. 4)Глюкокортикоиды повышают устойчивость организма к повреждающим факторам (травмы, инфекции, интоксикации, боль, холод, физическая нагрузка, тяжелые психические потрясения). 5)Глюкокортикоиды оказывают пермиссивное действие на организм, т.е. усиливают действие других гормонов. МИНЕРАЛОКОРТИКОИДЫ Представителями минералокортикоидов являются альдостерон (рис. 11) и дезоксикортикостерон. Они регулируют обмен натрия,
Главной тканью-мишенью для действия гормонов является эпителий дистальных канальцев почек, где альдостерон увеличивает реабсорбцию натрия из мочи в кровь. Поэтому альдостерон называют натрийзадерживающим гормоном. Поскольку натрий «тянет» за собой воду, то при избытке минералокортикоидов в организме повышается артериальное давление, усиливаются отеки и воспалительные процессы. Одновременно с увеличением реабсорбции натрия под действием альдостерона возрастает экскреция калия с мочой. Поэтому при избытке гормона в организме снижается концентрация калия в крови, что приводит к повышению возбудимости миокарда, нарушению работы сердца, возникают сильная слабость, характерные изменения на ЭКГ, и может развиться сердечная недостаточность. 27 Другой тканью-мишенью для минералокортикоидов являются потовые железы. В жару альдостерон препятствует чрезмерной потере натрия с потом. При недостаточном синтезе альдостерона натрий теряется с мочой, что приводит к потере воды, т.е. дегидратации организма. Глюкокортикоиды обладают частичным действием минералокортикоидов, поэтому при длительном применении с лечебной целью глюкокортикоидов больным обязательно назначают препараты калия. НАРУШЕНИЯ ГОРМОНАЛЬНОЙ ФУНКЦИИ КОРЫ НАДПОЧЕЧНИКОВ Гиперфункция коры надпочечников, или гиперкортицизм, может проявляться либо повышенной секрецией всех групп гормонов, либо преимущественно одной из групп гормонов. В последнем случае выделяют 3 вида гиперкортицизма. 1)Синдром Иценко-Кушинга (опухоль пучковой зоны коры надпочечников, синтезирующая, главным образом, кортизол) и болезнь Иценко-Кушинга (неопухолевая гиперплазия, то есть разрастание, коры надпочечников под влиянием избыточной секреции кортикотропина гипофизом). 2)Первичный альдостеронизм, или болезнь Конна – избыточное образование минералокортикоидов в организме (в клубочковой зоне коры надпочечников). 3)Адреналовый вирилизм, или адреногенитальный синдром – сопровождается гиперсекрецией мужских половых гормонов в сетчатой зоне коры надпочечников. При этом у женщин наблюдается появление мужских признаков, у мужчин – усиление мужских признаков, у детей – преждевременное половое созревание. Гипокортицизм, называемый Аддисоновой, или бронзовой болезнью, сопровождается дефицитом глюко- и минералокортикоидов и смешанными изменениями обмена веществ и функций организма. Причиной гипокортицизма может явиться туберкулёз или атрофия коры надпочечников. Недостаточное образование кортикостероидов приводит к сильной слабости, утомляемости, снижению артериального давления, наблюдаются пигментации кожи, тяга к соленой пище, высокая чувствительность к стрессам и инфекциям, непереносимость голода из-за выраженной 28 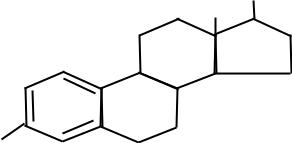 гипогликемии. В крови снижается концентрация натрия и увеличивается концентрация калия. ГОРМОНЫ ПОЛОВЫХ ЖЕЛЁЗ ЖЕНСКИЕ ПОЛОВЫЕ ГОРМОНЫ Женские половые гормоны представлены эстрогенами и прогестинами (гестагенами). К эстрогенам относятся: эстрадиол (рис. 12; образуется в фолликулах яичников), эстриол (гормон плаценты) и эстрон (синтезируется в коре надпочечников). Представителем прогестинов является прогестерон, который вырабатывается в желтом теле яичников. Небольшое количество женских половых гормонов вырабатывается в организме мужчин. OH Рис. 12. Строение эстрадиола. HO Ткани, чувствительные к действию эстрогенов, делятся на 2 группы: половые органы и неполовые органы. Действие женских половых гормонов на половые органы Вполовых органах женские половые гормоны способствуют развитию и функционированию этих органов и формированию вторичных половых признаков в период полового созревания. Вматке увеличивается рост железистого эпителия эндометрия игладкой мускулатуры миометрия, усиливается васкуляризация органа. Во влагалище увеличивается число слоев клеток, что является диагностическим критерием действия эстрогенов на организм. Вмолочной железе эстрогены стимулируют рост протоков, прогестерон – рост железистой ткани. 29 + Действие женских половых гормонов на неполовые органы В неполовых органах эстрогены оказывают также характерное действие. ЦНС, гипоталамус, гипофиз - под влиянием гормонов происходит формирование типичного полового поведения, инстинкта, психики женщины. Кости, хрящи, гортань - эстрогены способствуют формированию характерного «женского» типа скелета, гортани и голоса. Эстрогены ускоряют окостенение эпифизов, где находятся зоны роста кости, поэтому, если у девочки в период полового созревания образуется мало эстрогенов, замедляется окостенение эпифизов, и в этом случае девочка может иметь необычно высокий рост. У взрослых женщин при продолжительном введении эстрогенов или их избыточном образовании в организме происходит интенсивное обызвествление костей, и могут исчезать полости, в которых находится костный мозг, что приводит к развитию анемии. Кожа – эстрогены способствуют росту волос по женскому типу, тормозят рост волос на коже, снижают секреторную активность сальных желез (понижают сальность кожи). Печень – эстрогены стимулируют синтез специфических белков печени: ангиотензиногена, способствующего повышению артериального давления, и некоторых факторов свертывания крови (II, VII, IX, X). Поэтому при избытке эстрогенов в организме наблюдается склонность к гипертонии и тромбозам. Кроме этого, эстрогены, воздействуя на печень, увеличивают образование в ней липопротеинов очень низкой плотности (ЛПОНП) и липопротеинов высокой плотности (ЛПВП). ЛПОНП на 50 % состоят из триглицеридов (нейтрального жира), из печени они через кровь доставляются в жировую ткань, где жир откладывается. Поэтому у женщин мышцы всегда покрыты слоем подкожного жира. ЛПВП уменьшают концентрацию холестерина в крови, способствуют его выведению из организма. Поэтому женщины реже, чем мужчины, заболевают атеросклерозом и инфарктом миокарда. Жировая ткань – в ней эстрогены и прогестерон увеличивают синтез жира, тормозят его расщепление, способствуют формированию типично женских жировых отложений. Почки – эстрогены способствуют задержке натрия в организме, прогестерон усиливает потерю натрия с мочой. Поскольку при беременности образуется много прогестерона, натрий усиленно теряется организмом, отсюда – тяга к соленой пище. МУЖСКИЕ ПОЛОВЫЕ ГОРМОНЫ Мужские половые гормоны (андрогены) представлены тестостероном (рис. 13) и андростероном. Они образуются в семенниках, коре надпочечников, предстательной железе. Небольшое количество андрогенов синтезируется у женщин в яичниках. OH Рис. 13. Строение тестостерона. O Как и женские половые гормоны, андрогены действуют не только на половые, но и на неполовые органы. Действие мужских половых гормонов на половые органы В половых органах мужские половые гормоны оказывают андрогенное действие, то есть способствуют развитию и функционированию этих органов и формированию вторичных половых признаков в период полового созревания. Действие мужских половых гормонов на неполовые органы В неполовых органах андрогены обладают генерализованным анаболическим действием, то есть стимулируют синтез нуклеиновых кислот, белка, задерживают в организме азот и кальций, усиливают синтез фосфолипидов мембран. ЦНС, гипоталамус, гипофиз – под влиянием андрогенов происходит формирование типичного полового поведения, инстинкта и психики мужчины, то есть образуются поведенческие особенности мужского пола. Андрогены влияют на развитие мозга. Если во внутриутробном периоде в критические стадии развития и 31 дифференцировки мозга развивается недостаточность андрогенов, то в будущем у этого юноши или мужчины могут возникнуть варианты половой ориентации. Избыток андрогенов в организме способствует агрессивности. Кости, хрящи, гортань – андрогены способствуют формированию характерных физиологических особенностей мужского скелета, гортани, голоса, усиливают отложение фосфорнокальциевых солей в эпифизарных зонах роста. Чрезмерная выработка гормонов может приводить к преждевременному заращению эпифизов и развитию низкорослости. Мышцы – андрогены увеличивают мышечную массу и силу, создают характерную рельефность мышц. Кожа – андрогены обладают стимулирующим действием на сальные железы, повышая сальность кожи, усиливают пигментацию кожи (солнечный загар), увеличивают рост волос на лице и теле, способствуют росту волос по мужскому типу. Избыток гормонов может привести к облысению. Жировая ткань – андрогены ускоряют расщепление жира в жировой ткани, тормозят его синтез. В печени и почках андрогены резко увеличивают синтез белка, в кроветворных органах усиливают эритропоэз. Анаболические стероиды На основе мужских половых гормонов синтезированы аналоги этих соединений – анаболические стероиды, обладающие максимальной анаболической активностью и минимальной – андрогенной. Первоначально анаболические стероиды широко применяли для откорма скота. Однако анаболические стероиды очень плохо метаболизируют в организме животных и не разрушаются при термической обработке пищи. Поэтому, попадая с мясом в организм человека, анаболические стероиды вызывали тяжелые поражения печени, в том числе опухоли, поскольку продукты превращения этих соединений являются канцерогенами. В настоящее время применение анаболических стероидов в практике животноводства уменьшилось. Однако некоторые спортсмены продолжают применять этих средства для повышения спортивных результатов. Тем не менее, установлено, что даже относительно кратковременное (в течение 2 лет) применение 32 анаболиков в возрастном периоде с 18 до 26 лет (кроме перечисленных опасностей для здоровья спортсмена) может привести у мужчин к ранней импотенции, а у женщин – к раку молочной железы. Небольшие дозы анаболических стероидов применяют в лечебной практике у лиц после 35 лет при тяжелых травмах, инфаркте миокарда, после операций для ускорения заживления ран, увеличения массы тела и улучшения аппетита при истощении. | ||||||||||||||||||||||||||||||
