Глава 3. Химическая связь
 Скачать 2.92 Mb. Скачать 2.92 Mb.
|
|
Глава 3. Химическая связь. Химическая связь возникает благодаря взаимодействию электрических полей, создаваемых электронами и ядрами атомов, участвующих в образовании молекулы или кристалла. Она образуется, если электроны взаимодействующих атомов получают возможность двигаться одновременно вблизи положительных зарядов нескольких ядер. Задача заключается в том, чтобы правильно описать главные детали этого движения многих частиц и научиться рассчитывать в различных участках молекулы электронную плотность, обеспечивающую «связывание» атомов. Оказалось, что получить даже качественно правильные решения уравнения Шрёдингера удаётся не всегда. А из методов квантовой химии наиболее известны два приближенных подхода к расчёту молекулярных систем — метод валентных связей и метод молекулярных орбиталей. #1. История вопроса. Основные понятия о строении молекул были заложены в теории химического строения А. М. Бутлерова (1861 год). Основные положения теории: 1) Атомы в молекулах соединены друг с другом в определённой последовательности. Изменение этой последовательности приводит к образованию нового вещества с новыми свойствами. 2) Соединение атомов происходит в соответствии с их валентностью. 3) Свойства вещества зависят не только от состава, но и от их химического строения — порядка соединения атомов в молекулах и характера их взаимного влияния. Разрабатывая теорию электронной связи, Бутлеров не ставил перед собой задачу выяснения причины химической связи, полагая, что химия ещё не готова к решению данной задачи. Лишь после того, как стали известны основные черты электронной структуры атомов, появилась возможность для разработки такой теории. В 1916 году Дж. Льюис высказал предположение, что химическая связь возникает путем образования электронной пары, одновременно принадлежащей двум атомам. Эта идея послужила исходным пунктом для разработки теории ковалентной связи. В том же 1916 году В. Коссель предположил, что при взаимодействии двух атомов один из них отдаёт, а другой принимает электроны. При этом первый атом превращается в положительно заряженный, а другой в отрицательно заряженный ион. Взаимное электростатическое притяжение образовавшихся ионов и приводит к образованию устойчивого соединения. Дальнейшее развитие идей Косселя привело к созданию современных представлений об ионной связи. Сведения об электронном строении молекулы можно было бы получить из уравнения Шрёдингера для неё. Возникающая при этом трудность заключается в том, что решение этого уравнения возможно только для двух тел. В молекулах практически важных веществ содержится 100 и более электронов и большее число ядер атомов. Поэтому суть возможных теоретических методов исследования строения молекул заключается в нахождении приближенного способа решения уравнения Шрёдингера. Приближённые способы решения уравнения Шрёдингера для систем, состоящих из многих ядер и электронов, интерпретация полученных решениях в удобных понятиях и терминах и т.п. является объектом изучения квантовой химии. #2. Понятие о валентности. Валентность элемента — это мера способности его атомов соединяться с другими атомами в определённых соотношениях. Первоначально за единицу валентности принята валентность атома водорода. Валентность другого элемента можно выразить числом атомов водорода, которое присоединяет к себе или замещает один атом этого другого элемента. Определённая таким образом валентность называются валентностью в водородных соединениях или валентностью по водороду. Пример: в HCl валентность равна единице, в H2O двум, в NH3 трём и так далее. Валентность кислорода, как правило, равна двум. Поэтому, зная состав или формулу кислородного соединения того или иного элемента, можно определить как удвоенное число атомов кислорода, которое может присоединить один атом данного элемента. Определённая таким образом валентность называется валентностью по кислороду. Пример: в N2O валентность азота по кислороду равна единице. в CO валентность углерода по кислороду равна двум, в SiO2 валентность кремния равна четырём. Таким образом, охарактеризовать валентность элемента каким-нибудь числом, как правило, нельзя. Классическое определение валентности как числа ковалентных связей, образованных атомом с одновалентными атомами, не позволяет объяснить существование некоторых молекул. Пример: CO, O3. Более содержательное определение валентности v получено на основании метода молекулярных орбиталей и понятий ковалентности (vc) и электровалентности (ve). Валентность равна сумме ковалентности и модуля электровалентности. v=vc+|ve| Ковалентность атома характеризует степень участия атома в ковалентных химических связях или степень сосредоточенности электронной плотности в межъядерном пространстве. как правило, она принимает нецелочисленные значения. Аналогично, электровалентность атома определяемая величиной эффективного заряда атома, также бывает нецелочисленной. #3. Квантово-механические методы описания ковалентной химической связи. Приближённо ковалентность атома может быть оценена по порядку связи, являющемся в большинстве случаев косвенной характеристикой прочности ковалентной связи. Ковалентность примерно равна сумме порядков связей, образуемых этим атомом со всеми остальными атомами молекулы. Для двухатомных систем порядок связи равен полуразности числа электронов, располагающихся на связывающих молекулярных орбиталях., и числа электронов, располагающихся на разрыхляющих молекулярных орбиталях. Эти числа электронов, приходящихся на отдельные молекулярные орбитали, называются заселённостями орбиталей. Заселённость любой орбитали обозначается буквой ω. Потому порядок связи (Р) — полуразность заселённостей всех связывающих молекулярных орбиталей ω (Ψсв) и всех разрыхляющих молекулярных орбиталей ω (Ψ*). vc≈ P; P = [∑ ω (Ψсв) — ∑ ω (Ψ*)]/2 Первое суммирование ведётся по всем связывающим МО, а второе — по разрыхляющим. Так как наличие электрона на связывающей орбитали понижает энергию электрона, а на разрыхляющей повышает, то больший порядок связи соответствует более прочной ковалентной связи и большей ковалентности атомов. Ковалентная связь образуется одной или несколькими парами электронов с разными спинами. Происходит перекрывание электронных облаков. В результате атом теряет энергию — энергия связи. Ковалентная связь направлена в сторону максимального перекрывания электронных облаков (существует направленность). Обладает насыщаемостью, определяющейся механизмом образования (обменный или донорно-акцепторный). #4. Метод валентных связей (ВС). Приближённое решение уравнения Шрёдингера было впервые произведено в 1927 году В. Гейтлером и Лондоном. Сначала они рассмотрели систему из двух атомов водорода, находящихся на большом расстоянии (при таком рассмотрении можно учитывать взаимодействие электрона только со своим ядром), получив зависимость волновой функции рассматриваемой системы от координаты, и тем самым определили плотность общего электронного облака (электронную плотность) в любой точке пространства. Затем они решили, что найденная ими зависимость волновой функции от координат сохраняется при сближении атомов, однако возникают некоторые поправки (возмущения) к исходному состоянию электронов в свободных атомах водорода, которыми они ранее пренебрегали. В результате были получены уравнения, позволяющие найти зависимость потенциальной энергии Е системы, состоящей из двух атомов водорода, от расстояния r между ядрами этих атомов. При этом оказалось, что результаты расчёта зависят от того, одинаковые или разные спины у электронов взаимодействующих атомов. При совпадении спинов сближение атомов приводит к непрерывному возрастанию энергии системы. В последнем случае для сближения атомов требуется затрата энергии, так что такой процесс оказывается энергетически невыгодным и химическая связь между ними не возрастает. При противоположно направленных спинах сближение атомов до некоторого расстояния ro сопровождается уменьшением энергии системы. При r=ro система обладает наименьшей потенциальной энергией, т.е. находится в наиболее устойчивом состоянии. Дальнейшее сближение атомов приведёт к возрастанию энергии. Таким образом, в случае противоположно направленных спинов образуется молекула Н2 — устойчивая система из двух атомов водорода, находящихся на определённом расстоянии друг от друга. Образование химической связи между атомами водорода является результатом «перекрывания» электронных облаков, происходящего при сближении взаимодействующих атомов. Вследствие такого «перекрывания» плотность отрицательного электрического заряда в межъядерном пространстве возрастает. Положительно заряженные ядра притягиваются к области взаимного проникновения электронных облаков. Это притяжение преобладает над взаимным отталкиванием между электронами и молекула становится устойчивой. Таким образом, исследование позволило сделать вывод, что химическая связь в молекуле водорода осуществляется путём образования пары электронов с противоположными спинами, принадлежащих обоим атомам. Разработанная на этой основе теория химической связи и для более сложных молекул получила название метода валентных связей. Наличие спаренных электронов является «индикатором» наличия химической связи, но не причиной её образования. Изучение причины образования химической связи показало, что энергия системы из двух атомов понижается тогда, когда электроны с большой вероятности находятся в межъядерном пространстве. Такая задержка приводит к понижению их кинетической энергии. В результате отрицательная составляющая полной энергии молекулы преобладает, молекула становится устойчивой и образуется химическая связь. Основные положения метода ВС:
При оценке степени перекрывания электронных облаков следует учитывать знаки волновых функций электронов. Поскольку электронам присущи волновые свойства, то при взаимодействии двух электронов образуется общая «электронная волна». Там, где амплитуды исходных волн имеют одинаковые знаки, при их сложении возникает суммарная волна с амплитудой, имеющей большее абсолютное значение, чем исходные амплитуды. Напротив, там, где амплитуды исходных волн имеют различные знаки, волны будут «гасить» друг друга. Роль амплитуды электронной волны играет волновая функция — атомная орбиталь (АО). Поэтому в тех областях пространства, где атомная орбиталь взаимодействующих электронов имеют одинаковые знаки, абсолютное значение волновой функции образующегося общего электронного облака будет больше, чем значения АО у изолированных атомов. При этом будет возрастать и плотность электронного облака. Здесь происходит положительное перекрывание электронных облаков, которое приводит к взаимному притяжению ядер. В тех же областях пространства, где знаки волновых функций взаимодействующих электронов противоположны, абсолютное значение суммарной волновой функции будет меньше, чем у изолированных атомов. Здесь плотность электронного облака будет уменьшаться. В таком случае имеет место отталкивание ядер. #5. Гибридизация атомных орбиталей. Гибридизация атомных орбиталей - это изменение формы некоторых орбиталей при образовании ковалентной связи для достижения более эффективного перекрывания орбиталей. Химическая связь, образуемая с участием электронов гибридных орбиталей, более прочная, чем связь с участием электронов негибридных s- и р-орбиталей, так как происходит большее перекрывание.
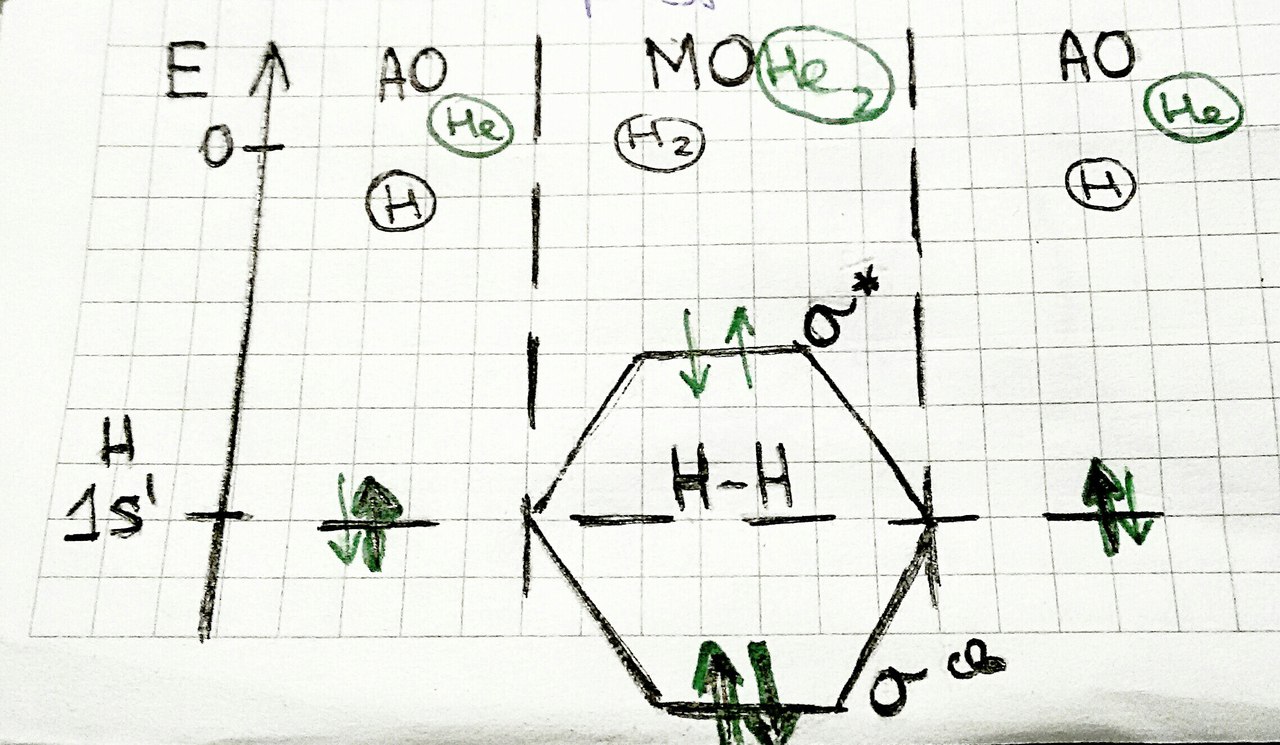
sp2-гибридизация – одна s-орбиталь и две p-орбитали превращаются в три одинаковые «гибридные» орбитали, угол между осями которых равен 120°. Молекулы, в которых осуществляется sp2-гибридизация, имеют плоскую геометрию (Например, BH3). 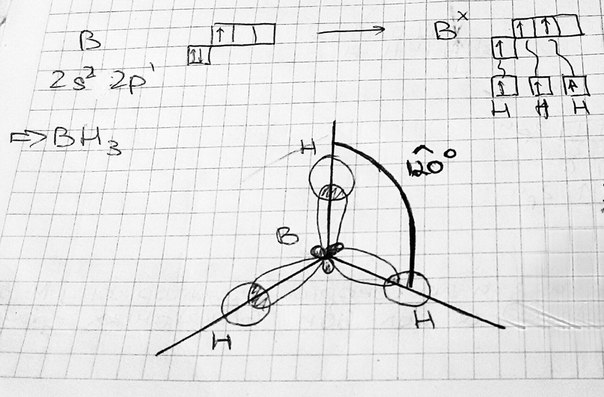 плоская фигура sp3-гибридизация – одна s-орбиталь и три p-орбитали превращаются в четыре одинаковые «гибридные» орбитали, угол между осями которых равен 109°28'. Молекулы, в которых осуществляется sp3-гибридизация, имеют тетраэдрическую геометрию (Например, CH4). 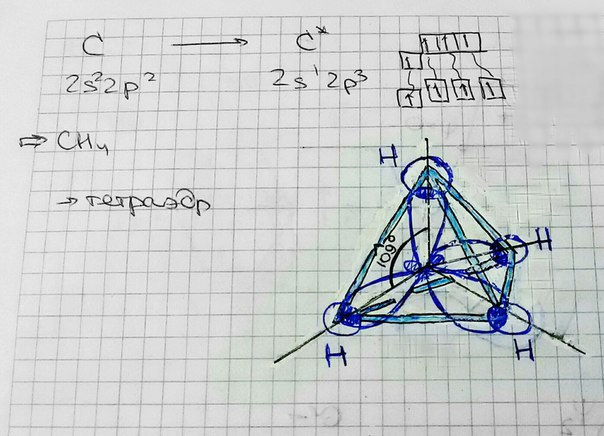 sp3-гибридизация тетраэдр #6. Метод молекулярных орбиталей (МО). Метод молекулярных орбиталей – это линейная комбинация атомных орбиталей. 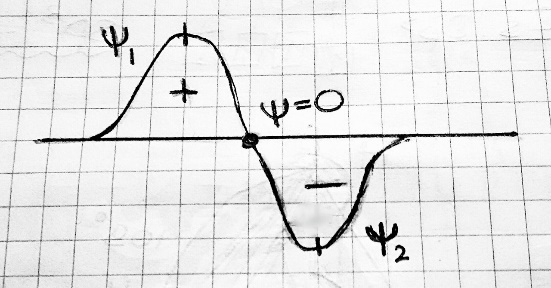 Ѱ=(Ѱ1+(Ѱ2+… H2 1s1 Ѱ=Ѱ1+Ѱ2 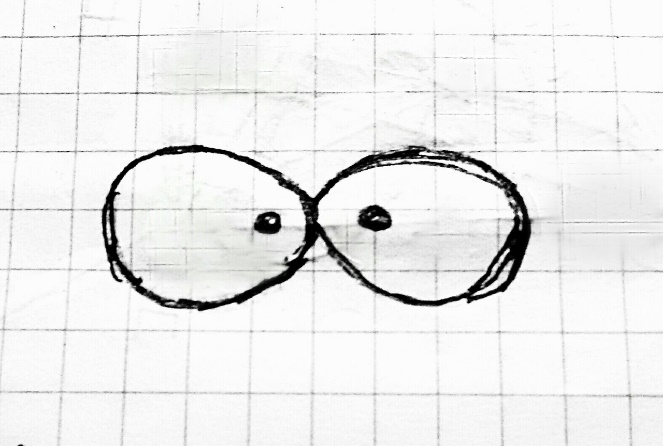 всплеск электронной плотности 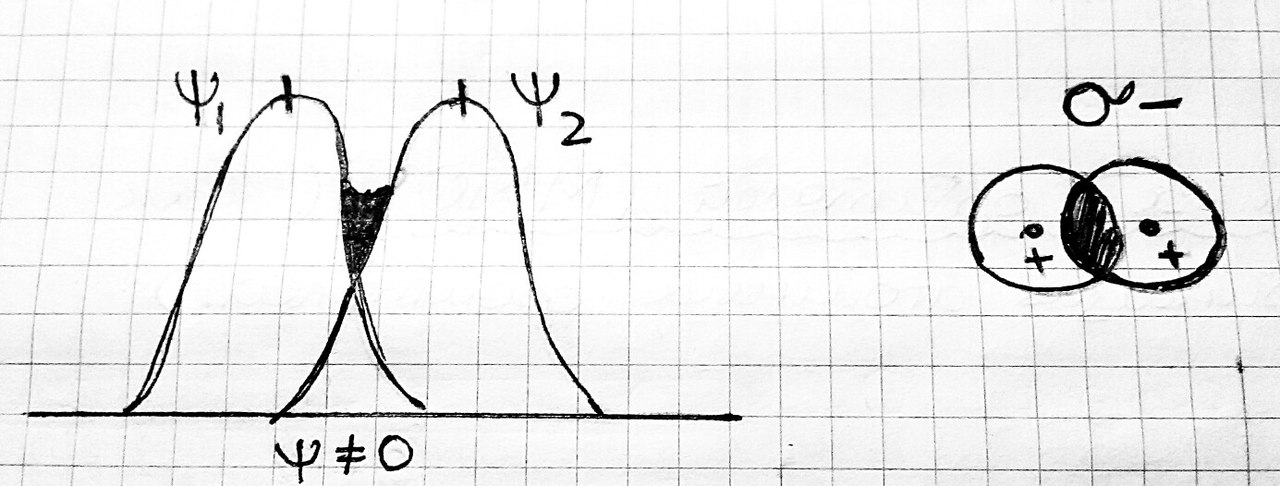 Типы молекулярных орбиталей:
Таким образом, He2 не существует, так как Eσсв=Eσ* . Порядок связи = (Nσсв - Nσ*)/(Nядер) Не2+ : 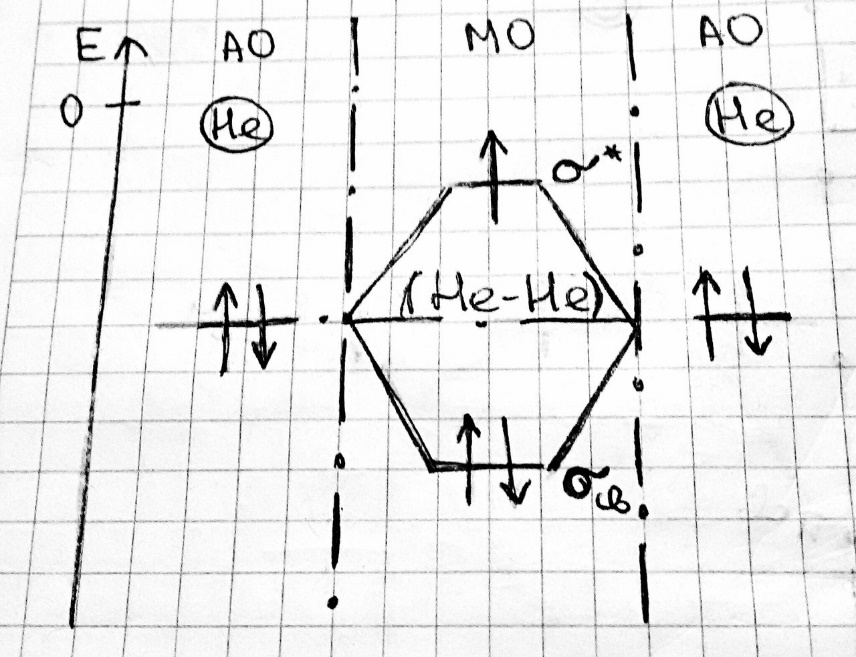 выполняется правило: Eσсв <Eσ* #7. Энергетические диаграммы гомо- и гетеро-атомных молекул. N2: 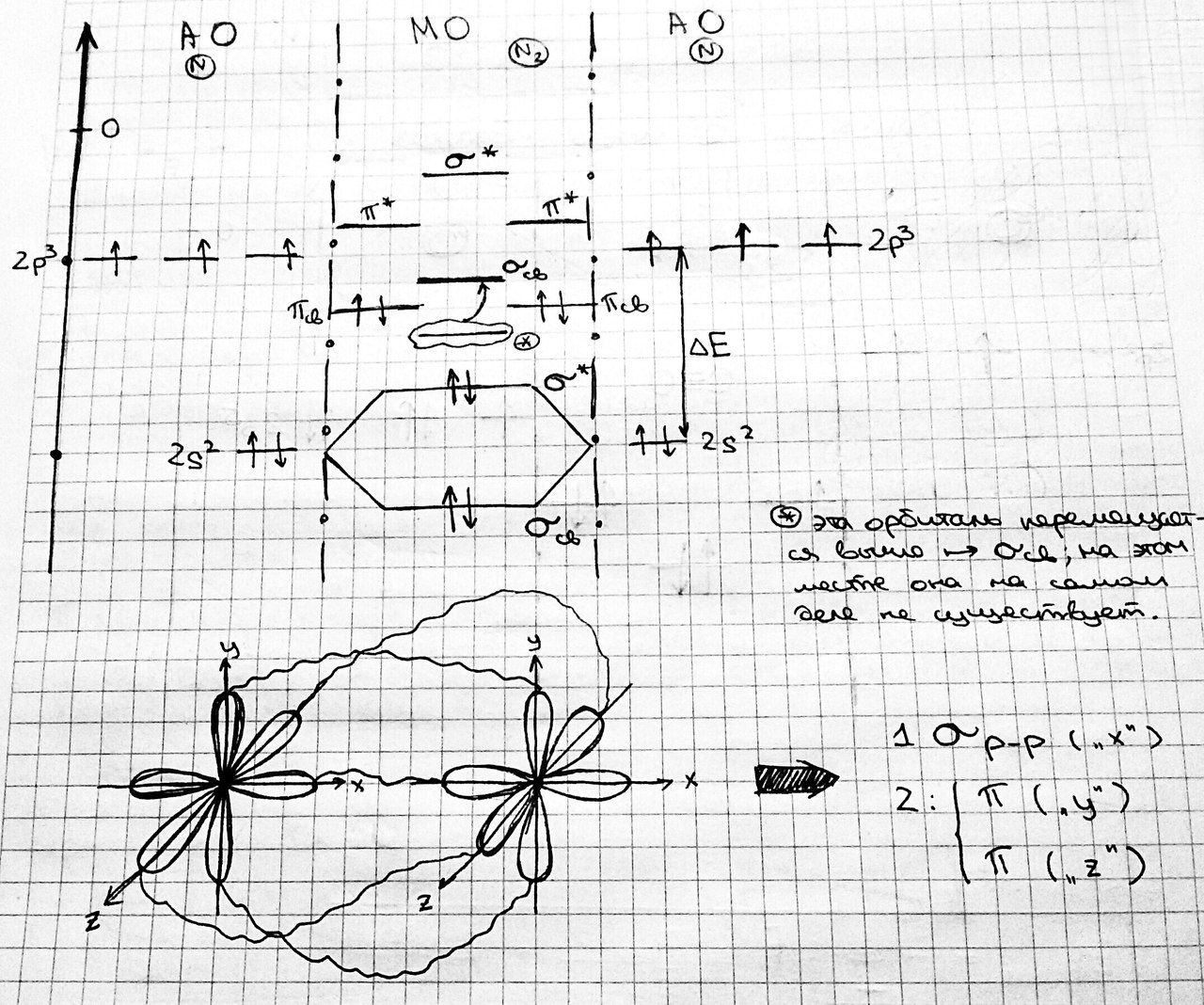 O2: CO: 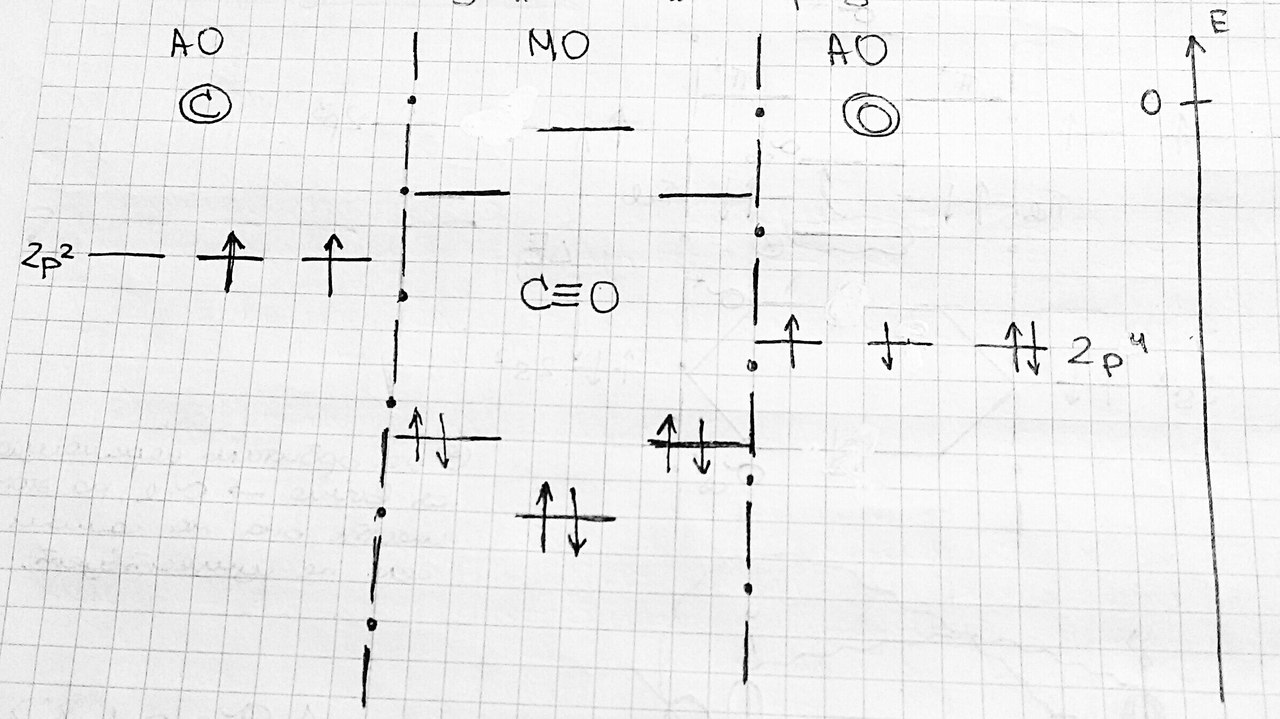 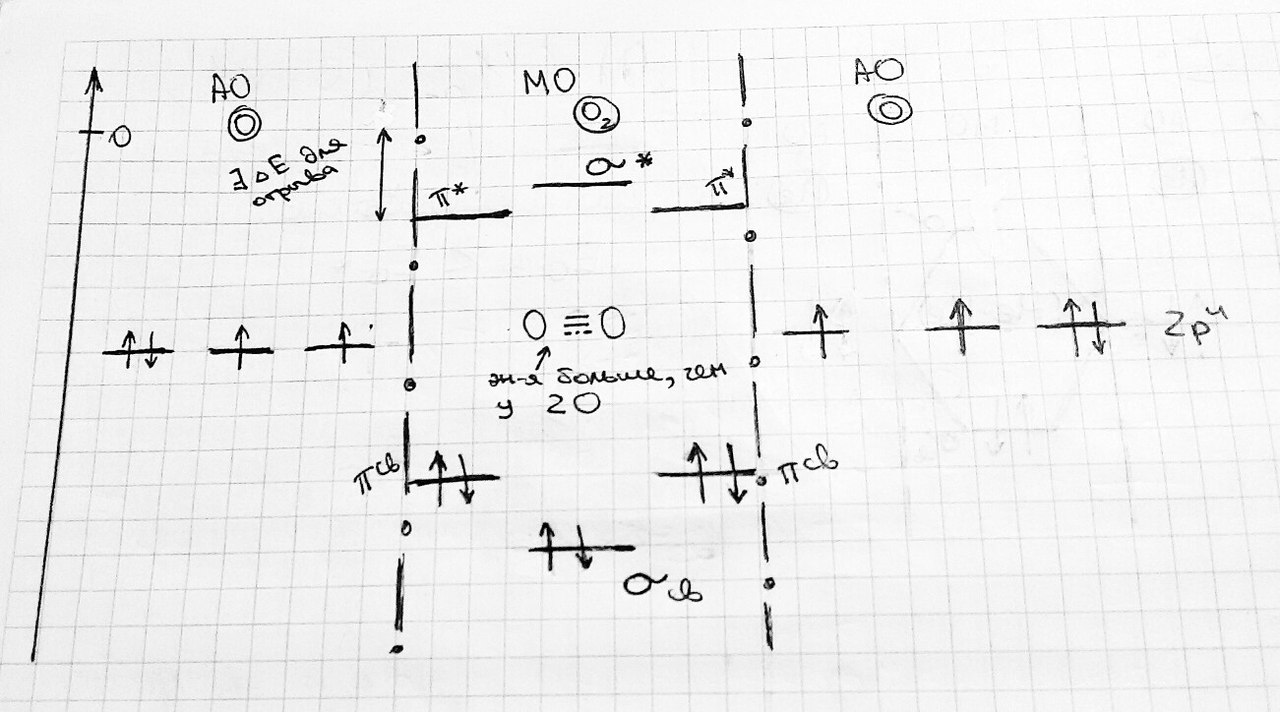 #8. Основные свойства ковалентной связи (дли-на, энергия, кратность, направленность, насы-щаемость). СВОЙСТВА КОВАЛЕНТНОЙ СВЯЗИ: Ковалентная связь образуется одной или несколькими парами электронов с разными спинами. В ходе образования ковалентной связи происходит перекрывание электронных облаков, в результате чего атом теряет энергию, называемую энергия связи. Ковалентная связь характеризуется:
I. Длина ковалентной связи. Длина связи – это межъядерное расстояние между химически связанными атомами. Она зависит от природы взаимодействующих атомов и от кратности связи. С увеличением кратности длина связи уменьшается, а, следовательно, увеличива-ется её прочность. II. Энергия ковалентной связи. Химическое соединение образуется из отдельных атомов только в том случае, если это энергетически выгодно. Если силы притяжения преобладают над силами отталкивания, потенциальная энергия взаимодействующих атомов понижается, и образуется химическая связь. На расстоянии, равном длине связи r0, эта энергия минимальна. 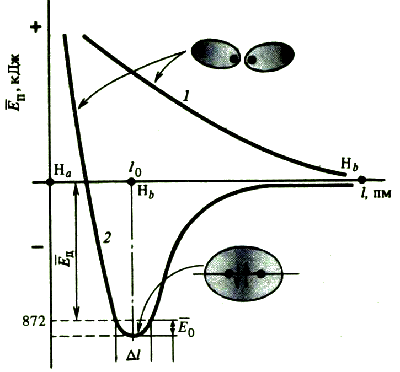 Таким образом, при образовании химической связи энергия выделяется, а при её разрыве поглощается. Энергия E0, необходимая для того, чтобы разъединить атомы и удалить их друг от друга на расстояние, на котором они не взаимодействуют, называется энергией связи. Она численно равна энергии, которая выделяется при образовании этой самой молекулы из атомов. Соответственно, для двухатомных молекул энергия связи определяется как энергия диссоциации молекулы на атомы. Она может быть измерена экспериментально. Для многоатомных молекул эта величина является условной и равна энергии такого процесса, при котором данная химическая связь исчезает, а все остальные остаются без изменения. Чем выше энергия химической связи, тем прочнее связь. Связь считается прочной или сильной, если её энергия превышает 500кДж/моль, а слабой, если её энергия меньше 100 кДж/моль. Если при взаимодействии атомов выделяется энергия менее 16 кДж/моль, то считают, что химическая связь не образуется, а наблюдается межмолекулярное взаимодействие. Прочность связи обычно уменьшается с увеличением её длины. Одинарная связь всегда слабее, чем кратные связи - двойная и тройная - между теми же атомами. III. Кратность ковалентной связи. Определяется количеством электронных связей – электронных пар – связывающих два атома (простая, донорно-акцепторная, семиполярная). С увеличением кратности энергия связи возрастает. IV. Направленность ковалентной связи в пространстве (угол связи). Направленность ковалентной связи означает, что связь образуется в направлении максимального перекрытия электронных облаков. Относительно линии соединяющей центры атомов образующих связь различают: σ-иπ-связи. σ-связь: образована перекрыванием АО по линии соединяющей центры взаимодействующих атомов, т.е. симметрична относительно линии, проходящей через атомные ядра в молекуле;  π-связь – это связь, возникающая в направлении оси перпендикулярной прямой, соединяющей ядра атома, т.е. симметрична относительно плоскости, в которой расположены ядра. 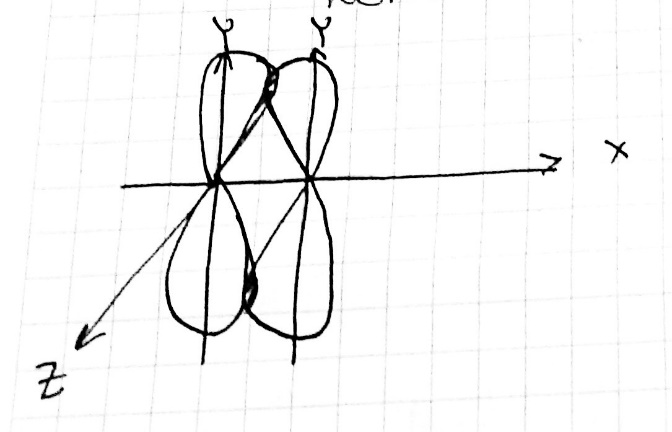 Направленность связи обусловливает пространственную структуру молекул, т. е. их геометрическую форму. Угол связи– угол между воображаемыми прямыми проходящими через ядра двух химически взаимосвязанных соседних атомов. Если в качестве признака химической связи выбрать степень перераспределения электронной плотности между атомами при образовании химической связи, то можно выделить неполярную, полярную и сильно полярную. Неполярная и полярная связи относятся к ковалентной химической связи, а сильно полярная химическая связь – ионная связь. 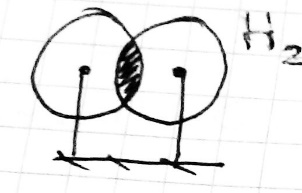 Неполярная ковалентная связь также называется гомеополярной, и она образована одинаковыми атомами. В такой ситуации электронная плотность расположена симметрично между атомами. Например, Н2. Полярная ковалентная связь также называется гетерополярной и образована разными атомами. В такой ситуации возникает смещение электронной плотности в сторону более электроотрицательного атома. В такой ситуации молекула превращается в диполь: диполь – это система, в которой имеется два электрических заряда, равных по величине, но противоположных по знаку, расположенных на некотором расстоянии друг от друга. Например, HCl. 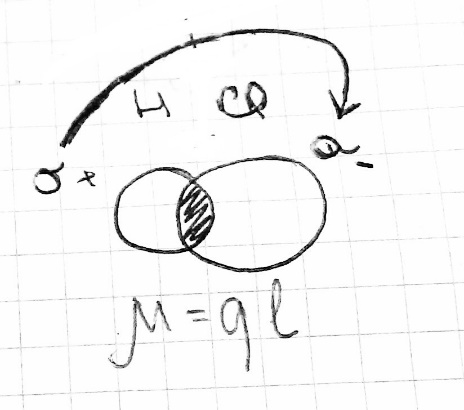 Произведение длины диполя l (расстояния между полюсами в молекуле) и величины заряда q называется дипольным моментом μ. μ= q l Чем больше длина диполя, т.е. её дипольный момент, тем больше полярность молекулы. Дипольный момент направлен от положительного конца диполя к отрицательному, поэтому дипольный момент многоатомной молекулы следует рассматривать как векторную сумму дипольных моментов связей: он зависит не только от полярности каждой связи, но и от взаимного расположения этих связей. V. Насыщаемость ковалентной химической связи — свойство атомов образовывать строго определенное число ковалентных связей. Благодаря насыщаемости связей молекулы имеют определенный состав. Насыщаемость ковалентной связи определяется механизмом образования ковалентной связи: либо обменный механизм, либо донорно-акцепторный.
Если ковалентная связь образована по обменному механизму, то насыщаемость определяется числом неспаренных электронов. 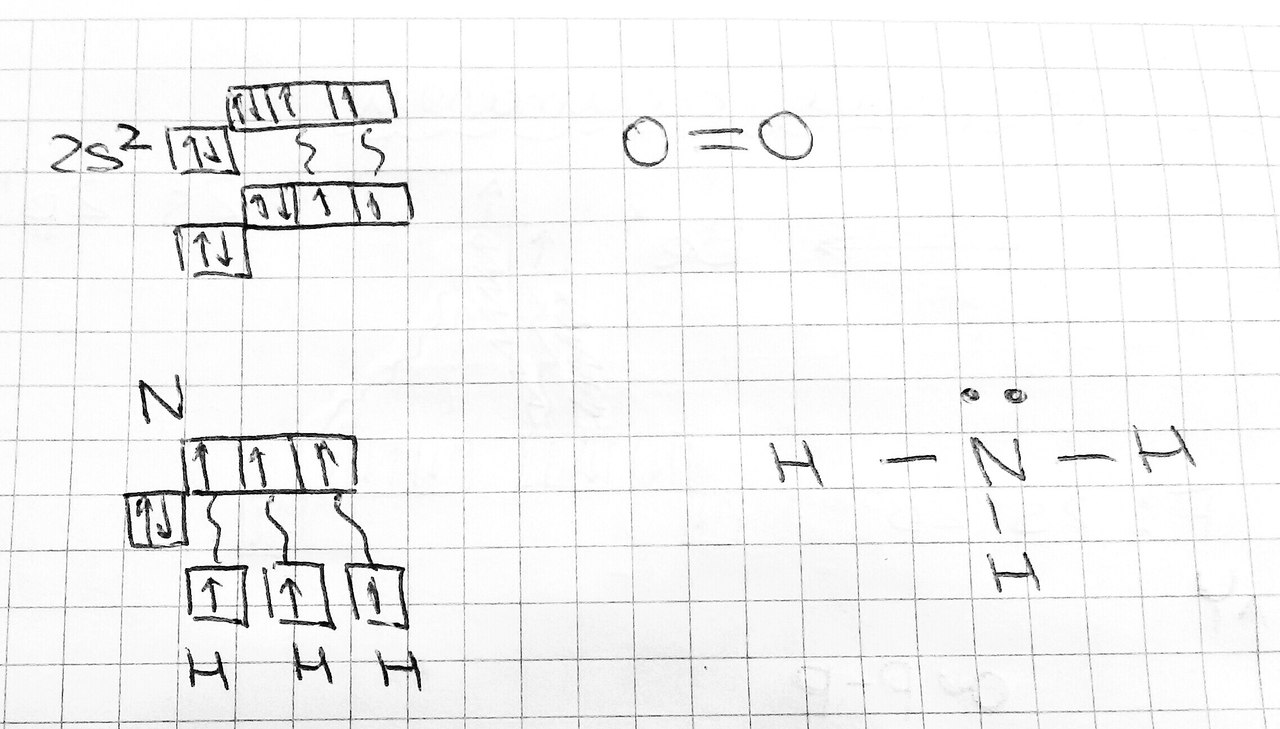 О2: NH3: Если энергии, выделяемой при образовании молекулы не хватит для того чтобы возбудить электроны, то реакция будет единичной и не пойдёт по всему объёму. 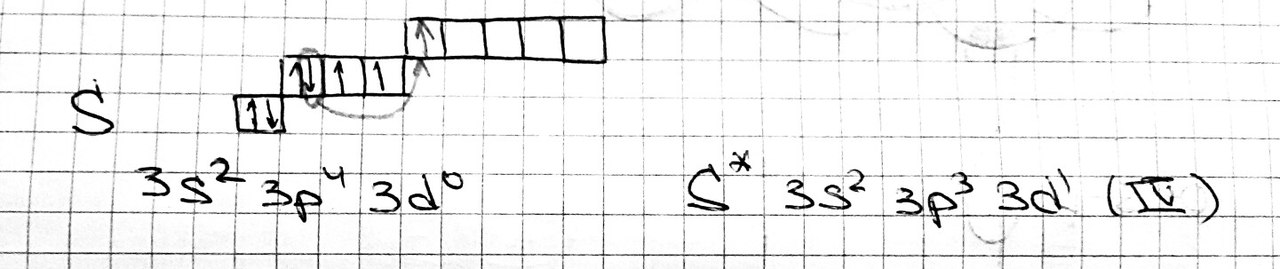
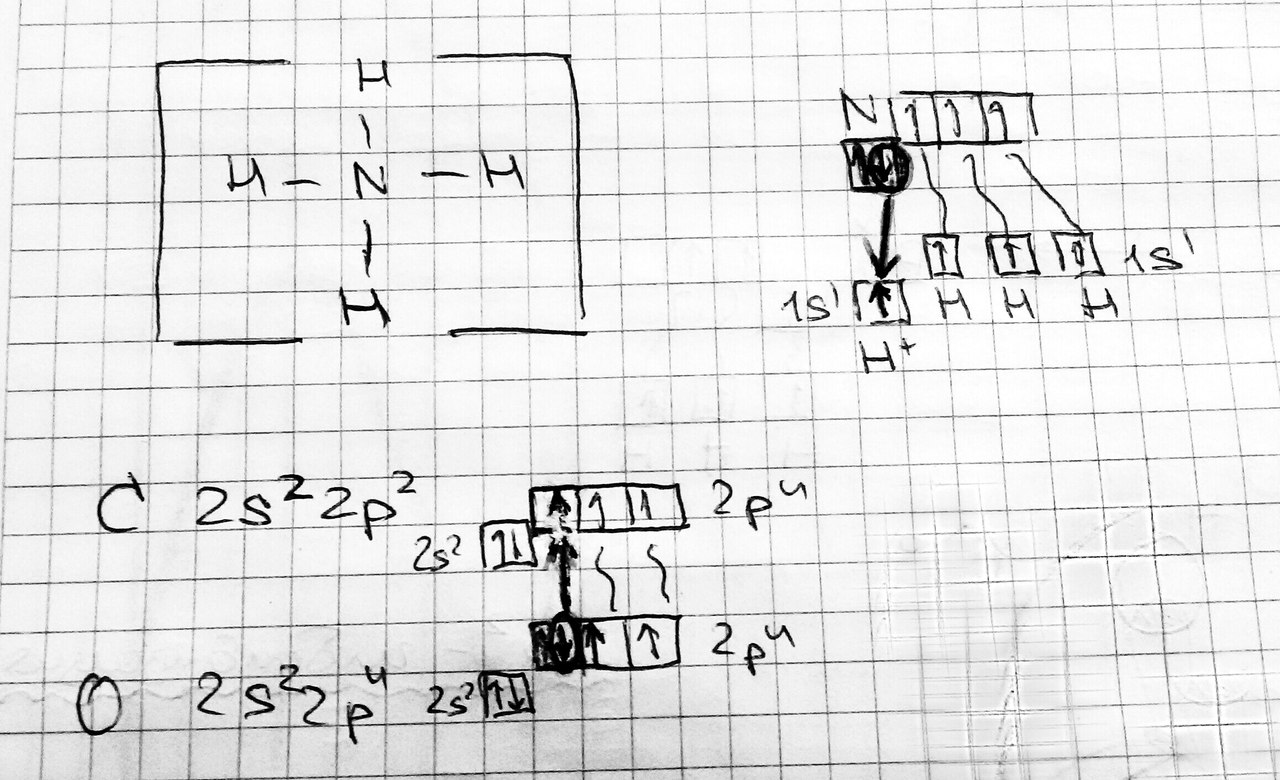 Если ковалентная связь образована по обменному механизму, то насыщаемость определяется числом вакантных орбиталей. #9. Ионная связь. Ионная связь – это сильно полярная химическая связь. Исторически она представлялась независимой от ковалентной и получила потому отдельное название. В основе ионной связи лежит электростатическое взаимодействие противоположно заряженных ионов. Согласно ионной связи, атомы элементов с числом электронов в наружном слое меньше восьми присоединяют или теряют такое число электронов, которое делает наружный электронный слой таким, как у атома ближайшего инертного газа (благородного газа). Атом, потерявший электроны, превращается в положительно заряженный ион - катион. Атом, присоединивший электроны, становится отрицательно заряженным ионом - анион. Разноименно заряженные ионы притягиваются друг к другу. Главное отличие ионной связи от ковалентной заключается в том, что ковалентная связь образуется в чистом виде между совершенно эквивалентными атомами, а ионная – между атомами, резко отличающимися по своим основным характеристикам, таким как энергия ионизации, сродство к электрону, размерам и другим. Ионных соединений немного. Их основные свойства заключаются в том, что в расплавленном состоянии они обладают электропроводностью, в воде легко диссоциируют на ионы, а также имеют высокую температуру плавления и кипения. Ионная связь характеризуется ненаправленностью (силовые поля ионов равномерно распределяются во всех направлениях в пространстве, поэтому они притягивают противоположный по знаку ион в любом направлении) и ненасыщаемостью (взаимодействие двух ионов не может привести к полной взаимной компенсации их силового поля, поэтому у них сохраняется способность притягивать ионы противоположного знака и по другим направлениям). Валентность элементов в ионных соединениях характеризуется числом отданных или присоединённых электроном и, таким образом, равна электровалентности. #10. Металлическая связь. Основы зонной теории.
Металлическая связьоснована на обобществлении валентных электронов, принадлежащих не двум, а практически всем атомам металла в кристалле. В металлах валентных электронов намного меньше, чем свободных орбиталей. Это создает условия для свободного перемещения электронов по орбиталям разных атомов металла. Таким образом, валентные электроны, осуществляющие химическую связь принадлежат не двум или нескольким атомам, а непрерывно и хаотично движутся от одного к другому, т.е. становятся общими для атомов всего кристалла металла. Связь является в высшей степени делокализованной. Образованную таким образом связь называют металлической связью, а совокупность делокализованных электронов – электронным газом. Граница между валентной зоной и зоной проводимости в металле на самом деле является размытой: вследствие теплового движения электроны могут переходить с верхних уровней валентной зоны на нижние уровни зоны проводимости. Способность этих электронов свободно передвигаться по кристаллу переносить энергию из одной его части в другую (из нагретой в холодную) служит причиной высокой теплопроводности металлов. Таким образом, электрическая проводимость и теплопроводность металлов обусловлены возможностью свободного передвижения электронов зоны проводимости. Именно поэтому для большинства металлов наблюдается параллелизм между этими величинами. Например, серебро и медь, которые являются лучшими проводниками электричества, так же обладают высокой теплопроводностью. Пластичность металлов объясняется тем, что при смещении слоёв кристаллической решётки в металле ввиду высокой степени делокализации электронов происходит лишь некоторое перераспределение электронной плотности, связывающей атомы в металле, но не происходит разрыва химических связей, поэтому металл деформируется, не разрушаясь. Непрозрачность объясняется тем, что ввиду близости большого количества занятых и свободных энергетических уровней всегда существует такая пара энергетических уровней, один из которых находится в валентной зоне, а другой в зоне проводимости, что разность их энергий E=hν. В таком случае электрон из валентной зоны, поглощая квант света, переходит в зону проводимости. Свет поглощается, а не отражается. В то же время металлам характерен блеск, который появляется в результате испускания света при возвращении возбуждённых светом электронов на более низкие энергетические уровни. Металлическая связь ненасыщена, так как она объединяет очень большое число атомов и при увеличении их количества делокализация электронов только лишь усиливается, а не исчезает. А также она ненаправлена. Это обусловлено сферической симметрией облаков s-электронов. Пример: перекрывание трёх и более сфер зависит только от расстояний между ними, а не направлений, по которым они сближаются. Именно по этой причине многие металлы не могут менять свою форму, не теряя прочности. Металлическая связь характерна для металлов, их сплавов и интерметаллических соединений. Металлической связи соответствует следующая картина электронного строения твёрдых металлов.
Пусть есть 2 изолированных атомов любого вещества. Схемы их энергетических уровней будут выглядеть следующим образом: одинаковая структура изолированных атомов 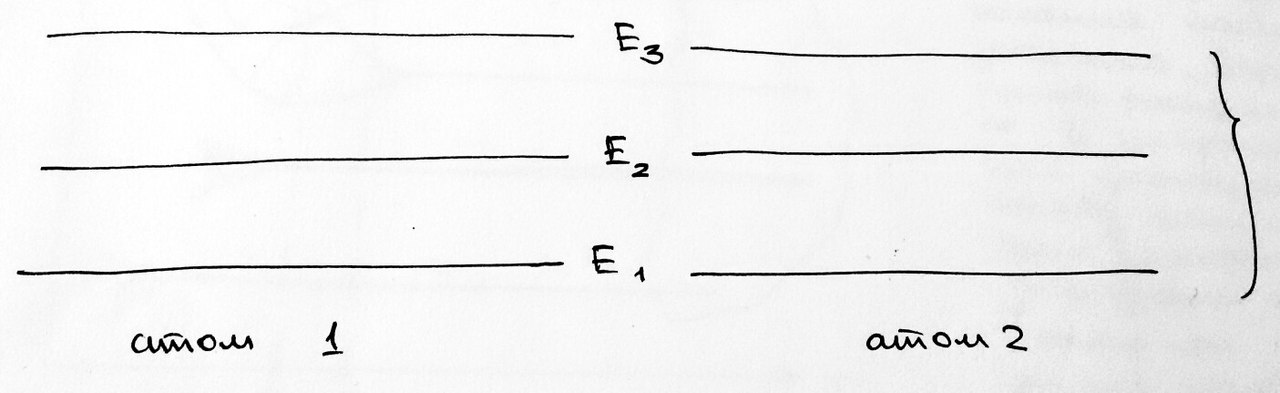 Пусть теперь два атома сближаются. При сближении двух атомов каждый из уровней энергии расщепляется на два: 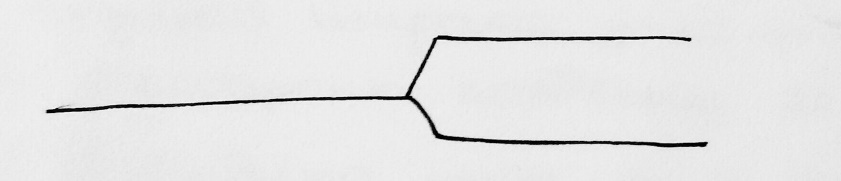 Если взаимодействуют три атома, то возникают три МО., принадлежащие всем атомам. При последовательном увеличении числа взаимодействующих атомов добавление каждого из них приводит к образованию ещё одного энергетического уровня и дальнейшей делокализации МО (к распространению их на большее число атомов). Общее число энергетических уровней будет равно числу взаимодействующих атомов. При сближении N атомов: 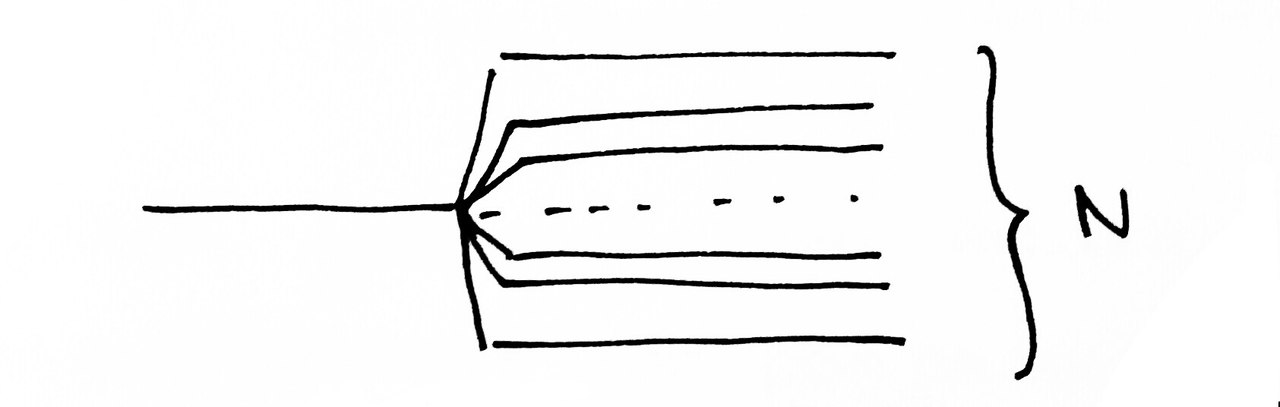 Т.е. при сближении атомов в кристалл вместо одного, одинакового для всех N атомов, уровня возникает N очень близких по энергии уровней. Тогда с ростом числа атомом возрастает и число разрешённых состояний. Таким образом, каждый уровень в изолированном атоме расщепляется в кристалле на N близко расположенных уровней, и при N порядка NA образует практически непрерывную энергетическую зону. 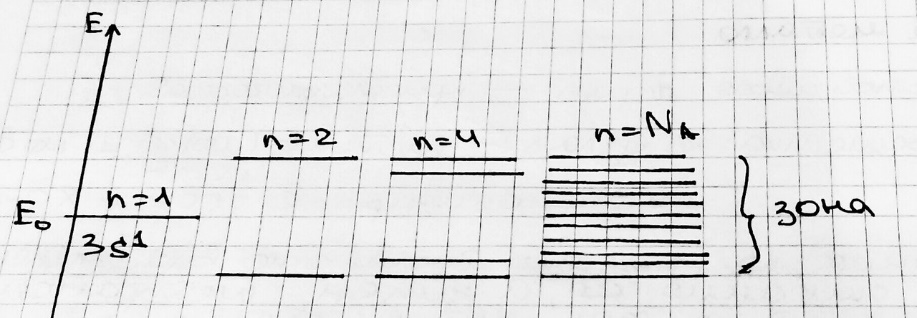 Тогда переход электрона на ближайший более высокий уровень энергии происходит при затрате ничтожно малой энергии. Если такой ближайший уровень не занят электронами, то находящийся на предшествующем уровне электрон ведёт себя как «свободный», т.е. вследствие делокализованности орбиталей он может свободно перемещаться по кристаллу. Заполнение МО происходит в соответствие с принципом запрета Паули: на каждой МО может размещаться по два электрона. В кристалле щелочного элемента, содержащего N атомов, из исходных s-АО внешней электронной оболочки образуется энергетическая зона, содержащая N орбиталей. В такой зоне размещается N электронов на N/2 энергетических уровней. Совокупность этих занятых зон называется валентной зоной. Остальные незаполненные уровни образуют зону проводимости. Здесь имеются свободные уровни, на которые могут переходить электроны под действием электрического поля, что создаёт возможность переноса тока электронами – обеспечивает электрическую проводимость металла. В кристалле элемента главной подгруппы второй группы (кальций) образуется зона, состоящая из N уровней. Но так как каждый атом имеет два внешних s-электрона, то они заполнят 2N орбиталей. Но при взаимодействии перекрываются не только s-, но и p-орбитали. Таким образом, всё равно образуется внешняя энергетическая зона, незаполненная электронами. Так что и в этом случае зона проводимости примыкает к валентной зоне. Таким образом, при сложном взаимодействии всех N атомов кристаллической решётки, число которых очень велико, вместо отдельных уровней энергии, разделённых промежутками для электрона в изолированном атоме, при переходе к кристаллам возникают разрешённые и запрещённые зоны энергии. При этом величина расщепления разная для нижних уровней, занятых электронами, и верхних, занятых внешними – валентными электронами. Зависимость расщепления от расстояния между атомами: 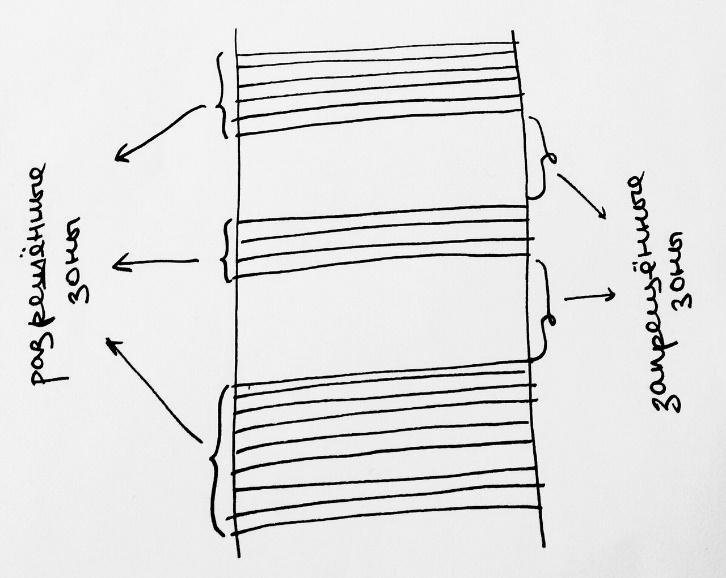 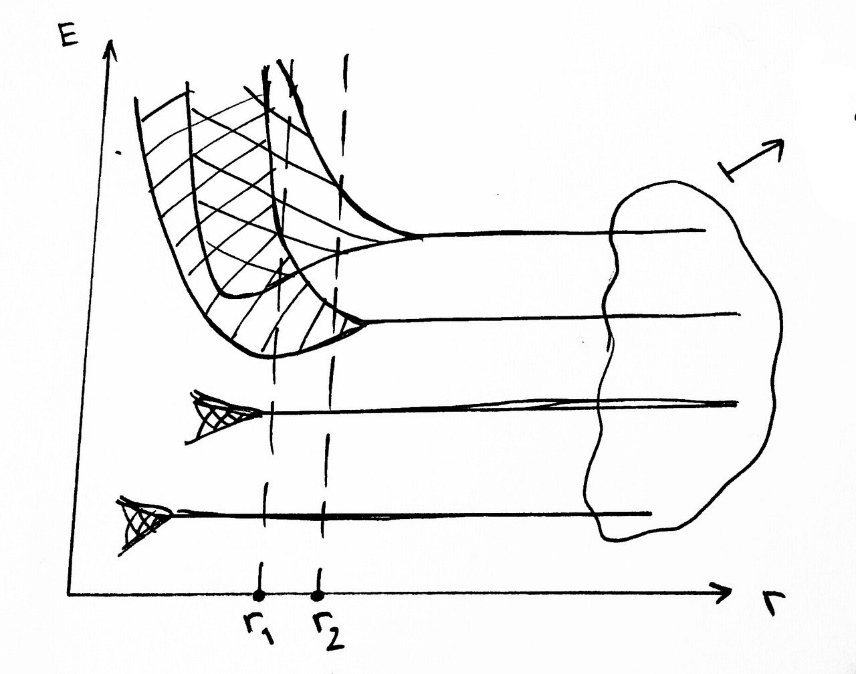 когда расстояние велико По мере уменьшения расстояния, начиная с некоторого значения, верхние уровни начинают расщепляться и превращаться в широкие зоны. При дальнейшем уменьшении расстояния между атомами зоны могут даже перекрываться, при этом нижние уровни это не затрагивает. Только при очень малых расстояниях между центрами атомов нижние уровни тоже начинают расщепляться. #11. Межмолекулярные взаимодействия. Межмолекулярные взаимодействия удерживают частицы (молекулы) жидкости или твёрдого тела около друг друга. Поэтому вещества в конденсированном состоянии, в отличие от газов, имеют постоянный при данной температуре объём. Межмолекулярные взаимодействия обусловлены электромагнитными полями атомных ядер и электронов молекул. Характер взаимодействия молекул может быть самым разным (притяжение или отталкивание, или и то, и то), но с уменьшением радиуса взаимодействия, они в конечном итоге всё равно начинают отталкиваться. Характер взаимодействия при сближении также зависит от состояния молекул – находятся они в основном или же в возбужденном состоянии.  жирная кривая: притяжение, а затем отталкивание обычная кривая: отталкивание, потом притяжение, потом снова отталкивание штриховая кривая: всё время отталкивание От обычных химических связей межмолекулярные взаимодействия отличаются меньшей энергией и большим расстоянием проявления. Силы ММВ по природе идентичны силам взаимодействия между атомами различной электроотрицательности, но меньше по величине. #12. Силы Ван-дер-Ваальса. Все межмолекулярные взаимодействия делятся на специфические и универсальные – проявляющиеся во всех молекулах – силы Ван-дер-Ваальса. Они слабее сил химической связи и являются первой причиной фазового перехода «газ-жидкость»; устойчивости молекулярных кристаллов и других явлений. Четыре составляющие:
Ориентационная составляющая связана с полярностью молекул: молекула, обладающая дипольным моментом, притягивает другую молекулу за счёт электростатических сил диполь-дипольного взаимодействия. Молекулы при этом: 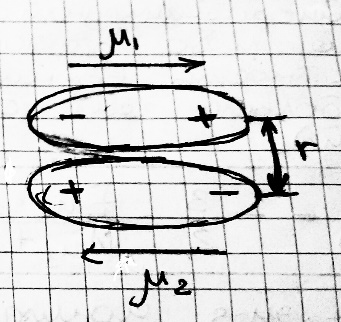 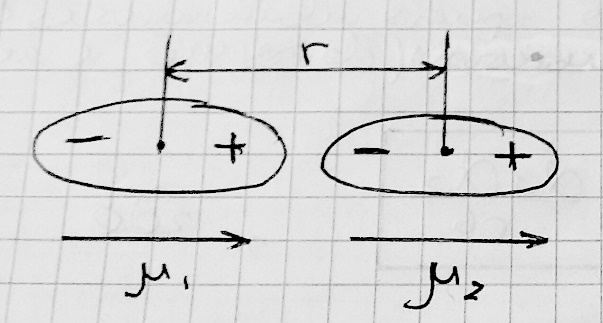 последовательно антипараллельно Такой ориентации препятствует тепловое движение (усиливается с увеличением температуры). Ориентационное взаимодействие ∽ μ (дипольный момент); 1/r ; 1/T. Eop = -2/3 μ12 μ22 1/kTr6 - формула Кеезома Сказывается на свойствах вещества: вещество кипит, когда Eк движения молекул > Eop . Индукционная составляющая возникает при взаимодействии полярой и неполярной молекул (Пример: HCl и Cl2). Следовательно, полярная молекула поляризует неполярную – появляется наведённый дипольный момент – диполь-дипольное притяжение. Еинд тем больше, чем больше дипольный момент полярной молекулы и поляризуемость неполярной. Поляризуемость (α) – мера смещения зарядов в молекуле в электрическом поле. Резко возрастает при увеличении электронной оболочки.  формула Дебая Ориентационные и индукционные силы зависят от присутствия других молекул, т.е. они неаддитивные. Дисперсионная составляющая притяжения молекул: универсальна, есть всегда. Эти силы сравнимы с силами полярного межмолекулярного взаимодействия. Причина возникновения: при движении электронов в молекуле мгновенно возникает асимметрия распределения положительных и отрицательных зарядов. В результате каждую молекулу можно рассматривать как место возникновения мгновенно существующих диполей разной направленности (tсущ∽10-8с). Попеременно возникающие диполи разных молекул в результате движения электронов ориентируются так, что возникает либо притяжение, либо отталкивание молекул, но, так как электроны очень подвижны, то вероятность возникновения притягивающихся диполей больше, чем отталкивающихся (связано с корреляцией). Eдисп = (-3/2)*(Eи1Eи2)/(Eи1 + Eи1)*( α1 α2 )/r6 Eи где Eи – энергия ионизации С характером изменения дисперсионных сил связано: Eпритяжения = - A/r6 (1) , 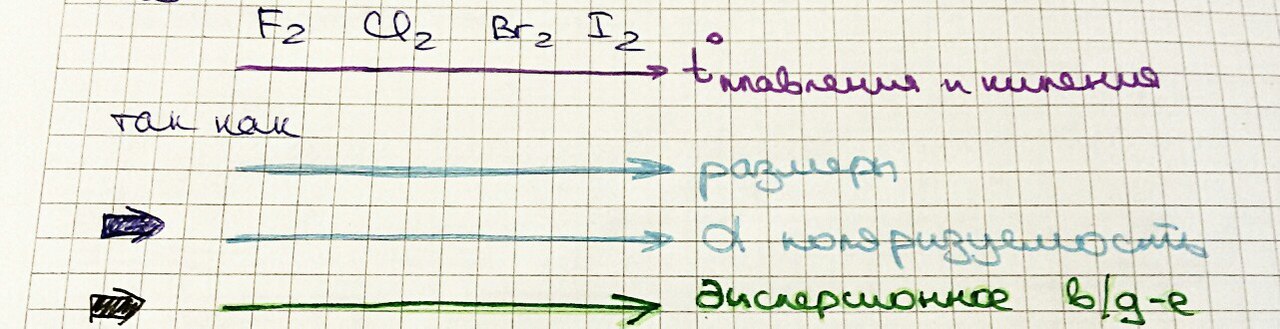 где A – обобщение всех составляющих взаимодействия для конкретного атома или молекулы Энергия отталкивания электронных оболочек молекул описывается формулой: Eотталкивания = B/rn (2) , где B=const, n = {9; 12; 15} Формула обобщающая (1) и (2) эмпирические уравнения: потенциал Леннард-Джонсона: ЕММВ = - A/r6 + B/rn ЕММВ ⩽ 16 кДж/моль ЕММВ >16 кДж/моль: молекулы с длинными цепями атомов (пример: полимерные углероды) #13. Водородная связь. Водородная связь — форма взаимодействия между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицатель-ным атомом. В качестве электроотрицательных атомов могут выступать N, O или F. Водородные связи могут быть межмолекулярными или внутримолекулярными. Часто водородную связь рассматривают как электростатическое взаимодействие, усиленное небольшим размером водорода, которое разрешает близость взаимодействующих диполей. Особенностями водородной связи, по которым её выделяют в отдельный вид, является её не очень высокая прочность, её распространенность и некоторые побочные эффекты, связанные с малыми размерами и отсутствием дополнительных электронов у водорода. В настоящее время в рамках теории молекулярных орбиталей водородная связь рассматривается как частный случай ковалентной с делокализация электронной плотности по цепи атомов. Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль). Однако этой энергии достаточно, чтобы вызвать объединение атомов в, например, полимеры. Именно образование молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак. 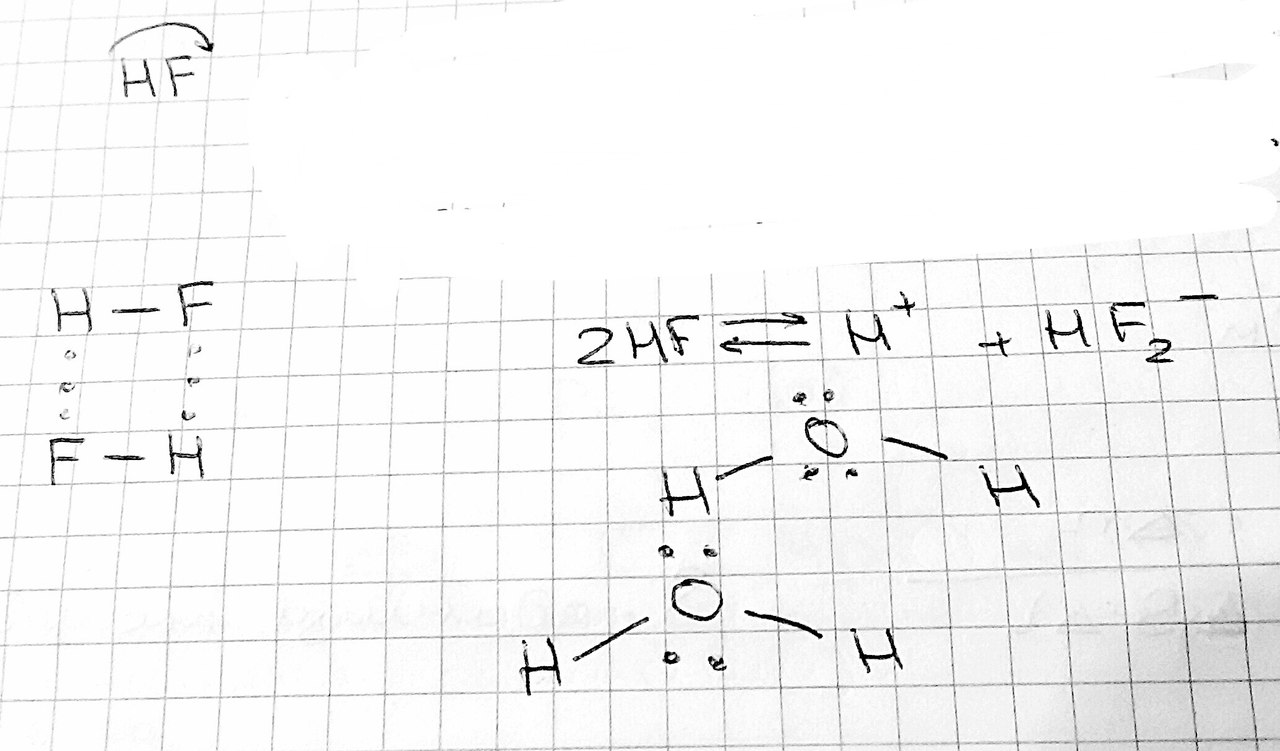 Водород точечно мал. Тогда электрон сильно оттянут в сторону F, следовательно, можно подобраться близко к F, который лишён электрона на внешнем уровне. Образуются водородные связи. |