Гидролиз отчет. Гидролиз отчет — копия. Исследование гидролиза солей
 Скачать 264.96 Kb. Скачать 264.96 Kb.
|
Цель работы – ознакомиться с процессом гидролиза солей и его следствиями, научиться составлять уравнения гидролиза Общие теоретические сведения. Гидролиз– процесс химического взаимодействия солей с водой. Продуктами гидролиза являются малодиссоциированные соединения в растворе, иногда – осадки или газы. Соответственно соли, образованные сильной кислотой и сильным основанием не гидролизуются (хлориды, нитраты, сульфаты щелочных металлов, стронция, бария). Различаюят три типа гидролизующихся солей: Соли, образованные сильной кислотой и слабым основанием, гидролизуются по катиону. В процессе реакции происходит выделение H+; реакция среды – кислая. Продуктами реакции могут являться слабое основание или растворимый гидроксокомплекс(pH<7). Соли, образованные слабой кислотой и сильным основанием, гидролизуются по аниону с образованием слабой кислоты или иона кислой соли. В растворах солей этой группы накапливаются ионы гидроксила OH-, в результате чего реакция среды щелочная (pH>7). Соли, образованные слабой кислотой и слабым основанием, гидролизуются по обоим составляющим их ионам с образованием сразу двух слабых электролитов. Среда в растворах таких солей зависит от относительной силы образующихся в результате гидролиза кислоты и основания, но в целом близка к нейтральной. Степень гидролиза многократно выше, чем у солей первых двух групп, гидролизующихся только по одному иону. Если продуктами реакции являются труднорастворимые соединения или газы, то гидролиз протекает полностью. Доля вещества, подвергающаяся гидролизу – степень гидролиза. Константа гидролиза – величина, характеризующая способность вещества подвергаться гидролизу. Порядок выполнения лабораторной работы Опыт 1:
Гидролиз сульфата цинка 𝑍𝑛2+ + 𝐻2𝑂 → 𝑍𝑛𝑂𝐻+ + 𝐻+(сокращённое ионное уравнение реакции гидролиза сульфата цинка) 𝑍𝑛𝑆𝑂4 + 𝐻2𝑂 → (𝑍𝑛𝑂𝐻)2𝑆𝑂4 + 𝐻2𝑆𝑂4 (молекулярное уравнение реакции гидролизасульфата цинка) 𝑍𝑛𝑂𝐻+ + 𝐻2𝑂 → 𝑍𝑛(𝑂𝐻)2 ↓ +2𝐻+ (сокращённое ионное уравнение реакции гидролиза сульфата цинка) (𝑍𝑛𝑂𝐻)2𝑆𝑂4 + 2𝐻2𝑂 → 2𝑍𝑛(𝑂𝐻)2 ↓ +𝐻2𝑆𝑂4 (молекулярное уравнение реакции гидролиза сульфата цинка) Гидролиз сульфата алюминия в воде) 2𝐴𝑙3+ + 3𝑆𝑂42− + 3𝐻2𝑂 → 𝐴𝑙(𝑂𝐻)3 ↓ +𝐴𝑙3+ + 3𝐻𝑆𝑂4− (полное ионное уравнение реакции гидролиза сульфата алюминия) 𝐴𝑙3+ + 3𝑂𝐻− → 𝐴𝑙(𝑂𝐻)3 ↓ (сокращённое ионное уравнение реакции гидролиза сульфата алюминия) 𝐴𝑙2(𝑆𝑂4)3 + 3𝐻2𝑂 → 𝐴𝑙(𝑂𝐻)3 ↓ +𝐴𝑙(𝐻𝑆𝑂4)3 (молекулярное уравнение реакции гидролиза сульфата алюминия) 𝐴𝑙3+ + 3𝐻2𝑂 → 𝐴𝑙(𝑂𝐻)3 + 3𝐻+ (сокращённое ионное уравнение реакции гидролиза сульфата алюминия) 𝐴𝑙(𝐻𝑆𝑂4)3 + 3𝐻2𝑂 → 𝐴𝑙(𝑂𝐻)3 ↓ +3𝐻2𝑆𝑂4 (молекулярное уравнение реакции гидролиза сульфата алюминия) Гидролиз карбоната натрия гидролиза карбоната натрия) 𝑁𝑎2𝐶𝑂3 + 𝐻2𝑂 → 𝑁𝑎𝑂𝐻 + 𝑁𝑎𝐻𝐶𝑂3 (молекулярное уравнение реакции гидролиза карбоната натрия) 𝐻𝐶𝑂32− + 𝐻2𝑂 → 𝐻2𝐶𝑂3 + 𝑂𝐻− (сокращённое ионное уравнение реакции гидролиза карбоната натрия) 𝑁𝑎𝐻𝐶𝑂3 + 𝐻2𝑂 → 𝑁𝑎𝑂𝐻 + 𝐻2𝐶𝑂3 (молекулярное уравнение реакции гидролиза карбоната натрия) Гидролиз сульфида натрия 2𝑁𝑎+ + 𝑆2− + 𝐻2𝑂 → 2𝑁𝑎+ + 𝑂𝐻− + 𝐻𝑆− (полное ионное уравнение реакции гидролиза сульфида натрия) 𝑆2− + 𝐻2𝑂 → 𝑂𝐻− + 𝐻𝑆− (сокращённое ионное уравнение реакции гидролиза сульфида натрия) 𝑁𝑎2𝑆 + 𝐻2𝑂 → 𝑁𝑎𝐻𝑆 + 𝑁𝑎𝑂𝐻 (молекулярное уравнение реакции гидролиза сульфида натрия) 𝑁𝑎+ + 𝐻𝑆− + 𝐻2𝑂 → 𝑁𝑎+ + 𝑂𝐻− + 𝐻2𝑆 (полное ионное уравнение реакции гидролиза гидросульфида натрия) 𝐻𝑆− + 𝐻2𝑂 → 𝑂𝐻− + 𝐻2𝑆 (сокращённое ионное уравнение реакции гидролиза гидросульфида натрия) 𝑁𝑎𝐻𝑆 + 𝐻2𝑂 → 𝑁𝑎𝑂𝐻 + 𝐻2𝑆 (молекулярное уравнение реакции гидролиза гидросульфида натрия) Гидролиз ацетата свинца в воде) 2𝐶𝐻3𝐶𝑂𝑂− + 𝑃𝑏2+ + 𝐻2𝑂 → 𝑃𝑏𝑂𝐻+ + 𝐶𝐻3𝐶𝑂𝑂− + 𝐶𝐻3𝐶𝑂𝑂𝐻 (полное ионное уравнение реакции гидролиза ацетата свинца) 𝐶𝐻3𝐶𝑂𝑂− + 𝑃𝑏2+ + 𝐻2𝑂 → 𝑃𝑏𝑂𝐻𝐶𝐻3𝐶𝑂𝑂 + 𝐶𝐻3𝐶𝑂𝑂𝐻 (сокращённое ионное уравнение реакции гидролиза ацетата свинца) (𝐶𝐻3𝐶𝑂𝑂)2𝑃𝑏 + 𝐻2𝑂 → 𝐶𝐻3𝐶𝑂𝑂𝐻 + 𝑃𝑏𝑂𝐻𝐶𝐻3𝐶𝑂𝑂 (молекулярное уравнение реакции гидролиза ацетата свинца) 𝑃𝑏𝑂𝐻+ + 𝐶𝐻3𝐶𝑂𝑂− + 𝐻2𝑂 → 𝑃𝑏(𝑂𝐻)2 ↓ +𝐶𝐻3𝐶𝑂𝑂𝐻 (сокращённое ионное уравнение реакции гидролиза ацетата свинца) 𝑃𝑏𝑂𝐻𝐶𝐻3𝐶𝑂𝑂 + 𝐻2𝑂 → 𝑃𝑏(𝑂𝐻)2 ↓ +𝐶𝐻3𝐶𝑂𝑂𝐻 (молекулярное уравнение реакции гидролиза ацетата свинца) Опыт 2(Б): Несколько капель 𝑁𝑎2𝑆𝑂3 поместили на кусочек индикаторной бумаги. Из того, что она окрасилась в зелёный цвет, можно сделать вывод, что её pH=8, то есть раствор 𝑁𝑎2𝑆𝑂3 является щелочной средой. Гидролиз сульфита натрия гидролизасульфита натрия) 𝑁𝑎2𝑆𝑂3 → 2𝑁𝑎+ + 𝑆𝑂32− (диссоциация сульфита натрия в воде) 2𝑁𝑎+ + 𝑆𝑂32− + 𝐻2𝑂 → 𝐻𝑆𝑂3− + 2𝑁𝑎+ + 𝑂𝐻− (полное ионное уравнение реакции гидролиза сульфита натрия) 𝑆𝑂32− + 𝐻2𝑂 → 𝐻𝑆𝑂3− + 𝑂𝐻−(сокращённое ионное уравнение реакции гидролиза сульфита натрия) 𝐻𝑆𝑂3− + 𝐻2𝑂 → 𝐻2𝑆𝑂3 + 𝑂𝐻−(сокращённое ионное уравнение реакции гидролиза сульфита натрия) 𝑁𝑎𝐻𝑆𝑂3 + 𝐻2𝑂 → 𝑁𝑎𝑂𝐻 + 𝐻2𝑆𝑂3(молекулярное уравнение реакции гидролиза сульфита натрия) Ответы на вопросы: На присутствие каких ионов в растворе указывает найденное значение pH раствора сульфита натрия? Найденное значение pH больше 7, что указывает на то, что средараствора – щелочная. В щелочной среде преобладают ионыкислотного остатка, то есть отрицательные ионы или анионы. В результате какого процесса эти ионы появились? Эти ионы появились в результате процесса электролитическойдиссоциации. Какая соль является продуктом гидролиза сульфита натрия по первой ступени? Кислая соль гидросульфит натрия. При гидролизе каких солей получаются кислые соли? При гидролизе солей слабых многоосновных кислот. Опыт 3(А):
Гидролиз сульфита натрия гидролиза сульфита натрия) сульфита натрия) 𝐻𝑆𝑂3− + 𝐻2𝑂 → 𝐻2𝑆𝑂3 + 𝑂𝐻−(сокращённое ионное уравнение реакции гидролиза сульфита натрия) 𝑁𝑎𝐻𝑆𝑂3 + 𝐻2𝑂 → 𝑁𝑎𝑂𝐻 + 𝐻2𝑆𝑂3(молекулярное уравнение реакции гидролиза сульфита натрия) Гидролиз ацетата натрия 𝐶𝐻3𝐶𝑂𝑂𝑁𝑎 → 𝐶𝐻3𝐶𝑂𝑂− + 𝑁𝑎+ (диссоциация ацетата натрияв воде) 𝐶𝐻3𝐶𝑂𝑂− + 𝑁𝑎+ + 𝐻2𝑂 → 𝐶𝐻3𝐶𝑂𝑂𝐻 + 𝑁𝑎+ + 𝑂𝐻− (полное ионное уравнение реакции гидролиза ацетата натрия) 𝐶𝐻3𝐶𝑂𝑂− + 𝐻2𝑂 → 𝐶𝐻3𝐶𝑂𝑂𝐻 + 𝑂𝐻−(сокращённое ионное уравнение реакции гидролиза ацетата натрия) 𝐶𝐻3𝐶𝑂𝑂𝑁𝑎 + 𝐻2𝑂 → 𝐶𝐻3𝐶𝑂𝑂𝐻 + 𝑁𝑎𝑂𝐻 (молекулярное уравнение реакции гидролиза ацетата натрия) Гидролиз карбоната натрия реакции гидролиза карбоната натрия) 𝐶𝑂32− + 𝐻2𝑂 → 𝐻𝐶𝑂3− + 𝑂𝐻− (сокращённое ионное уравнение реакции гидролиза карбоната натрия) 𝑁𝑎2𝐶𝑂3 + 𝐻2𝑂 → 𝑁𝑎𝑂𝐻 + 𝑁𝑎𝐻𝐶𝑂3 (молекулярное уравнение реакции гидролиза карбоната натрия) 𝐻𝐶𝑂32− + 𝐻2𝑂 → 𝐻2𝐶𝑂3 + 𝑂𝐻− (сокращённое ионное уравнение реакции гидролиза карбоната натрия) 𝑁𝑎𝐻𝐶𝑂3 + 𝐻2𝑂 → 𝑁𝑎𝑂𝐻 + 𝐻2𝐶𝑂3 (молекулярное уравнение реакции гидролиза карбоната натрия) Ответы на вопросы: В каком растворе в гидролизе по аниону концентрация ионов 𝑂𝐻− более высокая? pH определяет кислотность среды раствора. Чем больше pH, темсреда более щелочная, то есть в ней начинают преобладатьотрицательные ионы, то есть анионы. Значит, анионы будут болеепреобладать в том растворе, кислотность среды которого больше.Карбонат натрия. Степень гидролиза какой соли больше? Карбонат натрия, так как кислота, образующая эту соль болеерастворима, чем уксусная и сернистая. Степень гидролиза какой соли при одинаковых концентрации и температуре должна быть больше: 𝐴𝑙𝐶𝑙3 или 𝑀𝑔𝐶𝑙2? У хлорида алюминия, так как его основание более слабое, чем ухлорида магния. В какой соли концентрация ионов 𝐻+ выше? В растворе ацетата натрия, так как он имеет более кислую среду. Сделать общий вывод о влиянии силы кислоты и основания, образующих соль, на степень её гидролиза. Чем сильнее кислота или основание, тем больше константа еёдиссоциации, тем меньше константа гидролиза соли, её образующей. Опыт 3(В): К раствору 𝑺𝒃𝑪𝒍𝟑 добавили несколько капель воды, после чего на дне пробирки с раствором образовался осадок 𝑺𝒃𝑶𝑪𝒍. При дальнейшем добавлении хлороводорода к раствору осадок растворился. Гидролиз хлорида сурьмы 𝑆𝑏3+ + 3𝐶𝑙− + 𝐻2𝑂 → 𝑆𝑏𝑂𝐻𝐶𝑙2 + 𝐻+ + 𝐶𝑙− (полное ионное уравнение реакции гидролиза хлорида сурьмы) 𝑆𝑏3+ + 𝐻2𝑂 → 𝑆𝑏𝑂𝐻2+ + 𝐻+ (сокращённое ионное уравнение реакции гидролиза хлорида сурьмы) 𝑆𝑏𝐶𝑙3 + 𝐻2𝑂 → 𝑆𝑏𝑂𝐻𝐶𝑙2 + 𝐻𝐶𝑙 (молекулярное уравнение реакции гидролиза хлорида сурьмы) 𝑆𝑏𝑂𝐻2+ + 2𝐶𝑙− + 𝐻2𝑂 → 𝑆𝑏(𝑂𝐻)2𝐶𝑙 + 𝐻+ + 𝐶𝑙− (полное ионное уравнение реакции гидролиза хлорида сурьмы) гидролиза хлорида сурьмы) 𝑆𝑏𝑂𝐻𝐶𝑙2 + 𝐻2𝑂 → 𝑆𝑏(𝑂𝐻)2𝐶𝑙 + 𝐻𝐶𝑙 (молекулярное уравнение реакции гидролиза хлорида сурьмы) 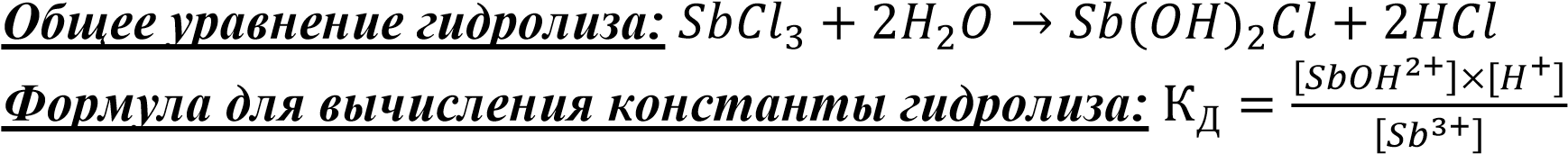 . Из . Из этой формулы следует, что чем меньше концентрация раствора, тем лучше он диссоциирует (тем степень его диссоциации больше). Ответы на вопросы: Сделать общий вывод о влиянии разведения на степень гидролиза солей. Вывод: Константа гидролиза соли тем больше, чем меньше еёконцентрация в данном растворе. Степень гидролиза каких солей не меняется при разбавлении раствора? Солей, образованных сильным основанием и сильной кислотой. Добавлением какого реактива можно уменьшить степень гидролиза хлорида сурьмы? Гидроксид сурьмы (III). Опыт 4: 𝐴𝑙2(𝑆𝑂4)3 → 2𝐴𝑙3+ + 3𝑆𝑂42− (диссоциация сульфата алюминия в воде) 2𝐴𝑙3+ + 3𝑆𝑂42− + 𝑍𝑛2+ + 2𝐻2𝑂 → 2𝐴𝑙𝑂𝐻𝑆𝑂4 + 𝑍𝑛2+ + 𝑆𝑂42− + 𝐻2 ↑ (полное ионное уравнение реакции гидролиза сульфата алюминия) 𝐴𝑙3+ + 𝐻2𝑂 → 𝐴𝑙𝑂𝐻2+ + 𝐻+ (сокращённое ионное уравнение реакции гидролиза сульфата алюминия) 2𝐴𝑙3+ + 3𝑆𝑂42− + 𝑍𝑛2+ + 2𝐻2𝑂 → 2𝐴𝑙𝑂𝐻𝑆𝑂4 + 𝑍𝑛𝑆𝑂4 + 𝐻2 ↑ (молекулярное уравнение реакции гидролиза сульфата алюминия) В растворе солей алюминия и цинка цинк растворяется, потому чтообразуется растворимый в воде гидроксид цинка и водород. Опыт 5(А): 𝐹𝑒𝐶𝑙3 → 𝐹𝑒3+ + 3𝐶𝑙−(диссоциация хлорида железа в воде) 𝑁𝑎2𝐶𝑂3 → 2𝑁𝑎+ + 𝐶𝑂32− (диссоциация карбоната натрия в водном растворе) 𝐹𝑒3+ + 3𝐶𝑙− + 2𝑁𝑎+ + 𝐶𝑂32− + 5𝐻2𝑂 → 𝐹𝑒(𝑂𝐻)3 ↓ +2𝑁𝑎+ + 2𝑂𝐻− + +𝐻2𝐶𝑂3 + 3𝐻+ + 3𝐶𝑙− (полное ионное уравнение реакции гидролиза хлорида железа и карбоната натрия) 𝐹𝑒3+ + 𝐶𝑂32− + 3𝑂𝐻− + 2𝐻+ → 𝐹𝑒(𝑂𝐻)3 ↓ +𝐻2𝐶𝑂3(сокращённое ионное уравнение реакции гидролиза хлорида железа и карбоната натрия) 𝐹𝑒𝐶𝑙3 + 𝑁𝑎2𝐶𝑂3 + 5𝐻2𝑂 → 𝐹𝑒(𝑂𝐻)3 ↓ +2𝑁𝑎𝑂𝐻 + 𝐻2𝐶𝑂3 + 3𝐻𝐶𝑙 (молекулярное уравнение реакции гидролиза хлорида железа и карбоната натрия) В пробирку с раствором хлоридом железа добавили несколько капель раствора карбоната натрия. В результате гидролиза выпал оранжевый осадок. Опыт 5(Б): 𝐶𝑢𝑆𝑂4 → 𝐶𝑢2+ + 𝑆𝑂42− (диссоциация сульфата меди в воде) 𝑁𝑎2𝐶𝑂3 → 2𝑁𝑎+ + 𝐶𝑂32− (диссоциация карбоната натрия в воде) 𝐶𝑢2+ + 𝑆𝑂42− + 2𝑁𝑎+ + 𝐶𝑂32− + 2𝐻2𝑂 → 𝐶𝑢(𝑂𝐻)2 ↓ +2𝑁𝑎+ + 𝑆𝑂42− + 𝐻2𝐶𝑂3 (полное ионное уравнение реакции гидролиза сульфата меди и карбоната натрия) 𝐶𝑢2+ + 𝐶𝑂32− + 2𝐻2𝑂 → 𝐶𝑢(𝑂𝐻)2 ↓ +𝐻2𝐶𝑂3 (сокращённое ионное уравнение реакции гидролиза сульфата меди и карбоната натрия) 𝐶𝑢𝑆𝑂4 + 𝑁𝑎2𝐶𝑂3 + 2𝐻2𝑂 → 𝐶𝑢(𝑂𝐻)2 ↓ +𝑁𝑎2𝑆𝑂4 + 𝐻2𝐶𝑂3 (молекулярное уравнение реакции гидролиза сульфата меди и карбоната натрия) В пробирку с раствором сульфатом меди добавили несколько капель раствора карбоната натрия. В результате гидролиза образовался бирюзовый осадок. Вывод: в результате лабораторной работы был изучен гидролиз солей и его следствия. Также научились составлять уравнения реакций гидролиза. |
