ТГиВ гептан. Курсовик-ТгиВ. Исследование пожароопасных свойств гептана
 Скачать 366.62 Kb. Скачать 366.62 Kb.
|
Расчет объема и процентного состава продуктов горения индивидуального веществаЗаписываем уравнение реакции горения: C7H16 + 11(O2 + 3,76N2)→ 7CO2 + 8H2O + 11× 3,76N2 По уравнение реакции горения определяем количество каждого из продуктов сгорания: n(CO2) = 7 кмоль n(H2O) = 8 кмоль n(N2) = 11*3,76 = 41.36 кмоль Поскольку горение протекает с избытком воздуха (α>1), необходимо учесть остаточный кислород в продуктах сгорания и азот в избытке воздуха: ∆𝑛(𝑂2) = 𝛽 ∗ (𝛼 − 1) = 11 ∗ (3,75 − 1) = 30,25 кмоль ∆𝑛(𝑁2) = 3,76 ∗ 𝛽 ∗ (𝛼 − 1) = 3,76 ∗ 11 ∗ (3,75 − 1) = 38,6 кмоль Таким образом, практический состав продуктов сгорания следующий: n(CO2) = 7 кмоль n(H2O) = 8 кмоль nпракт(N2) = n(N2) + ∆n(N2) = 41,36+ 38,6 = 79.96 кмоль nпракт (O2) = 30,25 кмоль Определяем общее количество продуктов сгорания при сжигании 1 кмоля горюче 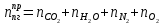 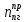 = 7 + 8 + 79,96 + 30,25 = 125.21 кмоль = 7 + 8 + 79,96 + 30,25 = 125.21 кмольОпределяем процентный состав продуктов горения: 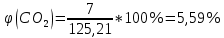 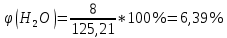 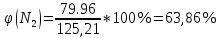 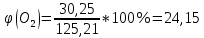 % %Поскольку известно, что 1 кмоль любого газа или пара при одинаковых условиях занимает одинаковый объем, то найденные концентрации будут являться объемными концентрациями продуктов сгорания. Определяем общее количество продуктов сгорания при сжигании 1 кг горючего, для этого необходимо составить пропорцию: 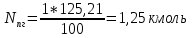 Рассчитаем, какой объем занимает 1 кмоль газообразных веществ при заданных температуре и давлении. 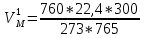 Объем продуктов сгорания составит: 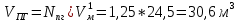 При сжигании 1 кг гептана при заданных условиях выделяется 30,6 м3 продуктов сгорания, из них : СО2 – 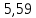 %; H2O – %; H2O – 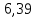 %; N2 – %; N2 – 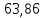 %; %;О2 – 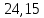 %. %.Расчет объема и процентного состава продуктов горения вещества сложного элементного состава В этом случае теоретический выход продуктов горения определяется как сумма продуктов горения каждого элемента, входящего в состав вещества. Представить гептан 𝐶7𝐻16 как вещество сложного элементного состава. Определить объем и состав в объемных % продуктов горения, образовавшихся при сгорании 1кг. этого вещества. Начальная температура окружающей среды 27 оС, давление 101,9 кПа, коэффициент избытка воздуха 𝛼 = 1,4 Решение: Вычислим массовые доли элементов в веществе. Молярная масса гептана составляет: 𝑀(𝐶7𝐻16) = 12 ∗ 7 + 1 ∗ 16 = 100 кг/кмоль; w(С) = (7× 12/100) × 100 = 84% w(H) = (16×1/100) × 100 = 16% Условия отличаются от нормальных, следовательно, необходимо определить, какой объем будем занимать 1 кмоль любого газообразного вещества при данных условиях (расчет Vм). Для заданных в задаче условий: 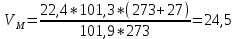 м3/кмоль м3/кмольВычислим число киломолей каждого компонента продуктов горения. 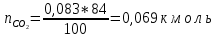 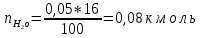 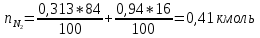 В состав продуктов горения входит избыточный воздух: Поскольку в рассматриваемом случае горение протекает с избытоком воздуха ( 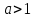 ), необходимо учесть остаточный кислород в продуктах сгорания и азот в избытке воздуха: ), необходимо учесть остаточный кислород в продуктах сгорания и азот в избытке воздуха: 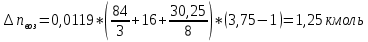 𝑛(ПГ) = 0,069 + 0,08 + 1,25+0,41= 1,8 кмоль Суммарный объем продуктов горения составит: 𝑉(ПГ) = 𝑛(ПГ) ∗ 𝑉𝑀 = 1,8 ∗ 30,6 = 55,08м3 Процентный состав продуктов горения: 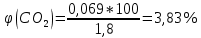 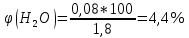 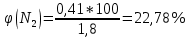 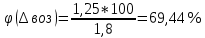 Ответ: Объем продуктов горения гептана при заданных условиях составляет 55,08м3, объемные доли продуктов горения составили: 𝜑(𝐶𝑂2) = 3,83%; 𝜑(𝐻2𝑂) = 4,4%; 𝜑(𝑁2) = 22,78%; 𝜑(∆возд) = 69,44%. |
