Для мед колледжа. 20.02.Анионы 1гр. 2. Качественные реакции на анионы первой аналитической группы
 Скачать 57.5 Kb. Скачать 57.5 Kb.
|
|
ТЕМА: «Качественные реакции на анионы первой аналитической группы». План: Классификация анионов. Качественные реакции на сульфат- , сульфит-, тиосульфат - анионы. Качественные реакции на фосфат-анион. Качественные реакции на карбонат - анион. Качественные реакции на оксалат – анион. Качественные реакции на борат - анионы. 1. В настоящее время не существует единой общепринятой классификации ионов на аналитические группы. В большинстве случаев анионы обнаруживают в отдельных порциях раствора в присутствии других анионов компромиссным методом, сочетающим дробный и систематический ход анализа. 1) По классификации И.П. Алимарина и Н.И. Блока анионы подразделяют на четыре группы, основываясь на различном отношении их к разбавленным кислотам, смеси растворимых солей бария и кальция и серебра нитрата в азотнокислой среде. 2) По классификации Н.А. Тананаева анионы подразделяют на три группы по их окислительно-восстановительным свойствам: анионы – окислители, анионы – восстановители и индифферентные. 3) По наиболее удобной классификации анионы делят на три группы. В основу классификации положена растворимость бариевых и серебряных солейсоответствующих кислот, то есть отношение анионов к двум реактивам – хлориду бария и серебра нитрату, с которыми они образуют такие химические соединения, которые легко можно обнаружить по их внешним признакам. Анионы имеют общие и групповые реакции. I группа SO42- ; SO32- ; S2O32- ; PO43- ; CO32- ; C2O42- ; BO33- групповой реактив хлорид бария в нейтральной или слабокислой среде. II группа Cl- ; Br- ; J- групповой реактив серебра нитрат в азотнокислой среде. III группа NO2- ; NO3- группового реактива нет. Серебряные и бариевые соли этих анионов растворимы в воде. 2. Качественные реакции на сульфат -, сульфит -, тиосульфат – анионы. SO42- Осаждение групповым реактивом хлоридом бария образуется белый осадок нерастворимый в кислотах и щелочах (этим он отличается от других бариевых солей анионов первой группы). (ГФ) Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl SO32- Реакция осаждения хлоридом бария образуется белый осадок, растворимый в хлороводородной, азотной кислотах, с выделением оксида серы (IV) SO2↑. Na2SO3 + BaCl2 → BaSO3↓ + 2NaCl BaSO3 + 2НCl → BaCl2 + H2O + SO2↑ Реакция разложения кислотами выделяется SO2↑ , который обнаруживается по запаху жженых спичек или по обесцвечиванию раствора йода или перманганата калия. Na2SO3 + 2HCl → SO2↑ + H2O +2NaCl SO2↑ +J2 + 2H2O → 2HJ + H2SO4 5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 +2H2SO4 Окисление раствором йода, происходит обесцвечивание раствора. Na2SO3 + J2 + 2HCl + H2O → 2HJ + H2SO4 + 2NaCl S2O32- Реакция осаждения хлоридом бария образуется белый осадок, растворимый в минеральных кислотах, кроме серной с выделением SO2↑ и S↓. Na2S2O3 + BaCl2 → BaS2O3↓ + 2NaCl BaS2O3 + 2HCl → BaCl2 + S↓ + SO2↑ + H2O Реакция осаждения, разложения, гидролиза с серебра нитратом, образуется белый, желтый, затем черный осадок. (ГФ) Na2S2O3 + 2AgNO3 → Ag2S2O3↓ + 2NaNO3 Ag2S2O3 → Ag2SO3↓ + S↓ Ag2SO3↓ +S+ H2O → Ag2S↓ + H2SO4 Реакция разложения кислотой хлороводородной образуется желтый осадок или помутнение раствора (за счет выделения свободной серы) и запах жженых спичек SO2↑. (ГФ) Na2S2O3 + 2HCl → S↓ + SO2↑ + H2O + 2NaCl Окисление раствором йода, раствор обесцвечивается. 2Na2S2O3 + J2 → 2NaJ + Na2S4O6 тетратионат натрия 3. Качественные реакции на фосфат – анион. PO43- Осаждение хлоридом бария образуется белый кристаллический осадок, растворимый в минеральных кислотах (кроме серной) и в уксусной кислоте. 2Na3PO4 + 3BaCl2 → Ba3(PO4)2↓ + 6NaCl Осаждение серебра нитратом образуется желтый кристаллический осадок, растворимый в азотной кислоте и в гидроксиде аммония. (ГФ) Na3PO4 + 3AgNO3 → Ag3PO4↓ + 3NaNO3 Ag3PO4 + 3НNO3 → Н3PO4 + 3AgNO3 Ag3PO4 + 6NH4OH → [Ag(NH3)2]3PO4 + 6H2O Осаждение магнезиальной смесью образуется белый кристаллический осадок, растворимый в минеральных кислотах и уксусной кислоте. (ГФ) NH4OH N  a3PO4 + MgCl2 + NH4Cl MgNH4PO4↓ + 3NaCl a3PO4 + MgCl2 + NH4Cl MgNH4PO4↓ + 3NaClMgNH4PO4↓ + 3НCl → Н3PO4 + MgCl2 + NH4Cl Качественные реакции на карбонат-ион. CO32- Осаждение хлоридом бария образуется белый осадок, растворимый в хлороводородной, азотной, уксусной кислотах. Na2CO3 + BaCl2 → BaCO3↓ + 2NaCl Разложение минеральными кислотами, образуется углекислый газ, который обнаруживают пропусканием его через известковую воду (мутнеет). (ГФ) Na2CO3 + 2HCl → 2NaCl + CO2↑ + H2O CO2 + Ca(OH)2 → CaCO3↓ + H2OОтличие карбонатов от гидрокарбонатов(ГФ) С насыщенным раствором магния сульфата карбонаты образуют белый осадок (гидроксокарбонат магния). Гидрокарбонаты образуют осадоктолько при кипячении. С фенолфталеином раствор карбоната дает красное окрашивание. Качественные реакции на оксалат – анион. C2O42- Осаждение хлоридом бария, образуется белый осадок, растворимый в минеральных кислотах (кроме серной) и в уксусной кислоте при нагревании. (NH4)2C2O4 + BaCl2 → BaC2O4↓ + 2NH4Cl BaC2O4 + 2HCl → BaCl2 + H2C2O4 Осаждение раствором кальция хлорида, образуется белый кристаллический осадок, растворимый в минеральных кислотах (кроме серной), нерастворим в уксусной кислоте. (ГФ) (NH4)2C2O4 + СaCl2 → СaC2O4↓ + 2NH4Cl Окисление перманганатом калия в кислой среде, наблюдают обесцвечивание раствора. 5(NH4)2C2O4 + 2KMnO4 + 8H2SO4 → 10CO2↑ + 5(NH4)2SO4 + 2MgSO4 + H2SO4 + 8H2O C  2O42- -2e → 2CO2 5 2O42- -2e → 2CO2 5Mn+7 +5e → Mn+2 2 Качественные реакции на борат – анионы. BO33-, В4О72- Реакция осаждения хлоридом бария образуется белый осадок, который растворим в уксусной, хлороводородной и азотной кислотах. Na2B4O7 + BaCl2 + 3H2O → Ba(BO2)2↓ + 2 H3BO3 + 2NaCl метаборат бария Реакция этерификации с этанолом в присутствии концентрированной серной кислоты, пламя горит с зеленой каймой. (ГФ) Na2B4O7 + H2SO4 + 5H2O → 4 Н3ВО3 + Na2SO4 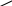 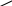 OH к. H2SO4 O-C2H5 OH к. H2SO4 O-C2H5 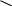    B OH + 3 C2H5OH B O-C2H5 + 3 H2O B OH + 3 C2H5OH B O-C2H5 + 3 H2OOH O-C2H5 Куркумовая бумага, смоченная подкисленным раствором борной кислоты (бората), после высыхании окрашивается в розовый цвет, после смачивания ее раствором гидроксида аммония – окраска становится зеленовато-черной. |
