Фармацевтическая технология. курсовая фт. Кафедра фармацевтической технологии
 Скачать 235.66 Kb. Скачать 235.66 Kb.
|
|
федеральное государственное бюджетное образовательное учреждение высшего образования «Курский государственный медицинский университет» Министерства здравоохранения Российской Федерации (ФГБОУ ВО КГМУ Минздрава РФ) Факультет фармацевтический КАФЕДРА ФАРМАЦЕВТИЧЕСКОЙ ТЕХНОЛОГИИ КУРСОВАЯ РАБОТА по дисциплине ФАРМАЦЕВТИЧЕСКАЯ ТЕХНОЛОГИЯ ПРОМЫШЛЕННОГО ПРОИЗВОДСТВА ТЕМА: " Вспомогательные вещества, применяемые в производстве жидких лекарственных форм". Исполнитель: Мацкевич А.М. курс 4 группа 5 Руководитель: Доцент кафедры, кандидат фармацевтических наук, Курилова О.О. Дата сдачи курсовой работы___________ Оценка_____________________________ Подпись руководителя________________ КУРСК – 2022 Содержание Введение…………………………………………………………………………..4 Глава 1. Характеристика и классификация вспомогательных веществ……….6Определение вспомогательных веществ………………………………….6Требования, предъявляемые вспомогательным веществам……………..7 Классификация вспомогательных веществ………………………………8 Влияния вспомогательных веществ на скорость растворения фармацевтических субстанций…………………………………………..10 Влияния вспомогательных веществ на скорость высвобождения фармацевтических субстанций…………………………………………..11 Влияния вспомогательных веществ на скорость всасывания фармацевтических субстанций…………………………………………..12 Влияния вспомогательных веществ на другие фармацевтические характеристики фармацевтических субстанций………………………..13 Глава 2. Статистическая обработка применения вспомогательных веществ в пероральных суспензиях………………………………………………………..14 2.1. Модификаторы вязкости, используемые в составах суспензий для приёма внутрь…………………………………………………………………………….14 2.2. Поверхностно-активные вещества, используемые в составах суспензий для приёма внутрь……………………………………………………………….17 2.3. Сорастворители, используемые в составах суспензий для приёма внутрь…………………………………………………………………………….19 2.4. Консерванты, используемые в составах суспензий для приёма внутрь..21 2.5. Антиоксиданты, используемые в составах суспензий для приёма внутрь……………………………………………………………………………..23 2.6. Наполнители, используемые в составах суспензий для приёма внутрь…23 2.7. Регуляторы pH и буферы, используемые в составах суспензий для приёма внутрь……………………………………………………………………………..26 2.8. Пеногасители, используемые в составах суспензий для приёма внутрь…27 2.9. Подсластители, используемые в составах суспензий для приёма внутрь……………………………………………………………………………28 2.10. Ароматизаторы, используемые в составах суспензий для приёма внутрь……………………………………………………………………………30 2.11. Красители, используемые в составах суспензий для приёма внутрь….31 Заключение………………………………………………………………………32 Список литературы……………………………………………………………..33 Введение Современное развитие химии высокомолекулярных соединений в настоящее время способствует их широкому использованию в различных отраслях промышленности, медицины, фармации и народного хозяйства. Особый интерес представляет применение высокомолекулярных материалов в фармации, которые используются в качестве вспомогательных веществ при производстве твердых, жидких и мягких лекарственных форм. Ни один фармацевтический фактор не оказывает столь значительного и сложного влияния на действие препарата, как вспомогательные вещества. В редких случаях в состав лекарственной формы не входят компоненты, являющиеся носителями лекарственных веществ, призванные повысить биологическую доступность, облегчить проведение технологического процесса, изменить органолептические характеристики препарата. Вспомогательные вещества являются обязательным компонентом лекарственной формы, составляют единую физико-химическую систему с лекарственным веществом и взаимодействуют с организмом человека. Они регулируют скорость наступления терапевтического эффекта действующего вещества, обеспечивают удобство применения, потребительские качества лекарственного препарата и оказывают влияние на фармакологическую активность лекарственных веществ. Вспомогательные вещества обеспечивают стабильность лекарственной формы в процессе их изготовления и хранения, что имеет медицинское и экономическое значение, так как позволяет увеличить срок годности лекарственного препарата. Благодаря успехам синтетической химии созданы препараты, разовые дозы лекарственных веществ в которых составляют миллиграммы или даже доли миллиграммов, а это приводит к необходимости обязательного использования вспомогательных веществ в лекарственной форме и усиливает их роль в фармакокинетике лекарственного вещества. В настоящее время в качестве вспомогательных веществ используются растворители; вещества, увеличивающие вязкость; стабилизаторы; консерванты; корригирующие вещества; красящие вещества и т.д. Необоснованное применение вспомогательных веществ может привести к снижению, извращению или полной потерей лечебного действия лекарственного препарата. Это происходит главным способом, вследствие взаимодействия лекарственных веществ при изготовлении препаратов в самой лекарственной форме или чаще после ее назначения больному. Цель: изучить значение вспомогательных веществ в производстве лекарственных препаратов. Глава 1. Характеристика и классификация вспомогательных веществ Определение вспомогательных веществ Почти все известные в настоящее время лекарственные формы изготавливают с использованием вспомогательных веществ, т.е. лекарственная форма представляет собой определенную систему, состоящую из лекарственных и вспомогательных веществ. Вспомогательные вещества – вещества неорганического или органического происхождения, используемые в процессе производства, изготовления лекарственных препаратов для придания им необходимых физико-химических свойств [5]. Выбор вспомогательных веществ должен осуществляться с учетом их влияния на стабильность и на биофармацевтические характеристики готового препарата. При разработке новых лекарственных форм проводят подбор вспомогательных веществ индивидуально для каждого препарата с учетом возможного их влияния на физико-химические свойства лекарственных веществ и на их терапевтическую эффективность. В результате взаимодействия лекарственных веществ и вспомогательных веществ на стадии приготовления и в процессе хранения могут образовываться токсические соединения и снижаться терапевтическая эффективность лекарственного препарата. Вспомогательные вещества определяют не только вид и характеристики лекарственных форм, но и интенсивность высвобождения лекарственных веществ из соответствующей лекарственной формы, а также динамику поступления лекарственного препарата в организм больного человека. Например, диметилсульфоксид, добавленный в глазные капли, ускоряет проникновение антибиотиков в ткани глаза. Использование же метилцеллюлозы позволяет удерживать лекарственные вещества в тканях длительное время, что обеспечивает пролонгированное действие, которое необходимо при многих хронических заболеваниях. Требования, предъявляемые вспомогательным веществам. Вспомогательные вещества являются обязательными ингредиентами почти всех лекарственных препаратов и при использовании вступают в контакт с органами и тканями организма, поэтому к ним предъявляются определенные требования. При этом необходимо учитывать, что многие вспомогательные вещества поступают от различных предприятий министерств и ведомств (химической, пищевой промышленности и др.), поэтому требования к вспомогательным веществам должны быть едиными. К вспомогательным веществам должны предъявляться следующие требования:соответствие медицинскому назначению лекарственного препарата, т.е. обеспечение проявления надлежащего фармакологического действия лекарственного средства с учетом его фармакокинетики. Вспомогательные вещества не должны оказывать влияния и изменять биологическую доступность лекарственного средства; используемые количества должны быть биологически безвредны и биосовместимы с тканями организма, а также не оказывать аллергизирующего и токсического действий; соответствие формообразующих свойств изготовляемой лекарственной форме. Вспомогательные вещества должны придавать лекарственной форме требуемые свойства: структурно-механические, физико-химические и, следовательно, обеспечивать биодоступность. Вспомогательные вещества не должны оказывать отрицательного влияния на органолептические свойства лекарственных препаратов: вкус, запах, цвет и др.; отсутствие химического или физико-химического взаимодействия с лекарственными веществами, упаковочными и укупорочными средствами, а также материалом технологического оборудования в процессе приготовления лекарственных препаратов и при их хранении. Следствием различных взаимодействий может быть снижение эффективности, а в отдельных случаях даже проявление токсических свойств лекарственного препарата; соответствие в зависимости от степени микробиологической чистоты изготовляемого препарата (как конечного продукта) требованиям предельно допустимой микробной контаминации; возможность подвергаться стерилизации, поскольку вспомогательные вещества иногда являются основным источником микробного загрязнения лекарственных препаратов; экономическая доступность и обеспечение отечественной промышленностью [5]. Качество и соответствие вышеуказанным требованиям вспомогательных материалов регулируется нормативной документацией: Государственной Фармакопеей, фармакопейными статьями или временными фармакопейными статьями на данное вещество. Использование веществ по ГОСТ или ТУ допускается, если имеется указание на применение данной квалификации вещества в фармакопейной статье на готовое лекарственное средство. Общее количество вспомогательных веществ не должно превышать 20% массы входящих в пропись лекарственных веществ. Отдельные исключения от этой нормы указаны в частных фармакопейных статьях. Классификация вспомогательных веществ По ряду причин: разнообразие химической природы, влияние на лекарственные формы (стабильность, пролонгирование, исправление вкуса и т.д.) и их терапевтическую эффективность, предлагаемая классификация не может считаться совершенной, хотя является достаточно удобной. В основе классификации вспомогательных веществ лежит ряд признаков: природа, влияние на технологические характеристики и фармакокинетику лекарственных форм. По происхождению вспомогательные вещества классифицируют: Природные: Органические: - Углеводы: крахмал, камеди, альгинаты, микробные полисахариды; - Белки: желатин, коллаген, желатоза; - Жиры: растительные масла, свиной жир. Неорганические: бентониты, тальк, аэросил. Синтетические и полусинтетические: модифицированные крахмалы, полиакрилаты, твины, ПВП, ПЭГ; Полученные методом биотехнологий. По химической структуре вспомогательные вещества можно разделить на: Мономеры и полимеры (производные целлюлозы, полиэтиленоксид); Катионные (тиония хлорид), анионные (медицинские мыла), неионогенные ПАВ (моноэфиры сахарозы, глицериды, эфиры жирных кислот). В зависимости от влияния на физико-химические характеристики и фармакокинетику лекарственных форм делятся на следующие группы: Формообразующие - эта группа вспомогательных веществ используется в качестве дисперсионных сред (вода или неводные среды – этанол, глицерин) в технологии жидких лекарственных форм (вода), наполнителей для твердых лекарственных форм (молочный сахар, крахмал, тальк), основ для мазей (вазелин, жиры) и суппозиториев (масло какао, желатин). Стабилизирующие, которые в свою очередь делятся на: - ингибиторы химических процессов – вещества, предотвращающие гидролиз, окисление, разложение и др. Имеют значение для неоднородных систем; - консерванты – вещества, предотвращающие микробную контаминацию; - структурообразователи и стабилизаторы термодинамических свойств системы – вещества, предотвращающие седиментацию, коагуляцию, коалесценцию, агрегацию, конденсацию. Имеет больше значение для лекарственных форм, подвергающихся различным видам стерилизации, особенно термической. Пролонгирующие (пролонгаторы) - вспомогательные вещества, увеличивающие время нахождения ЛВ в организме. Солюбилизирующие - вещества, способствующие растворению труднорастворимых и практически нерастворимых лекарственных веществ. Корригирующие – регулируют вкус, цвет, запах различных лекарственных веществ. По размеру (величине молекулы): - Олигомеры (4000 - 10000); - Низкомолекулярные вещества (10000 – 45000); - Среднемолекулярные (45000 – 150000); - Высокомолекулярные вещества – полимеры (150000 – 500000). Влияния вспомогательных веществ на скорость растворения фармацевтических субстанций Фармацевтическая разработка лекарственных препаратов – это неотъемлемая часть их жизненного цикла. Основная задача фармацевтической разработки заключается в создании качественного лекарственного препарата и производственного процесса, и одним из критериев качества является подбор и обоснование выбора вспомогательных веществ. При осуществлении фармацевтической разработки с целью получения информации о высвобождении фармацевтической субстанции из твердой лекарственной формы необходимо знать скорость растворения, то есть количество фармацевтической субстанции, высвободившейся за определенный промежуток времени в жидкую среду растворения в стандартных условиях [1,8]. Наибольшее влияние на скорость растворения оказывают вспомогательные вещества в составе твердых дисперсий. Так, например, наблюдается увеличение растворимости метилурацила, нифедипина индометацина при включении их в твердую дисперсию с полиэтиленгликолем и различной молекулярной массы [6,7,11,12,13]. Возрастает как растворимость, так и скорость растворения диклофенака в воде из твердой дисперсии с полиэтиленгликолем-1500 и поливинилпирролидоном 10000. Твердые лекарственные формы, как например, таблетки целекоксиба, содержащие в качестве антифрикционного вещества тальк (способный образовывать гидрофильный слой) имеют лучший профиль растворения по сравнению с таблетками, у которых используется магния стеарат или коллоидный диоксид кремния. Установлено также, что присутствие этих гидрофобных веществ замедляет процесс абсорбции [22]. Высокой степенью растворения и биодоступности в сочетании с и поливинилпирролидоном характеризуются следующие соединения: преднизолон, гризеофульвин, салициламид, хлорамфеникол [19]. Влияния вспомогательных веществ на скорость высвобождения фармацевтических субстанций Прежде чем фармацевтическая субстанция попадет в кровь, должно произойти ее высвобождение из лекарственной формы. В процессе фармацевтической разработки в зависимости от поставленных задач лекарственная форма должна способствовать либо быстрому и полному высвобождению лекарственного препарата, либо обеспечивать пролонгацию его действия. Ряд исследований показали влияние вспомогательных веществ на изменение скорости высвобождения фармацевтической субстанции из твердых лекарственных форм. Так, например, циклодекстрины часто применяются для увеличения биодоступности плохо растворимых в воде фармацевтических субстанций, повышают их скорость и полноту высвобождения, в том числе путем введения фармацевтической субстанции в комплексы включения [20]. Использование спиртового раствора связующего вещества в технологии получения таблеток методом влажного гранулирования увеличивает полноту и скорость высвобождения фармацевтической субстанции с неудовлетворительной растворимостью [21]. Поливинилпирролидон применяется для повышения биодоступности и ускорения процесса высвобождения фармацевтической субстанции. Стоит отметить, что в настоящее время активно развивается такое направление получения лекарственной формы, как 2D-технология, принцип которого заключается в нанесении чернил, содержащих на специальную подложку (субстрат). Подбор субстрата совместно с составом чернил также оказывает влияние на морфологические свойства и растворимость печатаемых лекарственных форм [23]. На примере индометацина и итраконазола было показано, что скорость высвобождения фармацевтических субстанций со съедобных субстратов (различных типов рисовой бумаги) была ниже в сравнении с образцами, напечатанными на диапозитивной пленке, что наиболее заметно в случае с индометацином. Увеличенное время высвобождения со съедобных субстратов объяснялось более пористой структурой субстратов, в результате чего частицы ФС включались в матрицу субстрата. Влияния вспомогательных веществ на скорость всасывания фармацевтических субстанций Всасывание – процесс, в результате которого фармацевтическая субстанция поступает из места введения в кровеносное русло. Всасывание фармацевтической субстанции начинается сразу после его введения. В результате фармацевтической разработки вспомогательных веществ, в зависимости от своей природы и характера взаимодействия с фармацевтической субстанцией, могут оказывать различное влияние на данный параметр. Применением поливинилпирролидона в лекарственной форме удается увеличить относительную биодоступность полимерных частиц тамоксифена после перорального применения более чем в 2 раза [2]. Установлено снижение абсорбции циметидина в присутствии гидроксипропилметилцеллюлозы и талька в составе капсул. Влияния вспомогательных веществ на другие фармацевтические характеристики фармацевтических субстанций. В результате осуществления фармацевтической разработки, помимо изменения скорости растворения, высвобождения и всасывания фармацевтических субстанций, вспомогательные вещества также могут оказывать существенное влияние на их фармацевтические показатели. Пероксидные примеси в повидоне, выступающем в роли связующего, и кросповидоне в роли дезинтегранта, приводили к деградации структуры ралоксифена гидрохлорида (модулятор эстрогеновых рецепторов). Пропиленгликоль ингибирует микросомальный цитохром Р450, который принимает участие в инактивации ядовитых веществ, распаде и образовании гормонов надпочечников; в обмене белков и сохранении генетической информации. Взаимодействие лактозы, выступающей в качестве наполнителя при измельчении совместно с 4-метилфениламиноацетатом гидрохлоридом ускоряет разрушение структуры последнего [8]. Глава 2. Статистическая обработка применения вспомогательных веществ в пероральных суспензиях 2.1. Модификаторы вязкости, используемые в составах суспензий для приема внутрь Эволюцию подходов к конструированию пероральных суспензий можно проследить по изменениям классификации вспомогательных веществ, используемых в их составе. Наиболее полно этот вопрос раскрывается в основополагающих учебных и научных изданиях, посвящённых технологии лекарственных форм. В состав суспензий, помимо действующего вещества и дисперсионной среды, в ряде случаев необходимо включать стабилизаторы агрегативной и седиментационной устойчивости, в качестве которых рекомендуется использовать электролиты и высокомолекулярные соединения, обладающие поверхностноактивными свойствами [3]. В качестве источника сведений о вспомогательных веществах, используемых в составах пероральных суспензий, представленных на фармацевтическом рынке России, использовались инструкции к лекарственным препаратам, внесённым в электронную версию Государственного реестра лекарственных средств [4], содержащие в ряде случаев также указания на количественные соотношения компонентов. Опираясь на данные сведения, были проанализированы составы 51 суспензии для приема внутрь, позволившие классифицировать и описать следующие группы вспомогательных веществ. Модификаторы вязкости (загустители) используются для повышения стабильности дисперсной системы путем повышения вязкости дисперсионной среды в соответствии с законом Стокса [16]. В составе этой группы можно выделить вещества синтетического, полусинтетического и природного происхождения, являющиеся растительными полисахаридами. В качестве модификаторов вязкости в пероральных суспензиях в настоящее время используются глинистые минералы, камеди, производные целлюлозы, а также карбополы, высокомолекулярный макрогол и повидон (Рисунок 1).  Рисунок 1. Модификаторы вязкости, используемые в составах суспензий для приёма внутрь (ГРЛС) В 35% составов пероральных суспензий для повышения вязкости вводят производные целлюлозы, причем наиболее популярным среди них является традиционное и хорошо известное в отечественной фармацевтической практике вещество – натриевая соль карбоксиметилцеллюлозы, упоминаемая в составах под названием «кармеллоза натрия» и используемая в 13,7% изученных составов. Следующим по востребованности производным целлюлозы является гидроксиэтилцеллюлоза (гиэтеллоза, ГЭЦ), упоминаемая в 9,8% составов, гидроксипропилметилцеллюлоза (ГПМЦ) используется в 7,8% изученных суспензий, а такие производные, как метилцеллюлоза и оксипропилметилцеллюлоза востребованы как загустители пероральных суспензий в значительно меньшей степени (упоминаются примерно в 2% суспензий). Что касается используемых концентраций, то согласно представленным в инструкциях к лекарственным препаратам сведениям ГЭЦ вводится в составы суспензий для внутреннего применения в количестве 0,1–0,3%, ГПМЦ – 0,3–1,0%, а натрий-КМЦ – около 1%. Самым популярным модификатором вязкости в суспензиях для внутреннего применения является камедь ксантановая (27,5% изученных составов), однако другие модификаторы вязкости группы камедей – гуаровая камедь и камедь акации – используются очень редко, всего в 2% составов. При этом ксантановая камедь использовалась в концентрации 0,3–0,6%, камедь акации упоминалась в составах в концентрации 1,5–6%. Для повышения вязкости дисперсионной среды суспензий для внутреннего применения также используют глинистые минералы – магния алюмосиликат (вээгум) в концентрации 0,25–0,57% и значительно реже бентонит. Также в составе пероральных суспензий достаточно широко применяются полимеры группы карбополов (карбомеров), например, карбомер 947P, однако их использование требует дополнительного введения в состав суспензии щелочных компонентов, чаще всего натрия гидроксида. Концентрация карбопола в рассмотренных составах суспензий находилась в диапазоне от 0,035% до 0,4%. Повидон, представляющий собой линейный полимер 1-винил-2-пирролидона, упоминался в составах около 6% рассмотренных пероральных суспензий. Удалось обнаружить только единичное упоминание вводимого количества повидона – около 0,06%. Столь невысокая концентрация может объясняться тем, что повидон в малых концентрациях используется не столько для повышения вязкости, сколько в качестве так называемого полимерного адсорбционного стабилизатора. При этом молекулы повидона сорбируются на поверхности частиц суспендированного вещества и осуществляют стерическую стабилизацию суспензии, препятствуя слипанию частиц. Кроме того, в ряде случаев повидон может использоваться и для понижения вязкости, точнее, для улучшения текучести суспензий с большим количеством дисперсной фазы [24]. Высокомолекулярный полиэтиленоксид (макрогол 4000) используется для модификации вязкости в крайне небольшом числе (около 2%) рассмотренных составов суспензий для внутреннего применения.  Таким образом, по частоте использования в составах пероральных суспензий можно выстроить следующий ряд модификаторов вязкости: камедь ксантановая > карбомер = натрий-КМЦ > магния алюмосиликат = ГЭЦ > повидон > ГПМЦ > прочие. 2.2. Поверхностно-активные вещества, используемые в составах суспензий для приёма внутрь Поверхностно-активные вещества, используемые в составах суспензий, в различных источниках могут носить названия смачивающих агентов или сурфактантов [24]. В этой роли могут выступать как индивидуальные соединения, так и, реже, смеси сходных по химической природе веществ синтетического (полисорбаты, стеараты) или природного (аммония глицирризинат, лецитин) происхождения.  Рисунок 2. Поверхностно-активные вещества, используемые в составах суспензий для приёма внутрь (ГРЛС) Безусловным лидером среди ПАВ, вводимых в составы суспензий для внутреннего применения, является полисорбат-80 (твин-80). Согласно проведённым исследованиям полисорбат-80 упоминался в более чем 30% рассмотренных составов. Указанные в доступных источниках используемые концентрации при этом укладывались в диапазон от 0,05% до 1%. На втором месте по частоте использования (около 6% изученных составов) стоит производное макрогола – макрогола глицерилгидроксистеарат, также встречающийся под названием Кремофор RH40. Для стабилизации суспензии его вводили в концентрациях 0,2–1,14%. Прочие поверхностно-активные вещества вводились в составы пероральных суспензий в единичных случаях. При этом использовались достаточно низкие концентрации: эфир полигликостеариловой кислоты – 0,01%, аммония глицирризинат и макрогола-400 стеарат – 0,1%, лецитин соевый – 0,25%.  2.3. Сорастворители, используемые в составах суспензий для приёма внутрь Сорастворители – группа вспомогательных веществ, как и ПАВ, используемая для снижения поверхностного натяжения жидкой фазы и улучшения смачивания поверхности суспендированных частиц. В западной литературе упоминается также под названием «растворители». Сорастворители вводились в 68% изученных составов, причём следует отметить, что при столь широком применении ассортимент используемых сорастворителей был весьма ограничен: в этом качестве в составах пероральных суспензий использовались всего 3 вещества (Рисунок 2). 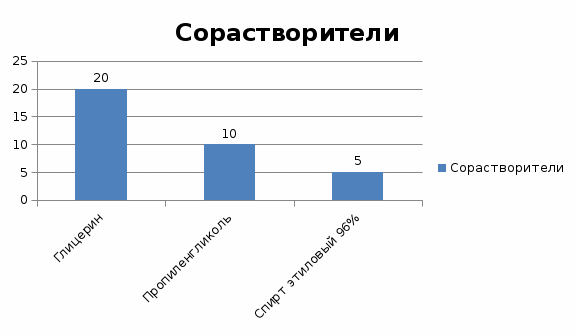 Рисунок 3. Сорастворители, используемые в составах суспензий для приёма внутрь (ГРЛС) Наиболее часто в пероральных суспензиях используется глицерин (39% исследованных составов). Пропиленгликоль использовался примерно в 20% составов пероральных суспензий, при этом вводимая концентрация колебалась от 0,12% до 2,5%. Наиболее редко в состав суспензий для внутреннего применения вводился спирт этиловый – всего в 10% составов, что может быть связано с ограничением круга возможных потребителей суспензии при введении в её состав спирта этилового. При этом концентрация спирта в суспензиях колебалась от 0,05% до 2%. 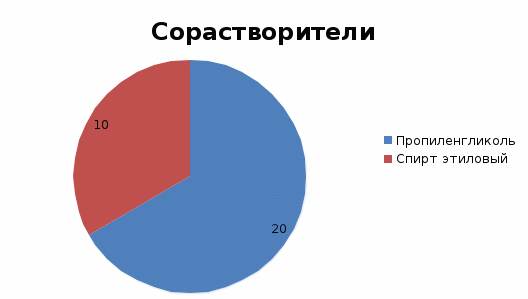 2.4. Консерванты, используемые в составах суспензий для приёма внутрь Группа консервантов традиционно включает в себя вещества, повышающие микробиологическую устойчивость лекарственной формы. Как следует из данных, приведённых на рисунке 3, перечень используемых в составах пероральных суспензий консервантов довольно обширен. Среди них можно выделить группы бензоатов, парагидроксибензоатов и сорбатов, а также несколько консервирующих веществ, не входящих в эти группы. Наиболее часто в суспензиях для внутреннего применения использовались консерванты группы парагидроксибензоатов (парабенов). Безусловным лидером как внутри этой группы, так и среди всех использованных консервантов является метилпарагидроксибензоат (нипагин), немного уступает ему по частоте применения пропилпарагидроксибензоат (нипазол). Также в этой группе следует отметить достаточно экзотический консервант – натрия нипасепт, представляющий собой комбинацию натриевых солей нипагина, нипазола и этипарагидроксибензоата. На втором месте по частоте применения располагаются консерванты группы бензоатов, включающей в себя бензоат натрия и собственно кислоту бензойную. Следует отметить, что если в случае бензоатов натриевая соль значительно более популярна, чем чистая кислота, то в случае сорбатов ситуация противоположная: сорбиновая кислота оказалась значительно популярнее, чем также используемая соль калия. Прочие консерванты (бронопол, домифена бромид, натрия гипохлорит и хлоргексидина биглюконат) применяются в единичных случаях. 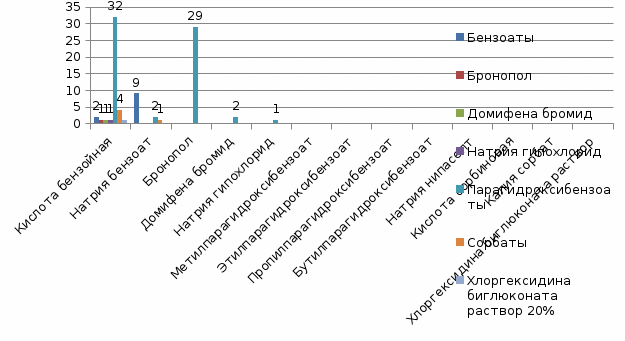 Рисунок 4. Консерванты, используемые в составах суспензий для приема внутрь. Что касается используемых концентраций, то, по имеющимся данным, нипагин вводился в концентрациях, находящихся в интервале от 0,05–0,4%, нипазол – 0,01–0,06%.Бутилпарагидроксибензоат применялся в пероральных суспензиях в концентрациях 0,05–0,27%, а для этилпарагидроксибензоата была указана концентрация 0,16%. Консерванты других групп использовались в концентрациях 0,15% (кислота бензойная), 0,15–0,24% (натрия бензоат), 0,05% (кислота сорбиновая) и 0,2% (хлоргексидина биглюконат). 2.5. Антиоксиданты, используемые в составах суспензий для приёма внутрь Антиоксиданты препятствуют протеканию в пероральных суспензиях окислительных реакций. К ним относят также и секвестранты (хелатирующие соединения), которые, однако, выделяются некоторыми авторами в отдельную группу [24]. Как следует из данных рисунка 5, антиоксиданты вводились в составы пероральных суспензий в единичных случаях. При этом использовались такие соединения, как аскорбиновая кислота (вводилась в концентрациях до 1%), натрия дисульфит (вводился в концентрации 0,05%) и натрия эдетат. 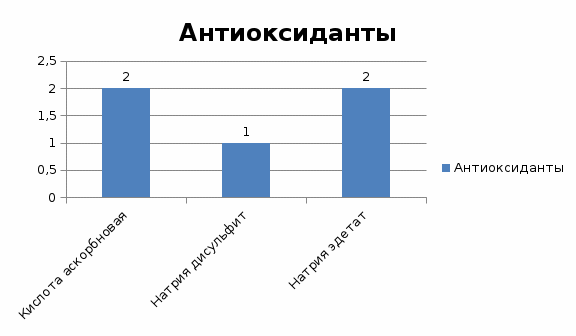 Рисунок 5. Антиоксиданты, используемые в составах суспензий для приема внутрь. 2.6. Наполнители, используемые в составах суспензий для приёма внутрь Наполнители, или вспомогательные суспендирующие агенты [24], – группа вспомогательных веществ суспензий, обычно обходимая вниманием в отечественной технологической литературе. Как правило, о наполнителях упоминают, когда речь идёт о твёрдых лекарственных формах, в первую очередь таблетках [15, 18]. В то же время зарубежные авторы выделяют эту группу вспомогательных веществ и в жидких лекарственных формах – суспензиях. Наполнители предлагается вводить в состав суспензий в том случае, когда доза действующего вещества слишком мала, чтобы обеспечить достаточное количество частиц в разовой дозе суспензии [24]. В качестве наполнителей в суспензиях могут использоваться неорганические твёрдые вещества, нерастворимые производные целлюлозы и нерастворимые синтетические полимеры [18,24]. Перечень наполнителей, используемых в изученных пероральных суспензиях, представлен в рисунке 6. 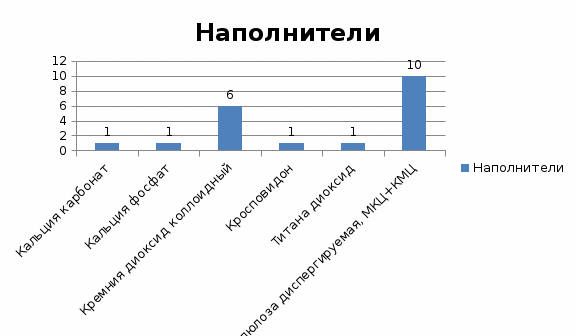 Рисунок 6. Наполнители, используемые в составах суспензий для приема внутрь. Наиболее часто в качестве наполнителя использовалась микрокристаллическая целлюлоза (МКЦ) в так называемой коллоидной форме. Данная модификация МКЦ является сочетанием собственно микрокристаллической целлюлозы и натриевой соли карбоксиметилцеллюлозы и выпускается под различными марками, наиболее популярной из которых является RC-591, используемая примерно в 20% изученных составов в концентрациях 1,2–1,5%. Столь широкое применение этого вспомогательного вещества может объясняться тем, что, кроме формирования суспензионной взвеси, его введение позволяет также регулировать вязкость получаемой композиции. На втором месте по частоте использования находился такой инертный наполнитель неорганической природы как кремния диоксид коллоидный (аэросил), – его вводили примерно в 12% составов, при этом используемая концентрация колебалась в пределах 0,2–1%. Кальция карбонат и фосфат, а также титана диоксид использовались в единичных случаях. Используемая концентрация была приведена только для диоксида титана и составляла 0,4%. Следует также отметить, что титана диоксид часто используют в фармацевтических составах в качестве пигмента, дающего белый цвет [15]. Не исключено, что эту функцию он выполняет и при включении в состав суспензионных препаратов. Так же единично был использован и кросповидон – аналог синтетического гидрофильного полимера повидона, отличающийся наличием поперечной сшивки между молекулами, из-за чего он теряет способность к растворению в воде. Преимущественно используется в качестве дезинтегранта в таблетках [16, 18]. По данным литературы, в состав суспензий рекомендуется включать микронизированную форму кросповидона [16]. 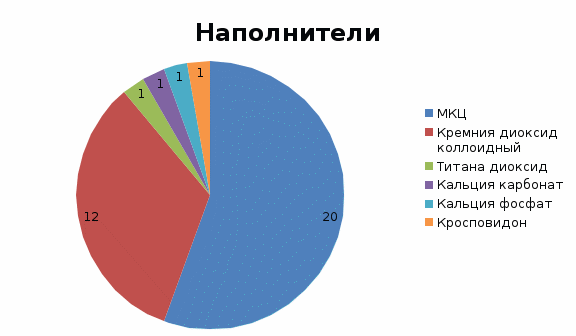 2.7. Регуляторы pH и буферы, используемые в составах суспензий для приёма внутрь Регуляторы pH и буферы используются для повышения химической и физической стабильности пероральных суспензий за счёт создания оптимального значения pH среды. Необходимость введения вспомогательных веществ этой группы обусловлена тем, что вязкость растворов ряда полимеров, используемых в фармацевтической практике и в составе пероральных суспензий в частности, зависит от величины pH. 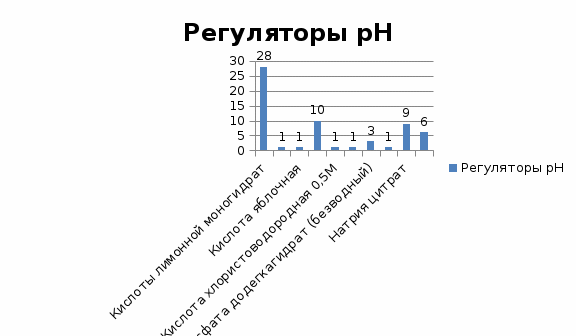 Рисунок 7. Регуляторы pH и буферы, используемые в составах суспензий для приема внутрь. Самым популярным регулятором кислотности является лимонная кислота, упоминавшаяся более чем в половине рассмотренных составов пероральных суспензий. Используемая концентрация в композициях согласно приводимым в инструкциях данным колебалась в пределах примерно от 0,017% до 0,91%. В качестве закисляющих компонентов единично использовались также кислота яблочная и кислота хлористоводородная (в виде 0,12% раствора), которая вводилась в суспензию из расчёта 0,018 мл на 100 мл. Второе место занимают различные натриевые соли (цитрат, гидрофосфат, дигидрофосфат), которые в совокупности вводились примерно в 25% изученных составов. Несмотря на достаточно широкое применение натрия цитрата (в 9 из 51 пероральной суспензии), в инструкциях указывалась лишь одна величина концентрации – 0,06%. Для натрия гидрофосфата удалось обнаружить указания на две используемые концентрации – 0,264% и 0,46%. Натрия дигидрофосфат вводился в одну пропись в концентрации 2%. Для повышения уровня pH в состав суспензий вводился натрия гидроксид (около 20% композиций), причём в 60% случаев его применения напрямую указывалась цель введения – повышение вязкости карбомера, используемого в данных суспензиях в качестве загустителя. Отдельно следует указать использование в двух составах пар «кислота – основание». В этом качестве выступали сочетания 0,5 М растворов натрия гидроксида и кислоты хлористоводородной и 5% растворов натрия гидроортофосфата и кислоты лимонной моногидрата. Последняя пара использовалась для достижения показателя pH 5,8±0,2. 2.8. Пеногасители, используемые в составах суспензий для приёма внутрь Пеногасители относительно редко включаются в состав пероральных суспензий. Тем не менее среди рассмотренных нами суспензий было установлено использование таких пеногосителей, как эмульсия силиконовая (в концентрации 0,05%), симетикон (в концентрации 0,3%) и эмульсия симетикона «Q7-2587» (представляет собой водоразбавляемую неионогенную эмульсию, содержащую 30% масс. симетикона, производство Dow Corning Corporation), которая вводилась в составы в количестве от 0,05% до 0,72%. 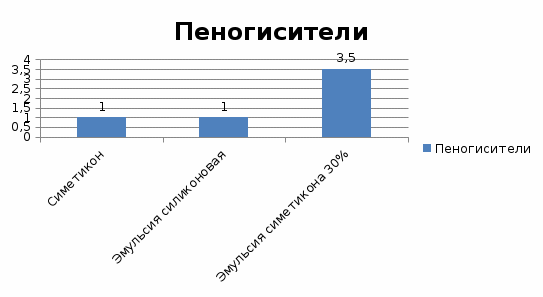 Рисунок 8.Пеногасители, используемые в составах суспензий для приема внутрь. 2.9. Подсластители, используемые в составах суспензий для приёма внутрь Обширная группа корригентов используется в составах пероральных суспензий преимущественно для маскировки неприятного цвета или запаха. Следует отметить, что в отличие от красителей и ароматизаторов корригенты вкуса (подсластители и вкусовые добавки) часто сочетают между собой, вводя в состав суспензий композицию из нескольких подсластителей или из подсластителей и вкусовой добавки. 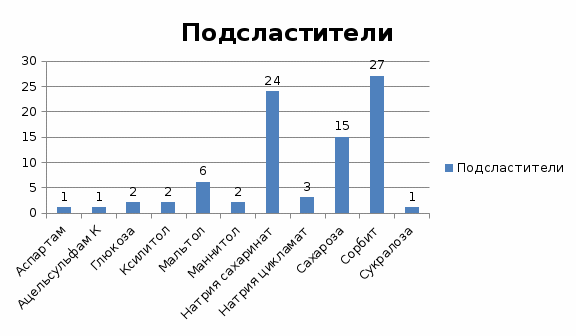 Рисунок 9.Подсластители, используемые в составах суспензий для приема внутрь. Наиболее популярными фармацевтическими подсластителями являются сахароза (сукроза), глюкоза, фруктоза, сорбит и глицерин. Среди подсластителей суспензий лидером является сорбит, входящий примерно в 52,9% рассмотренных составов. Указываемая в инструкциях к препаратам концентрация при этом колебалась в достаточно широких пределах, от 1,4% до 35%, однако следует учитывать тот факт, что в составах часто указывался не чистый сорбит, а раствор сорбита 70% (или сорбитол-70). Второе место среди подсластителей уверенно занимает натрия сахаринат, указанный в 47% изученных составов. Согласно имевшимся данным в пероральные суспензии он вводился в концентрациях 0,01–0,25%. На третьем месте (24,9% рассмотренных составов) расположился такой традиционный подсластитель, как сахароза, вводимая также в составы пероральных суспензий в виде сиропа и сахара-рафинада в весьма значительных количествах – 20–34,2%. Прочие подсластители серьёзно уступают по частоте применения первой тройке. Так, мальтол вводили только в 11,7% проанализированных составов (были указаны концентрации в пределах до 0,1%), натрия цикламат – в 5,9% (указаны концентрации в пределах 0,2–0,5%), ксилитол (указаны концентрации в пределах 15–32%), глюкоза и маннитол (указана концентрация 0,25%) – в 3,9%. Единично использовались такие подсластители, как аспартам, ацесульфам К (сунетт) и сукралоза. 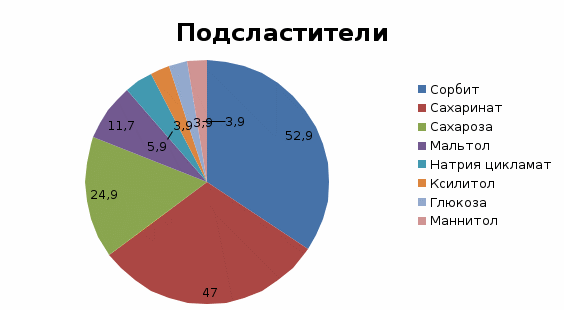 Что касается вкусовых добавок, то их в пероральные суспензии вводят относительно редко: в изученных составах были указаны вкусовые добавки «ваниль» (в количестве 0,0436 мл на 100 мл суспензии), «манго» (0,081 мл на 100 мл суспензии), а также эссенции шоколадная, мороженого и фруктовая смешанная. 2.10. Ароматизаторы, используемые в составах суспензий для приёма внутрь Ассортимент корригентов запаха (ароматизаторов), используемых в пероральных суспензиях, весьма обширен (рисунок 10). Широко представлены как фруктово-ягодные ароматы (ананасовый, вишнёвый и др.), так и такие индивидуальные запахи, как сливочный, карамельный и др. Следует отметить, что наиболее популярными являлись цитрусовые запахи (лимонный, апельсиновый) и запах мяты (левоментол, масло мяты перечной и др.). Обычно ароматизаторы вводились в состав пероральных суспензий в относительно низких концентрациях (сотые доли процента), однако в единичных случаях вводимое количество может достигать величины 1%. 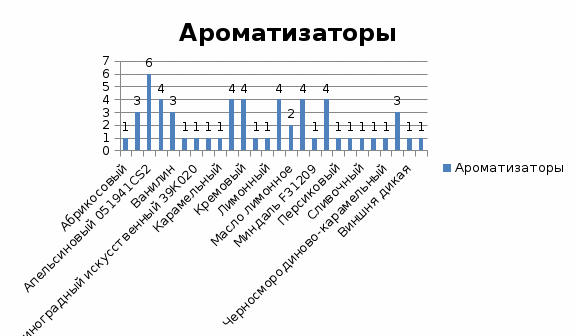 Рисунок 10. Ароматизаторы, используемые в составах суспензий для приема внутрь. 2.11. Красители, используемые в составах суспензий для приёма внутрь Достаточно редко в пероральные суспензии включаются красители (рисунок 11): только в 10 из 51 рассмотренного состава были указаны вспомогательные вещества данной группы. Из 5 используемых соединений только одно относится к так называемым натуральным красителям (рибофлавин), а остальные – синтетические соединения, продукты переработки каменноугольной смолы или нефтепродуктов. 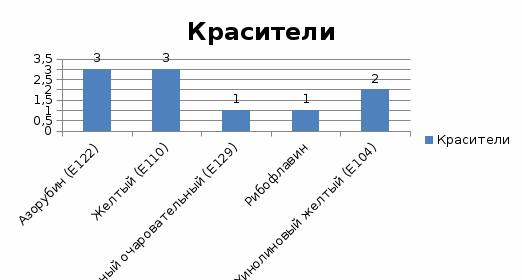 Рисунок 11. Красители, используемые в составах суспензий для приёма внутрь. Заключение. Ни один фармацевтический фактор не оказывает такого влияния на биологическую активность препаратов, как вспомогательные вещества. Вспомогательные вещества должны быть разрешены к медицинскому применению соответствующей нормативной документацией. Применение вспомогательных веществ представляет актуальную проблему современной технологии лекарственных форм, а получение же новых позволит создавать принципиально новые высокоэффективные лекарственные формы, удобные для применения и имеющие достаточно длительные сроки годности. Проведённый анализ составов пероральных суспензий лекарственных препаратов, включённых в Государственный реестр лекарственных средств, позволяет сделать вывод о широком использовании в их рецептуре вспомогательных веществ разных групп, значительно превосходящем ассортимент, традиционно описываемый в отечественной базовой фармацевтической литературе. Список литературы: Алексеев К.В., Турчинская К.Г., Блынская Е.В. и др. Применение самомикроэмульгирующихся систем доставки для увеличения растворимости и биодоступности вещества // Фармация. – 2015. – №4. – С. 37. Буховец А.В., Николаева Э.В., Ситенков А.Ю. Интерполиэлектролитные комплексы на основе EUDRAGIT® EPO как перспективные системы для контролируемой доставки лекарственных веществ // Фундаментальные исследования. – 2014. – №12(6). – 1226-1230 с. Верниковский В.В., Третьякова Е.В. Вспомогательные вещества в пероральных суспензиях //Разработка и регистрация лекарственных средств. 2017. № 2 (19). С. 116-123. Государственный реестр лекарственных средств. URL: http:// grls.rosminzdrav.ru/grls.aspx Государственная фармакопея Российской Федерации XIV издание [Электронный ресурс]: Т. I-IV. – М. : МЗ РФ. – 2018. URL: https://femb.ru/record/pharmacopea14 Грих В.В., Краснюк И.И., Беляцкая А.В. и др. Изучение растворимости нифедипина в присутствии полиэтиленгликоля в твердых дисперсиях // Материалы LXXI Международной научно-практической конференции студентов и молодых ученых «Актуальные проблемы современной медицины и фармации». Минск, 2017. – С. 1531 Грих В.В., Краснюк И.И., Краснюк И.И. (мл.) и др. Повышение растворимости метилурацила путем получения его твердых дисперсий // Материалы X Юбилейной Международной научно-практической конференции молодых ученых-медиков. Курск, 2016. – 210-212 с. Гулякин И.Д., Николаева Л.Л., Оборотова Н.А. и др. Основные методы повышения растворимости гидрофобных и труднорастворимых веществ // Разработка и регистрация лекарственных средств. – 2016. – №2(15). – 52-59 с. Иванникова Е.В., Бойко С.С., Жердев В.П. и др. Фармакокинетика трех лекарственных форм нового дипептидного анксиолитика ГБ-115 для приема внутрь // Экспериментальная и клиническая фармакология. – 2014. – №77(7). – 31-34 с. Кабанова Т.В., Буховец А.В., Гарипова В.Р. и др. Поликомплексная матричная система доставки в толстый отдел кишечника на основе CARBOMER 940/EUDRAGIT® ЕРО // Электронный сборник научных трудов «Здоровье и образование в XXI веке». М., 2010. – 521-522 с. Кошелева Т.М., Краснюк И.И. (мл.), Беляцкая А.В. и др. Изучение микрокристаллической картины твердых дисперсий индометацина // Национальная Ассоциация Ученых. – 2017. – № 6(33). – 50-51 с. Кошелева Т.М., Краснюк И.И. (мл.), Краснюк И.И. и др. Повышение растворимости противовоспалительного средства из твердых дисперсий // Сборник материалов XXIII Российского национального конгресса «Человек и лекарство». М., 2016. – С. 185. Краснюк И.И. (мл.), Кошелева Т.М., Беляцкая А.В. и др. Влияние твердых дисперсий с полиэтиленгликолем на растворимость индометацина // Химико-фармацевтический журнал. – 2018. – №3. – 46-49 с. DOI: https://doi.org/10.30906/0023-1134-2018-52-3- 46-49. Краснюк И.И. (мл.), Овсянникова Л.В., Никулина О.И. и др. Изучение растворимости кислотной формы диклофенака из твердых дисперсий // Химико-фармацевтический журнал. – 2014. – №48(11). – 23-27 с. DOI: 10.1007/s11094-015- 1183-2. Н.В. Меньшутина и др. Инновационные технологии и оборудование фармацевтического производства. Т. 1. – М.: БИНОМ, 2012. 328 с. Н.В. Меньшутина и др. Инновационные технологии и оборудование фармацевтического производства. Т. 2. – М.: БИНОМ, 2013. 480 с. Овсянникова Л.В., Краснюк И.И.М., Беляцкая А.В. и др. Роль твердых дисперсий с полимерами в изменении оптических свойств растворов и кристаллического строения диклофенака // Вопросы биологической, медицинской и фармацевтической химии. – 2014. – №12. – 59-60 с Полимеры для фармацевтической технологии / Под ред. проф. С.А. Кедика. – М. 2011. 511 с. Сеткина С.Б., Хишова О.М. Биофармацевтические аспекты технологии лекарственных средств и пути модификации биодоступности // Вестник ВГМУ. – 2014. – №13(4). – 162-172 с. Тюкова В.С., Кедик С.А, Панов А.В. и др. Изучение солюбилизирующей способности гидроксипропил-β-циклодекстрина и получение водорастворимых комплексов на его основе // Международный научно-исследовательский журнал: Сборник по результатам XXXII заочной научной конференции Research Journal of International Studies. Екатеринбург, 2014. – 73-75 с Юдина Д.В., Блынская Е.В., Минаев С.В. и др. Влияние выбора гранулирующего агента на профиль высвобождения оригинальной фармацевтической субстанции ГМЛ-1 из таблеток, полученных методом влажной грануляции // Фармацевтические науки. – 2018. – №2(36). – 103- 105 с. Bozdağ-Pehlivan S, Subaşi B, Vural I, et al. Evaluation of drug-excipient interaction in the formulation of celecoxib tablets // Drug Research. – 2011. – Vol. 68(3). – 423-433 p Geninaa N., Forsb D., Paloa M. et al. Behavior of printable formulations of loperamide and caffeine on different substrates—Effect of print density in inkjet printing // International Journal of Pharmaceutics. – 2013. – Vol. 453. – 488-497 p. Pharmaceutical suspensions: From formulation development to manufacturing / Ed. by A.K. Kulshreshtha, O.N. Singh, G.M. Wall. – Springer, 2010. 328 p. |
