Методы количественного анализа производных изохинолина. Методы кличественного анализа производных изохинолина. Кафедра фармацевтической, токсикологической и аналитической химии
 Скачать 227.1 Kb. Скачать 227.1 Kb.
|
|
ФЕДЕРАЛЬНОЕ ГОСУДАРСВТЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ОБРАЗОВАНИЯ «КУРСКИЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ» МИНИСТЕРСТВА ЗДРАВООХРАНЕНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ Фармацевтический факультет КАФЕДРА ФАРМАЦЕВТИЧЕСКОЙ, ТОКСИКОЛОГИЧЕСКОЙ И АНАЛИТИЧЕСКОЙ ХИМИИ КУРСОВАЯ РАБОТА по дисциплине общая фармацевтическая химия Методы определения качества лекарственных средств, производных изохинолина Исполнитель: Брагина Юлия Константиновна, 5 курс, 2 группа. Руководитель Кукурека А.В., доцент кафедры фармацевтической, токсикологической и аналитической химии, канд-т фарм.н. Дата сдачи (защиты) курсовой работы______________ Оценка________________________________________ Подпись руководителя___________________________ Курск – 2022 Содержание Введение…………………………………………………………………………..3 Глава 1. Физико-химические свойства лекарственных средств производных изохинолина………………………………………………………………………5 Строение и синтез лекарственных средств группы производные изохинолина…………………………………………………………………..5 Методы качественного анализа производных группы изохинолина……. 1.3 Методы количественного анализа производных группы изохинолина… 1.4 Фармакологическое действие лекарственных средств из группы производные изохинолина……………………………………………………... Глава 2. Определение качества таблеток папаверина гидрохлорида……….. 2.1. Характеристика объекта исследования…………………………………… 2.2. Определение подлинности таблеток папаверина гидрохлорида………... 2.3. Количественное определение таблеток папаверина гидрохлорида……... 2.4. Статистическая обработка результатов анализа………………………….. Заключение………………………………………………………………………. Список литературы……………………………………………………………… ВведениеЛекарственные средства из группы производные изохинолина впервые были выделены и исследованы в первой половине XIX века. Изохинолиновые алкалоиды били обнаружены преимущественно в семействах Маковые, Барбарисовые, Мениспермовые и Лютиковые. Наиболее известными представителями лекарственных средств группы производных изохинолина являются морфин, папаверин, кодеин, и дротаверин. Производные изохинолина оказывают разнообразное фармакологическое действие на организм. Так, папаверина гидрохлорид применяется в медицине как спазмолитическое средство при спазмах гладких мышц органов брюшной полости, периферических сосудов, сосудов головного мозга, сердца и при бронхоспазме. Морфина гидрохлорид назначают как болеутоляющее. Кодеина фосфат применяется в качестве противокашлевого средства. Дротаверин применяется как спазмолитическое стредство. В настоящее время папаверина гидрохлорид выпускается в виде 2% раствора для инъекций, ректальных суппозиториев, а также в виде таблеток 40 мг; кодеина фосфат входит в состав многих противокашлевых комбинированных препаратов; морфина гидрохлорид – в виде раствора для инъекций 1мг/мл, раствора для приема внутрь и таблеток, покрытых пленочной оболочкой. В связи с широким применением лекарственных средств из группы производные изохинолина в медицине, знание физико-химических свойств, методик качественного и количественного анализа для проведения контроля качества является особо актуальным. Цель исследования – изучить основные методы определения качества лекарственных средств из группы производные изохинолина. Объекты исследования – таблетки папаверина гидрохлорида 40 мг. Задачи исследования: изучить строение, физико-химические свойства лекарственных средств из группы производные изохинолина; овладеть методиками качественного анализа производных изохинолина; овладеть методиками количественного анализа производных изохинолина; провести определение подлинности таблеток папаверина гидрохлорида; провести количественное определение таблеток папаверина гидрохлорида. Провести статистическую обработку результатов анализа. Методы исследования: - теоретические (анализ научной литературы); - эмпирические (проведение эксперимента); - математические (расчет результатов эксперимента). Глава 1. Физико-химические средства лекарственных средств из группы производных изохинолина. 1.1. Строение и синтез лекарственных средств из группы производные изохинолина. Изохинолин представляет собой гетероциклическое ароматическое органическое соединение. Это структурный изомер хинолина. Изохинолин и хинолин представляют собой бензопиридины, которые состоят из бензольного кольца, сплавленного с пиридиновым кольцом. Изохинолиновое кольцо образуется из ароматической аминокислоты тирозина. [25][26]. 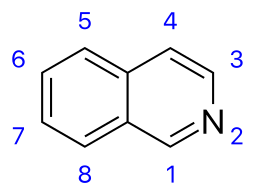 Рис.1 Строение изохинолина Изохинолин был впервые выделен из каменноугольной смолы в 1885 году Хоогеверфом и ван Дорпом. Они выделили его путем фракционной кристаллизации сульфата кислоты. Вайсгербер разработал более быстрый способ в 1914 году путем селективного извлечения каменноугольной смолы, используя тот факт, что изохинолин является более основным, чем хинолин. Затем изохинолин может быть выделен из смеси путем фракционной кристаллизации сульфата кислоты. Хотя производные изохинолина могут быть синтезированы несколькими способами, относительно немногие прямые способы доставляют незамещенный изохинолин. Реакция Померанца–Фрича обеспечивает эффективный метод получения изохинолина. В этой реакции используются бензальдегид и аминоацетоальдегид диэтилацеталь, которые в кислой среде вступают в реакцию с образованием изохинолина. В качестве альтернативы можно использовать бензиламин и ацеталь глиоксаля для получения того же результата с использованием модификации Шлиттлера-Мюллера.[11] 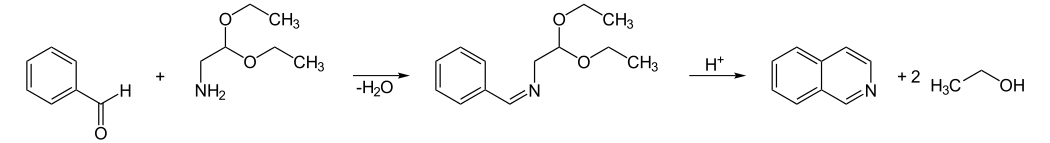 Рис.2 Реакция Шитлера- Мюллера. Несколько других способов полезны для получения различных производных изохинолина. В реакции Бишлера–Напиеральского β-фенилэтиламин ацилируется и циклодегидрируется кислотой Льюиса, такой как фосфорилхлорид или пятиокись фосфора. Полученный 1-замещенный 3,4-дигидроизохинолин затем может быть дегидрирован с использованием палладия. В результате следующей реакции Бишлера–Напиеральского образуется папаверин. 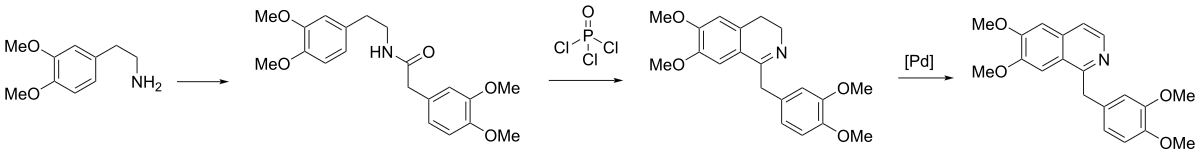 Рис. 3 Реакция Бишлера- Напиеральского. Химические свойства изохинолина заключаются в реакциях электрофильного и нуклеофильного замещения. Реакции электрофильного замещения происходят в положении 5. Бромирование легче протекает в присутствии AlCl3, нитрование идёт при действии серной и азотной кислот. Сульфирование при действии 40%-ного олеума при температуре 180оС приводит обычно к изохинолин-8-сульфокислоте. Сульфирование 60%-ной серной кислотой при 300оС ведёт к смеси изохинолин-5- и изохинолин-8-сульфокислот. [24] При высокой температуре изохинолин вступает в реакции бромирования по радикальному механизму с образованием 1-бромизохинолина. Нуклеофильное замещение протекает как правило в положение 1. С гидроксидом калия при 200оС изохинолин образует 1-гидроксиизохинолин, с амидом натрия — 1-аминоизохинолин. Папаверина гидрохлорид представляет собой белый кристаллический порошок со слегка горьковатым вкусом, без запаха. Температура плавления - 225ºС. Хорошо растворяется в воде, плохо - в этиловом спирте, хлороформе, диэтиловом эфире. 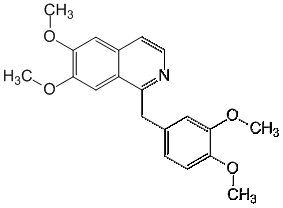 Рис. 4 Структурная формула папаверина гидрохлорида. Реакции электрофильного замещения протекают по наименее электронодефицитному бензольному кольцу и направляются в хинолине в положения 6 и 8. Нуклеофильные реагенты атакуют пиридиниевый цикл хинолина в положение 2. 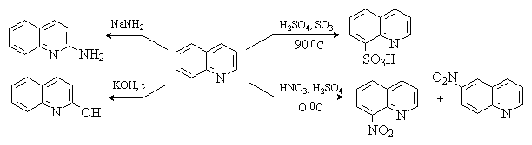 При каталитическом гидрировании хинолина в первую очередь затрагивается пиридиниевый цикл. При окислении разрушается бензольный цикл и образуется 2,3- пиридиндикарбоновая кислота. 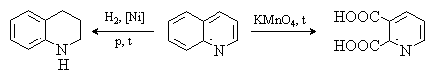 Процесс замещения атома водорода в хинолине и изохинолине на атом галогена достаточно сложный, и образование того или иного продукта реакции замещения зависит от условий проведения реакции. При бромировании в концентрированной серной кислоте хинолин образует смесь 5- и 8-бромпроизводных, а изохинолин в присутствии хлорида алюминия превращается в 5-бромизохинолин. Все эти процессы проходят с участием протонированных гетероциклов. Морфина гидрохлорид представляет собой белые игольчатые кристаллы или белый кристаллический порошок; слегка желтеющий или сереющий при хранении. Медленно растворим в воде, трудно растворим в спирте (1:50), несовместим со щелочами. [23] 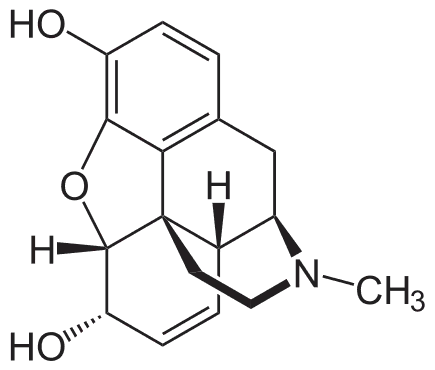 Рис. 5 Структурная формула морфина гидрохлорида. Впервые полный синтез морфина был осуществлён в 1952 году американским химиком Маршаллом Гейтсом. Синтез включал, в общей сложности, 31 стадию и имел крайне низкий выход конечного продукта (на уровне 0,06%). В дальнейшем был предложен ряд более совершенных методов синтеза морфина, но и в настоящее время природный морфин по-прежнему дешевле синтетического [10]. 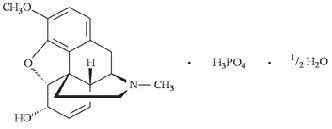 Рис. 6 Структурная формула кодеина фосфата. Кодеина фосфат представляет собой белый кристаллический порошок, без запаха, горького вкуса. На воздухе выветривается. Легко растворим в воде (1 г. вещества в 10 мл воды), мало или очень мало растворим в 96% спирте(0,01г. вещества в 10 мл спирта). Методы качественного анализа производных группы изохинолина Большинство реакций, подтверждающих подлинность папаверина, основаны на способности его окисляться, что обусловлено наличием в его молекуле метоксильных групп. В зависимости от характера окислителя продукты окисления окрашены в разные цвета. Так, например, при действии на препарат концентрированной азотной кислотой появляется желтое окрашивание, которое при нагревании на водяной бане переходит в оранжевое. При действии концентрированной серной кислотой продукты окисления окрашены в фиолетовый цвет. При действии бромной воды образуется осадок желтого цвета, с реактивом Марки (формальдегид-концентрированная серная кислота) - красное окрашивание, переходящее в желтое, а затем в ярко-оранжевое. В фильтрате подтверждается хлор-ион. [22] Папаверин образует осадки с реактивами группового осаждения алкалоидов. Реакция с хлоридом кадмия. На предметное стекло наносят несколько капель исследуемого раствора и выпаривают досуха. К сухому остатку прибавляют каплю 0,1 н. раствора соляной кислоты. Рядом наносят каплю 10 %-го раствора хлорида кадмия, а затем соединяют эти растворы. При наличии папаверина появляются сростки из тонких пластинок, имеющих форму куба. Морфин даёт осадки с реактивами группового осаждения алкалоидов (реактивы Бушарда, Драгендорфа, Майера, Зонненшейна и др.). Морфин даёт реакции с концентрированной азотной кислотой (кроваво-красное, переходящее в оранжево-жёлтое). С реактивом Эрдмана (концентрированная серная кислота с концентрированной азотной кислотой) даёт красно-жёлтое окрашивание. С реактивом Фреде (концентрированная серная кислота с молибденовой кислотой) даёт фиолетовое окрашивание. С реактивом Манделина (концентрированная серная кислота с ванадиевой кислотой) даёт фиолетовое окрашивание. [22] С реактивом Марки (концентрированная серная кислота и формальдегид) даёт фиолетовое окрашивание. Реакция конденсации с альдегидами. Реакция основана на способности кодеина фосфата образовывать с реактивом Марки комплексные соединения, окрашенные в сине - фиолетовый цвет, усиливающийся при стоянии. Реакция комплексообразования с ионами железа (III) Реакция основана на кислотных свойствах продукта гидролиза (морфина). Образуются комплексные соединения окрашенные в синий цвет, переходящий в красный при добавлении 1 капли азотной кислоты. Реакция на фосфат ион. Реакция основана на способности вещества осаждаться серебра нитратом. Образуется желтый осадок, растворимый в разведенной азотной кислоте и растворе аммиака. Н3РО4 + 3AgNO3 → AgPO4↓ + 3HNO3 Реакция с раствором молибдата аммония на фосфат ион. Реакция основана на способности вещества осаждаться молибдатом аммония. Выпадает желтый кристалический осадок. H3PO4 + 12(NH4)2MoO4 + 21HNO3 → (NH4)3PO4 • 12MoO3↓ + 21NH4NO3 + 12H2O Реакция основана на способности вещества образовывать с магнезиальной смесью белый осадок растворимый в разведенных минеральных кислотах и уксусной кислоте. [3] Н3PO4 + MgSO4 + 3NH4OH + NH4CI → MgNH4PO4↓ + (NH4)2SO4 + 3H2O Реакция с реактивом Драгендорфа. Реакция основана на основных свойствах третичного атома азота в составе кодеина фосфата. Образуются соединения кармино-красного цвета. [12] Реакция с реактивом Эрдмана. Реакция основана на способности кодеина фосфата окисляться под действием концентрированных серой и азотной кислот. Образуется осадок интенсивного краснного цвета. [3] Методы количественного анализа производных группы изохинолина.Метод кислотно-основного титрования в среде протогенного растворителя (прямое титрование).Метод основан на способности протогенного растворителя усиливать слабые основные свойства третичного атома азота. Титрант - раствор кислоты хлорной в ледяной уксусной кислоте. Индикатор - кристаллический фиолетовый. Титрование ведется до голубовато - зеленого окрашивания | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| | Объем титранта, пошедшего на титрование V, мл | Содержание папаверина гидрохлорида в ЛФ Х, г | Отклонение результатов 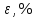 | НДО, % |
| 1 | 1,54 | 0,0403 | -0,74 | 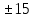 |
| 2 | 1,50 | 0,0390 | -3,94 | |
| 3 | 1,52 | 0,0398 | -1,97 | |
| 4 | 1,56 | 0,0409 | 0,74 | |
| 5 | 1,62 | 0,0424 | 4,43 | |
| 6 | 1,58 | 0,0414 | 1,97 |
Максимальное содержание рибофлавина в лекарственной форме составляет 0,0424 г, минимальное - 0,0390 г. Данные показатели находятся в пределах нормы допустимых отклонений.
В результате проведенного анализа, можно заключить, таблетки папаверина гидрохлорида 40 мг соответствуют требованиям нормативной документации по показателю «Количественное определение». Полученные значения по всем образцам находятся в пределах нормы допустимых отклонений.
2.4 Статистическая обработка результатов анализа.
Для подтверждения результатов количественного определения была проведена их статистическая обработка в соответствии с ОФС.1.1.013.15 «Статистическая обработка результатов химического эксперимента» [5].
Мы провели расчет статистических характеристик по формулам, представленным в шапке таблицы. (Таблица 2).
Таблица 2 – Расчет статистических характеристик для таблеток папаверина гидрохлорид 40 мг
| № п/п | Найдено | Среднее значение выборки 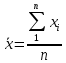 | Отклонение от среднего значения 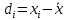 | 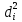 | 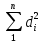 | |
| Сод-е в г | % от номинальной концентрации, Хi | |||||
| 1 | 0,0403 | 100,75 | 101,5 (0,0406) | -0,75 | 0,56 | 45,37 |
| 2 | 0,0390 | 97.5 | -4 | 16 | ||
| 3 | 0,0398 | 99,5 | -2 | 4 | ||
| 4 | 0,0409 | 102,25 | 0,75 | 0,56 | ||
| 5 | 0,0424 | 106 | 4,5 | 20,25 | ||
| 6 | 0,0414 | 103,5 | 2 | 4 | ||
Для проверки однородности выборки были проведены расчеты размаха варьирования и контрольных критериев идентификации грубых ошибок для всех лекарственных форм, полученные результаты представлены в Таблице 3.
Таблица 3 – Проверка однородности выборки
| Образец | Размах варьирования, R=|X6-X1| | Контрольные критерии идентификации грубых ошибок 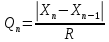 | ||||
| Q1 | Q2 | Q3 | Q4 | Q5 | ||
| №1 | 0,0011 | 1,181 | 0,727 | 1 | 1,364 | 0,909 |
| №2 | 0,0024 | 0,542 | 0,333 | 0,458 | 0,625 | 0,417 |
| №3 | 0,0016 | 0,8125 | 0,5 | 0,6875 | 0,9375 | 0,625 |
| №4 | 0,0005 | 2,3 | 1,6 | 2,2 | 3 | 2 |
| №5 | 0,001 | 1,3 | 0,8 | 1,1 | 1,36 | 1 |
Выборка признается неоднородной, если хотя бы одно из вычисленных значений Q превышает табличное значение Q (Р,n) = 2,44, найденное с доверительной вероятностью Р = 95% и n = 6.
Значения, для которых контрольный критерий превышает табличное значение Q > Q (Р,n) , являются промахами или грубыми ошибками, отбрасываются и для полученной выборки уменьшенного объема выполняют новый цикл вычислений.
Исходя из полученных результатов, мы видим, что выборка является однородной, а следовательно, результаты, полученные при статистической обработке выборки, будут достоверны.
Полученные данные были использованы для расчета метрологических характеристик. Для этого использовались следующие формулы:
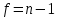 (3)
(3)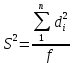 (4)
(4)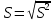 (5)
(5)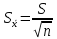 (6)
(6)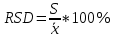 (7)
(7)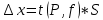 (8)
(8)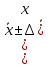 (9)
(9)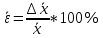 (10)
(10)Полученные результаты представлены в Таблице 4 .
Таблица 4 – Метрологические характеристики среднего результата
| Число опытов, n | Число степеней свободы, 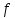 | Среднее арифметическое в выборке, 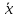 | Выборочная дисперсия, S2 | Среднеквадратическое отклонение, S | Стандартное отклонение среднего результата, 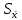 | Относительное стандартное отклонение, RSD | Доверительная вероятность, P | Критерий Стьюдента, T(P, 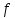 ) ) | Полуширина доверительного интервала, 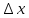 | Граничные значения доверительного интервала, 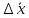 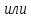 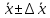 | Относительная погрешность среднего результата, 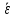 | ||||||||
| 1 | 5 | 0,0406 | | | 1,48 | 3,66 | 95% | 2,44 | 9,300 | 98,83 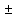 3,80 3,80 | 3,84 | ||||||||
| 1 | 5 | 0,0406 | | | 3,40 | 8,61 | 95% | 2,44 | 21,430 | 96,90 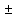 8,75 8,75 | 9,03 | ||||||||
| 1 | 5 | 0,0406 | | | 3,88 | 9,47 | 95% | 2,44 | 24,415 | 100,33 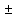 9,97 9,97 | 9,94 | ||||||||
| 1 | 5 | 0,0406 | | | 1,67 | 4,15 | 95% | 2,44 | 10,490 | 98,33 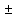 4,28 4,28 | 4,36 | ||||||||
| 1 | 5 | 0,0406 | | | | | | | | | | ||||||||
| 1 | 5 | 0,0406 | | | | | | | | | | ||||||||
Величина систематической ошибки составила:
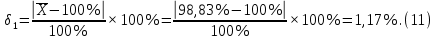
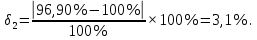
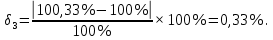
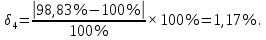
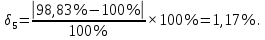
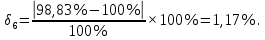
Заключение
Лекарственные средства из группы производные изохинолина играют важную роль в жизни человека. Они широко применяются в медицине благодаря тому, что обладают различным фармакологическим действием.
В результате проведенного исследования были изучены физико-химические и фармакологические свойства лекарственных средств из группы производные изохинолина: папаверина гидрохлорида, морфина гидрохлорида, кодеина фосфата; а также метод их качественного и количественного анализа.
Подлинность таблеток папаверина гидрохлорида 40 мг подтвердили с помощью химических тестов. По результатам анализа сделали вывод, что препарат соответствует требованиям нормативной документации по показателю «подлинность».
Количественное определение таблеток папаверина гидрохлорида 40 мг проводили алкалиметрическим титрованием. В результате шести независимых исследований содержание папаверина гидрохлорида в таблетках оказалось в пределах нормы (N= 0,038-0,042 г). Соответственно, сделали вывод, что препарат соответствует требованиям нормативной документации по показателю «количественное определение».
Выполнили статистическую обработку результатов количественного определения папаверина гидрохлорида в таблетках. Граничные значения доверительного интервала для фурацилина составили 98,83 ± 3,80 и 96,90 ± 8,75; для рибофлавина 100,33 ± 9,97 и 98,33 ± 4,28. Максимальное значение относительного стандартного отклонения равно 9,47%, что не превышает предельного значения ± 20%.
Таким образом, в ходе проведения эксперимента, мы доказали, что таблетки папаверина гидрохлорида 40 мг соответствуют требованиям нормативной документации.
Список литературы
Аксенова, Э.Н. Фармацевтическая химия / Э.Н.Аксенова, О.П.Андрианова, А.П. Арзамасцев. ̶ Учебное пособие. ̶ Изд-во: ГЭОТАР-Медиа. – 2008. ̶ 640с.
Афонина, Н. Д. Методическое пособие для выполнения самостоятельной работы студентами 4 курса фармацевтического факультета : учеб. пособие для студентов, обучающихся по специальности 040500 – «Фармация» / Н. Д. Афонина, Л. Е. Сипливая. – Курск : Изд-во КГМУ, 2009. – 101 с.
Беликов, В. Г. Фармацевтическая химия : учебное пособие для студентов, обучающихся по специальности 060108 (404500) – «Фармация» / В. Г. Беликов, 2009, МЕДпресс-информ. – 615 с.
Гилкрист, Т.Л. (1997). Гетероциклическая химия (3-е изд.). Эссекс, Великобритания: Эддисон Уэсли Лонгман.
Глущенко Н.Н. Фармацевтическая химия: Учебник для студ. сред. проф. учеб. заведений / Н.Н. Глущенко, Т.В. Плетенева, В.А. Попков; Под ред. Т.В. Плетеневой. – М.: Издательский центр «Академия», 2004. – 384 с.
Государственная фармакопея Российской Федерации XIV издание. М., 2018. Федеральная электронная медицинская библиотека. [Электронный ресурс]. – URL: – http://www.femb.ru/feml (дата обращения 15.06.2022).
Государственный реестр лекарственных средств [Электронный ресурс]. Режим доступа: https://grls.rosminzdrav.ru (дата обращения 15.06.2022).
Кнорре, Д. Г. Биологическая химия / Д. Г. Кнорре, С. Д. Мызина. – Москва: Высшая школа, 2000. – 479 с.
Кобзарь, А.Н. Аналитическая химия. Аналитика / А.Н. Кобзарь // Аналитическая химия. Оборудование лабораторий. – 2005. – № 12. – С. 4-6
Кредик С.А. Алкалоиды: синтез, методы выделения и анализа / С.А. Кредик – М.: Высшая школа, 2002. – 380 с.
Кузнецова А.В. Фармакопейный анализ производных фурана, пиррола, пиразола, имидазола, пиридина, хинолина. Учебное пособие для студентов 4 курса специальности «Фармация» - Пензенский государственный университет. – 2013. – с. 99.
Ли, Джей Джей (2014). "Schlittler–Müller modification". Название Реакции: Сборник подробных механизмов и синтетических приложений (5-е изд.). Спрингер. с. 492.
Методическое пособие «Фармацевтический анализ по функциональным группам и общие титриметрические методы анализа». - г. Пермь, 2011. - 95 с.
Петрухина, В.Н. Актуальные проблемы теоретической и клинической медицины / В.Н. Петрухина, Н.Ю. Стрельцова, К.А. Чекотаева // Донецкий национальный медицинский университет имени М. Горького. – 2020. – С. 505-506
Практикум по фармацевтической химии для студентов 5 курса фармацевтического факультета по специальности "Фармация" / А.В. Нестерова [и др.]. – Курск : КГМУ, 2017.
Практическое руководство для лабораторий: Специальные методы: пер. с нем. / под ред. И. Г. Зенкевича, Н. А. Шурдуба, И. В. Болдырева. – Профессия, 2014. – 470 с.
Сипливая, Л. Е. Методическое пособие для самоподготовки и выполнения лабораторно-практических работ по фармацевтической химии для студентов 4 курса / Л. Е. Сипливая, Н. Д. Афонина. – Курск : Изд-во КГМУ, 2004. – 84 с.
Кукурека А.В., Сипливая Л.Е. Лекарственные средства, содержащие гетероциклы. Практикум для студентов фармацевтического факультета по специальности «Фармация»// Курск: Издательство КГМУ, 2019. – 264 с.
Справочник лекарственных средств Vidal [Электронный ресурс]. – Режим доступа: https://www.vidal.ru/drugs/papaverine__21403#influence
. – Дата доступа: 18.06.2022.
Справочник лекарственных средств Vidal [Электронный ресурс]. – Режим доступа: https://www.vidal.ru/drugs/morphine__5361#influence . – Дата доступа: 18.06.2022.
Справочник лекарственных средств Vidal [Электронный ресурс]. – Режим доступа: https://www.vidal.ru/drugs/molecule/262#influence / - Дата доступа – 18.06.22.
Фармацевтическая химия [Электронный ресурс] : учебное пособие / под ред. А. П. Арзамасцева. – 2-е изд., испр. – М. : ГЭОТАР-Медиа, 2008. – URL: http://www.studmedlib.ru
Фармацевтическая химия [Электронный ресурс]: учебник / Э. Н. Аксенова [и др.]. – Электрон. текстовые данные. – М. : БИНОМ. Лаборатория знаний, 2015. – 468 c.: URL: http://www.iprbookshop.ru/42305 (дата обращения 16.06.2022).
Фармацевтическая химия: учеб. пособие для студентов мед. вузов, обучающихся по специальности 040500 – «Фармация» / под ред. А. П. Арзамасцева. – 3-е изд., испр. – М. : ГЭОТАР-Медиа, 2006. – 635 с.
Функциональный анализ [Электронный ресурс]: учеб.-метод. пособие для студентов фармацевт. фак. очного и заочного обучения / А. В. Нестерова, Б. В. Кузьмин, Н. Д. Огнещикова: под ред. Л.Е. Сипливой. – Курск : [б. и.], 2012. – 1 эл. опт. диск (CD-ROM). URL: http://library.kursksmu.net/cgi-bin/irbis64r_15/cgiirbis_64.exe?LNG=&P21DBN=MIXED&I21DBN=MIXED_PRINT&S21FMT=fullw_print&C21COM=F&Z21MFN=15859
Пожарский А.Ф. (2000). Справочник по гетероциклической химии (2-е изд.). Оксфорд, Великобритания: Elsevier.
Титриметрические методы анализа: основные понятия, термины и расчеты: методические указания / сост.: Т.Е. Гулимова. - Рязань: РГМУ, 2000. - 25 с.
Фармакология / Под ред. Д.А. Харкевича. – 10-е изд. перераб. и доп. – М. : ГЭОТАР-медиа, 2010. – 908 с.

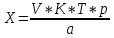 (2)
(2)