Каталитическая конверсия природного газа в синтезгаз. Паровая, углекислотная конверсия метана. Парциальное окисление метана. Основные и побочные реакции. Катализ. Технологическая схема производства синтезгаза автотермической конверсией метана
 Скачать 1.72 Mb. Скачать 1.72 Mb.
|
|
По дисциплине «Каталитические процессы переработки лёгкого углеводородного сырья» Каталитическая конверсия природного газа в синтез-газ. Паровая, углекислотная конверсия метана. Парциальное окисление метана. Основные и побочные реакции. Катализ. Технологическая схема производства синтез-газа автотермической конверсией метана. Паровая конверсия метана: Основная реакция: СН4 + Н2О = СО + 3Н2 – каталитическая, обратимая, с большим поглощением тепла, с увеличением объема реакции, на выходе Н2 : СО = (3 и выше) : 1; Кр=1 при 780оС; Избыток Н2О снижает коксообразование; – Рраб = 2…3 МПа, хотя равновесие смещено влево, но скорость реакции растет и последующие синтезы из синтез газа ведут под давлением. Побочная реакция: СО + Н2О = СО2 + Н2 Катализаторы: переходные металлы 8ой группы (Активность Rh, Ru, Ni, Ir, Pd. Pt, Co,Fe) Но Rh и Ru дорого применять, Co и Fe окисляются и дезактивируются. Углекислотная конверсия метана. Основная реакция: СН4 + СО2 = 2СО + 2Н2 Реакция – с поглощением тепла, с увеличением реакционного объема. – скорость меньше, чем у паровой, – На выходе Н2 : СО = 1 : 1 Побочная реакция: СН4 + 2СО2 = С + 2СО + 2Н2О Катализ: переходные металлы 8ой группы ( Rh, Ni, Pt, Pd. Ir, Ru), Носители: Al2O3, ThO2, SiO2, MgO Для снижения закоксовывания катализатора добавляют 0,01…2% благород. металла. Парциальное окисление метана. СН4 + ½ О2 = СО + 2Н2 3 варианта проведения процесса: 1. При увеличении времени контакта и небольшой объемной скорости: Т = 750-900 С; Р = 1 атм, Соотн. СН4 : О2 = 2 : 1, катализатор – Ni на носителе. В первых слоях катализатора – глубокое окисление: СН4 + 2О2 = СО + 2Н2О, В последних слоях – углекислотная и паровая конверсии. Побочные реакции: СО + Н2О = СО2 + Н2. СО2 + Н2 = СО + Н2О. СН4 + 1,5О2 = СО + 2Н2О Недостатки: высокая стоимость О2, взрывоопасность, возможен перегрев катализатора и его дезактивация, закоксовывание катализатора. 2. При малом времени контакта и высокой объемной скорости: Катализатор – металлическая сетка; Время контакта 10-5…10-1 с. Нет реакций углекислот. и паровой конверсий. конверсия метана практически 100%. Размеры реактора минимальны 3. Гомогенное некаталитическое окисление. T = 1100…1300 С На выходе Н2 : СО = 2:1 Тех.схема: Исходный метан, сжимают турбокомпрессором 1 до 2…3 МПа и смешивают с водяного пара и СО2. Смесь подогревают в теплообменнике 2 и подают в смеситель конвертора 3, куда поступает предварительно приготовленная смесь кислорода с равным объёмом водяного пара. охлаждение синтез-газа осуществляют в скруббере 6 водой, циркулирующей через холодильник 8 насосом 7. П 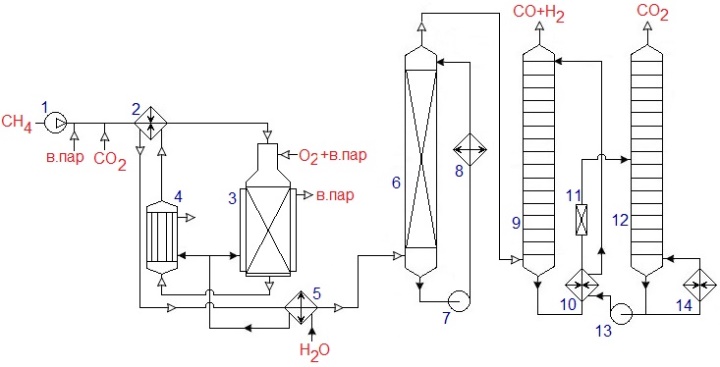 олученный синтез-газ поступает далее в абсорбер 9, где происходит очистка от СО2 хемосорбцией водным раствором моноэтаноламина (МЭА) или карбоната калия. олученный синтез-газ поступает далее в абсорбер 9, где происходит очистка от СО2 хемосорбцией водным раствором моноэтаноламина (МЭА) или карбоната калия. Полученный синтез-газ поступает далее в абсорбер 9, где происходит очистка от СО2 хемосорбцией водным раствором моноэтаноламина (МЭА) или карбоната калия. Химизм процесса заключается во взаимодействии МЭА с CO2 и образованием химических соединений. Очищенный синтез-газ выходит с верха абсорбера. Насыщенный раствор абсорбента выходит с низа абсорбера, нагревается в теплообменнике 10 и поступает через дроссель в десорбер 12. С верха десорбера уходит СО2, с низа – регенерированный абсорбент, который насосом 13 через теплообменник 10 опять подают на верх абсорбера. СО2 компримируют до соответствующего давления и возвращают на конверсию, смешивая с метаном и водяным паром перед теплообменником 2. Производство метанола из синтез-газа. Химизм и катализ. Варианты реакционных узлов синтеза метанола. Технологическая схема производства метанола из синтез-газа. Химизм и катализ. СО + 2Н2 = СН3ОН Катализаторы: СuO·Cr2O3; ZnO·СuO·Cr2O3, Механизм: К + СО ↔ К = С = О (+Н2)↔ К = СНОН (+Н2)↔ К + СН3ОН, Реакция – обратимая, с уменьшением числа молей, с выделением тепла. Побочные реакции: СО + 3Н2 → СН4 + Н2О, СО + Н2О → СО2 + Н2, СН3ОН → СН4 + Н2О Образование более тяжелых УВ и спиртов (С2-С4): nCO + (2n+1)H2 → CnH2n+2 + nH2O nCO + 2nH2 → CnH2n+1OH + (n-1)H2O Параметры: Т = 250 – 420 С – зависит от активности катализатора. Чем выше Т, тем выше Р. Варианты реакционных узлов. 1. Трубчатый реактор Конструкция – кожухотрубчатый ТО, катализатор и реакционная масса в трубках, в межтрубном пространстве – кипящая вода. Высокая металлоемкость реактора – на реакц. зону приходится небольшая часть общ.объема реактора. 2. Адиабатический реактор несколько неподвиж.слоя катализатора. Теплообменные устройства отсутсвтуют, съем тепла подачей холодного синтез-газа между слоями катализатора. Для подогрева сырья используют только часть реакц.газов. Основ.масса тепла идет на выработку пара. 3. Реактор синтеза в трехфазной системе (эмульсионный) Процесс в жидкой фазе инертного УВ. Катализатор – гетерогенный, в виде суспензии в жидкости. Тепло реакции отводится циркуляцией жидкости через парогенератор. Снижаются расходы на рецикл синтез-газа. Тех.схема: Очищенный синтез-газ сжимают турбокомпрессором 1 и смешивают с циркулирующим газом, который дожимают до рабочего давления турбокомпрессором 8. Смесь проходит адсорбер 2, где очищается от пентакарбонила железа. После адсорбера газ разделяют на два потока: один подогревают в теплообменнике 4 и подают на синтез в верхнюю часть реактора 3, а другой вводят в реактор 3 между слоями катализатора в холодном виде для регулирования температуры и отвода тепла. 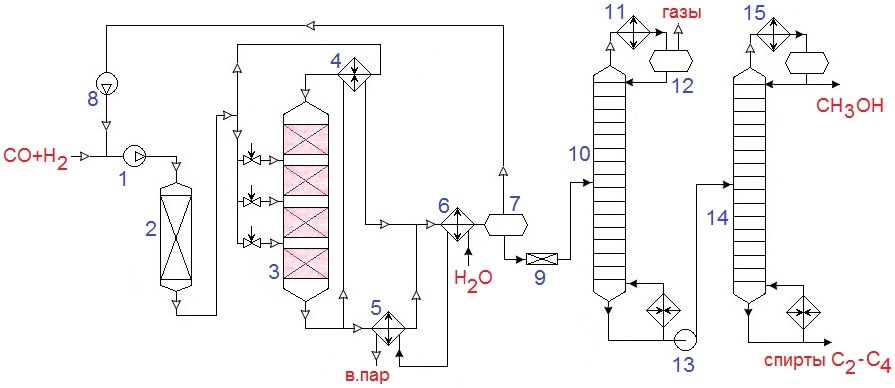 Газ проходит сверху вниз через все слои катализатора и выходит из реактора. Этот газ тоже разделяют на два потока: один проходит теплообменник 4 и служит для подогрева части исходной смеси до температуры синтеза, а другой направляют в парогенератор 5, где его тепло используют для получения пара высокого давления. Потоки газа после этого объединяют и охлаждают в холодильнике 6, где метанол конденсируется и отделяется от газа в сепараторе 7 высокого давления. Газ с верха сепаратора дожимают компрессором 8 и возвращают на синтез. Конденсат с низа сепаратора дросселируют в 9 и в ректификационной колонне 10 отделяют метанол от растворённых газов и летучих продуктов , которые уходят с верха колонны через холодильник 11 и поступают в рефлюксную ёмкость 12. Остаток колонны 10 насосом 13 подаётся в колонну 14. С верха колонны отбирается метанол, с низа колонны – тяжёлые примеси. Технология GTL. Назначение, химизм процесса. Основные и побочные реакции. Катализ. Варианты реакторов процесса. Применение продуктов технологии GTL. Назначение – превращение синтез-газа в высшие УВ (получение синтетической нефти из синтез-газа) Химизм процесса. Основные и побочные реакции: Основные продукты: парафины и линейные а-олефины С1…С100 и выше. nCO + (2n+1)H2 → CnH2n+2 + nH2O nCO + 2nH2 → CnH2n + nH2O Могут образовываться О-содерж.соединения: спирты, кетоны, альдегиды, карбоновые кислоты. Побочные реакции: Метанирование СО + 3Н2 → СН4 + Н2О Диспропорционирование СО: 2СО →С + СО2 Реакция вод. пара: СО + Н2О ↔ СО2 + Н2 Катализ: Металлы 8ой группы: Co, Fe, Ni, Ru; носители: Al2O3, SiO2, цеолиты; промоторы: оксиды или соли щелочных металлов Со-катализатор Т = 180..240 С, Р = 0,1…1,0 МПа, образуется 80% и выше н-парафинов, 15-20% н-олефинов, около 5% изо-парафинов, изо-олефинов и О-сод.соединений. ДТ обладает высоким ЦЧ. Инертность к реакции вод.пара, при t>240 С растет выход метана. Fe-катализатор Т = 200..350 С, Р = 2,5…4,0 МПа. образуется до 50% н-олефинов и О-сод.соединений. Бензин обладает более высоким ОЧ. Варианты реакторов процесса: 1. Трубчатый реактор Конструкция – кожухотрубчатые ТО. Катализатор в виду гранул – в трубках, в межтрубном пространстве – кипящая вода. Недостаток: из-за смачиваемости частиц катализатора продуктами реакции образуются агломераты и застойные зоны. 2. Реактор с псевдоожиженным слоем катализатора – традиционный вариант реактора с кипящим слоем катализатора. Недостатки: образование пленки на поверхности частиц катализатора, слипание частиц, внутридиффузионные торможения, локальные зоны перегрева. 3. Реактор с псевдоожиженным циркулирующим слоем катализатора Конц-ция катализатора в реакц.объеме 100-200 кг/м3; производительность 450-500 т/год Недостатки: сложность и дороговизна конструкции, низкая конц-ция катализатора в реакц.объеме, образование пленки на поверхности частиц катализатора, слипание частиц, ухудшение гидродинамических характеристик слоя. 4. Суспензионный реактор реакция протекает в суспензии частиц катализатора (трехфазная система). синтез-газ в виде пузырьков проходит через суспензию, процессы внутр.диффузии не влияют на скорость и селективность реакции Недостатки: невысокая конц-ция катализатора в суспензии, большая высота реактора, сложная стадия отделения продуктов реакции от катализатора. Применение продуктов технологии GTL Этилен. пропилен применяются в качестве базовых мономеров, бензин идет на облагораживание и пиролиз, дизтопливо используется для получения моторного топлива с высоким ЦЧ, тяжелые парафины высокой чистоты применяются при получении синтетических масел, в пищевой и парфюмерной промышленностях. высшие олефины используются в производстве ПАВ, а О-содержащие соединения применяются для получения ацетона, этанола, уксусной кислоты. Производство водорода паровой каталитической конверсией лёгких углеводородов. Основные и побочные реакции. Катализ. Технологические стадии процесса. Технологическая схема производства водорода. 1) Первая стадия – основная реакция: СН4 + Н2О ↔ 3Н2 + СО. СnHm + nH2O ↔ (n+m/2)H2 + nCO Может идти без катализатора при 1250-1350 С, с катализатором при 800-900 С. Катализатор: Ni на Al2O3 с добавками CaO, MgO Побочные: СnHm ↔ (m/2)H2 + nC 2) Вторая стадия – конверсия СО: СО + Н2О ↔ СО2 + Н2 Проводят в 2 ступени: 1. При 480-530 С на Fe-Cr-катализаторе – среднетемпературная конверсия; 2. При 400-450 С на Zn-Cu-катализаторе – низкотемпературная конверсия. 3) Третья стадия – метанизация (удаление остатков СО и СО2): СО + 3Н2 ↔ СН4 + Н2О СО2 + 4Н2 ↔ СН4 + 2Н2О Катализатор: Ni на Al2O3 с промоторами Cr2O3, MgO. Технологические стадии процесса: Сырье → гидроочистка → паровой риформинг УВ → двухступенчатая конверсия СО → Очистка от СО2 хемосорбцией К2СО3 → метанирование → водород Технологическая схема процесса: Сырье (газ) сжимают компрессором 1, подогревают в подогревателе, расположенном в конвекционной секции печи 2, до температуры 300…400 °С и подают в реакторы 3 и 4 для очистки от соединений серы. В реакторе 3, заполненном алюмокобальтмолибденовым (Al-Co-Mo) катализатором, осуществляется гидрогенолиз сернистых соединений, в реакторе 4 – адсорбция образующегося в реакторе 3 сероводорода. К очищенному газу добавляют водяной пар, перегретый до 400…500°С в пароперегревателе, также расположенном в конвекционной секции печи 2. 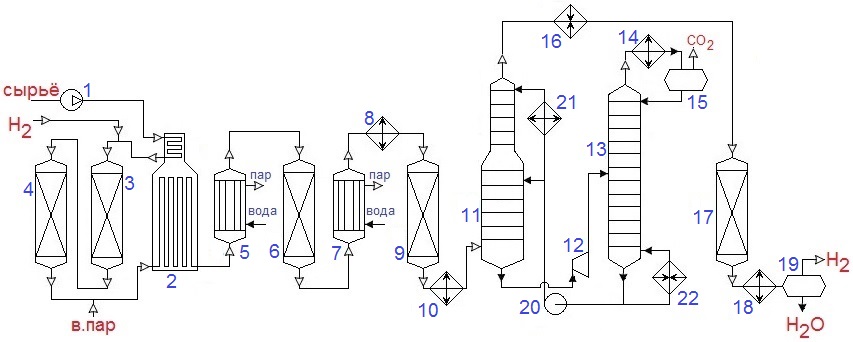 Полученная парогазовая смесь поступает в печь паровой конверсии 2. Парогазовая смесь с температурой 400…500°С подается в реакционную трубу через верхний коллектор, а конвертированный газ отводится снизу. Конвертированный газ, охладившийся до 400…450°С в паровом котле-утилизаторе 5, поступает в реактор 6 среднетемпературной конверсии CO в CO2 над железохромовым катализатором. После понижения температуры в котле-утилизаторе 7 и подогревателе воды 8 парогазовая смесь поступает в реактор 9 низкотемпературной конверсии СО над цинк-медным катализатором. Смесь водорода, диоксида углерода и водяного пара охлаждают далее в теплообменнике 10 и направляют в абсорбер 11 на очистку горячим водным раствором карбоната калия от диоксида углерода методом хемосорбции. Насыщенный диоксидом углерода раствор поступает из абсорбера 11 в турбину 12, где его давление снижается, а затем в десорбер 13. Здесь в результате подогрева раствора в теплообменнике 22 и снижения давления гидрокарбонат калия разлагается (реакция идёт в обратную сторону), из раствора выделяется диоксид углерода и вместе с парами воды выводится в атмосферу через холодильник 14 и рефлюксную ёмкость 15. Из ёмкости 15 сконденсировавшаяся вода возвращается в десорбер. Вместо карбоната калия для удаления СО2 можно использовать раствор моноэтаноламина. Водородсодержащий газ из абсорбера 11 подогревается до 300 °С в теплообменнике 16, поступает в реактор метанирования 17, где непревращенный оксид и неудаленный диоксид углерода гидрируются с образованием метана. После метанирования водород охлаждается в теплообменных аппаратах 18 до 30…40 °С и далее в сепараторе 19 отделяется от сконденсировавшегося водяного пара. Далее водород компримируют до давлений, требуемых потребителю. Процесс «Цеоформинг». Назначение процесса, основные реакции. Катализ. Параметры процесса. Технологическая схема процесса «Цеоформинг». Назначение – безводородный процесс каталитической переработки прямогонных фракций бензинов, газовых конденсатов в высокооктановый бензин. Основные и побочные реакции: 1. Крекинг: С8Н18 →С5Н12 + С3Н6 2. Олигомеризация олефинов: 2С2Н4 → С4Н8 3. Изомеризация: а) н-парафинов (образование ответвлений) б) олефинов (образование ответвление или изменяется положение кратной связи) в)нафтенов г) диалкилбензолов 4. Дегидрирование нафтенов: С6Н12 → С6Н6 + 3Н2 5. Коксообразовани 6. Алкилирование парафиновых и ароматических ув 7. Диспропорционирование спиртов и алкилбензола Катализаторы: Цеолитсодержащие катализаторы. позволяют перерабатывать негидроочищенное сырье. НК-30-1 высококремноземный цеолитсодержащий катализатор типа пентасил КН-30 на основе цеолита ZSM-5 высокая термостабильность, не содержит драгоценных металлов, не вызывает коррозию. Параметры процесса: Температура: происходит снижение tн.к. и увеличение tк.к. катализата. При увеличении Т с 300 до 450 с: – снижается выход целевого бензина; – растет выход С1-С; – снижается выход н-парафинов от С7 и выше, нафтенов; – растет выход ароматики, изопарафинов Сначала 320 конец 450 Давление: При увеличении Р с 0,2 до 1,0 МПа: – растет выход ароматики; – снижается выход н-парафинов от С7 и выше; – выход целевого бензина проходит через максимум. При повышении давления более 3 МПа: – снижается выход целевого бензина; – снижается ОЧ бензина Объемная скорость подачи сырья: При увеличении w более 3 ч-1: – снижается выход целевого бензина; – снижается ОЧ бензина Технологическая схема процесса: Сырьё – прямогонная бензиновая фракция или стабильный газовый конденсат нагревается сначала в теплообменнике 1, затем в печи 2 и подаётся сверху вниз в реактор 3 или 4, который находится на стадии реакции. Реакционные газы с низа реактора направляются в теплообменник 1, где они отдают часть своего тепла сырью, затем охлаждаются в воздушном холодильнике-конденсаторе 5. Далее продукты реакции проходят дроссель, и поступают в сепаратор 6, где отделяется несконденсировавшийся газ, который используется как топливо. С низа сепаратора 6 нестабильный бензин подаётся сначала в теплообменник 7, затем в паровой нагреватель 8 и далее в стабилизационную колонну 9. В колонне 9 происходит отделение пропан-бутановой фракции, которая уходит с верха колонны через АВО 10 и рефлюксную ёмкость 11. С низа колонны 9 стабильный бензин через дроссель (на схеме не показан) поступает в колонну 13 вторичной перегонки. С верха колонны 13 отводится целевой продукт – высокооктановый бензин, который через теплообменник 7, АВО 14 поступает в рефлюкс 15. Часть бензина идёт на орошение колонны 13. С низа колонны 13 отводится тяжёлая фракция 180оС – к.к. 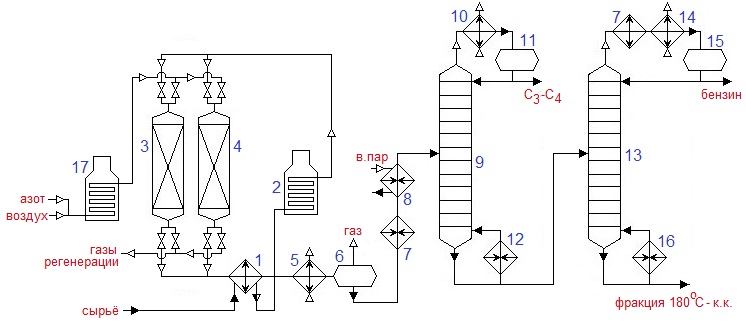 Процесс «Циклар». Назначение процесса, основные и побочные реакции. Катализ. Параметры процесса. Технологическая схема процесса «Циклар». Назначение – каталитический процесс ароматизации пропан-бутановой фракции, получение бензола. толуола, ксилолов нефтехим. качества. Основные и побочные реакции: основные реакции: 1. Дегидрирование пропана и бутана: С3Н8 → С3Н6 + Н2; 2. Олигомеризация. циклизация и дегидрирование:2С3Н6 → С6Н12 → ц-С6Н12 → С6Н6 + 3Н2 побочные реакции: 1. Крекинг пропана и бутана: С3Н8 → С2Н4 + Н2 2. крекинг олигомеров: Cm+nH2(n+m) → Cm+H2m + CnH2n 3. коксообразование: CnHm → C + H2 + CH4 образованные этилен бутилен пропилен могут участвовать в целевых реациях. 4. Гидрирование олефинов Катализ: Высококремниевый цеолит типа ZSM-5 на носителе 0,01-2,0% Zn и Ga, Другие актив.компоненты: Pt, оксиды Al, Cr, Катализатор высокотермоустойчивый и малочувствителен к примесям. Параметры процесса: С увеличением давления: – растет скорость реакции; – снижается необходимое количество катализатора; – повышается доля реакций гидрокрекинга, снижая выход ароматики. Технологическая схема процесса: С 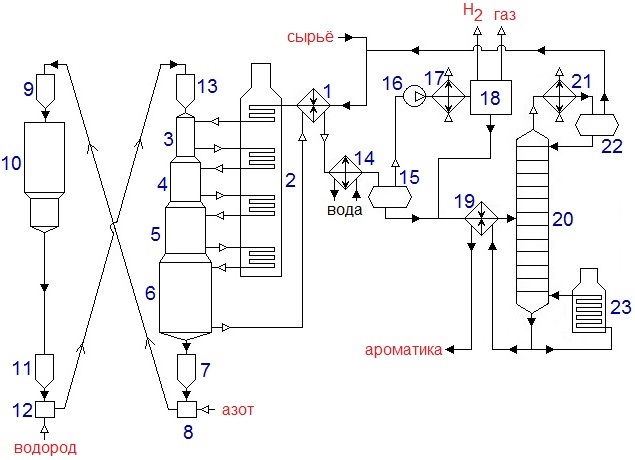 вежее сырьё и рециркулирующий поток углеводородов С3-С4 смешиваются и подогреваются в теплообменнике 1 реакционными газами. Затем объединённое сырьё нагревается в первой секции многопоточной печи 2 до температуры реакции и подаётся в реактор 3. Четыре адиабатических реактора 3, 4, 5 и 6 имеют соосную конфигурацию. Катализатор под действием силы тяжести опускается вертикально вниз, в то время как загруженное сырьё подаётся радиально через кольцеобразные слои катализатора. Так как реакция идёт с большим поглощением тепла, между реакторами сырьё подогревается в соответствующих секциях печи 2. вежее сырьё и рециркулирующий поток углеводородов С3-С4 смешиваются и подогреваются в теплообменнике 1 реакционными газами. Затем объединённое сырьё нагревается в первой секции многопоточной печи 2 до температуры реакции и подаётся в реактор 3. Четыре адиабатических реактора 3, 4, 5 и 6 имеют соосную конфигурацию. Катализатор под действием силы тяжести опускается вертикально вниз, в то время как загруженное сырьё подаётся радиально через кольцеобразные слои катализатора. Так как реакция идёт с большим поглощением тепла, между реакторами сырьё подогревается в соответствующих секциях печи 2.Поскольку коксовые отложения постепенно накапливаются на катализаторе, частично дезактивированный катализатор непрерывно выводится для регенерации из нижней части реактора 6. Фиксированное количество катализатора поступает в затворный бункер 7, где происходит его продувка азотом для удаления остатков углеводородов. После продувки катализатор поступает в дозатор 8 и оттуда потоком азота поднимается в бункер 9 для отделения катализатора от азота и газообразных продуктов реакции. Азот возвращается в дозатор 8. Катализатор из бункера 9 опускается в регенератор 10, где происходит выжиг кокса. Регенерированный катализатор спускается в бункер 11, где он продувается водородом и затем поступает в дозатор 12, откуда поднимается потоком водорода в бункер 13. Из бункера 13 регенерированный катализатор непрерывно стекает в верхний реактор 3. Реакционные газы с нижнего 6 реактора поступают в теплообменник 1, где отдают своё тепло сырью, затем дополнительно охлаждаются в водяном холодильнике 14, при этом тяжёлые углеводороды конденсируются и отделяются от газообразных продуктов реакции в сепараторе 15. Газы из сепаратора 15 компрессором 16 подаются на охлаждение в АВО 17 и далее в блок газоразделения 18 на потоки водорода (чистотой 95%), топливного газа (С1-С2) и смеси сжиженных газов С3-С4 с частично унесёнными ароматическими углеводородами. Жидкие углеводороды из блока 18 и сепаратора 15 поступают на разделение в ректификационную колонну 20. С верха колонны отбирается пропан-бутановая фракция через АВО 21 и рефлюксную ёмкость 22. Часть дистиллята идёт на орошение колонны 20, остальное количество – на рециркуляцию в реакторный блок. С низа колонны 20 выводятся ароматические углеводороды на разделение ректификацией (на схеме не показано). Каталитическое алкилирование изобутана олефинами. Назначение процесса, сырьё, целевой продукт. Химизм и механизм алкилирования. Катализаторы алкилирования, их преимущества и недостатки. Влияние параметров процесса на выход продукта и его качество. Технологическая схема установки сернокислотного алкилирования изобутана бутиленами. Назначение процесса, сырье, целевой продукт – производство высокооктанового компонента бензинов алкилированием изобутана бутиленами или пропиленом. Целевой продукт процесса - алкилат, состоящий практически из изопарафинов, имеет высокое октановое число. Химизм и механизм алкилирования: Из парафинов к каталитическому алкилированию способны только изопарафины, имеющие третичный атом углерода. Олефины могут быть различными, но чаще всего применяют бутилены, алкилирующие изобутан с образованием изо-С8Н18. механизм алкилирования Первой стадией процесса (возникновения цепи) является протонирование олефина образование третичного карбений-иона 2а. Возможна также изомеризация первичного бутильного катиона 3. третичный бутильный карбениевый ион вступает в реакцию с бутеном 4. Далее вторичный октильный карбкатион изомеризуется в более устойчивый третичный 5. Изомеризованные октильные карбкатионы образуют целевой продукт процесса 6. Обрыв цепи Катализаторы алкилирования, их преимущества и недостатки: Серная и фтористоводородная кислоты. HF более предпочтителен, чем H2SO4. Преимущество HF по сравнению с сернокислотным: - меньший выход побочных продуктов, следовательно, более высокая селективность; - более высокий выход и качество алкилата; - применения простых реакторных устройств; - небольшая металлоѐмкость реактора Однако большая летучесть и высокая токсичность фтороводорода ограничивают его более широкое применение в процессах алкилирования. Влияние параметров процесса на выход продукта и его качество: Давление. давления не оказывает существенного влияния на процесс. Обычно поддерживают давление 0,6…1,0 МПа. Температура. При повышении температуры снижается вязкость кислоты и углеводородов и создаются более благоприятные условия для их перемешивания и диспергирования. повышение температуры выше 15°С интенсифицирует побочные реакции деструктивного алкилирования, полимеризации. Снижение температуры в определенных пределах оказывает благоприятное влияние на селективность реакций, выход и качество алкилата. На практике оптимальный интервал температур составляет 5…15°С. Соотношение изобутан : олефин. Избыток изобутана интенсифицирует целевую и подавляет побочные реакции алкилирования. Чрезмерное повышение этого соотношения увеличивает капитальные и эксплуатационные затраты. Концентрация кислоты. Для алкилирования обычно используют серную кислоту, содержащую от 88 до 98 % моногидрата. Если концентрация кислоты становится ниже 88%, усиливаются побочные реакции, приводящие к ухудшению качества алкилата. Применение более концентрированной кислоты приводит к окислению углеводородов, выделению диоксида серы и снижению выхода алкилата. Соотношение серная кислота : сырье должно быть в оптимальных пределах, при которых достигается максимальный выход алкилата высокого качества. Объемная скорость подачи сырья. При оптимальных значениях остальных оперативных параметров продолжительность пребывания сырья в реакторе составляет 200…1200 с, что соответствует объемной скорости подачи олефинов 0,3...0,5 ч –1 . Т 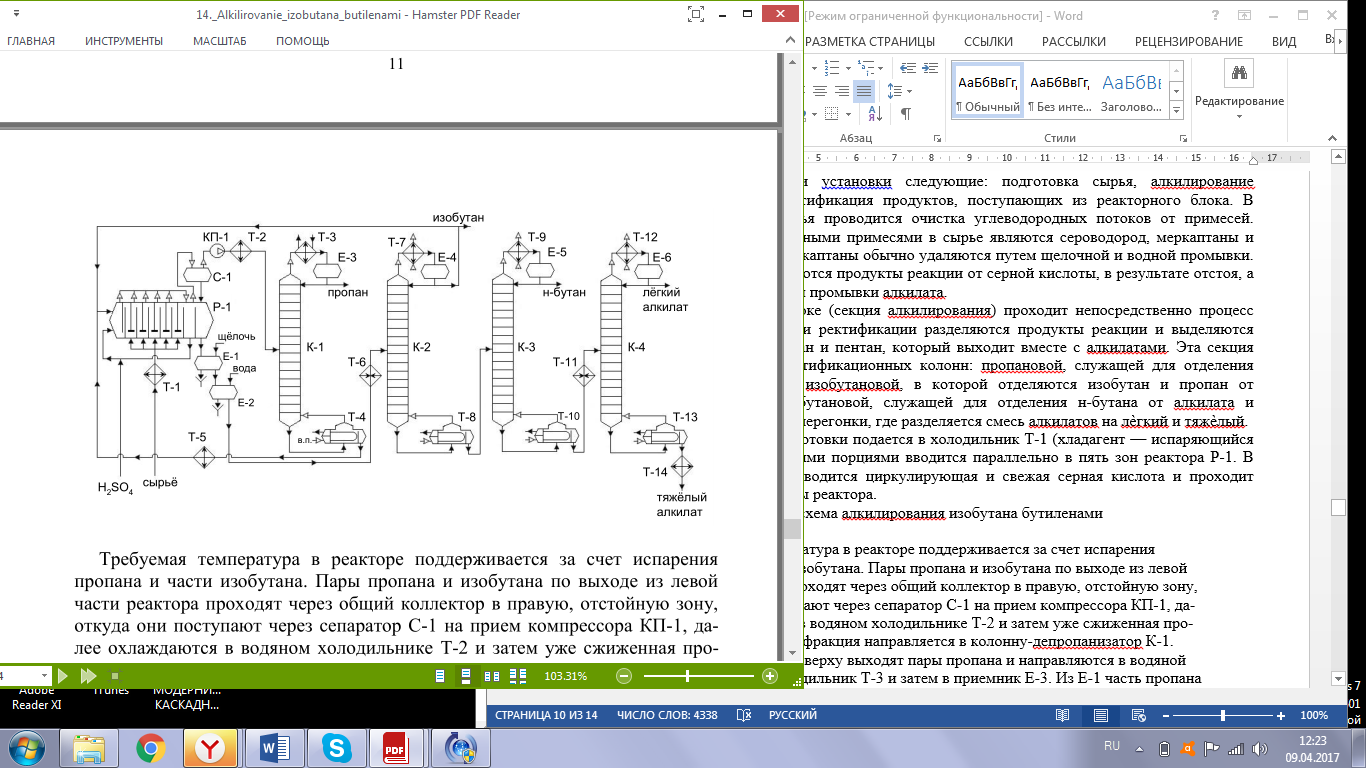 ехнологическая схема установки: Сырье подается в холодильник Т-1, а затем вводится параллельно в пять зон реактора Р-1. Пары пропана и изобутана по выходе из левой части реактора проходят через общий коллектор в правую, отстойную зону, откуда они поступают через сепаратор С-1 на прием компрессора КП-1, далее охлаждаются в холодильнике Т-2 и затем уже сжиженная пропан-изобутановая фракция направляется в колонну-депропанизатор К-1. Из этой колонны сверху выходят пары пропана и направляются в конденсатор-холодильник Т-3 и затем в приемник Е-3. Нижний продукт колонны К-1 − изобутан – поступает в подогреватель с паровым пространством Т-4, частично испаряется, пары возвращаются в низ колонны. Неиспарѐнная жидкая часть возвращается в реактор Р-1. Продукты реакции из последней секции Р-1 проходят последовательно ѐмкость Е-1, где осуществляется «защелачивание», затем ѐмкость Е-2, где промываются водой. Далее продукты реакции нагреваются в Т-6 и поступают в колонну К-2 для выделения изобутана. С верха колонны К-2 отбирается изобутан, который после конденсации в АВО Т-7 собирается в приемнике Е-4. часть изобутана подается качестве орошения, а основная часть возвращается как рециркулят в реактор Р-1. Нижний продукт колонны К-2 через рибойлер Т-8 подается в колонну-дебутанизатор К-3. Верхним продуктом колонны К-3 является н-бутан, который после конденсации в АВО Т-9 собирается в приемнике Е-5. Отсюда часть н-бутана подается 3 в качестве орошения, а основная часть отводится с установки. Нижний продукт колонны К-3 через рибойлер Т-10 и подогреватель Т-11 подается в колонну вторичной перегонки К-4. Верхним продуктом колонны К-4 является лѐгкий алкилат. Он конденсируется в АВО Т-12 и собирается в приемнике Е-6. Отсюда часть лѐгкого алкилата подается в качестве орошения, а основная часть выводится с установки. Нижний продукт колонны К-4 – тяжѐлый алкилат – через рибойлер Т-13 подается в холодильник Т-14 и выводится с установки. Тяжѐлый алкилат обычно используется как компонент дизельного топлива. Производство метилтретбутилового эфира (МТБЭ). Химизм, катализ, сырьё, параметры процесса. Технологическая схема установки производства МТБЭ. Химизм: Реакция синтеза МТБЭ из изобутилена и метанола протекает по цепному карбкатионному механизму с выделением тепла, а ее равновесие смещается вправо при повышении давления и снижении температуры. 1. Первой стадией алкилирования метанола изобутеном является протонирование: 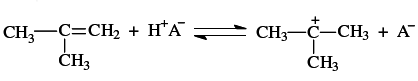 2. Образовавшийся третичный бутеновый карбкатион вступает в реакцию с метанолом:  3. Образовавшийся протон далее реагирует с изобутеном (стадия 1). 4. Причиной обрыва цепи может стать возврат протона к катализатору: При синтезе МТБЭ протекают следующие побочные реакции: — гидратация изобутилена водой; — межмолекулярная дегидратация метанола с образованием диметиловогоэфира: — если в метаноле содержится этанол, то образуется этилтретбутиловый эфир (ЭТБЭ) и т. д. Катализ: Из гомогенных и гетерогенных кислотных катализаторов в промышленных процессах синтеза МТБЭ наибольшее распространение получили сульфированные ионообменные смолы. Сырье – бутан-бутиленовая фракция (ББФ) каталитического крекинга и пиролиза. Параметры процесса: Процесс ведут при избытке метанола по отношению к изобутилену, чтобы получить после реакции фракцию С4, содержащую бутаны и н-бутилены с минимальной примесью изобутилена. Температура в зоне реакции, °С – 60…70 Давление, МПа – 0,7…0,75 Объемная скорость подачи ББФ каталитического крекинга, ч-1 – 1,5 Мольное соотношение метанол : изобутилен – 4 : 1 Тех.схема: Очищенная бутан-бутиленовая фракция и циркулирующий метанол нагреваются в теплообменнике Т-1 до 60° и поступает в зону синтеза под каждый слой катализатора Р-1. В верхнюю часть реакционной зоны во избежание перегрева катализатора подается также подогретый в теплообменнике Т-2 свежий метанол. Жидкие продукты реакции, состоящие из МТБЭ с примесью метанола и углеводородов, выводят из куба Р-1 и направляют на сухую отпарку примесей в отпарную колонну К-2, снабженную паровым кипятильником Т-4. Целевой продукт — МТБЭ — выводят с куба К-2 и после охлаждения в Т-5 откачивают в товарный парк. П 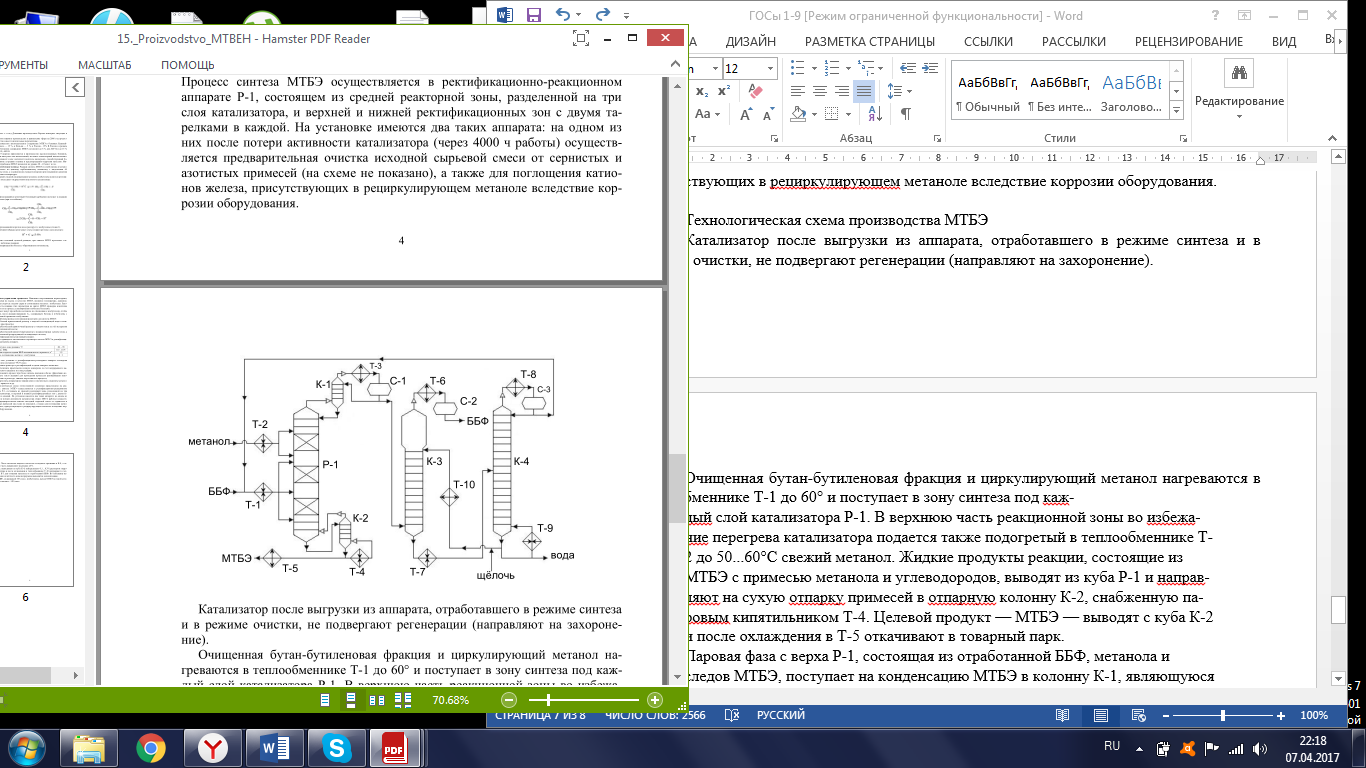 аровая фаза с верха Р-1, состоящая из отработанной ББФ, метанола и следов МТБЭ, поступает в колонну К-1. Конденсированный МТБЭ возвращают на верхнюю тарелку Р-1 в качестве холодного орошения. С верха К-1 отводят несконденсировавшиеся пары отработанной ББФ и метанола, которые после охлаждения и конденсации в холодильнике Т-3 поступают в емкостьсепаратор С-1. Разделение конденсата из С-1 на отработанную ББФ и метанол осуществляют в экстракторе К-3. Отработанная ББФ с верха К-3 охлаждается в холодильнике Т-6, поступает в ѐмкость С-2 и направляется в товарный парк. Отгонку циркуляционного метанола от воды производят в ректификационной колонне К-4. Метанол, выводимый с верха К-4, охлаждают и конденсируют в воздушных и водяных конденсаторах-холодильниках Т-8 и собирают в рефлюксной емкости С-3. Часть метанола подают в качестве холодного орошения в К-4, а остальную часть направляют на рецикл в Р-1. Воду, выводимую из куба К-4, нейтрализуют 0,1…0,3% раствором гидроксида натрия и после охлаждения в теплообменнике Т-10 направляют в экстрактор К-3 для отмывки метанола от отработанной ББФ. Каталитическая изомеризация пентан-гексановой фракции. Назначение процесса. Термодинамика и механизм процесса изомеризации. Катализ. Основные параметры процесса. Технологическая схема установки низкотемпературной изомеризации. Назначение процесса – получение высокооктановых изокомпонентов автобензинов или сырья нефтехимии. Термодинамика и механизм процесса изомеризации. Реакции изомеризации парафинов являются обратимыми, протекают без изменения объема, с небольшим экзотермическим эффектом. Поэтому термодинамическое равновесие зависит только от температуры: низкие температуры благоприятствуют образованию более разветвленных изомеров и получению, изомеризата с более высокими октановыми числами. На бифункциональных катализаторах, обладающих дегидрогидрирующей и кислотной активностями, изомеризация протекает по следующей схеме: Вначале происходит дегидрирование н-парафина на металлических центрах катализатора. Образовавшийся олефин на кислотном центре превращается в карбений-ион, который легко изомеризуется. Изомерные карбений-ионы, возвращая протон кислотному центру катализатора, превращаются в соответствующие олефины, которые затем гидрируются на металлических центрах катализаторов изомеризации. Катализ. В современных бифункциональных катализаторах изомеризации н-алканов в качестве металлического компонента используются платина и палладий, а в качестве носителя — фторированный или хлорированный оксид алюминия, а также алюмосиликаты или цеолиты, внесенные в матрицу оксида алюминия. Алюмоплатиновые фторированные катализаторы называются высокотемпературными. Металлцеолитные катализаторы названы среднетемпературными. Алюмоплатиновые катализаторы, промотированные хлором, названы низкотемпературными. Наибольшее распространение в нефтепереработке получили низко- и высокотемпературные процессы. О 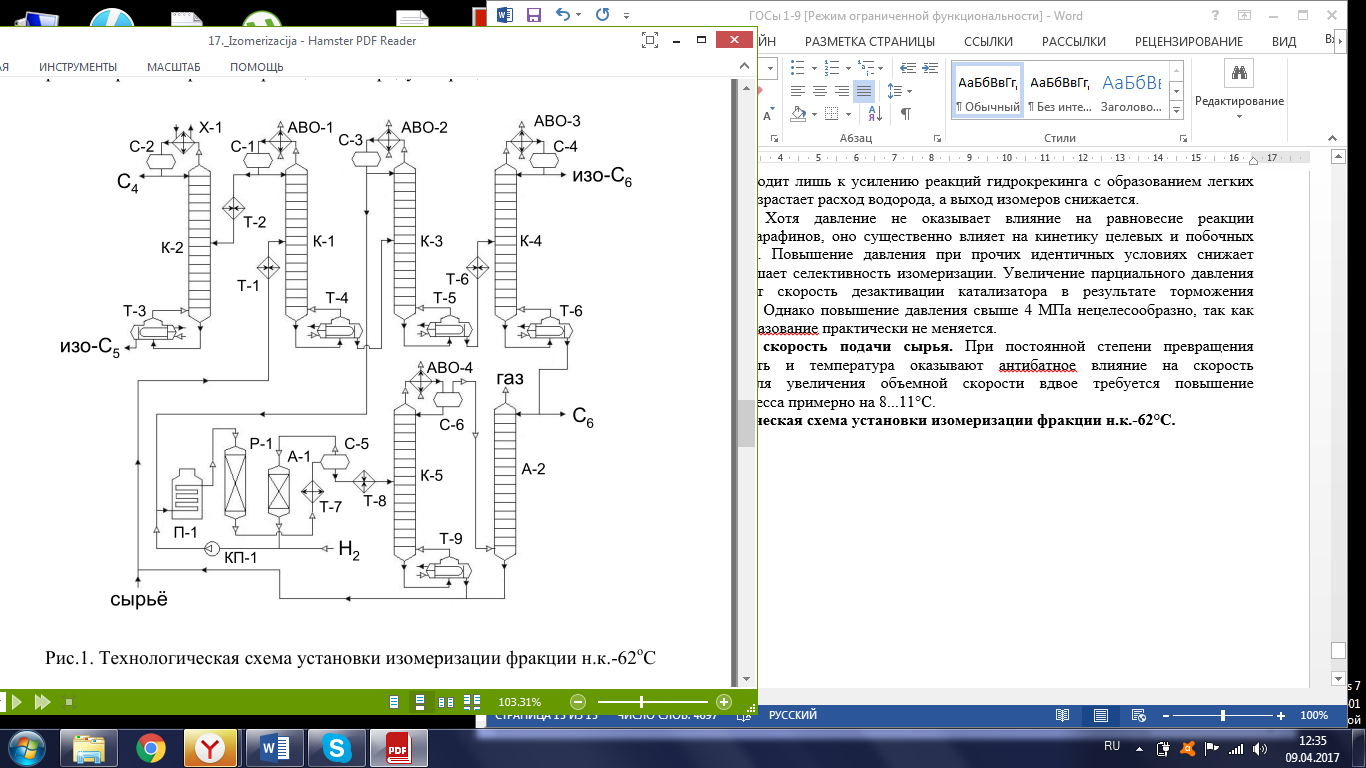 сновные параметры процесса. Температура. С повышением температуры скорость реакции изомеризации возрастает до ограничиваемого равновесием предела. Дальнейшее повышение температуры приводит лишь к усилению реакций гидрокрекинга с образованием легких газов. При этом возрастает расход водорода, а выход изомеров снижается. Давление. давление не оказывает влияние на равновесие реакции, оно существенно влияет на кинетику целевых и побочных реакций процесса. Повышение давления при прочих идентичных условиях снижает глубину, но повышает селективность изомеризации. Объемная скорость подачи сырья. При постоянной степени превращения объемная скорость и температура оказывают антибатное влияние на скорость изомеризации. Для увеличения объемной скорости вдвое требуется повышение температуры процесса. сновные параметры процесса. Температура. С повышением температуры скорость реакции изомеризации возрастает до ограничиваемого равновесием предела. Дальнейшее повышение температуры приводит лишь к усилению реакций гидрокрекинга с образованием легких газов. При этом возрастает расход водорода, а выход изомеров снижается. Давление. давление не оказывает влияние на равновесие реакции, оно существенно влияет на кинетику целевых и побочных реакций процесса. Повышение давления при прочих идентичных условиях снижает глубину, но повышает селективность изомеризации. Объемная скорость подачи сырья. При постоянной степени превращения объемная скорость и температура оказывают антибатное влияние на скорость изомеризации. Для увеличения объемной скорости вдвое требуется повышение температуры процесса.Технологическая схема. Смесь исходного сырья, рециркулирующего стабильного изомеризата и тощего абсорбента после подогрева в теплообменниках Т-1 подают на разделение в колонну К-1, сверху которой отбирают бутановую и изопентаную фракцию, которая охлаждается в АВО-1 и поступает в рефлюкс С-1. Из С-1 конденсат частично идѐт на орошение К-1, остальное количество после нагрева в Т-2 подвергается дальнейшей ректификации в бутановой колонне К-2, где происходит отделение целевого изопентана от бутанов. Нижний продукт колонны К-1 подают в пентановую колонну К-3. Нижний продукт этой колонны направляют на фракционирование в изогексановую колонну К-4, с верха которой отбирают второй целевой продукт процесса — изогексан. Отбираемую с верха К-3 пентановую фракцию, содержащую около 91% масс. н-пентана, смешивают с ВСГ и после нагрева в трубчатой печи П-1 до требуемой температуры направляют в реактор изомеризации со стационарным слоем катализатора Р-1. Парогазовую смесь продуктов реакции охлаждают и конденсируют в теплообменниках и холодильниках Т-7 и подают в сепаратор С-5, а циркулирующий ВСГ из С-5 после осушки на цеолитах в адсорбере А-1 компрессором КП-1 подают на смешение с сырьем.Жидкий изомеризат из С-5 после нагрева в Т-8 подвергается стабилизации в колонне К-5. С верха К-5 уходят газы, а стабильный изомеризат с низа К-5 направляют на ректификацию вместе с сырьем в К-1. Из газов стабилизации в абсорбере А-2 извлекают изопентан подачей в качестве абсорбента части гексановой фракции, отбираемой с низа К-4. С верха абсорбера А-2 уходит сухой газ, используемый как топливный . Термический крекинг дистилятного сырья. Сырье и целевые продукты процесса. Параметры процесса. Технологическая схема. Термическая подготовка дистиллятных видов сырья для установок коксованияи производства термогазойля. Сырье: ароматизированные высококипящие дистиляты: тяжелый газойль кат.крекинга, тяжелая смола пиролиза, экстракты селективной очистки масел. Целевые продукты: Термогазойль 200-480, дистиллятный крекинг-отаток, газ, бензин. Температура 500-550 Давление5-6МПа 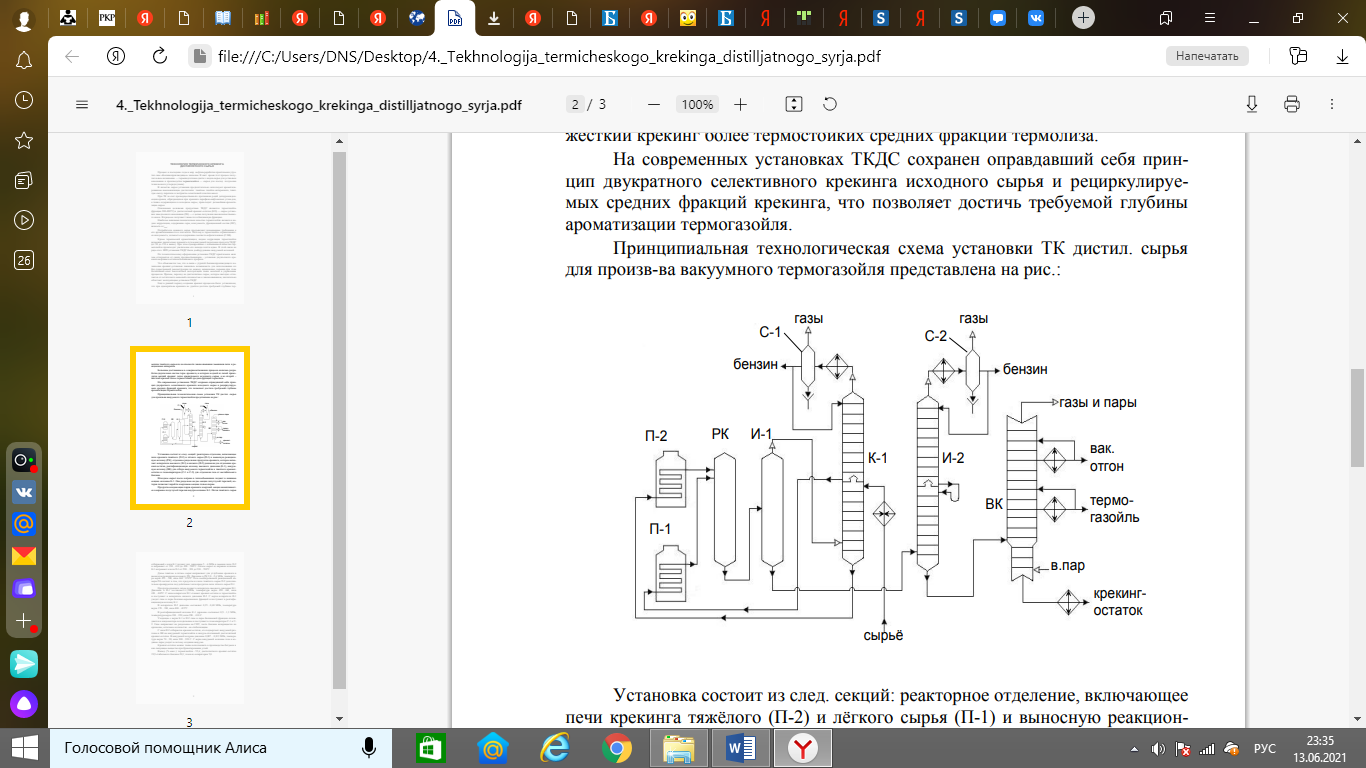 Исходное сырьѐ после нагрева в теплообменниках подают в нижнюю секцию колонны К-1. Она разделена на две секции полуглухой тарелкой, которая позволяет перейти в верхнюю секцию только парам. Продукты конденсации паров крекинга в верхней секции накапливаются в кармане полуглухой тарелки внутри колонны К-1. Поток тяжѐлого сырья 3 отбираемый с низа К-1 подают под давлением 5…6 МПа в змеевик печи П-2 и нагревают. Лѐгкое сырьѐ из кармана колонны К-1 нагревают в печи П-1. Далее тяжѐлое и лѐгкое сырьѐ направляют для углубления крекинга в выносную реакционную камеру РК. Давление в РК 2,0…2,6 МПа, температура верха 495…500, низа 460…470оС. Роль необогреваемой реакционной камеры РК состоит в том, что продукты из печи тяжѐлого сырья П-2 дополнительно крекируются под действием тепла продуктов печи лѐгкого сырья П-1. Продукты крекинга затем подают в испаритель высокого давления И-1. Давление в И-1. С низа испарителя И-1 стекают крекинг-остаток и термогазойль и поступают в испаритель низкого давления И-2. С верха испарителя И-1 уходят газы и пары бензино-керосиновых фракций и поступают в ректификационную колонну К-1. Уходящие с верха К-1 и И-2 газы и пары бензиновой фракции охлаждаются в конденсаторе-холодильнике и поступают в газосепараторы С-1 и С2. Газы направляют на разделение на ГФУ, часть бензина возвращается на орошение, остальное количество - на стабилизацию. С низа И-2 отбирается крекинг-остаток, его подвергают вакуумной разгонке в ВК на вакуумный термогазойль и вакуум-отогнанный дистиллятный крекинг-остаток. В вакуумной колонне давление 0,007…0,013 МПа, температура верха 70…90, низа 300…320оС. С верха вакуумной колонны газа и водяные пары уходят в систему создания вакуума. Крекинг-остаток можно также использовать в производстве битумов и как связующее вещество при брикетировании углей. Висбрекинг тяжелого сырья. Назначение процесса, сырье, продукты, параметры. Технологическая схема Неглубокая переработка гудронов с целью снижения вязкости и их последующего использования как котельных топлив Сырье: Гудрон свыше 500 Продукты: Газы, бензин, керосино-газойлевая фракция, висбрекинг-остаток Тепература 500 Давление 5-6 МПа 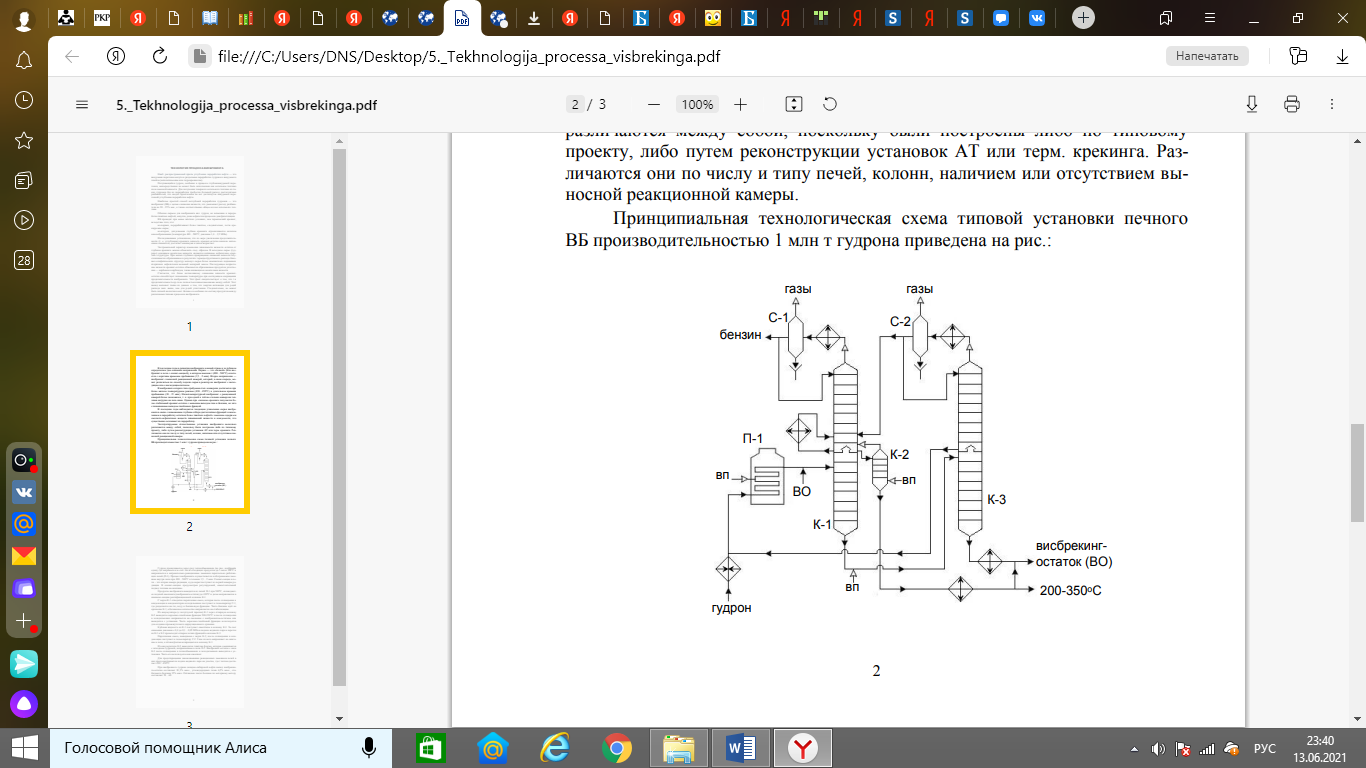 Гудрон прокачивается через ряд теплообменников, где нагревается за счѐт тепла отходящих продуктов до t около 300°С и направляется в нагревательно-реакционные змеевики параллельно работающих печей (П-1). Процесс висбрекинга осуществляется в обогреваемом змеевике внутри печи при 480…500оС в течении 1,5…2 мин. Сокинг-секция в печи – это вторая камера радиации, куда сырьѐ поступает из первой камеры радиации. В сокинг-секцию предусмотрен регулируемый, самостоятельный подвод топлива на сжигание. Продукты висбрекинга выводятся из печей П-1, охлаждаются подачей квенчинга (висбрекинга остатка) и далее направляются в нижнюю секцию ректификационной колонны К-1. С верха К-1 отводится парогазовая смесь, которая после охлаждения и конденсации в конденсаторах-холодильниках поступает в газосепаратор С-1, где разделяется на газ, воду и бензиновую фракцию. Часть бензина идѐт на орошение К-1, а балансовое количество направляется на стабилизацию. Из аккумулятора (с полуглухой тарелки) К-1 через отпарную колонну К-2 выводится керосино-газойлевая фракция 200-350°С и после охлаждения в холодильниках направляется на смешение с висбрекингом-остатком или выводится с установки. Часть керосино-газойлевой фракции используется для создания промежуточного циркуляционного оршения. Кубовая жидкость из К-1 поступает самотѐком в колонну К-3. За счет снижения давления и подачи водяного пара в переток из К-1 в К-3 происходит отпарка легких фракций в колонне К-3. Парогазовая смесь, выводимая с верха К-3, после охлаждения и конденсации поступает в газосепаратор С-2. Газы из него направляют на сжигание в печи, а лѐгкая флегма возвращается в колонну К-1. Из аккумулятора К-3 выводится тяжѐлая флегма, которая смешивается с исходным гудроном, направляемым в печи П-1. Висбрекинг-остаток с низа К-3 после охлаждения в теплообменниках и холодильниках выводится с установки. Часть его используется как квенчинг. Технология производства нефтяных пеков. Технологическая схема установки. Пек- битуминозный материал черного или бурого цвета с блестящим раковистым изломом. При н.у твердое вещество, при нагревании размягчается Температура 360-420 Давление 0,1-0,5 МПа 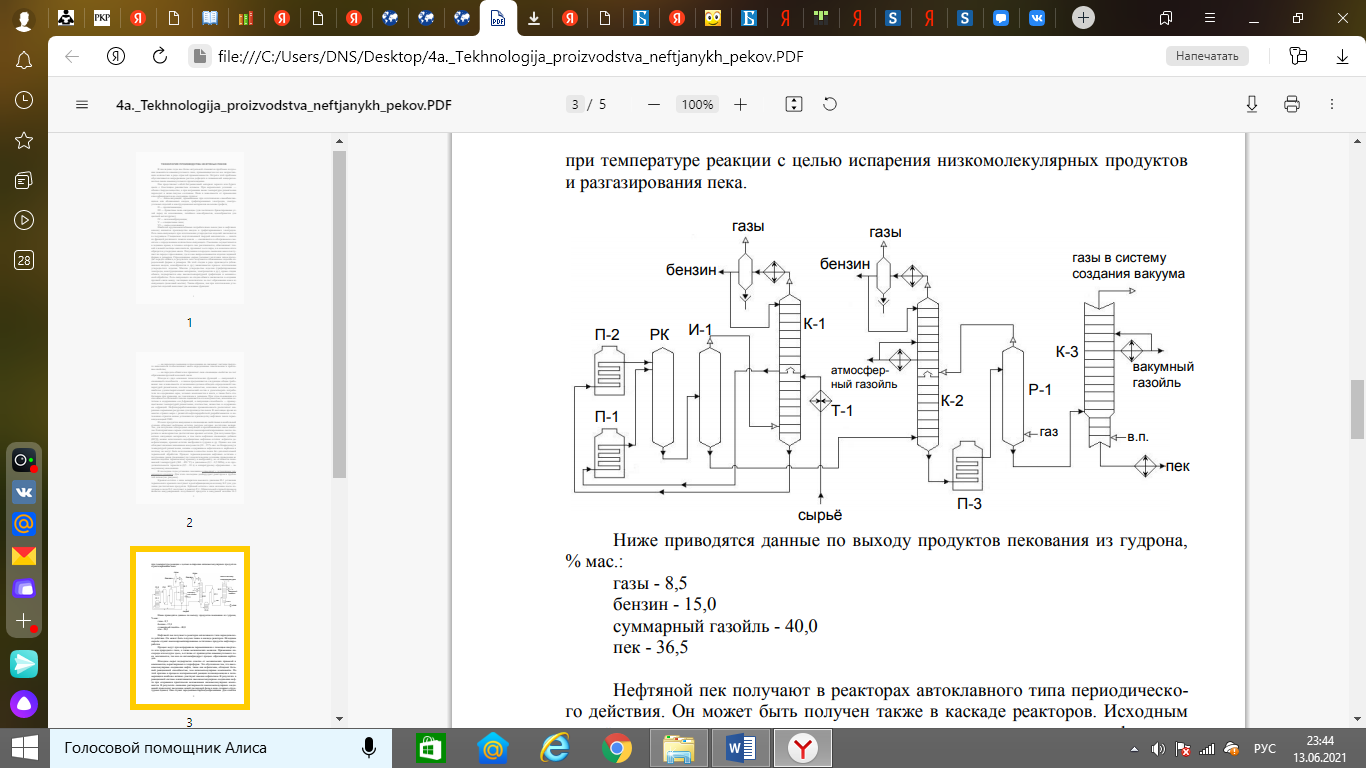 В последние годы установки пекования совмещают с установками термического крекинга. Для этого последние дооборудуют реактором и трубчатой печьюКрекинг-остаток с низа испарителя высокого давления И-1 установки термического крекинга поступает в ректификационную колонну К-2 для удаления дистиллятных продуктов. Кубовый остаток с низа колонны после подогрева в печи П-3 поступает в реактор Р-1. Обязательной стадией процесса является вакуумирование полученного продукта в вакуумной колонне К-3 3 при температуре реакции с целью испарения низкомолекулярных продуктов и разгазирования пека. |
