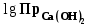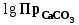Каустификация. каустификация. Каустификация содового раствора
 Скачать 275.64 Kb. Скачать 275.64 Kb.
|
|
КАУСТИФИКАЦИЯ СОДОВОГО РАСТВОРА Процесс каустификации содового раствора лежит в основе промышленного способа получения едкого натра. Это типичный пример обратимой реакции в гетерогенной системе жидкость-твердые (Ж-Т). В данной работе подробно рассматривается связь физико-химических особенностей процесса каустификации с основными технологическими и экономическими вопросами производства: видом технологической схемы, производительностью оборудования, энергетическими затратами и уровнем потерь. 4.1. Свойства едкого натра, его применение и методы получения В промышленности едкий натр производят электрохимическим или химическими способами. Среди последних наиболее распространен известковый способ, основанный на взаимодействии растворов соды с гашеной известью: 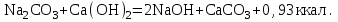 (1) (1)Будучи лишь слабощелочной, сода, благодаря этой обработке, становится едкой, каустической (от греческого слова жгучий, едкий). Поэтому полученную таким путем гидроокись натрия называют также каустической содой, а процесс получения ‑ каустификацией. В соответствии с ГОСТ 2263-79 и 11078-78 едкий натр выпускается промышленностью в твердом (94-98,5% 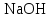 ) и жидком (42-50% ) и жидком (42-50% 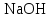 ) видах. Кроме основного вещества в данных продуктах нормируется содержание примесей ) видах. Кроме основного вещества в данных продуктах нормируется содержание примесей  (0,6-2,0%), (0,6-2,0%), 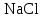 (0,05-4,0%), (0,05-4,0%), 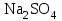 (0,03-0,9%), (0,03-0,9%), 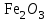 (0,0015-0,2%) и др. (0,0015-0,2%) и др.Едкий натр широко применяется в промышленности. Основные области применения ‑ химическая, нефтеперерабатывающая, металлургическая, мыловаренная, текстильная и целлюлозно-бумажная промышленность. Около 40% едкогo натpa в химической промышленности потребляется в производстве искусственных волокон, а также потребляется для синтеза фенола, бетанафтола, капролактама, моющих средств, химических средств защиты растений и целого ряда неорганических продуктов. При кипячении соломы или древесины с натровой щелочью образуется целлюлоза. В металлургической промышленности много каустической соды используется для получения глинозема из бокситов по методу Байера, в нефтехимической промышленности ‑ для очистки нефтепродуктов. 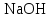 ‑ часто используемый реактив в аналитической химии. В частности, сплавление с едким натром является замечательным средством для вскрытия образцов в анализе. ‑ часто используемый реактив в аналитической химии. В частности, сплавление с едким натром является замечательным средством для вскрытия образцов в анализе.4.2. Физико-химические основы каустификации содового раствора Каустификация содового раствора представляет собой основную операцию известкового способа получения едкого натра. Это типичный гетерогенный некаталитический процесс типа жидкость–твердое (Ж-Т). В осадке при каустификации всегда присутствует две твердые фазы ‑ 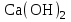 и и 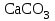 (реакция 1). (реакция 1). 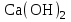 берется в избытке для максимального использования соды. Очевидно, что степень превращения соды в едкий натр, или степень каустификации (К), зависит от соотношения растворимостей берется в избытке для максимального использования соды. Очевидно, что степень превращения соды в едкий натр, или степень каустификации (К), зависит от соотношения растворимостей 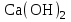 и и 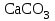 , равновесие которых с раствором подчиняется правилу произведения растворимости: , равновесие которых с раствором подчиняется правилу произведения растворимости: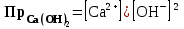 (2) (2)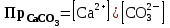 (3) (3)При одновременном присутствии в осадке 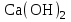 и и 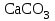 в уравнения (2) и (3) входит одно и то же значение в уравнения (2) и (3) входит одно и то же значение 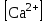 , т.е. в условиях равновесия , т.е. в условиях равновесия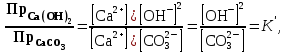 (4) (4)где К’ является константой равновесия реакции (1). В этом легко можно убедиться, если вывести выражение этой константы, исходя из известных законов химического равновесия и учтя при этом, что активность твердых участников реакции принимается за единицу: 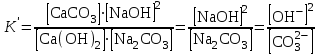 . (5) . (5)В табл.4.1 приведены температурные зависимости рассматриваемых равновесий. Величина константы равновесия К’ свидетельствует о том, что реакция (1) хотя и значительно сдвинута вправо, но относится к разряду практически обратимых реакций. Влияние температуры на равновесие (см. табл.4.1) слабо отрицательно. Это результат того, что с повышением температуры растворимость 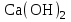 уменьшается быстрее, чем растворимость уменьшается быстрее, чем растворимость 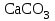 . .Таблица 4.1 Влияние температуры на произведение активности 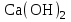 и и 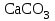 и константу равновесия реакции (1) и константу равновесия реакции (1)
Значительное влияние на степень каустификации оказывает концентрация исходного содового раствора. В табл.4.2 приведены результаты экспериментального исследования данной зависимости. Как видно, увеличение концентрации исходного содового раствора сопровождается снижением степени каустификации. К такому же выводу модно придти чисто умозрительно: если увеличивается концентрация исходного содового раствора, то рост достаточной концентрации 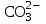 при сохранении равенств (4) и (5) должен обгонять прирост концентрации ионов при сохранении равенств (4) и (5) должен обгонять прирост концентрации ионов 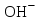 , так как концентрация последних в этих равенствах имеет более высокий показатель степени. , так как концентрация последних в этих равенствах имеет более высокий показатель степени.При выборе условий каустификации и технологической схемы производства в целом следует учитывать ограничения ГОСТа по содержанию  в готовых продуктах. Например, в жидком каустике марок РХ-1 и PХ-2 (ГОСТ 2269-71) весовое соотношение в готовых продуктах. Например, в жидком каустике марок РХ-1 и PХ-2 (ГОСТ 2269-71) весовое соотношение 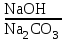 должно быть не меньше соответственно 37,5 и 21,5. В равновесных растворах такое соотношение обеспечивается только при концентрациях исходного содового раствора не больше 7-10,5% (см. табл.4.2). должно быть не меньше соответственно 37,5 и 21,5. В равновесных растворах такое соотношение обеспечивается только при концентрациях исходного содового раствора не больше 7-10,5% (см. табл.4.2). Таблица 4.2 Влияние концентрации исходного содового раствора на степень каустификации при 1000С и 20%-м избытке
Однако применять столь разбавленные растворы в промышленности экономически невыгодно, так как для получения продукционного каустика пришлось бы выпаривать слишком много воды. Кроме того, с уменьшением концентрации щелочи существенно снижается производительность основного оборудования в пересчете на конечный продукт. Для устранения указанных недостатков в промышленности стремятся увеличить концентрацию исходного содового раствора. Появление при этом избыточных количеств  в растворе каустификации не препятствует получению стандартного продукта, так как при упарке этих растворов в растворе каустификации не препятствует получению стандартного продукта, так как при упарке этих растворов  выделяется в осадок из-за высаливающего действия второго компонента ‑ выделяется в осадок из-за высаливающего действия второго компонента ‑ 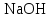 (табл.4.2). Выделившуюся в осадок соду возвращают в голову процесса для предотвращения ее потерь. Таким образом, производство каустической соды является примером применения циклической схемы в условиях обратимости основного процесса, относящегося к системам Ж-Т. (табл.4.2). Выделившуюся в осадок соду возвращают в голову процесса для предотвращения ее потерь. Таким образом, производство каустической соды является примером применения циклической схемы в условиях обратимости основного процесса, относящегося к системам Ж-Т. На основании вышеприведенного можно сделать выводы о том, что применение циклической схемы с возвратом части содового раствора в известковом способе позволяет получить следующие технологические и экономические выводы: 1) снизить расходы на упаривание слабых растворов каустификации за счет повышения концентрации исходного содового раствора; 2) повысить пропускную способность основного оборудования по 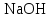 , т.е. производительность оборудования из-за увеличения концентрации растворов; , т.е. производительность оборудования из-за увеличения концентрации растворов;3) увеличить выход продукта и повысить eго качество за счет выделения  и возвращения его на стадию каустификации. и возвращения его на стадию каустификации. Хотя благоприятные условия растворимости в системе 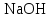 - -  - - 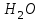 (табл. 4.3) предоставляют очень широкие возможности для повышения концентрации исходного содового раствора, однако в промышленности ограничиваются повышением этой концентрации до 14-18% (табл. 4.3) предоставляют очень широкие возможности для повышения концентрации исходного содового раствора, однако в промышленности ограничиваются повышением этой концентрации до 14-18%  . При этом степень каустификации, как правило, не превышает 90%. Такие ограничения связаны с тем, что повышение концентрации исходного раствора содового связано с рядом отрицательных последствий, основными из которых является следующие: . При этом степень каустификации, как правило, не превышает 90%. Такие ограничения связаны с тем, что повышение концентрации исходного раствора содового связано с рядом отрицательных последствий, основными из которых является следующие:1. Если начальная концентрация  превысит 24%, то в данной фазе образуется персонит превысит 24%, то в данной фазе образуется персонит 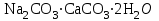 , с которым теряется дорогое сырье ‑ сода. , с которым теряется дорогое сырье ‑ сода.Таблица 4.3 Совместная растворимость 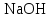 и и 
2. Разделение суспензий и промывка осадка при известковом способе производится, главным образом, отстаиванием. От условий проведения этой операции сильно зависит уровень потерь щелочи с отбросным шламом и производительность оборудования, в частности, многое зависит от физических свойств твердой и жидкой фаз. Так, по закону Стокса скорость отстаивания малых частиц можно определить по формуле: 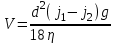 (6) (6)где V ‑ скорость осаждения частиц, d ‑ диаметр частиц, j1иj2 ‑ соответственно плотность частиц и среды, g ‑ ускорение силы тяжести, η ‑ вязкость среды. В соответствии с этим законом скорость отстаивания частиц осадка уменьшается с увеличением концентрации, а значит вязкость и плотность раствора. Аналогичные закономерности действуют и на последних стадиях отстаивания, когда процесс осаждения становится консолидированным. Таким образом, уменьшение концентрации маточного раствора способствует увеличению скорости отстаивания, лучшему уплотнению, а, следовательно, и лучшему качеству промывки осадка путем отстаивания. 3. Качество промывки осадков улучшается с увеличением количества промывных вод. Для достаточно полной отмывки дорогих щелочей от осадка в производстве каустической соды расходуется большое количество промывных вод, которые для переработки их на товарный каустик подаются на стадию каустификации. Это приводит к неизбежному разбавлению раствора на этой стадии. Таким образом, выбор концентрации исходного содового раствора обусловливается минимумом производственных затрат, найти который можно на основе анализа противоречивых тенденций, связанных с изменением этого показателя. Большое влияние на конечные результаты оказывает температура каустификации. Проведение процесса каустификации при 90-1000С позволяет резко интенсифицировать химический процесс и получать осадок с более крупными частицами. Вместе с каустификацией при повышенной температуре проводятся последующие операции отделения суспензии и промывки осадка отстаиванием. Связанные с повышением температуры укрупнения осадка и уменьшение вязкости и плотности растворов значительно улучшают, как это было показано выше, технологические показатели производства каустической соды. Поддержанию повышенной температуры на стадии каустификации способствует применение негашеной извести вместо суспензии гидроокиси кальция: 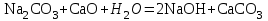 +16,52 ккал . (7) +16,52 ккал . (7)Добавление стадии гашения извести резко повышает экзотермичность процесса каустификации. Однако основной эффект применения негашеной извести заключается в снижении количества вносимой в систему воды и в получении более крупного осадка 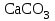 , который лучше отстаивается и промывается. Замечено, что не просто повышение температуры, а именно совмещение процессов гашения извести и каустификации позволяет добиться особенно хороших успехов в укрупнении частиц осадков. , который лучше отстаивается и промывается. Замечено, что не просто повышение температуры, а именно совмещение процессов гашения извести и каустификации позволяет добиться особенно хороших успехов в укрупнении частиц осадков.Итак, подробное рассмотрение физико-химических основ каустификации содового раствора показывает, что от выбора условий проведения этого процесса во многом зависят технологические и экономические показатели производства каустической соды. Очень большое влияние на эти показатели оказывает также выбор технологической схемы. Как видно из анализа, в условиях обратимости основногo процесса весьма целесообразным оказывается выбор циклической схемы с рециркуляцией содового раствора. 4.3. Описание технологической схемы производства каустической соды Сырьем для производства каустической соды известковым способом служат водный раствор кальцинированной соды и негашеная известь, содержащая 80-87% свободной 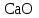 примеси примеси 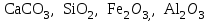 и др. Переработка этого сырья производится по схеме, изображенной на рис. 4.1. На этой схеме изображены только основные аппараты и для упрощения не приведено вспомогательное оборудование (дозаторы, промежуточные емкости, насосы и др.). и др. Переработка этого сырья производится по схеме, изображенной на рис. 4.1. На этой схеме изображены только основные аппараты и для упрощения не приведено вспомогательное оборудование (дозаторы, промежуточные емкости, насосы и др.).Содовый раствор получается декарбонизацией суспензии бикарбоната натрия, являющегося полупродуктом в производстве кальцинированной соды. В декарбонаторе 1 эта суспензия нагревается до 105-1100С паром, при этом происходит термическая диссоциация бикарбоната: 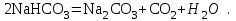 (8) (8)Образующийся при этом 18-20%-й содовый раствор собирается в сборнике 4, откуда он расходуется на получение исходного содового раствора для основной каустификации и для обработки шлама этой основной, так называемой 1-й каустификации, в аппарате 9. Для приготовления исходного содового раствора 1-й каустификации жидкость декарбонатора смешивается в мешалке 5 с промывными водами и с раствором солей выпарки, выделяющихся при последующем концентрировании слабого щелочного раствора в вакуум-выпарных аппаратах. Резервуары 2 и 3 служат соответственно для сбора раствора солей выпарки и промывных вод. Полученный исходный содовый раствор с концентрацией 13-15%  и температурой 60-80° подается в гаситель-каустификатор 6, где он смешивается с негашеной известью. Известь дается с избытком 5-10% для обеспечения достаточно высокой степени использования и температурой 60-80° подается в гаситель-каустификатор 6, где он смешивается с негашеной известью. Известь дается с избытком 5-10% для обеспечения достаточно высокой степени использования  на стадии основной каустификации. За счет тепла реакции температура смеси поднимается до 100-105°. Конструкция аппарата обеспечивает хорошее перемешивание суспензии и при времени пребывания ее 12 мин степень каустификации достигает 75%. на стадии основной каустификации. За счет тепла реакции температура смеси поднимается до 100-105°. Конструкция аппарата обеспечивает хорошее перемешивание суспензии и при времени пребывания ее 12 мин степень каустификации достигает 75%. В каскаде вертикальных цилиндрических аппаратов-каустификаторах первой каустификации 7 реакционная смесь выдерживается при перемешивании еще 3-4 ч. За это время степень каустификации поднимается до 85-90%, завершается химическая реакция, укрупняются частицы осадка, суспензия разделяется в отстойнике 8. Получаемый в отстойнике 8 осветленный раствор с содержанием 130–140 г/л  и 25-30 г/л и 25-30 г/л  (j=1;13) подается в сборник 2 и далее на упарку, а осадок, так называемый шлам первой каустификации, вместе с примесью маточного раствора подается в аппарат с мешалкой 9 на вторую каустификацию. (j=1;13) подается в сборник 2 и далее на упарку, а осадок, так называемый шлам первой каустификации, вместе с примесью маточного раствора подается в аппарат с мешалкой 9 на вторую каустификацию.Так как этот шлам содержит избыточную гидроокись кальция, то он обрабатывается в этом аппарате содовым раствором декарбонатора для полного использования извести. Для этого сода подается с большим избытком, так что на этой стадии степень каустификации достигает только 50–55%. Избыток соды, пройдя затем последующие стадий, возвращается вместе с образовавшимся едким натром на первую каустификацию. Это позволяет полностью использовать известь в производстве, несмотря на то что на стадии основной первой каустификации она берется с избытком. Рис. 4.1. Технологическая схема получения каустической соды известковым способом 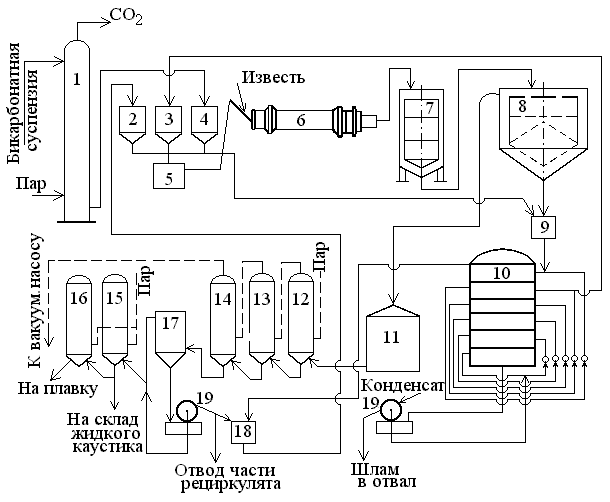  Перед выбрасыванием шлам второй каустификации отделяется от маточного раствора и промывается в многоярусном отстойнике-промывателе 10 и, наконец, на вакуум-фильтре 19. В промывателе 10 шлам отделяется от маточного раствора на верхнем ярусе и затем последовательно проходит сверху вниз все ярусы навстречу промывной воде. Промывка осуществляется по принципу противотока, так что чистым конденсатом шлам промывается на вакуум-фильтре 19 перед самым выбрасыванием этого шлама в отвал. Далее промывная вода при помощи центробежных насосов проходит последовательно все пять ярусов и подается на стадию приготовления исходного содового раствора. Применение многостадийной противоточной промывки позволяет резко снизить расход промывной воды – до 4-5 м3/т каустика. Однако этот расход все же велик и приводит к значительному разбавлению исходного содового раствора, зато потери дорогой щелочи с отбросным шламом сведены к минимуму и составляют около 0,007 г на 1 т продукционного каустика (92% NaOH). Слабый щелочной раствор первой каустификации упаривается в выпарных установках с большим числом корпусов. В предложенной схеме их пять: первые три корпуса 12, 13 и 14 объединены по типу работы 3-корпусной установки для снижения расхода пара, два последних корпуса 15 и 16 работают отдельно. В первых трех корпусах концентрация доводится до 600-610 г/л (41-42 вес.%), при этом основная часть (90-95%) не прореагировавшего на стадии каустификации карбоната натрия выделяется в осадок в соответствия с условиями растворимости в системе 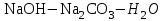 (табл.4.3). Вместе с (табл.4.3). Вместе с  из раствора выделяются примеси из раствора выделяются примеси 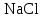 и и 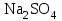 , поступающие в производство с сырьем. Поэтому осадок, отделяемый от маточного раствора в аппаратах 17 и 19 и содержащих несколько компонентов, называется солями выпарки. Эти соли растворяются в аппарате 18 поступающей из отстойника 10 смесью маточного раствора второй каустификации и промывных вод, и полученный раствор подается на стадию приготовления исходного содового раствора в сборник 2. Таким образом, часть соды циркулирует в производстве каустической соды. Вместе с содой в цикле циркулируют примеси , поступающие в производство с сырьем. Поэтому осадок, отделяемый от маточного раствора в аппаратах 17 и 19 и содержащих несколько компонентов, называется солями выпарки. Эти соли растворяются в аппарате 18 поступающей из отстойника 10 смесью маточного раствора второй каустификации и промывных вод, и полученный раствор подается на стадию приготовления исходного содового раствора в сборник 2. Таким образом, часть соды циркулирует в производстве каустической соды. Вместе с содой в цикле циркулируют примеси 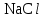 и и 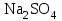 ,которые непрерывно поступают с исходным сырьем и только частично отводятся из цикла с готовым продуктом. Поэтому для предотвращения их излишнего накопления в системе часть содового рециркулята периодически выводится из цикла. ,которые непрерывно поступают с исходным сырьем и только частично отводятся из цикла с готовым продуктом. Поэтому для предотвращения их излишнего накопления в системе часть содового рециркулята периодически выводится из цикла.Освобожденный от солей выпарки раствор едкого натра доупаривается в следующих корпусах и выпускается в виде жидкого каустика (42-45% 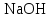 ) или же отправляется нa плавку для получения твердого продукта. ) или же отправляется нa плавку для получения твердого продукта.4.4. Схема экспериментальной установки Лабораторная установка для каустификации содового раствора состоит из реактора 1, снабженного электронагревом и мешалкой (рис.4.2). Регулировка температуры осуществляется при помощи электроспирали 3, контактного термометра 6 и реле 7. Реле замыкает или размыкает цепь электроспирали в зависимости от состояния цепи контактного термометра. В цепь контактного термометра входит столбик ртути, который, поднимаясь при нагреве, соприкасается с подвижным контактом. При этом замыкание цепи термометра сопровождается через реле размыканием цепи нагрева реактора, и наоборот ‑ за размыканием цепи термометра при опускании столбика ртути следует замыкание цепи нагрева. 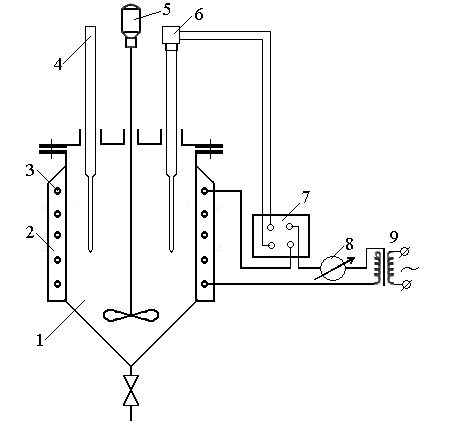 Рис.4.2. Установка для каустификации содового раствора: 1–реактор; 2–теплоизоляция; 3–электроспираль; 4–контрольный термометр; 5–электродвигатель; 6–контактный термометр; 7–реле; 8–амперметр; 9–лабораторный трансформатор  Таким образом обеспечивается поддержание заданной температуры. Заданный температурный уровень устанавливается подвижным контактом. Интенсивность нагрева регулируется лабораторным трансформатором 9 с контролем силы тока по амперметру 8. Таким образом обеспечивается поддержание заданной температуры. Заданный температурный уровень устанавливается подвижным контактом. Интенсивность нагрева регулируется лабораторным трансформатором 9 с контролем силы тока по амперметру 8. 4.5. Методы измерений и ход анализов Для определения концентрации 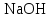 и и  в растворах используется 0,1N в растворах используется 0,1N 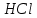 с учетом коэффициента нормальности К. с учетом коэффициента нормальности К.Фильтрат после отделения от шлама анализируется на содержание 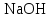 и и  . Для этого 10 мл анализируемого раствора разбавляется в мерной колбе на 100 мл, из которой берется 10 мл на определение общей щелочности ( . Для этого 10 мл анализируемого раствора разбавляется в мерной колбе на 100 мл, из которой берется 10 мл на определение общей щелочности (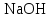 и и  ) и ) и 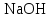 . При определении общей щелочности к 10 мл, взятым из мерной колбы, добавляют 40-50 мл дистиллированной воды, 3-4 капли метилового оранжевого и титруют соляной кислотой до перехода желтой окраски в розовую. Количество израсходованной кислоты V1эквивалентно сумме . При определении общей щелочности к 10 мл, взятым из мерной колбы, добавляют 40-50 мл дистиллированной воды, 3-4 капли метилового оранжевого и титруют соляной кислотой до перехода желтой окраски в розовую. Количество израсходованной кислоты V1эквивалентно сумме 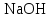 и и  в титруемом растворе. в титруемом растворе.Для определения едкого натра к 10 мл раствора, взятого из мерной колбы, добавляют 40-50 мл дистиллированной воды, 5 мл 10%-го раствора 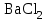 несколько капель фенолфталеина и титруют соляной кислотой до обесцвечивания раствора. Количество израсходованной кислоты V2 эквивалентно содержанию несколько капель фенолфталеина и титруют соляной кислотой до обесцвечивания раствора. Количество израсходованной кислоты V2 эквивалентно содержанию 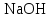 в титруемом растворе. в титруемом растворе.Расчеты концентраций 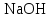 и и  (г/л) ведутся по формулам: (г/л) ведутся по формулам: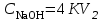 ; ;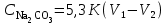 . .Анализ промывных вод ведут так же, как и в случае фильтрата, только без разбавления этих вод в мерной колбе. Для анализа отбирают две пробы по 10 мл, из которых одну анализируют на общую щелочность, другую – на содержание 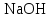 . Расчеты ведут по формулам: . Расчеты ведут по формулам: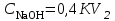 ; ;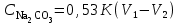 . .4.6. Методика работы В опытах используется исходный содовый раствор концентрацией от 5 до 15 мас.% (по заданию преподавателя). Удельный вес растворов можно определить по данным рис.4.3. В реактор заливается 250 мл этого раствора, включается мешалка и электрообогрев. Последнее осуществляется подключением сети и включением реле. Сила тока 3-4 А устанавливается при помощи трансформатора. При подъеме температуры до уровня ниже заданного на 10-l5° в реактор небольшими порциями добавляется тонкоизмельченная окись кальция, которая берется с 10%-ным избытком от стехиометрического состава, рассчитанного по уравнению 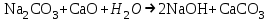 . . Рис. 4.3. Зависимость удельного веса растворов  от концентрации при различных температурах от концентрации при различных температурах(1-20°С; 2-40°С; 3-53°С) 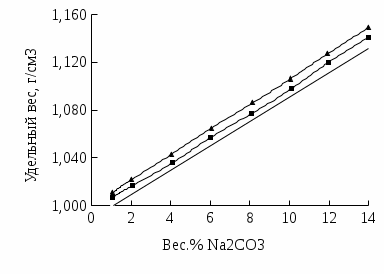 Потребное количество окиси кальция рассчитывается студентами перед началом опыта и отвешивается на технических весах с точностью до 0,01 г. После внесения в реактор всего рассчитанного количества извести отмечается время начала опыта. Каустификация длится 20 мин. Температура контролируется термометром 4. По окончании каустификации выключается реле и отключается сеть электронагрева реактора. При работающей мешалке суспензия через нижний кран сливается в стакан (при опорожнении реактора число оборотов мешалки целесообразно уменьшить). Из стакана суспензия переносится на воронку Бюхнера при включенном вакуум-насосе. Фильтрование длится до полного прекращения стекания капель и фильтрата в колбу Бунзена. Мерным цилиндром замеряется объем фильтрата, ареометром ‑ его плотность, после чего раствор анализируется на содержание 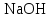 и и  . Полученные данные служат для расчета степени каустификации и количеств всех компонентов маточного раствора при составлении материального баланса. . Полученные данные служат для расчета степени каустификации и количеств всех компонентов маточного раствора при составлении материального баланса.В некоторых опытах хорошо отжатый влажный осадок взвешивается на технических весах с точностью до 0,01г, после этого от него берется с той же точностью навеска 1,5-2 г, которая промывается на конической воронке дистиллированной водой, взятой в количестве 100 мл. Это количество воды пропускается через фильтр с навеской в 3-4 приема. Промывная вода анализируется на содержание 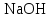 и и  , количество которых пересчитывается на всю массу осадка. , количество которых пересчитывается на всю массу осадка. По окончании каустификации реактор тщательно промывается. Для этого его два раза заполняют водой в количестве 300 мл. Данная работа включает два варианта заданий, каждый из которых предусматривает составление материального баланса каустификации по результатам одного из опытов. ВАРИАНТ I Исследуется влияние концентрации исходного содового раствора на степень каустификации, количества упариваемой воды и выделившейся в осадок соды при упарке слабого щелоке после каустификации до концентрации 42 мас.% 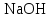 (жидкий продукционный каустик). Каустификацию ведут при концентрации исходного содового раствора 15 и 5 мас. % (жидкий продукционный каустик). Каустификацию ведут при концентрации исходного содового раствора 15 и 5 мас. % 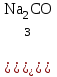 . .По результатам первого опыта составляется материальный баланс каустификации, включая и стадию фильтрации. Результаты опытов заносятся в таблицу приведенного образца (табл. 4.4), а также представляются в виде графика в координатах «степень каустификации (К) ‑ концентрация исходного содового раствора (мас.%)». При этом две экспериментальные точки дополняются третьей в предположении, что при стремлении концентрации содового раствора к нулю степень каустификации приближается к 100%. Результаты расчета материального баланса заносятся в таблицу (табл. 4.5). С помощью данных рис.4.4 определяется состав жидкого продукционного каустика (42 мас. % 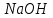 ) и рассчитываются количества упариваемой воды и выделившейся в осадок соды в расчете на 1т продукта. На рис.4.4 используется кривая 3 в предположении, что отделение соды после упарки происходит при 90°С. Расчет проводится по данным обоих опытов, результаты сравниваются по количеству упариваемой воды. ) и рассчитываются количества упариваемой воды и выделившейся в осадок соды в расчете на 1т продукта. На рис.4.4 используется кривая 3 в предположении, что отделение соды после упарки происходит при 90°С. Расчет проводится по данным обоих опытов, результаты сравниваются по количеству упариваемой воды.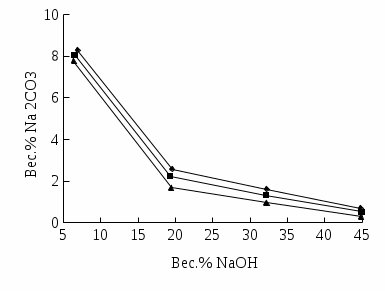 Рис. 4.4. Влияние концентрации NaOH на растворимость Na2CO3 в системе NaOH – Na2CO3 при различных температурах 1–50°С; 2–70°С; 3–90°С  По данным опыта с концентрацией содового раствора 15 мас.% рассчитывается выход соды в продукт в предположении, что сода теряется только с продукционным раствором. Выход сравнивается со степенью превращения (степенью каустификации) в циклической схеме. При обсуждении результатов работы следует обосновать целесообразность организации циклической технологии и использования при этом содовых растворов повышенной концентрации. ВАРИАНТ II Исследуется влияние температуры на степень каустификации, количества упариваемой воды и выделившейся в осадок соды при упарке слабого щелока после каустификации до концентрации 42 мас.% 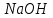 (жидкий продукционный каустик). Всего проводится два опыта с исходным содовым раствором, содержащим 15 мас.% (жидкий продукционный каустик). Всего проводится два опыта с исходным содовым раствором, содержащим 15 мас.% 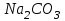 , при двух температурах: 90° и начальной комнатной температуре. Результаты опытов заносятся в таблицу указанного образца (табл.4.4). По результатам опыта при 90° составляется материальный баланс, как в варианте I (табл.4.5). , при двух температурах: 90° и начальной комнатной температуре. Результаты опытов заносятся в таблицу указанного образца (табл.4.4). По результатам опыта при 90° составляется материальный баланс, как в варианте I (табл.4.5).Таблица 4.4 Влияние концентрации исходного содового раствора на процессы каустификации и фильтрации
Так же, как и в варианте I, производится расчет процесса упаривания слабых щелоков по результатам обоих опытов. Опыты сравниваются по количеству упариваемой воды и количеству выделяющейся соды. Таблица 4.5 Материальный баланс каустификации и фильтрации на 250 мл исходного содового раствора с концентрацией 15 мас.% 
По данным опыта с каустификацией при 90° рассчитывается выход соды в продукт в предположении, что сода теряется только с продукционным раствором, содержащим 42 масс.% 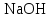 . Выход сравнивается со степенью превращения в циклической схеме. . Выход сравнивается со степенью превращения в циклической схеме.При обсуждении результатов работы обосновать целесообразность проведения процесса каустификации при повышенной температуре и организации циклической технологии. При этом учесть также благоприятное влияние повышенной температуры на последующие после каустификации процессы. 4.7. Инструкция к лабораторной работе 1. Залить 250 мл содового раствора в peaктор, включить мешалку и обогрев реактора. Положение подвижного контакта термометра должно соответствовать минимальной заданной температуре. 2. Рассчитать необходимое количество окиси кальция и отвесить его на технических весах с точностью до 0,01г. 3. При достижении температуры на 10-15° ниже заданной, засыпать окись кальция в реактор. 4. По окончании каустификации выключить нагрев реактора и при медленно работающей мешалке вылить cycпeнзию в стакан и перенести на воронку Бюхнера при включенном вакуум-насосе. 5. По окончании фильтрации замерить объем и плотность фильтрата. Влажный осадок взвесить. 6. Реактор промыть, заполняя два раза водой по 300 мл. 7. Выполнить необходимые анализы и расчеты, построить графики, составить материальный баланс и сделать выводы к результатам работы 4.8. Задание к работе 1. Исследовать зависимость степени каустификаци от состава исходного раствора: концентрация содового раствора 5; 10 и 15 масс.%; температура проведения процесса 90 оС; время каустификации 30 мин. 2. Исследовать зависимость степени каустификации от температуры: концентрация содового раствора 10 или 15 масс.%; температура проведения процесса комнатная, 60, 90 оС; время каустификации 30 мин. 3. Исследовать зависимость степени каустификации от времени: концентрация содового раствора 10 масс.%; температура проведения процесса 50 оС; время каустификации 20, 30, 45, 60 мин. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||