шпоры по химии. КОЛЛОИДНАЯ ХИМИЯ. Коллоидная химия
 Скачать 78.25 Kb. Скачать 78.25 Kb.
|
|
КОЛЛОИДНАЯ ХИМИЯ Дисперсная фаза – мелко раздробленные частицы, равномерно распределённые в дисперсионной среде. Дисперсионная среда – сплошная фаза, составная часть дисперсной системы, в которой равномерно распределены частицы дисперсной фазы. Два общих признака дисперсных систем: гетерогенность и дисперсность. Гетерогенность –– неоднородность, наличие поверхностей раздела фаз. Дисперсность характеризуется удельной поверхностью Sуд: Классификация дисперсных систем Дисперсные системы — это гетерогенные смеси двух и более составных частей, с высокоразвитой поверхностью раздела между ними. По агрегатному состоянию дисперсной фазы и дисперсионной среды. Для удобства, дисперсные системы принято условно обозначать через дробь, где в числителе указывают агрегатное состояние дисперсной фазы, а в числителе – дисперсионной среды: 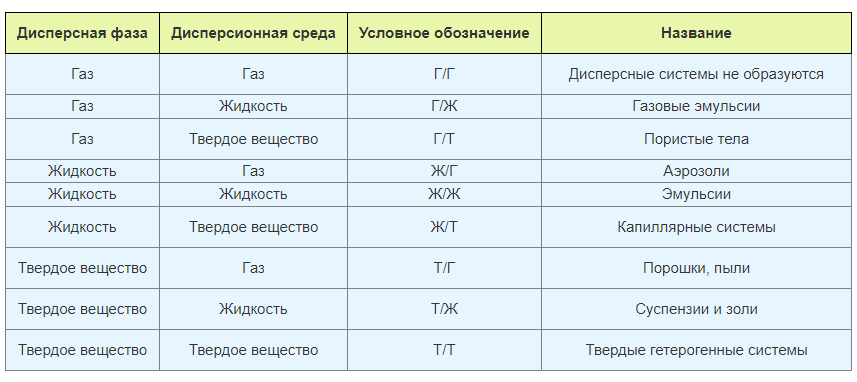 По размеру частиц дисперсной фазы-Грубодисперсные – размер частиц > 10 мкм; -Среднедисперсные – размер частиц от 0,1 до 10 мкм; -Высокодисперсные – размер частиц от 1 до 100 нм; -Наноразмерные – размер частиц от 1 до 10 нм. Предметом изучения коллоидной химии являются высокодисперсные или коллоидные системы (10-9-10-7 м). По наличию взаимодействия частиц дисперсной фазы с молекулами дисперсионной среды— лиофильные – значительное взаимодействие частиц дисперсной фазы с молекулами дисперсионной среды. К ним могут относиться как природные, так и синтетические высокомолекулярные вещества. — лиофобные – слабое взаимодействие частиц дисперсной фазы с молекулами дисперсионной среды. Это коллоидные растворы металлов, их оксидов, гидроксидов и солей. Методы получения дисперсных системМетоды диспергирования. Затрачивая работу против молекулярных сил сцепления, можно различными способами достичь нужной степени дисперсности. 1. Механическое диспергирование. Способ заключается в энергичном и продолжительном растирании, размалывании или распыливании вещества дисперсной фазы и смешивании его с жидкостью, которая служит дисперсионной средой. Крупные частицы дробят, пользуясь ступками, коллоидными мельницами, краскотёрками. Способом механического диспергирования получают фармацевтические препараты, смазочные материалы, пищевые продукты. 2. Диспергирование ультразвуком. В основе метода лежит использование ультразвуковых колебаний (более 20000 колебаний в секунду). Диспергирование при помощи ультразвука эффективно лишь для веществ, имеющих небольшую прочность: сера, графит, краски, крахмал, каучук, желатин. Очень легко получаются этим методом эмульсии, например, эмульсии какао, высококачественные кремы и др. Методы конденсации. В основе конденсационных методов лежат процессы образования частиц дисперсной фазы из веществ, находящихся в молекулярном или ионном состоянии. Процессы эти могут носить как физический, так и химический характер. Физическая конденсация. 1. Метод замены растворителя. Сущность метода заключается в том, что растворитель, в котором вещество растворяется, образуя истинный раствор, заменяется растворителем, в котором это вещество нерастворимо. Например, если спиртовой раствор серы, фосфора или канифоли влить в воду, то раствор становится насыщенным, происходит конденсация, и образуются частицы дисперсной фазы. Это происходит потому, что указанные вещества плохо растворяются в водно-спиртовой смеси. 2. Конденсация при охлаждении пара. Наиболее наглядный пример конденсации из паров – образование тумана или дыма. Другим примером возникновения коллоидных частиц в результате конденсации пара можно назвать камеру Вильсона, используемую в ядерной физике. Химическая конденсация. Получение дисперсных систем методами химической конденсации сводится к образованию молекул нерастворимых веществ в результате химической реакции с последующим укрупнением их до размеров коллоидных частиц. Химические конденсационные методы классифицируются в зависимости от типа химической реакции, лежащей в основе получения золя. К числу реакций, в результате которых при соответствующих условиях могут образовываться вещества в коллоидном состоянии, относятся реакции окисления, восстановления, обмена, гидролиза. МЕЖФАЗНЫЕ ВЗАИМОДЕЙСТВИЯ МЕЖДУ КОНДЕНСИРОВАННЫМИ ФАЗАМИК межфазным взаимодействиям между конденсированными фазами относятся смачивание, растекание и адгезия. Как правило, адгезия и смачивание сопровождают друг друга. Эти явления широко распространены в природе и в различных отраслях промышленности (нанесение лакокрасочных покрытий, получение материалов на основе связующих и наполнителей - бетон, резина и т. д.) Если когезия — это притяжение молекул воды друг к другу, то адгезия — это их притяжение к сторонним телам, например, стенкам сосудов. Тут важно вспомнить, что вода ко всему прочему является полярной жидкостью, то есть каждая ее молекула представляет собой диполь — частицу, у которой один конец заряжен чуть более положительно, а другой — чуть более отрицательно. Растекание – самопроизвольный процесс течения жидкости по поверхности другой конденсированной фазы (при нулевом краевом угле), в результате че-го система переходит в состояние с минимальной энергией Гиббса. Сма́чивание — физическое взаимодействие жидкости с поверхностью твёрдого тела или другой жидкости. Смачивание бывает двух видов: Иммерсионное (вся поверхность твёрдого тела контактирует с жидкостью) Контактное (состоит из трёх фаз — твердая, жидкая, газообразная)  Адгезия обусловливает взаимодействие между твердым телом и находящейся в контакте с ним жидкостью, а смачивание – это явление, которое имеет место на границе трех фаз, из которых одна является твердым телом, а две другие либо несмешивающимися между собой жидкостями, либо жидкостью и газом. |
