Токс. Юданова Т.О_56-1фип_к.р.№2. Контрольная работа 2 по дисциплине токсикологическая химия для подготовки специальности 33. 05. 01 Фармация вариант 8 семестр 9
 Скачать 114.59 Kb. Скачать 114.59 Kb.
|
|
ХК=Д1/Д2. Большинство применяемых пестицидов в той или иной степени токсично для человека и теплокровных животных. Проникнув в организм, пестициды быстро распространяются в нем, избирательно накапливаясь в отдельных частях или органах тела. При этом одни связываются белками или другими компонентами клеток, другие подвергаются метаболизму и выводятся из организма. В больших количествах пестициды накапливаются в печени, почках, сердце. Процессы метаболизма наиболее активно происходят в печени, почках и тканях кишечника. Его продукты выводятся через почки, желудочно-кишечный тракт, легкие, кожу и молочные железы. Под влиянием многих пестицидов нарушается синтез гемоглобина, возникают изменения морфологического состава крови. Некоторые инсектициды вызывают кожные заболевания, действуют на органы дыхания, стимулируют образование опухолей, вызывают нежелательные мутации, нарушают процесс оплодотворения и развития плода. В зависимости от токсичности и степени опасности для человека и теплокровных животных создана гигиеническая классификация пестицидов в целом. Она основана на токсическом воздействии пестицидов, вводимых в желудок экспериментальным животным (крысам), и определяется в миллиграммах на 1 кг живой массы. По этому принципу пестициды делят на четыре группы: - сильнодействующие – ЛД50 – до 50 мг/кг; - высокотоксичные – ЛД50 – от 50 до 200 мг/кг; - среднетоксичные – ЛД50 – от 200 до 1000 мг/кг; - малотоксичные – ЛД50 – более 1000 мг/кг. Все пестициды, применяющиеся в сельском и лесном хозяйстве, распределены по этим группам. Использование сильнодействующих и высокотоксичных пестицидов ежегодно уменьшается. Работа с ними требует особых мер предосторожности, проводится по специальным инструкциям обученным персоналом. Токсичность пестицидов может быть классифицирована по способности проник5ать через кожные покровы, по кумуляции, способности накапливаться в организме, по стойкости сохранения в почве, по способности вызывать опухоли у животных и мутагенности. Степень опасности пестицидов для организмов характеризуется летальной (смертельной), сублетальной и пороговой дозами. Летальная (смертельная) доза (ЛД) вызывает гибель подопытного объекта. Сублетальная доза нарушает жизнедеятельность организма, но не приводит его к гибели. Пороговая доза — это наименьшее количество вещества, которое вызывает изменения в организме, определяемые наиболее чувствительными биохимическими и физиологическими тестами при отсутствии внешних признаков отравления животного. В практике о токсичности пестицидов судят по усредненной характеристике, чаще всего по дозам, вызывающим 50 %-ый эффект, – средне-летальным дозам (ЛД50). Токсичность зависит от целого ряда факторов, главнейшими из которых являются свойства самих пестицидов, биологические особенности живых организмов, против которых они применяются, и влияние внешних условий. Для защиты растений предпочтительны высокотоксичные для вредителей химически стойкие пестициды, не обладающие другими отрицательными свойствами. Для большей сохранности высоколетучих веществ в состав препаратов вводят специальные вещества - антииспарители. Большое значение имеют такие свойства пестицида, как прилипаемость и смачивающая способность, которые увеличивают удерживаемость яда на обработанной поверхности и улучшают контакт вещества с вредителем. Для улучшения этих свойств к препаратам добавляют вспомогательные вещества - прилипатели и смачиватели. Из условий внешней среды наибольшее влияние на токсичность пестицидов оказывает температура. Под ее воздействием может изменяться как активность самого вещества, так и реакция организма. С повышением температуры увеличиваются потери пестицида с обработанной поверхности, но одновременно токсичность его может повышаться, например, в результате образования более токсичных веществ. В то же время в условиях оптимальной температуры организм становится более чувствительным к яду, так как усиливаются процессы обмена веществ. Пестициды, токсичность которых увеличивается с повышением температуры, относят к веществам с положительным температурным коэффициентом, а токсичность которых с повышением температуры снижается - к пестицидам с отрицательным температурным коэффициентом. Большинство современных препаратов принадлежит к первой группе. Продолжительность сохранения токсичности резко уменьшается под воздействием влажности воздуха, солнечной радиации, ветра и осадков. Эти факторы косвенно снижают токсичность ядовитого вещества. На токсичность пестицидов оказывают большое влияние и анатомо-морфологические особенности вредителей. Например, взрослые особи щитовок, защищенные восковым щитком, не погибают после обработки контактными инсектицидами, против них эффективны лишь системные пестициды. В разных фазах развития организм насекомого неодинаково воспринимает воздействие яда. Во многих случаях фазы яйца и куколки устойчивее личинок и взрослых насекомых, но некоторые пестициды действуют преимущественно на яйца насекомых. Ежегодно утверждается и доводится до сведения потребителей и специалистов защиты растений межведомственной комиссией, в которукю входят кроме специалистов защиты растений, токсикологи, экологи, специалисты водного хозяйства и здравоохранения, Список пестицидов и агрохимикатов, разрешенных к применению на территории Российской федерации. В нем приводится перечень инсектицидов и акарицидов, наименование препаративной формы, указания изготовителей, нормы расходов препаратов и их концентрации, объект, против которого они используются и ограничения по пользованию территорией, на которых они применялись. Химическая структура, изолирование и методы определения карбарила. 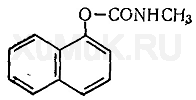 Карбарил (севин, арилат, ветокс, динапон, карбамат, карботокс, севинокс и др.) — 1-нафтил-N-метилкарбамат — является представителем ариловых эфиров N-метил-карбаминовой кислоты. Карбарил — белое кристаллическое вещество (т. пл. 142 °С) слаборастворимое в воде (менее 0,1 % при 20 °С), хорошо растворимое в большинстве органических растворителей. В нейтральных, кислых и щелочных растворах карбарил гидролизуется. Одним из продуктов его гидролиза является 1-нафтол. Этот препарат выпускается в виде 50—85 %-го смачивающегося порошка, дуста и гранул. Применяется как высокоэффективный инсектицид контактно-кишечного действия для борьбы с вредителями сельскохозяйственных культур и деревьев. В течение сезона его используют 1—2 раза, чередуя с такими препаратами, как фосфамид и др. При длительном воздействии карбарила на организм нарушаются функции печени. Карбарил быстро всасывается из желудка. Через 5 мин после поступления карбарила в желудок он появляется в крови, а через 30 мин отмечается максимальное накопление его в органах. Через 2—3 сут после попадания в организм карбарил не обнаруживается в биоматериале. Метаболитом карбарила является 1-нафтол и ряд других соединений. Выделение карбарила из биологического материала. 100 г измельченного биологического материала вносят в колбу вместимостью 500 мл, прибавляют воду до получения кашицеобразной массы, а затем прибавляют 100 мл бензола. Содержимое колбы настаивают 4 ч при периодическом взбалтывании. После этого бензольную вытяжку сливают с биологического материала, который еще 2 раза настаивают по 2 ч с новыми порциями бензола (по 50 мл). Бензольные вытяжки соединяют и фильтруют через бумажный фильтр. Профильтрованные объединенные бензольные вытяжки вносят в колбу, из которой под вытяжным шкафом на водяной бане отгоняют бензол до небольшого остатка. Неперегнавшийся остаток бензола переносят из колбы в фарфоровую чашку, которую помещают в вытяжной шкаф с хорошей тягой, и при комнатной температуре бензол выпаривают досуха. Сухой остаток растворяют в 5 мл этилового спирта, полученный раствор используют для обнаружения карбарила. Обнаружение карбарила Для обнаружения карбарила применяют цветные реакции и метод хроматографии в тонком слое сорбента. Реакция__с_пикриновой_кислотой_.'>Реакция с пикриновой кислотой. На предметное стекло наносят каплю исследуемого раствора, который выпаривают досуха. К сухому остатку прибавляют каплю 1 %-го раствора пикриновой кислоты. Через 10—15 мин появляются темно-желтые кристаллы, собранные в пучки. При малом содержании карбарила в пробе кристаллы могут появляться только через 5—10 ч. Реакция с 4-аминоантипирином. В пробирку вносят 1 мл спиртового раствора исследуемого вещества и 0,5 мл аммиачной буферной смеси. Пробирку закрывают пробкой с воздушным холодильником и нагревают на водяной бане (55—60 °С) в течение 15 мин. После охлаждения жидкости прибавляют 3 капли 0,5 %-го раствора 4-аминоантипирина и 5 капель раствора гексацианоферрата (II) калия. В присутствии карбарила появляется оранжево-красная окраска, которая при экстракции хлороформом переходит в органическую фазу. Эту реакцию дает и 1-нафтол. Приготовление аммиачной буферной смеси (см. Приложение 1, реактив Б4). Реакция со смесью хлорида меди и бромида натрия. В пробирку вносят 1 мл спиртового раствора исследуемого вещества и 0,4 мл 0,5 н. раствора гидроксида натрия. Пробирку закрывают пробкой с воздушным холодильником и нагревают на водяной бане (55 °С) в течение 10 мин. После охлаждения жидкости к ней прибавляют 0,5 н. раствор соляной кислоты до рН = 5...6 и 1 мл свежеприготовленной смеси хлорида меди и бромида натрия. Если в растворе присутствует карбарил, то при нагревании жидкости до 60 °С появляется красно-фиолетовая или сине-фиолетовая окраска. При взбалтывании этой жидкости с хлороформом окрашенное соединение переходит в слой органического растворителя. Эту реакцию дает и 1-нафтол. Приготовление смеси хлорида меди и бромида натрия . Обнаружение карбарила глетодом хроматографии. На линию старта на хроматографической пластинке наносят каплю исследуемого раствора и каплю раствора «свидетеля» (0,01 %-го спиртового раствора карбарила). Пятна подсушивают на воздухе, а затем пластинку вносят в камеру для хроматографирования, на дно которой налит хлороформ. После того как жидкость поднимется на 10 см выше линии старта, пластинку вынимают из камеры, подсушивают на воздухе и облучают УФ-светом. При наличии карбарила и его метаболита (1-нафтола) в пробе пятна их флуоресцируют. После облучения пластинки УФ-светом ее опрыскивают раствором диазотированной сульфаниловой кислоты. При этом пятна на пластинке приобретают красную окраску. Побочные эффекты компонентов биологически активных добавок. |
