Контрольная работа 3 Витамины. Понятие о витаминах. Заслуги ученых в развитии учения о витаминах
 Скачать 0.66 Mb. Скачать 0.66 Mb.
|
|
Контрольная работа № 3 Витамины. 1. Понятие о витаминах. Заслуги ученых в развитии учения о витаминах. 2. Классификация и номенклатура витаминов. Провитамины. 3. Гиповитаминозы, авитаминозы, гипервитаминозы, причины их возникновения. 4. Механизм действия жирорастворимых витаминов. 5. Механизм действия водорастворимых витаминов. 6. Витамин А.Химическое строение, суточная потребность, биологическая роль, явление недостаточности. 7. Витамин Д. Химическое строение, суточная потребность, биологическая роль, явление недостаточности. 8.Витамин Е. Химическое строение, суточная потребность, биологическая роль, явление недостаточности. 9.Витамин К. Химическое строение, суточная потребность, биологическая роль, явление недостаточности. 10. Витамин С. Химическое строение, суточная потребность, биологическая роль, явление недостаточности. 11. Витамины В1. Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 12. Витамин В2. Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 13. Витамин В6. Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 14. Витамин В12. Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 15. Витамин Вс, Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 16. Витамин РР, Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 17. Витамин В5, Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 18. Витамин Н. Химическое строение, распространение, суточная потребность, биологическая роль, явление недостаточности. 19. Антивитамины. Механизм действия. Примеры. 1. Понятие о витаминах. Заслуги ученых в развитии учения о витаминах. Витамины – это низкомолекулярные орган. содеин. различной хим. природы и строения, не явл. источников энергии и пласт. материалом, не синтезируются в организме человека или частично синтезируются микрофлорой кишечника (К, Н, В6, В12, пантотеновая кислота), необходимы человеку в небольших кол-вах (мг, мкг). История развития: 1) Японский врач К. Татаки пришёл к заключению, что в мясе, молоке и свежих овощах содержатся вещ-ва, предотвращающие заболевание бери-бери. 2) Голландский врач К. Эйкман заметил, что у кур, получавших полированный рис, развивалось подобие бери-бери, а если ели неочищенный рис – они выздоравливали. 3) Н.Н. Лунин открыл витамины в 1880 году. Лунин утверждал, что для сохранения жизни животного, помимо белков, жиров, углеводов, солей и воды, необходимы ещё и другие, дополнительные вещества. Придавая им большое значение, Н. И. Лунин писал: «Обнаружить эти вещества и изучить их значение в питании было бы исследованием, представляющим большой интерес». Вывод Лунина был принят в штыки научным сообществом, так как другие ученые не смогли воспроизвести его результаты. Одна из причин была в том, что Лунин в своих опытах использовал тростниковый сахар, в то время как другие исследователи использовали молочный — плохо очищенный и содержащий некоторое количество витамина B. 4) В 1895 году В.В. Пашутин пришел к выводу, что цинга является одной из форм голодания и развивается от недостатка в пище какого-то органического вещества, создаваемого растениями, но не синтезируемого организмом человека. Автор отметил, что это вещество не является источником энергии, но необходимо организму и что при его отсутствии нарушаются ферментативные процессы, что приводит к развитию цинги. Тем самым В. В. Пашутин предсказал некоторые основные свойства витамина C. 5) Первым выделил витамин в кристалл. виде Казимир Функ в 1911. Год спустя придумал название от vita – жизнь. 2. Классификация и номенклатура витаминов. Провитамины.
3) Витаминоподобные: холин, липоевая кислота, В15 (пангамовая к-та), убихинон, витамин U (противоязвенный), линолевая и линоленовая кислота. Провитамины – это предшественники витаминов, или неактивные формы витаминов. Основные провитамины: Каротин — жёлто-оранжевый пигмент, непредельный углеводород из группы каротиноидов, провитамин витамина А-Триптофан — незаменимая аминокислота в организме человека, является своего рода провитамином, так как бактериальная флора кишечника человека может синтезировать из неё витамин B. Эргостерин (под действием УФО) — провитамин витамина D2, полициклический спирт (стероид), содержащийся в дрожжах, грибах, некоторых водорослях. 7-Дегидрохолестерин — провитамин витамина D3, содержится в коже человека. 3. Гиповитаминозы, авитаминозы, гипервитаминозы, причины их возникновения. Гиповитаминозы – состояния, которые возникают вследствие недостаточности содержания какого-либо витамина в организме, при этом отсутствует четкая клиническая картина. Симптомы: слабость, головная боль, быстрая утомляемость, низкая сопротивляемость по отношению к инфекциям. Причины гиповитаминозов: 1) недостаток витаминов в пище. 2) нарушения всасывания в ЖКТ. 3) врождённые дефекты ферментов, участвующих в превращениях витаминов. 4) действие структурных аналогов витаминов (антивитамины). Авитаминозы – заболевания, связанные с отсутствием того или иного витамина в организме. Авитаминозы являются следствием гиповитаминозов и имеют четкую клиническую картину, характерную для данного авитаминоза. Например: цинга, рахит, куриная слепота, пеллагра. Причины возникновения гипо- и авитаминозов делятся на 2 группы:
Гипервитаминозы – заболевания, связанные с избытком какого-либо витамина в организме. Их часто вызывают жирораств. витамины, способные накапливаться в организме. В наст. время наблюдаются редко. 4. Механизм действия жирорастворимых витаминов. Механизм действия жирорастворимых витаминов объясняется тем, что они влияют на генетический аппарат клетки-мишени, то есть проникают в мембрану и вызывают биосинтез белков.
5. Механизм действия водорастворимых витаминов. Связь витаминов с ферментами можно рассмотреть на примере водорастворимых витаминов. Они входят в состав ферментов в активных (коферментных) формах и участвуют в углеводном, белковом, липидном и минеральном обменах. Это является и механизмом действия водорастворимых витаминов.
6. Витамин А. Хим. строение, суточная потребность, био. роль, явление недостаточности. Витамин А (ретинол, антексерофтальмический) - циклический ненасыщенный одноатомный спирт, состоящий из 6-членого кольца (бета-ионон), 2х остатков изопрена и ЩР группы. Содержание: 2,7 мг. 2-5 мг в виде бета-каротина. Печень крупного рогатого скота, яичный желток, молоко, масло, сметана, сливки, красномякотные овощи (в виде провитаминов - каротидов). Откладывание – печень (200 мг на 100 г ткани). С  труктура: А1, А2, цис-форма – неовитамин А. В витамине А2 дополнительная связь в кольце бета-ионона. Хорошо растворим в жирах и жирорастворителях: бензоле, хлороформе, эфире, ацетоне. В организме легко окси. при участии спец. ферментов с образованием ретиненов (ретиналя). труктура: А1, А2, цис-форма – неовитамин А. В витамине А2 дополнительная связь в кольце бета-ионона. Хорошо растворим в жирах и жирорастворителях: бензоле, хлороформе, эфире, ацетоне. В организме легко окси. при участии спец. ферментов с образованием ретиненов (ретиналя). Гиповитаминоз: торможение роста, снижение массы, истощение, спец. поражения кожи (ороговевание). Авитаминоз: поражение эпителия ЖКТ, мочеполового и дых. аппаратов, сухость роговицы – куриная слепота (гемералопия). Хсерофтальмия – закупорка слёзного канала в связи с ороговением эпителия. Кератомаляция – размягчение роговицы. Гиперкератоз – повышенная сухость эпителия. Гипервитаминоз (печень медведя, тюленя): воспаление глаз, выпадение волос, потеря аппетита, головные боли, рвота, тошнота, бессонница. Механизм/ Био. роль: 1) Оказывает влияние на барьерную фун-ю кожи, слиз. оболочек, обладает антиоксид. действием. 2) Связывание витамина А с цитозольными рецепторами, где он связывается с ядром (внутриклеточный механизм). В ядре вызывает репрессию генов, регулируя биосинтез белков (гликопротеинов и родопсина). 3) Обеспечивает рост, дифференцировку ткани. 7. Витамин Д. Хим. строение, суточная потребность, био. роль, явление недостаточности. Витамин D (кальциферолы, антирахитический). Содержание: 10-25 мкг. Масло, желток яиц, печень, икра, рыбий жир, УФ- излучение. D2 – подсолн, оливк. масло. Структура: бесцветные кристаллы, t плав. = 115-117 С, нераств. в воде, но растворимы в жирах и жирорастворителях. Н  едостаток: авитаминоз проявляется в рахите, характерным для детей в грудном и раннем возрасте, обусловлен нарушением Р-Са обмена. В начальном периоде заболевания (204 нед.) преобладают невролог. и вегет. симптоматика: дети капризны, беспокойны, раздражительны, плохо спят, нарушается аппетит, часто возникает чрезмерная потливость, особенно волосистой части головы. При этом возникает сильный зуд, и ребёнок трётся головой о подушку. Так возникает характерное для рахита облысения затылочной области. Тонус мышц ослаблен. едостаток: авитаминоз проявляется в рахите, характерным для детей в грудном и раннем возрасте, обусловлен нарушением Р-Са обмена. В начальном периоде заболевания (204 нед.) преобладают невролог. и вегет. симптоматика: дети капризны, беспокойны, раздражительны, плохо спят, нарушается аппетит, часто возникает чрезмерная потливость, особенно волосистой части головы. При этом возникает сильный зуд, и ребёнок трётся головой о подушку. Так возникает характерное для рахита облысения затылочной области. Тонус мышц ослаблен.В 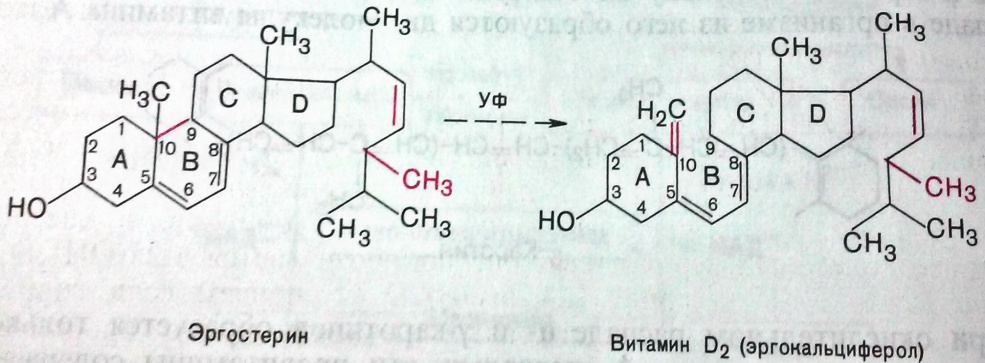 период разгара заболевания начинают прогрессировать костные изменения: возникают остеомаляция грудной клетки, черепа, нижних конечностей. Ребёнок может отставать в психомоторном и физ. развитии. Профилактика – прогулки не менее 30 мин. в день. период разгара заболевания начинают прогрессировать костные изменения: возникают остеомаляция грудной клетки, черепа, нижних конечностей. Ребёнок может отставать в психомоторном и физ. развитии. Профилактика – прогулки не менее 30 мин. в день. Авитаминоз у взрослых – остеопороз вследствие вымывания отложившихся солей (хрупкие). Механизм/ Био. роль: Витамин D регулирует обмен Са и Р. 1) Индуцирует синтез иРНК, кодирующий Са-связывающий белок. 2) Усиливает транспорт Са через эпителий слиз. оболочки тонкого кишечника при всасывании с участием Са-связ. белка, Са-зависимой АТФазы и ионов Na+. 3) Способствует мобилизации Са из костной ткани. 4) Стимулирует реабсорбцию Са и Р в почечных канальцах. 8. Витамин Е. Хим. строение, суточная потребность, био. роль, явление недостаточности. Витамин Е (токоферолы, антистерильный). Представляют собой производные токола. Содержание: 5 мг. Масла, салат, капуста, семена злаков; мясо, сливочное масло, яичный желток. Откладывается в мышцах, ПЖЖ, жировой ткани, поэтому долго нет авитаминоза. Структура: это бесцветные маслянистые жидкости, хорошо раств. в жирах (маслах), устойчивы к нагреванию, быстро разрушаются под действием УФ-излучений. Недостаточность: в основном в тропических странах, где в рационе преобладают углеводы. У животных – нарушение эмбриогенеза, у самцов – атрофия половых желез, что ведёт к стерильности. К спец. проявлениям недостаточности витамина относятся мышечная дистрофия, жировая инфильтрация печени, дегенерация спинного мозга. Механизм/ Био. роль: 1) явл. наиболее активными жирорастворимыми антиоксидантами: разрушают наиболее реактивные формы О2, т.о. предохраняют от окисления полиненасыщенные жирные кислоты. 2) играют спец. роль в обмене селезёнки. 9. Витамин К. Хим. строение, суточная потребность, био. роль, явление недостаточности. Витамин К (нафтохиноны, антигеморрагический). К1 – филлохинон, К2 – метахинон. Содержание: 1 мг. Зелёные листья каштана, крапивы, люцерны. Капуста, шпинат, тыква, зелёные томаты, арахисовое масло, ягоды рябины; печень свиньи. Структура: К1 – производное 2-метил-1,4-нафтохинона, в 3м положении фитильный радикал, содержат 20 атом С; светло-жёлтая жидкость, неустойчивая при нагреваниив щел. среде и при облучении. К2 – содержит в бок. цепи от 6 до 9 изопреновых единиц; жёлтые кристаллы, также неустойчив. Оба нерастворимы в воде, но растворимы в бензоле, хлороформе, ацетоне и гексане. Авитаминоз: самопроизвольные и паренхиматозные кровотечения, любые поражения сосудов могут привести к кровотечению. Обычно развивается при нарушении процесса всасывания жиров в кишечнике. У детей грудного возраста часто обильные подкожные кровотечения, которые наблюдаются при геморрагическом диатезе, который явл. следствием недостаточности свёртывания крови у матери. Механизм/ Био. роль: 1) участие в процессе свёртывания крови. Он участвует в активации факторов свёртывания крови: протромбина (фактор II), проконвертина (фактор VII), фактора Кристмаса (фактор IX) и фактора Стюарта (фактор X). Эти белковые факторы синтезируются как неактивные предшественники. Один из этапов активации - их карбоксилирование по остаткам глутаминовой кислоты с образованием γ-карбоксиглутаминовой кислоты, необходимой для связывания ионов кальция. 2) Витамин К участвует в реакциях карбоксилирования в качестве кофермента. 3) Антивитамином явл. дикумарол, который вызывает уменьшение протромбина, что ведёт к кровотечению. Антикоагулянтом при этом явл. проивзодное витамина К – варфарин. 10. Витамин С. Хим. строение, суточная потребность, био. роль, явление недостаточности. Витамин С (аскорбиновая кислота, антискорбутный). Это лактон кислоты, близкой по структуре к глюкозе. 2 формы: восстановленная (АК) и окисленная (дегидроаскорбиновая кислота, ДАК). Содержание: 75мг. Шиповник, облепиха, чёрная смородина, цитрусовые, перец, салат, капуста, хрен, ягоды рябины, картофель, хвоя. С  труктура: аксорбиновая кислота относится к сильным к-там, кислый характер её обусловлен наличием 2х обратимо диссоциирующих енольных гидроксилов у 2-го и 30го угл. атомов. Аксорбиновая к-та содержит 2 асиммерт. атома углерода в 4-ом и 5-м положениях, что позволяет образовывать 4 оптических изомера. труктура: аксорбиновая кислота относится к сильным к-там, кислый характер её обусловлен наличием 2х обратимо диссоциирующих енольных гидроксилов у 2-го и 30го угл. атомов. Аксорбиновая к-та содержит 2 асиммерт. атома углерода в 4-ом и 5-м положениях, что позволяет образовывать 4 оптических изомера. В слабощелочной и нейтр. среде происходит гидролиз лактонового кольца, и ДАГ превращ. в дикетогулоновую к-ту, лишённую био. активности. Недостаток: потеря способности депонировать межклет. «цементирующие» вещ-ва, что вызывает поражения сосуд. стенок и опорных тканей. У человека при недостаточности вит. С отмечается уменьшение массы, общая слабость, одышка, боль в сердце, сердцебиение. При цинге в первую очередь поражается кров. система: сосуды становятся хрупкими и проницаемыми, т.о. происходят кровоизлияния под кожу (петехии); кровоизлияния во внутр. органы и слиз. оболочки. Также характерно кровоточивость дёсен; дегенеративные изменения со стороны одонтобластов и остеобластой приводят к кариесу, расшатыванию, размалыванию и выпадению зубов. Механизм/ Био. роль: 1  ) Участвует в гидроксилировании пролина и лизина в оксипролин и оксилизин, которые принимают участие в синтезе коллагена соед. ткани, сосудов и дентина зуба; оксипролин и оксилизин участвует в синтезе гликозаминогликанов (гиалуроновой кислоты). ) Участвует в гидроксилировании пролина и лизина в оксипролин и оксилизин, которые принимают участие в синтезе коллагена соед. ткани, сосудов и дентина зуба; оксипролин и оксилизин участвует в синтезе гликозаминогликанов (гиалуроновой кислоты).2) Участвует в процессе кроветворения: а) защищает гемоглобин от окисления; б) участвует во всасывании и транспорте железа; в) ускоряет высвобождение железа из ферритина; г) влияет на процесс образования активной формы фолиевой к-ты; д) принимает участие в превращении Fe3+ в Fe2+. 3) Участвует в синтезе гормонов: а) коркового вещ-ва надпочечников – кортикостероидов; б) мозгового вещ-ва надпочечников – адреналина (ДОФА переходит в тирозин); в) простангландинов; г) гормонов щит. железы. 4) Активирует неспецифическую защиту организма: а) активирует синтез интерферона; б) стимулирует фагоцитоз; в) явл. природным антиоксидантом. 11. Витамины В1. Хим. строение, распространение, суточная потребность, био. роль, явление недостаточности. Витамин В1 (тиамин, антиневритный). Содержание: 1,2–2,2 мг. Дрожжи, пшенич. хлеб из муки, солее, фасоль, горох, печень, почки, мозг. С  труктура: Наряду с аминогруппой содержит атом S. 2 кольца – пиримидиновое и тиазоловое, соединены метиленовой связью. Водные рры в кислой среде выдерживают нагревании до высоких t без снижения био. активности (в др. средах разрушается при t>). При окислении образуется тиохром, дающий синюю флюоресценцию при УФ-облучении. труктура: Наряду с аминогруппой содержит атом S. 2 кольца – пиримидиновое и тиазоловое, соединены метиленовой связью. Водные рры в кислой среде выдерживают нагревании до высоких t без снижения био. активности (в др. средах разрушается при t>). При окислении образуется тиохром, дающий синюю флюоресценцию при УФ-облучении. Легко всасывается в кишечнике, но не накапливается в тканях и не обладает и не обладает токсическими св-вами. Избыток быстро выводится мочой. Недостаток: при авитаминозе развивается бери-бери. В Европе: синдром Вернике (энцефалопатия), синдром Вейса (поражение ССС). Полиневритная (сухая) форма – нарушение ПНС. Пернициозная форма – летальный исход из-за поражения ССС. Ранние симптомы: нарушения моторной и секреторной фун-и пищ. тракта: потеря аппетита, атония кишечника, потеря памяти на недавние события; одышка, сердцебиение. Дальше: нарушения ПНС (ощущения покалывания, онемения и боли по ходу нервов). В этот же период - явления серд. недостаточности. Развитие отриц. азотистого баланса. Механизм / Био. роль: В превращении витамина В1 в его активную форму – тиаминпиро(ди)фосфат (ТДФ, ТПФ), участвует спец. АТФ-зависимый фермент тиаминпирофосфокиназа. ТПФ входит в состав 3х ферментных систем: пируват- и альфа-кетоглутаратдегидрогеназных комплексов, катализирующих окис-восстан. декарбоксилирование пировиноградной и альфа-кетоглутаровой к-т, и транкетоназных комплексов. В составе транскетоназы ТПФ участвует в переносе гликоальдегидного радикала от кетосахаров на альдосахара. ТПФ явл. коферментом пируватдекарбоксилазы клеток дрожжей. ТПФ участвует в окси. декарбоксилировании гликосиловой к-ты и альфа-кетокислот. 12. Витамин В2. Хим. строение, распространение, суточная потребность, био. роль, явление недостаточности. Витамин В2 (рибофлавин, витамин роста). С 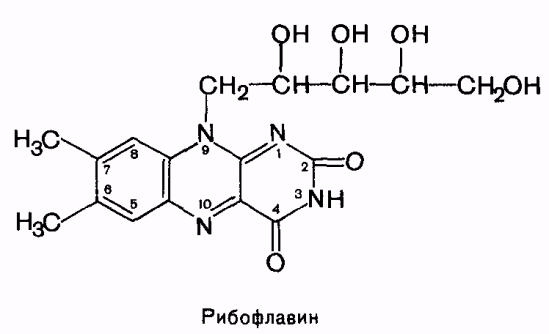 одержание: 1,7 мг (больше в стар. возрасте и при тяжёлой физ. работе). Почти во всех тканях и растениях; хлеб, яйца, молоко, семена злаков. В молоке в свободном состоянии, а в печени и почках животных прочно связан с белками в составе ФАД и ФМН. одержание: 1,7 мг (больше в стар. возрасте и при тяжёлой физ. работе). Почти во всех тканях и растениях; хлеб, яйца, молоко, семена злаков. В молоке в свободном состоянии, а в печени и почках животных прочно связан с белками в составе ФАД и ФМН.Структура: в основе гетероцикл. соединения изоаллоксазил, к которому в положении 9 присоединён 5-атомный спирт рибитол. Хорошо растворим в Н2О, устойчив в кислых ррах, разруш. в рН>=7. Чувствителен к УФ. Легко оксил. и восстанавливается. Жёлтый – в окис. форме, в восстан – бесцветный. Недостаток: остановка роста, выпадение волос, воспалит. процессы языка, губ, углов рта, катаракта, кератиты, васкуляризация роговой оболочки. Авитаминоз: общая мыш. слабость и слабость сердечной мышцы. Механизм/ Био. роль: Входит в состав флавиновых коферментов, в частности ФМН, ФАД. 2 типа реакций, катализируемых этими ферментами: 1) фермент осущ. прямое окисление с участием О2 (дегидрирования). Это оксидазы L- и D-аминк-т, альдегидроксидаза, ксантиноксидаза и др; 2) вторая группа реакций, катализируемых флавопротеинами, характеризуется переносом электронов и протонов не от исходного субстрата, а от восстановленных пиридиновых коферментов. ФМН синтезируется в организме животных из свободного рибофлавина и АТФ при участии спец. фермента рибофлавинкиназы: Рибофлавин + АТФ =Mg2+= Рибофлавин-5’-фосфат (ФМН) + АДФ. Образование ФАД в тканях также протекает при участии спец. АТФ-зависимого фермента ФМН-аденилтрансферазы: ФМН + АТФ =Mg2+= ФАД + пирифосфат. 13. Витамин В6. Хим. строение, распространение, суточная потребность, био. роль, явление недостаточности. Витамин В6 (пиридоксин, антидерматидный). С  одержание: 2 мг (косвенные подсчёты, т.к. синтезируется микрофлорой кишечника). Хлеб, горох, фасоль, мясо, почки, печень. одержание: 2 мг (косвенные подсчёты, т.к. синтезируется микрофлорой кишечника). Хлеб, горох, фасоль, мясо, почки, печень. Структура: Производное 3-оксипиридина. 3 производных: пиридоксин, пиридоксаль и пиридоксамин. В6 хорошо растворим в Н2О и С2Н5ОН. Чувствительны к влиянию света при рН=7. Недостаточность: акродиния (поражение кожи лапок, хвоста, носа, ушей). Шелушение кожи, её изъязвления. У человека недостаточность реже, хотя некоторые паллегроподобные дерматиты, не поддающиеся лечению РР, легко проходят при введении пиридоксина. У детей дерматиды, поражение НС (эпилептиформные припадки. Из биохим. нарушений при недостаточности В6 – гомоцистинурия и цистатионинурия, нарушения обмена типтофана, выражающиеся в повышении экскреции с мочой ксантуреновой к-ты и снижении кол-ва экскретируемой кинуреновой к-ты. Механизм/ Био. роль: К 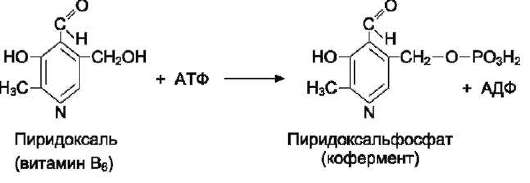 оферментные фун-и выполняют только фосфорилированные производные пиридоксаля и пиридоксамина. Пиридоксалькиназа активна в ткани мозга: оферментные фун-и выполняют только фосфорилированные производные пиридоксаля и пиридоксамина. Пиридоксалькиназа активна в ткани мозга:Пиридоксаль +АТФ = Пиридоксальфосфат + АДФ. В животных тканях происходит взаимопревращения пиридоксальфосфата и пиридоксаминфсофата, в частности в реакциях трансаминирования, дезаминирования и декарбоксилирования аминок-т. Пиридоксальфосфат явл. простетической группой аминотрансфераз, катализирующих обратимый перенос аминогруппы от аминок-т на альфа-кетокислоту, и декарбоксилаз аминок-т, осуществляющих необратимое отщепление СО2 от СООН-группы с образованием биогенных аминов. Установлена коферментная роль пиридоксальфосфата в ферментативных реакциях неоксиленного дезаминирования серина и треонина, оксиления трипфтофана, превращение S-содержащих аминок-т, взаимопревращения серина и глицина. 14. Витамин В12. Хим. строение, распр., сут. потребность, био. роль, явление недостаточности. Витамин В12 (кобаламин, антианемический). Содержание: 3 мкг (0,003 мг). Единственный витамин, синтез которого осущ. исключительно микроорганизмами. Мясо, говяжья печень, рыба, молоко, яйца. Накопление – печень. Структура: центральный атом кобальта соединен с атомами азота четырех восстановленных пиррольных колец, образующих порфириноподобное корриновое ядро, и с атомом азота 5,6-диметилбензимидазола. Недостаток: Первыми симптомами дефицита (гиповитаминоза) витамина В12 становятся: неприятный запах от тела; ощущение жжения и покалывания в языке; язвочки в полости рта и на языке; нервозность и невриты; слабость, быстрая утомляемость; головокружение; сердцебиение и отдышка при физических нагрузках; снижение аппетита; бледность с легкой желтушностью кожи; чувство онемения и ползания мурашек по телу; боли в спине, затруднения при ходьбе. Авитаминозвитамина В12 приводит в пернициозная анемии. Увеличение размеров эритроцитов, снижение количества эритроцитов в кровотоке, снижение концентрации гемоглобина в крови. Нарушение кроветворения связано в первую очередь с нарушением обмена нуклеиновых кислот, в частности синтеза ДНК в быстроделящихся клетках кроветворной системы. Также нарушения деятельности нервной системы и резкое снижение кислотности желудочного сока. Оказалось, что для активного процесса всасывания витамина В12 в тонкой кишке обязательным условием является наличие в желудочном соке особого белка – гастромукопротеина (внутреннего фактора Касла), который специфически связывает витамин В12 в особый сложный комплекс. Нарушение синтеза внутреннего фактора в слизистой оболочке желудка приводит к развитию авитаминоза В12 даже при наличии в пище достаточного количества кобаламина. Механизм/ Био. роль: Ферментативная форма: метилкобаламин и дезоксиаденокобаламин. 1) Синтез пуриновых и пиримидиновых оснований. 2) Реакции трансметилирования, в которых метилкобаламин выполняет роль промежуточного переносчика СН3-группы, например, реакция синтеза метионина.  3) Осуществление внутримолекулярный перенос H2 в реакциях изомеризации.  15. Витамин Вс, Хим. строение, распространение, суточная потребность, био. роль, явление недостаточности. Вс (В9, фолиевая к-та, антианемический). Содержание: 1-2 мг. Зелёные листья растений, дрожжи. Печень, почки, мясо, микроорганизмы кишечника. Структура: сост. из остатка 2-амино-4-окси-6-метилптеридина, парааминобензойной и L-глутаминовой к-т. Ограничено растворима в Н2О, но хорошо растворима в разбавленных р-рах спирта, имеет спектры поглощения УФ-области. Недостаток: У человека наблюдается клиническая картина макроцитарной анемии, похожая на проявления пернициозной анемии, хотя нарушения НС отсутствуеют. Иногда диарея. Нарушения биосинтеза ДНК в клетках костного мозга, в которых в норме осущ. гемопоэз, поэтому в периф. крови появляются мегалобласты с относительно меньшим содержанием ДНК. Дефект нервной трубки у эмбриона, у подростков – суицидальные наклонности. Механизм/ Био. роль: Коферментная форма – тетрагидрофолиевая кислота. Её фун-и связаны с переносом одноуглеродных групп, первичными источниками которых в организме явл. бета-углеродный атом серина, альфа-углеродный атом глицина, углерод метильных групп метионина и др. Производные ТГФК участвуют в переносе одноуглеродных фрагментов при биосинтезе метионина и тимина (перенос метильной группы СН3), серина (перенос оксиметильной грпыы СН2ОН), образовании пуриновых и пиримидиновых оснований (перенос формильной группы СН-NН) и др. 16. Витамин РР, Хим. строение, распространение, суточная потребность, био. роль, явление недостаточности. Витамин РР (никотинамид, никотиновая кислота, В3, антипелагрический). С  одержание: 18 мг. Рис, злеб, картофель, мясо, печень, почки, морковь. одержание: 18 мг. Рис, злеб, картофель, мясо, печень, почки, морковь.Структура: Соединение пиримидинового ряда. Малорастворим в Н2О (1%), хорошо в ррах щелочей. Недостаток: Авитаминоз – пеллагра. Дерматиты, диарея, нарушение нерв. деятельности (деменция). Дерматиты симметричны, участки, подверженные УФ. Поражения кишечника: анорексия, тошнота, боли в области живота. Стоматиты, гингивиты, поражения языка со вздутием и трещинами. Симптомы особенно резко выражены у больных с недостаточным белковым питанием (это объясняется недостатком триптофана, который явл. предшественником витамина). Механизм/ Био. роль: Входит в состав НАД и НАДФ, являющихся коферментами большого числа обратимо действующих в ОВР дегидрогеназ. В процессе био. окисления НАД и НАДФ выполняют роль промежуточных переносчиков электронов и протонов между оксиляемым субстратом и флавиновыми ферментами. 17. Витамин В5, Хим. строение, распространение, суточная потребность, био.роль, явление недостаточности. B5 (пантотеновая к-та, антидерматидный). Содержание: 3-5 мг. Печень, яичный желток, дрожжи, зелёные части растений, микрофлора кишечника. Структура: комплексное соединение бета-аланина и 2,4-диокси-3,3-диметилмасляной к-ты. Вязкая светло-жёлтая жидкость, хорошо раствор. в Н2О, малоустойчивая и легко гидролизуется по месту пептидной связи под действием слабых к-т и щелочей. Недостаток: дерматиды, поражения слиз. оболочек, дистрофические изменения ЖВС и НС, изменения в сердце и в почках, депигментация волос, потеря аппетита, истощение. Механизм/ Био. роль: Используется в клетках для синтеза коферментов: 4-фосфопантотеина и КоА. 4-фосфопантотеин - кофермент пальмитоилсинтазы. КоА участвует в активировании и переносе ацильных радикалов СН3СО в реакциях общего пути катаболизма, активации жирных кислот, синтеза холестерина и кетоновых тел, синтеза ацетилглюкозаминов, обезвреживания чужеродных веществ в печени. 18. Витамин Н. Хим. строение, распространение, суточная потребность, био. роль, явление недостаточности. Витамин Н (коэнзим R, биотин, антисеборейный, В7). Содержание:0,25 мг. Печень, почки, молоко, желток яйца (связанный). Катофель, лук, салат, томат, шпинат (свободное и связанное состояние). Микрофлора. Структура: циклическое производное мочевины, а боковая цепь представлена валериановой кислотой. Карбонильная группа биотина связывается амидной связью с ε-амино-группой лизина, образуя ε-N-биотиниллизин (биоцитин), обладающий био. активностью. Природные сложные белки, содержащие биотин, при попадании в организм подвергаются протеолизу с освобождением свободного биоцитина; последний подвергается гидролизу под действием биоцитиназы печени и сыворотки крови с образованием биотина и лизина. Недостаток: проявляется в случае употребления большого количества сырого яичного белка или приема сульфаниламидных препаратов и антибиотиков, подавляющих рост бактерий в кишечнике. У человека отмечаются воспалительные процессы кожи (дерматиты), сопровождающиеся усиленной деятельностью сальных желез, выпадением волос, поражением ногтей, часто отмечаются боли в мышцах, усталость, сонливость, депрессия, а также анорексия и анемия. Механизм/ Био. роль: Известные к настоящему времени биотиновые ферменты катализируют два типа реакций: 1) реакции карбоксилирования (также декарбоксирирование) (с участием СО2 или НСО3–), сопряженные с распадом АТФ RH + HCO3 – + АТФ <=> R-COOH + АДФ + Н3РО4; 2) реакции транскарбоксилирования (протекающие без участия АТФ), при которых субстраты обмениваются карбоксильной группой R1 -COOH + R2H <=> R1H + R2 -COOH. К реакциям первого типа относятся, например, ацетил-КоА- и пируват-карбоксилазные реакции: CH3–CO–S-KoA + CO2 + АТФ <=> HOOC–CH 2 –CO–Ko A + АДФ + Pi. Пируваткарбоксилаза является высокоспецифичным ферментом, катализирующим уникальную реакцию усвоения СО2 в организме животных. Примером второго типа реакций является метилмалонил-оксалоацетат-транскарбоксилазная реакция, катализирующая обратимое превращение пировиноградной и щавелевоуксусной кислот:  Реакции карбоксилирования и транскарбоксилирования имеют важное значение в организме при синтезе высших жирных кислот, белков, пуриновых нуклеотидов (соответственно нукл. кислот) и др. 19. Антивитамины. Механизм действия. Примеры. Антивитамины - любые вещества, вызывающие независимо от механизма их действия снижение или полную потерю биологической активности витаминов. I–я группа их представлена структурными аналогами витаминов. Они встраиваются вместо витамина в кофермент, но коферментные функции не выполняют. Антивитамины вступают с витаминами в конкурентные отношения в соответствующих биохимических реакциях обмена веществ. Они частично или полностью выключают витамины из обменных реакций организма. Структуроподобные по существу представляют собой антиметаболиты и при взаимодействии с апоферментом образуют неактивный ферментный комплекс, выключая энзиматическую реакцию со всеми вытекающими отсюда последствиями. II–группа антивитаминов представлена ферментами, которые участвуют в биодеградации витаминов. Это антивитамины биологического происхождения, в том числе ферменты и белки, вызывающие расщепление или связывание молекул витаминов, лишая их физиологического действия. К ним относятся, например, тиаминазы I и II, вызывающие распад молекулы витамина В1 , аскорбатоксидаза, катализирующая разрушение витамина С, белок авидин, связывающий биотин в биологически неактивный комплекс. Большинство этих антивитаминов применяют как лечебные средства со строго направленным действием на некоторые биохим. и физиолог. процессы. В частности, из антивитаминов жирорастворимых витаминов используются дикумарол, варфарин и тромексан (антагонисты витамина К) в качестве антисвертывающих препаратов. Хорошо изученными антивитаминами тиамина являются окситиамин, пири- и неопиритиамин, рибофлавина – атербин, акрихин, галактофлавин, изорибофлавин (все они конкурируют с витамином В2 при биосинтезе коферментов ФАД и ФМН), пиридоксина – дезоксипиридоксин, циклосерин, изоникотиноилгидразид (изониазид), оказывающий антибактериальное действие на микобактерии туберкулеза. Антивитаминами фолиевой кислоты являются амино- и аметоптерины, витамина В12 – производные 2-аминометилпропанол-В12, никотиновой кислоты – изониазид и 3-ацетилпиридин, парааминобензойной кислоты – сульфаниламидные препараты; все они нашли широкое применение в качестве противоопухолевых или антибактериальных средств, тормозя синтез белка и нуклеиновых кислот в клетках. Парааминобензойная кислота (ПАБК) является витамином роста для тех бактерий, в клетках которых она служит основой для образования фолиевой кислоты. Сульфаниламиды являются структурным аналогом ПАБК. При попадании в клетку бактерий сульфаниламидный препарат подавляет синтез фолиевой кислоты. Это происходит по двум причинам: 1) Сульфаниламиды ингибируют ферменты, субстратом которых при синтезе фолиевой кислоты служит ПАБК. 2) Эти ферменты вследствие недостаточности субстратной специфичности могут использовать в качестве субстрата сульфаниламинидазы, при этом синтезируется не фолиевая кислота, а ее аналог, содержащий сульфаниламидный компонент вместо остатка ПАБК. Такое соединение не может выполнять коферментные функции. |
