ТеплоФИЗИКА. Теплофизика. Контрольная работа по теплофизике Работу выполнил Курсант (слушатель) 343 учебной группы Горбатовский А. Н
 Скачать 89.42 Kb. Скачать 89.42 Kb.
|
|
Министерство Российской Федерации по делам гражданской обороны, чрезвычайным ситуациям и ликвидации последствий стихийных бедствий ФГБОУ ВО Сибирская пожарно-спасательная академия ГПС МЧС России Кафедра гуманитарных и социально-экономических дисциплин Контрольная работа по теплофизике Работу выполнил Курсант (слушатель) 343 учебной группы Горбатовский А.Н. Научный руководитель (проверяющий) Малый В.П. Дата проверки работы______________ Оценка:__________________________ Роспись проверяющего работу_______ Железногорск, 2022 Горизонтально расположенный неизолированный электропровод диаметром d и длиной l, охлаждается воздухом, температура которого t1. Определить коэффициент теплоотдачи от поверхности провода воздуху, тепловой поток и допустимую силу тока в электропроводе. Температура провода по условиям пожарной безопасности не должна превышать tw. Провод изготовлен из стали, удельное сопротивление которой ρ = 1,2∙10-7 Ом·м. Задачу решить для двух случаев: а) воздух неподвижен; б) поток воздуха обдувает провод со скоростью w, угол атаки ψ. Исходные данные для расчета: d = 0,5 мм; ψ = 50°; l = 10 м; w = 2 м/с; t1 = 15°C; tw = 95°C. Решение: 1 случай – воздух неподвижен. Определяющая температура – температура воздуха t1 = 150C. По определяющей температуре определяем необходимые для расчета теплофизические свойства воздуха. - теплопроводность воздуха = 0,0255 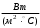 ; ;– кинематическая вязкость жидкости =14,61∙10-6 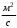 ; ;– температурный коэффициент объемного расширения =1/Т1 = 1/288 К-1; – разность температур t = (tw – t1 ) = 95 – 15 = 80С; – критерий Прандтля Pr = 0,704. Число Грасгофа: 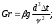 Gr = 9,81 = 1,596. Произведение (Gr∙Pr) = 1,596∙0,704 = 1,124. Вычисляем критерий (число) Нуссельта для случая естественной конвекции. Nu1 = 1,18∙(Gr∙Pr)0,125 = 1,18∙1,1240,125 = 1,20. Определяем коэффициент теплоотдачи от поверхности электропровода к неподвижному воздуху. α = Nu, α = 1,2 = 61,2 Вт/(м∙К). Определяем максимально возможное значение теплового потока Q1 при отводе от поверхности электропровода к неподвижному воздуху. Q1 = α∙(tw- t1)∙π∙d∙l = 61,2∙(95 - 15)∙3,14∙0,0005∙10 = 76,87 Вт. Определяем допустимый ток в проводе из соотношения Q1= I2 R, откуда I = (Q1/R)0,5; R = ρ∙l/S = 4ρ∙l/πd2 = 4∙1,2∙10-7∙10/(3,14∙0,00052) = 61,15 Ом; I1 = (76,87/61,15)0,5 = 1,12 А. 2 случай - поток воздуха обдувает провод со скоростью потока w, а угол атаки потока составляет . 1.Определяем режим течения воздуха (по критерию Рейнольдса) при обдуве электропровода потоком воздуха. Re = w∙d/ν = 2∙0,0005/(14,61∙10-6) = 68; 2.Вычисляем значение числа (критерий) Нуссельта при вынужденной конвекции. При R = 5 - 1000 Nu = 0,43∙Re0,5 = 0,43∙680,5 = 3,55. 3.Определяем поправку на угол атаки потока воздуха. При = 500 εψ = 0,87; тогда Nu2 = Nu∙ εψ = 3,55∙0,87 = 3,09. 4.Определяем коэффициент теплоотдачи от поверхности электропровода к потоку воздуха. α = 3,09 = 157,6 Вт/(м∙К). 5.Определяем максимально возможное значение теплового потока Q2 при отводе от поверхности электропровода к потоку воздуха. Q2 = α∙(tw- t1)∙π∙d∙l = 157,6∙(95 - 15)∙3,14∙0,0005∙10 = 197,95 Вт. 6.Определяем допустимый ток в проводе из соотношения I2 = (197,95/61,15)0,5 = 1,80 А. Результаты расчета
В производственном помещении размером 10х9х4 (м) проходит газопровод, по которому протекает метан температурой t1, и избыточным давлением Р1. В результате аварии на поверхности газопровода образовалось отверстие площадью S. Оценить время образования взрывоопасной концентрации в помещении, а также скорость газового потока на срезе отверстия. Условия в помещении до аварии считать нормальными. Нижний концентрационный предел распределения пламени (НКПР) для метана при заданных условиях считать равным 5 % (по объему). Дано: А = 10 м; В = 9 м; Н = 4 м; P0 = 101,325∙103 Па; Р1 = 1,1∙103 Па; t1 = 2 ºС; S = 1,6 мм2 = 1,6∙10-6 м2.; Газ СН4 (k = 1,333; 16∙10-3 кг/моль; НКПР = 5%). Решение: Абсолютное давление в газопроводе: Pг = Р1 + Р0 = 1,1∙103 + 101,325∙103 = 102,425∙103 Па. Определяем величину отношений давлений: β = = = 0,99. Величина критического отношения давлений: βк = k/(k-1) = 1,333/(1,333-1) = 0,54. Т.к. βк < β, то режим истечения – докритический. Абсолютная температура газа: T = t1 + 273 = 2 + 273 = 275 К. Газовая постоянная R = = = 520 Дж/(кг∙К) Удельный объем газа в трубопроводе: v1 = = = 1,396 м3/кг. Скорость истечения газа через свищ: w = = = 55,53 м/с. Массовый расход газа через свищ: G = S G = 1,6∙10-6 = 9,13∙10-6 кг/с. Объем помещения: Vп = АВН = 10∙9∙4 = 360 м3 Объем газа, образующего концентрацию, равную НКПР: V0 = Vп∙НКПР = 360∙5% = 18,00 м3 Температура в помещении при нормальных условиях: T2 = 273К. Масса газа, образующего концентрацию, равную НКПР: Мг = = = 0,206 кг. Время образования в помещении концентрации газа, равную НКПР: τ = = = 22,563∙103c = 6,27 часов. Результаты расчетов сводим в таблицу:
Смесь газов находится в баллоне. В результате пожара температура газовой смеси изменилась от t1 до t2. Найти количество теплоты Q, подведенное к газовой смеси, а также физические величины, характеризующие газовую смесь до и после нагревания. Результаты расчета представить в виде таблиц. Исходные данные для расчета: t1 = -250C; t2 = 3000C; P1 = 200 кПа; V = 10 м3; gНе = 0,20; gN2 = 0,50; gNH3 = 0,30; µНе = 4 кг/кмоль; µN2 = 28кг/кмоль; µNH3 = 17 кг/кмоль. Решение: 1. Кажущаяся молекулярная масса смеси: µсм = = µсм = 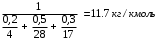 . .где gi – объёмная доля i-го компонента смеси; µi -молекулярная масса i-го компонента смеси. 2.Объемные доли компонентов смеси: ri = , rНе = = 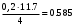 ; ;rN2 = = 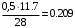 ; ;rNH3 = = 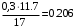 . .3.Количества вещества газовой смеси найдем из уравнения Менделеева-Клапейрона: P1V1 = ν∙R∙T1, откуда ν = = 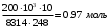 . .4.Масса газовой смеси: m = ν∙µсм = 0,97∙11,7 = 11,35 кг. 5.Масса компонентов смеси: mi = gi∙m; mНе = gНе∙m = 0,2∙11,35 = 2,27 кг; mN2 = gN2∙m = 0,5∙11,35 = 5,68 кг; mNH3 = gNH3∙m = 0,3∙11,35 = 3,41 кг. 6.Количество вещества компонентов смеси: xi = ri∙ ν; νНе = rНе∙ν = 0,585∙0,97 = 0,567 моль; νN2 = rN2∙ν = 0,209∙0,97 = 0,203 моль; νNH3 = rNH3∙ν = 0,206∙0,97 = 0,2 моль. 7.Молярная теплоёмкость компонентов смеси при постоянном объёме: где i – число степеней свободы молекулы газа. Для молекул одноатомных газов число степеней свободы молекулы i=3, для двухатомных i=5, а для многоатомных i=6. СµV(Не) = (3/2)R = (3/2)∙8314 = 12471 Дж/(моль∙К); СµV(N2) = (5/2)R = (5/2)∙8314 = 20785 Дж/(моль∙К); СµV(NH3) = (6/2)R = (6/2)∙8314 = 24942 Дж/(моль∙К). 8. Молярная теплоёмкость компонентов смеси при постоянном давлении найдем из уравнения Майера: СµР(Не) = СµV(Не) + R = 12471 + 8314 = 20785 Дж/(моль∙К); СµР(N2) = СµV(N2) + R = 20785 + 8314 = 29099 Дж/(моль∙К); СµР(NH3) = СµV(NH3) + R = 24942 + 8314 = 33256 Дж/(моль∙К). 9.Удельная теплоёмкость компонентов смеси при постоянном объёме: СVi = СV(Не) = = 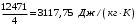 ; ;СV(N2) = = 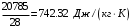 ; ;СV(NH3) = = 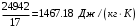 . .10.Удельная теплоёмкость компонентов смеси при постоянном давлении: СРi = , СР(Не) = = 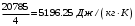 ; ;СР(N2) = = 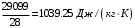 ; ;СР(NH3) = = 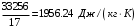 . .11.Объёмная теплоёмкость компонентов смеси при постоянном объёме: СVi = ; СV(Не) = = 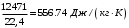 ; ;СV(N2) = = 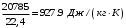 ; ;СV(NH3) = = 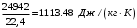 . .12.Объёмная теплоёмкость компонентов смеси при постоянном давлении: СPi = ; СP(Не) = = 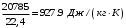 ; ;СP(N2) = = 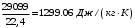 ; ;СP(NH3) = = 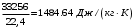 . .13. Молярная теплоемкость смеси при постоянном объёме: СµV(СМ) = rНе∙СµV(Не) + rN2∙СµV(N2) + rNH3∙СµV(NH3); СµV(СМ) = 0,585∙12471 + 0,209∙20785 + 0,206∙24942 = 16778 Дж/(моль∙К). 14. Молярная теплоемкость смеси при постоянном давлении: СµР(СМ) = rНе∙СµР(Не) + rN2∙СµР(N2) + rNH3∙СµР(NH3); СµР(СМ)= 0,585∙20785 + 0,209∙29099 + 0,206∙33256 = 25092 Дж/(моль∙К). 15. Удельная теплоемкость смеси при постоянном объёме: СV(СМ) = gНе∙СV(Не) + gN2∙СV(N2) + gNH3∙СV(NH3); СV(СМ) = 0,2∙3117,75 + 0,5∙742,32 + 0,3∙1467,18 = 1435 Дж/(кг∙К). 16. Удельная теплоемкость смеси при постоянном давлении: СР(СМ) = gНе∙СР(Не) + gN2∙СР(N2) + gNH3∙СР(NH3); СР(СМ)= 0,2∙927,9 + 0,5∙1299,06 + 0,3∙1484,64 = 1281 Дж/(кг∙К). 17. Давление смеси после нагрева найдем из уравнения для изохорного процесса = , откуда Р2 = Р1 = 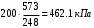 . .18. Парциальные давления компонентов смеси до нагрева: P1Не = rНе∙P1 = 0,585∙200 = 117 кПа; P1N2 = rN2∙P1 = 0,209∙200 = 41,8 кПа; P1NH3 = rNH3∙P1 = 0,206∙200 = 41,2 кПа. 19. Парциальные давления компонентов смеси после нагрева: P2Не = rНе∙P2 = 0,585∙462,1 = 270,3 кПа; P2N2 = rN2∙P2 = 0,209∙462,1 = 96,58 кПа; P2NH3 = rNH3∙P2 = 0,206∙462,1 = 95,2 кПа. 20. Количество теплоты Q, подведенное к газовой смеси: Q = m∙Cv(T2 – T1) = 11,35∙1435(573 – 248) = 5293356 Дж. Результаты расчета
|
