Никель2. Курсовая работа 22. 04. 02. 02 Металлургия цветных металлов
 Скачать 0.85 Mb. Скачать 0.85 Mb.
|
|
Состав золы кокса, %: FeО – 5,0; SiO2 – 52,5; Al2O3 – 37,0; MgO – 1,0; CaO – 2,0; SO3 – 2.0; прочие – 0,5.
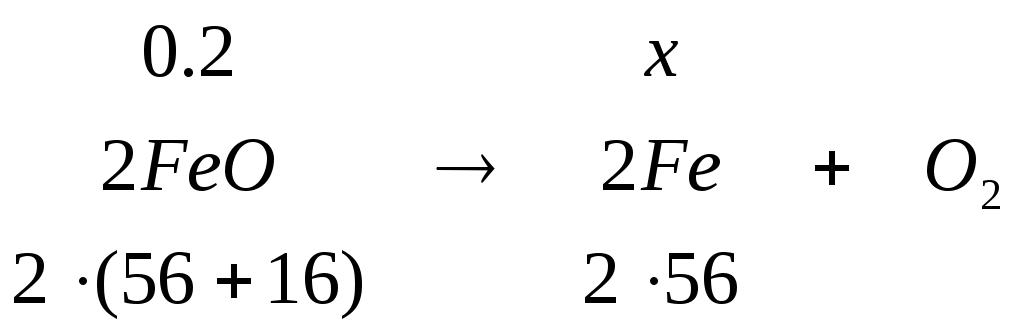 , ,
m(O) = 0.20085 – 0.15621 = 0.04463 кг. Таблица 3.7 – Состав золы кокса при плавке, кг
3.7 Распределение состава гипса при плавке Примем в качестве сульфудизатора гипс ( Для образования штейна требуется 1,65 кг серы. В 100 кг агломерата имеется 0,08 кг серы и в рабочей части кокса 0,49 кг. Следовательно, серы необходимо подать: 1,65 – (0,08 + 0,49) = 1,0807 кг. Степень десульфуризации при шахтной плавке составляет 30 – 50%. Часть серы гипса теряется с газами в виде SO2. Принимаем степень десульфуризации 40%. В процесс необходимо ввести серы: Это потребует загрузки сухого гипса: Учитывая унос части гипса в пыль Так как влажность гипса можно принять 4%, то с гипсом поступает воды: 11.27138 * 0,04 = 0,45086 кг. Общий вес влажного гипса составляет: 11.27138 + 0,45086 = 11.72224 кг. Произведем расчет рационального состава гипса. 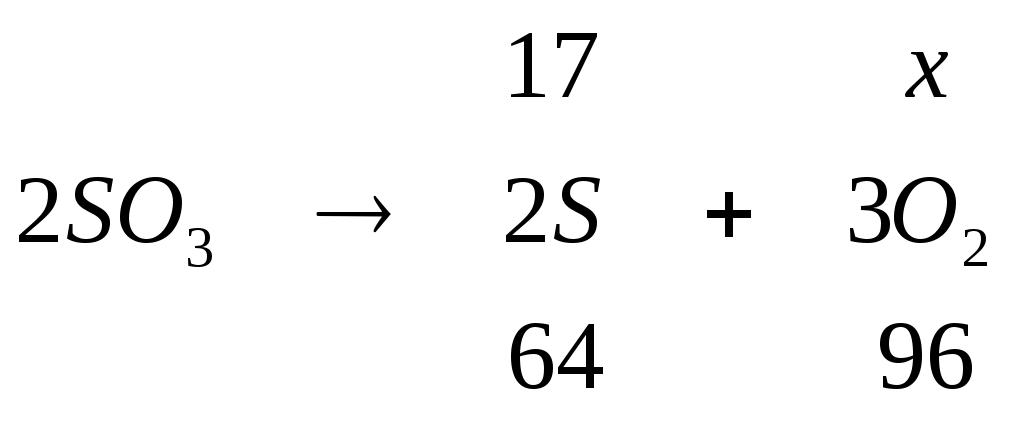 , m(О) = , m(О) = 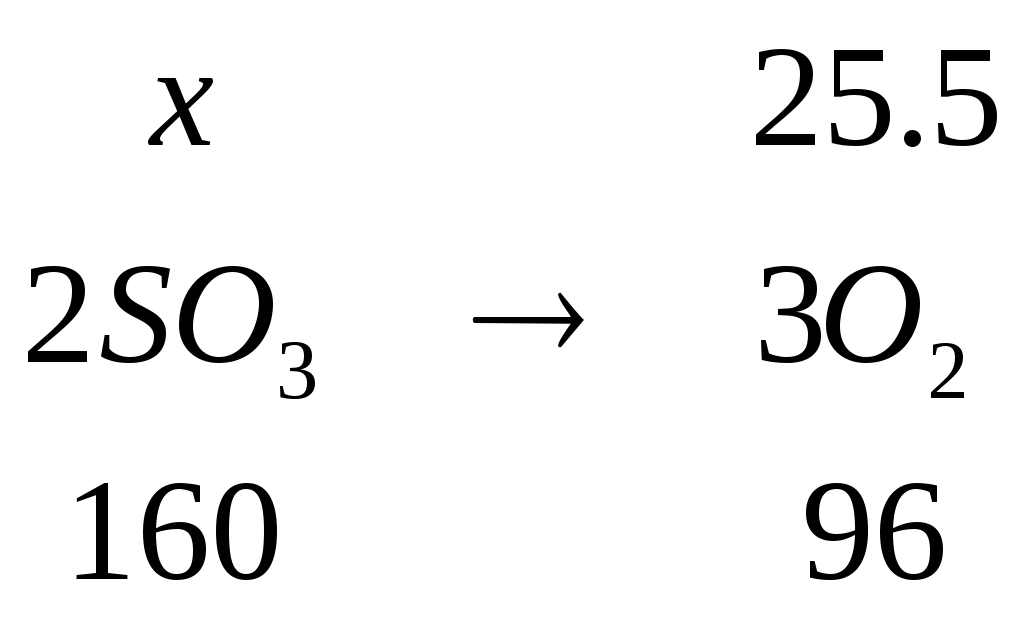 , m(SО3) = , m(SО3) = 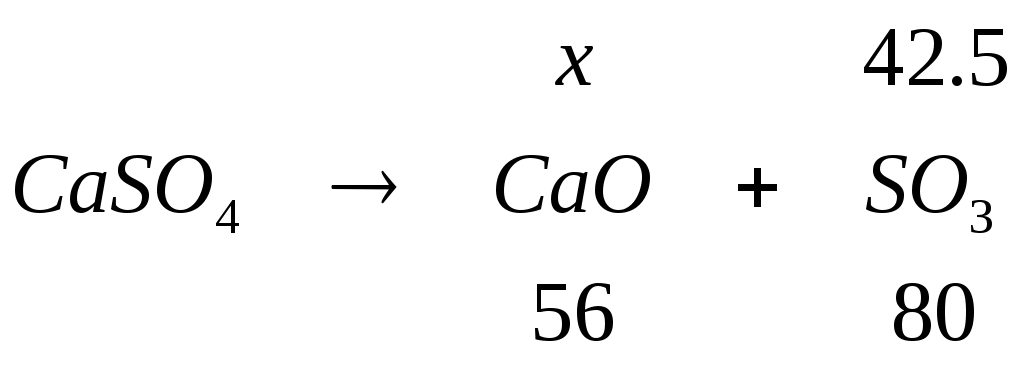 , m(CaО) = , m(CaО) = 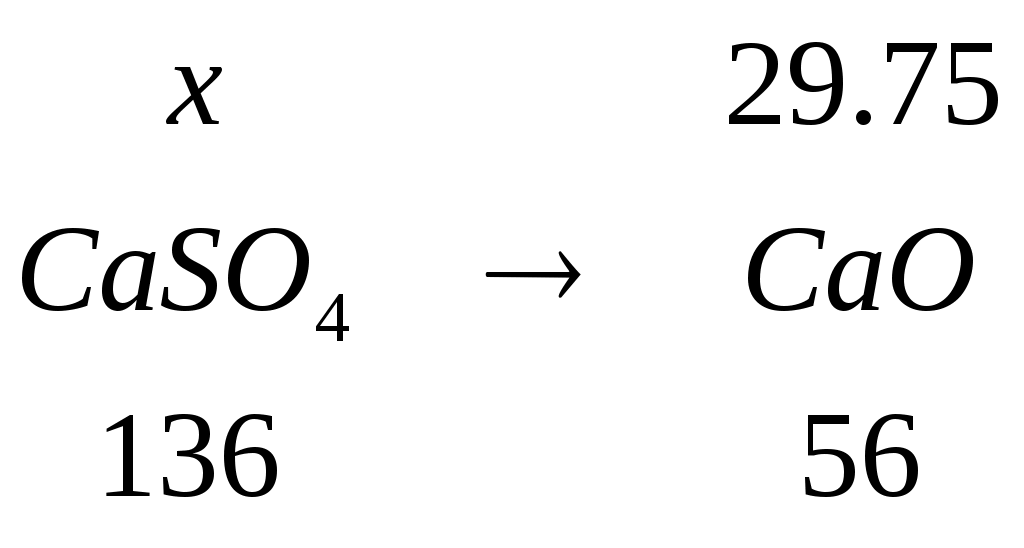 , m(CaSО4) = , m(CaSО4) = 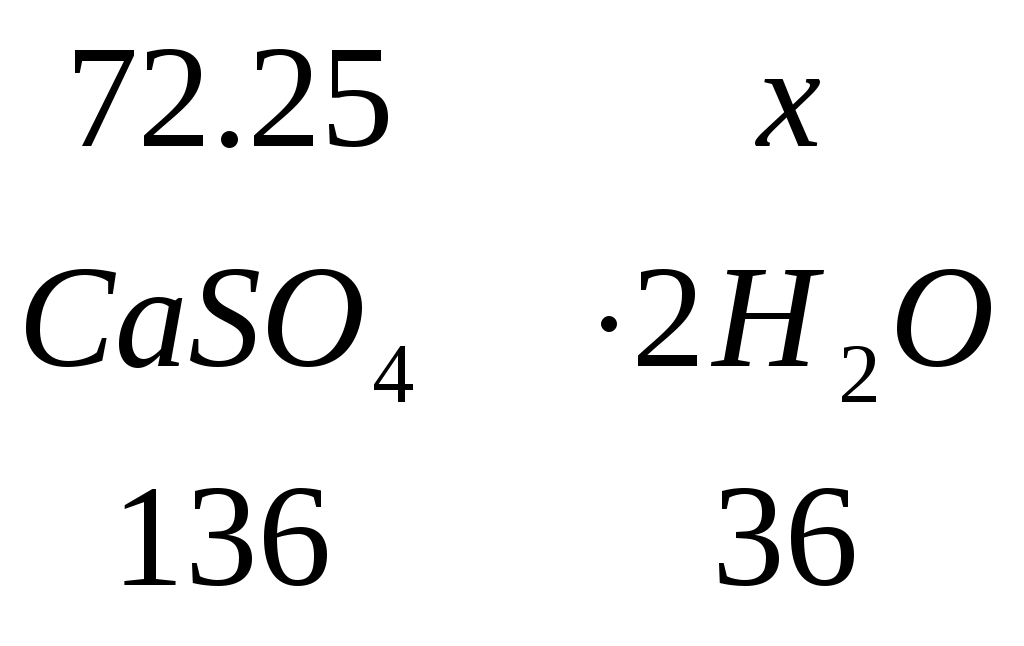 , m(H2О) = , m(H2О) = m( 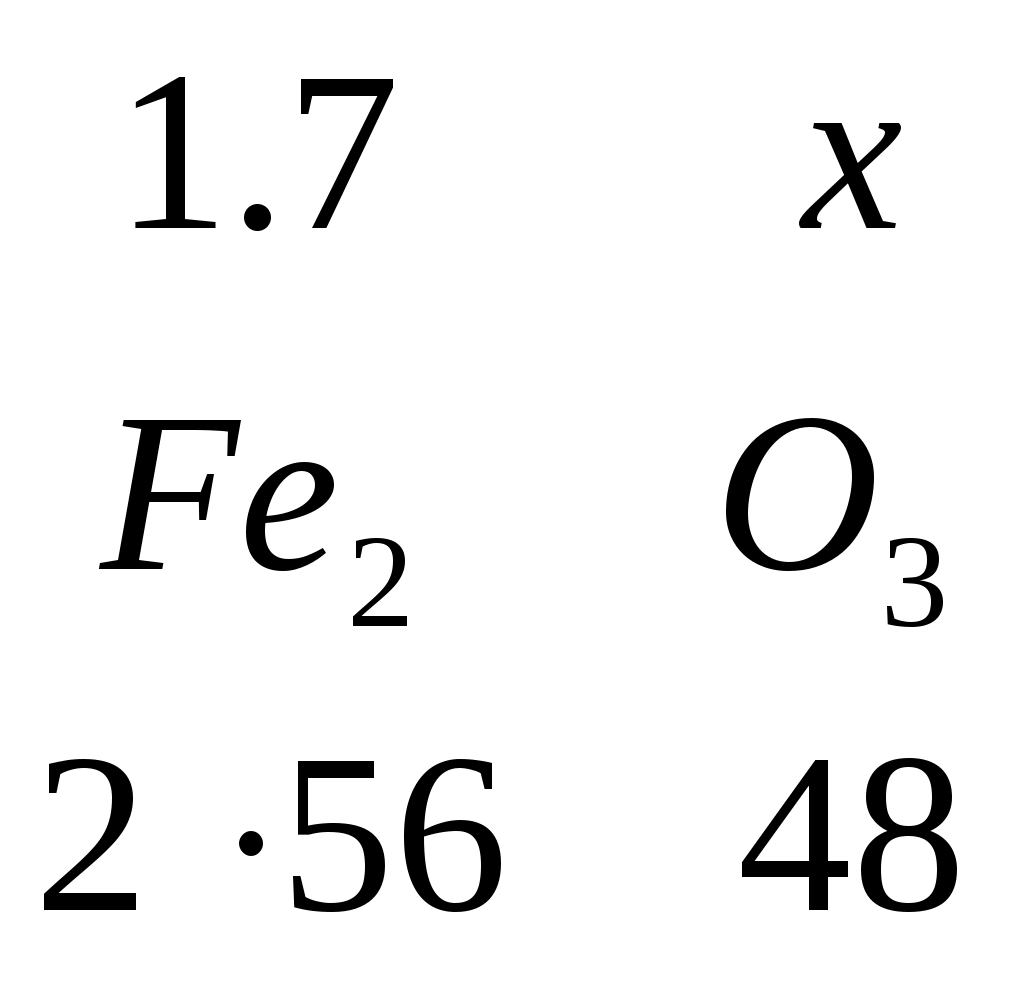 , , m(Fe2O3) = 1.7 + 0.72857 = 2.42857кг Аналогично рассчитывается масса остальных соединений. Полученные данные сведем в таблицу. Таблица 3.8 – Рациональный состав гипса (на сухой вес), кг
Рассчитаем распределение состава гипса в процессе плавки. Всего сухого гипса 11.27138 кг. Пересчитаем на эту массу массу каждого из компонентов. m(Fe) = Аналогично рассчитываем массу остальных компонентов. Унос в пыль составляет 6%: Рассчитаем по компонентам, какое их количество уносится в пыль. m(Fe) = Аналогично рассчитываем массу остальных компонентов. Полученные данные сведем в таблицу. Таблица 3.9 – Распределение состава гипса в процессе плавки, кг
3.8 Расчет шлака и флюсов 3.8.1 Расчет шлака Железо вводится с агломератом, коксом и гипсом. Масса введенного железа: m(Fe) = m(Fe)агл + m(Fe)кокс + m(Fe)гипс = 21,34 + 1,7 + 0,15622 = 23,19622 кг. В штейн переходит 0,56*23,19622 = 12,9899 кг. На шлак остается 23,19622 – 12,9899 = 10,2063 кг. Определим массу FeO в шлаке. 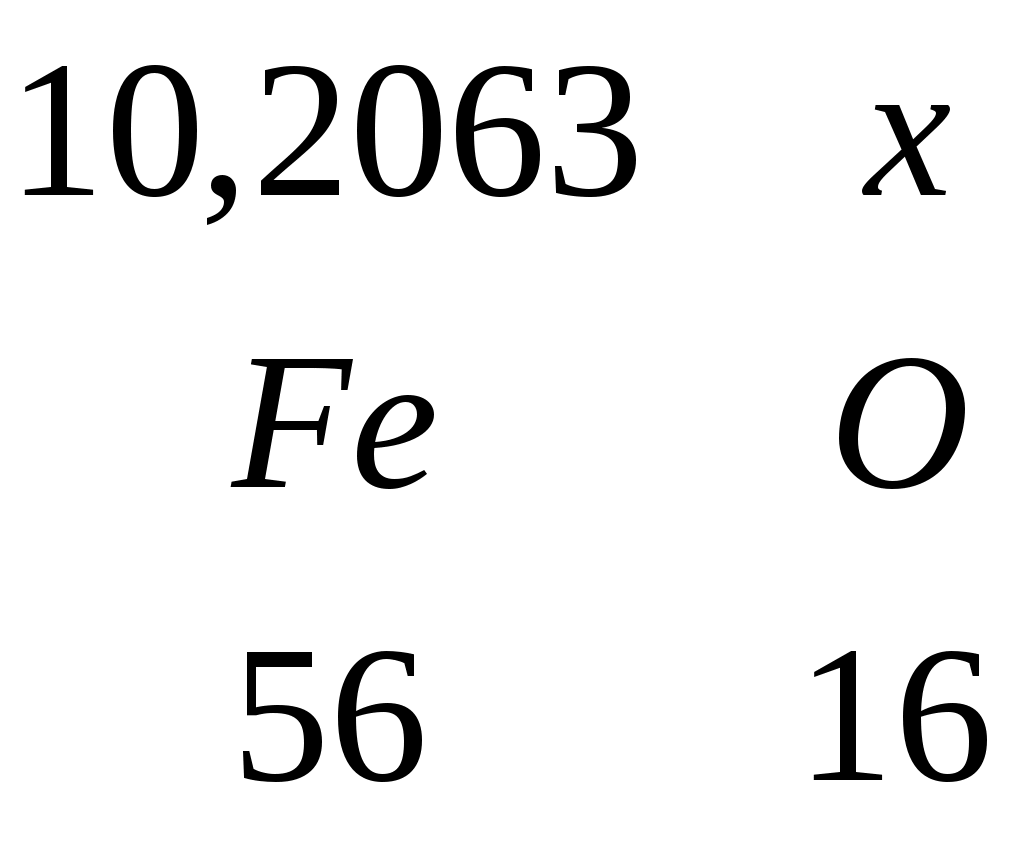 , , m(Fe2O3) = 10,2063 + 2,91609 = 13,12239 кг В агломерате содержится FeO: 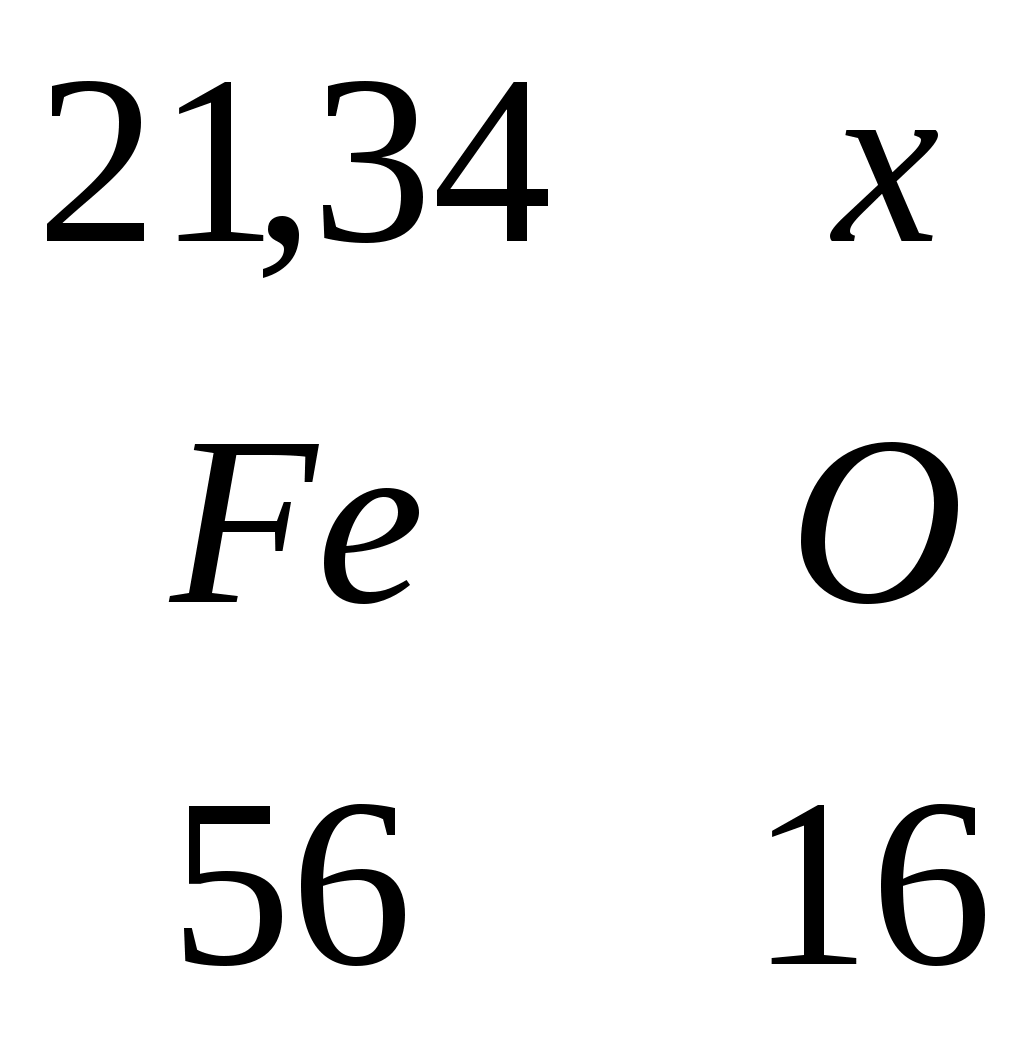 , , m(Fe2O3) = 21,34 + 6,09714 = 27,43714 кг В гипсе содержится FeO: 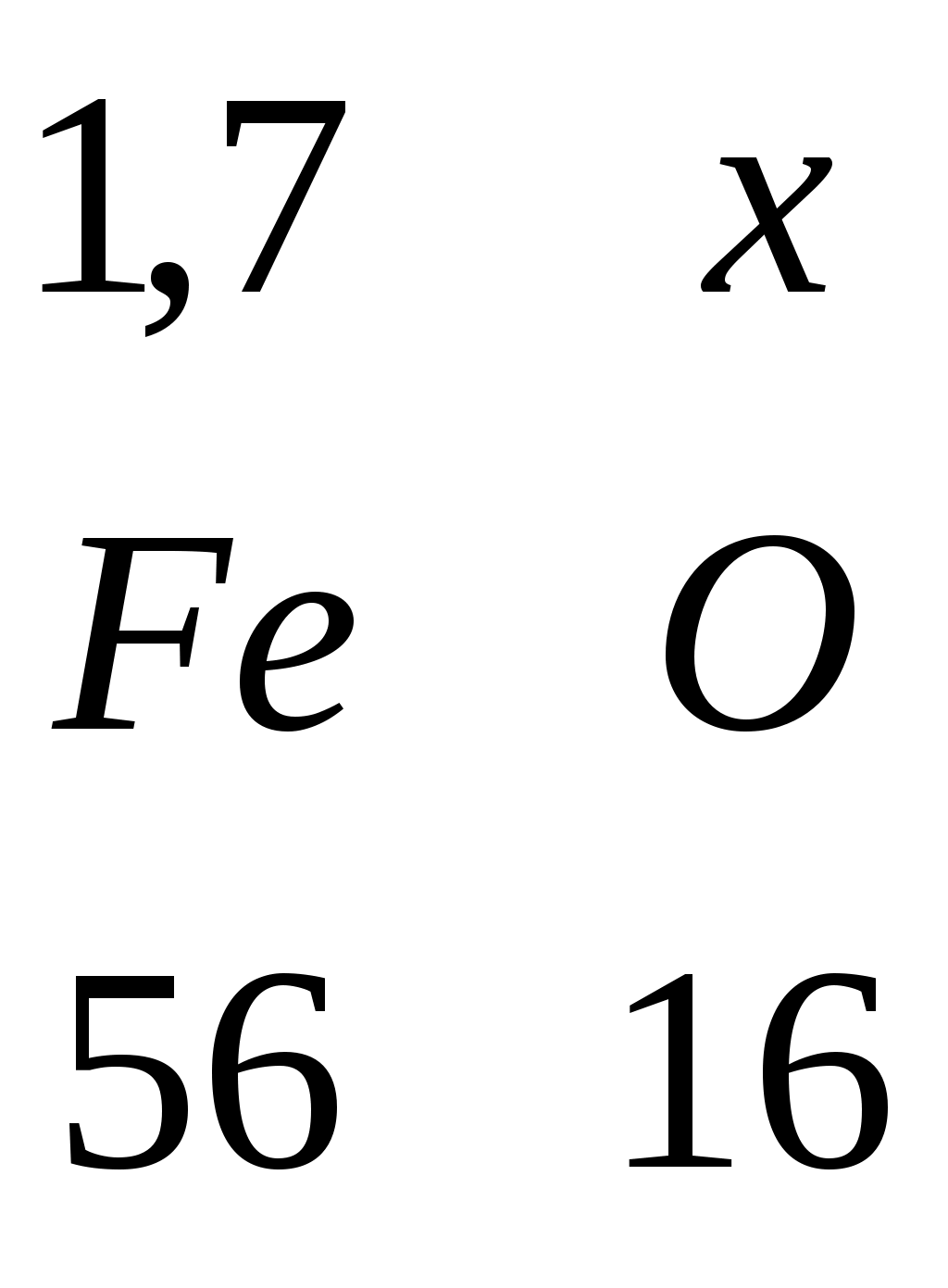 , , m(Fe2O3) = 1,7 + 0,48571 = 2,18571 кг Таблица 3.10 – Состав шлака, образующегося из шлакообразующих компонентов агломерата, кокса и гипса, кг
3.8.2 Расчет флюса Допуск Al2O3 + SiO2 в шлаке должен составлять Таблица 3.11 – Рациональный состав флюса (известняка), кг
Х – количество окиси кальция (CaO) для получения суммы Al2O3 + SiO2. Составляем пропорцию: х = m(CaO) = 2,3273 кг. Потребный вес известняка при 52% содержании CaO: 2,3273/0,52 = 4,47558 кг. В пыль уносится 9,5% от веса загруженного известняка. Тогда сухого известняка необходимо загрузить: 4,47558/0,095 = 47,11137 кг. Рассчитаем массы каждого из компонентов, входящих в состав флюса. Пример для Fe: m(Fe) = Аналогично рассчитываем массу остальных компонентов. Унос в пыль составляет 9,5%: 47,11137*9,5/100 = 4,4756 кг. Унос в пыль по каждому элементу: Пример для Fe: m(Fe) = Аналогично рассчитываем массу остальных компонентов. Полученные данные сведем в таблицу. Таблица 3.12 – Распределение составляющих известняка при плавке, кг
3.9 Расчет шлака Приняв влажность известняка 3,5%, получим вес влаги: 47,111*3,5%/100% = 1,64889кг. Общий вес влажного известняка: 47,111 + 1,64889 = 48,7603 кг. По таблице 11 считаем массы элементов в известняке. m(Fe) = 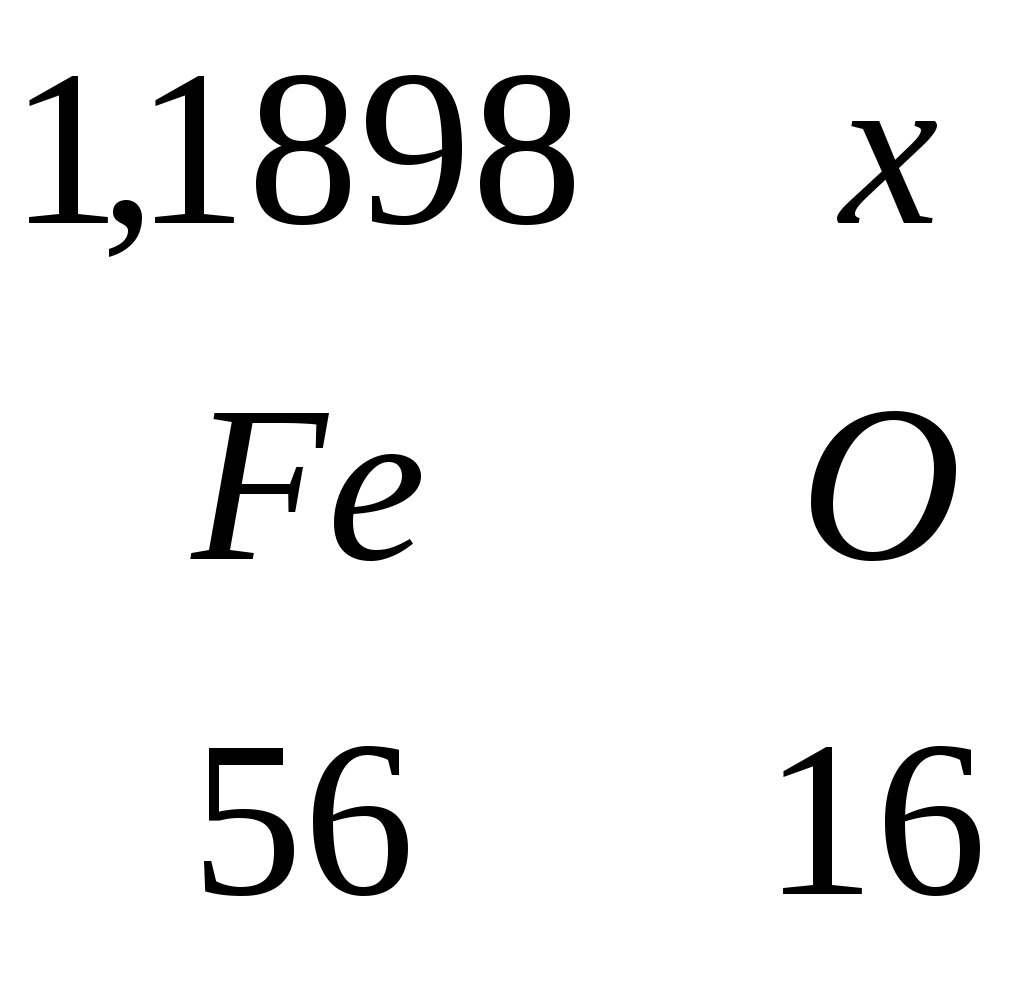 , , m(FeO) = 1,1898 + 0,3399 = 1,5297 кг Аналогично рассчитываем массы остальных соединений. Рассчитаем, сколько процентов составляет масса каждого элемента от общего веса. Пример для FeO: Таблица 3.13 – Предварительный состав шлака с подфлюсовкой известняком, кг
Окончательный состав шлака получим, учтя потерю никеля в шлаках. Определим, сколько никеля остается в шлаке: m(Ni) = m(Ni)агл - m(Ni)штейн = 2,76 – 2,07 = 0,69 кг. Примем, что весь никель в шлаке находится в виде запутавшихся корольков штейна. Количество штейна: 0,69/0,20 = 3,45 кг. Определяем содержание в корольках штейна отдельных компонентов в соответствии с рациональным составом штейна:
3.9.1 Расчет распределения железа 1. Общее количество железа в пересчете с закиси: m(Fe) = 10,2063 кг. 2. Из этого количества в корольках штейна содержится: 0,9789 + 0,9530 = 1,9319 кг. 3. Окисленного железа в шлаке: 24,9719 кг. 4. Примем, что в шлаке железо содержится в виде магнетита – 10%, В виде фаялита – 90%. а) масса железа в магнетите: 24,9719 * 0,1 = 2,4972кг, масса кислорода в магнетите: 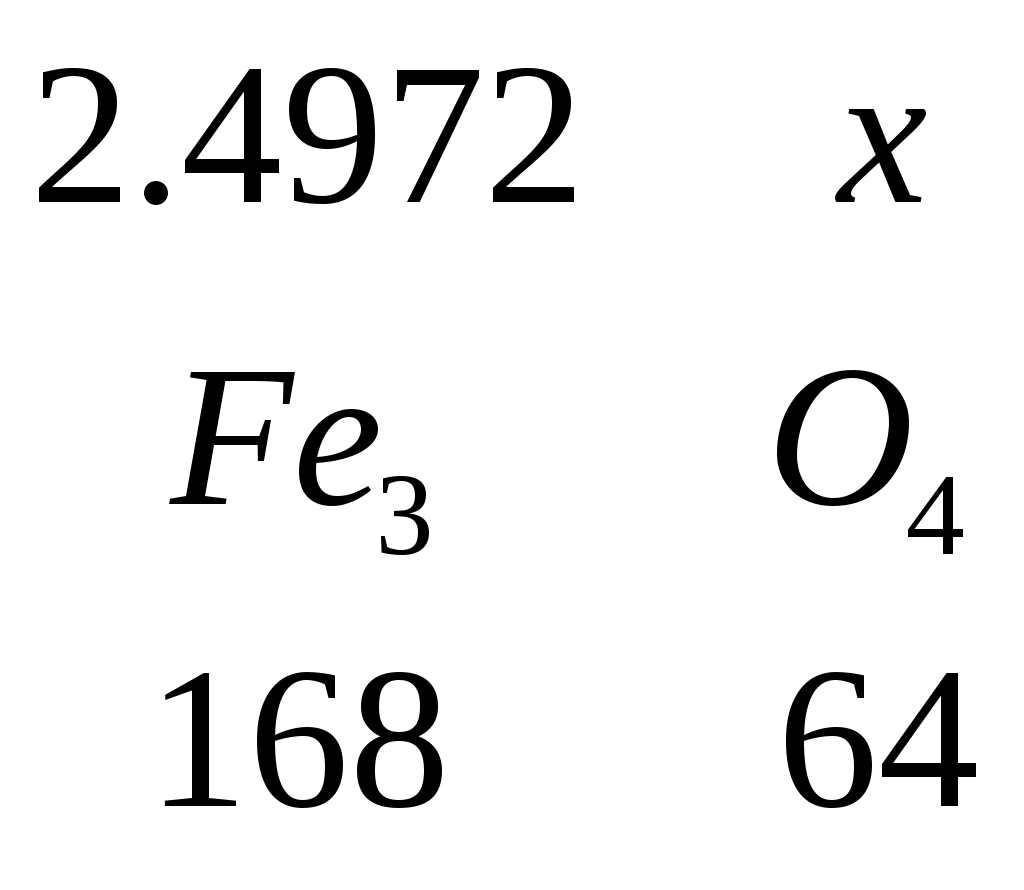 , , общая масса магнетита: m(Fe3O4) = 2,4972 + 0,9513 = 3,4485 кг; б) масса железа в фаялите: 24,9719 * 0,9 = 22,4747кг, масса кислорода в закиси: 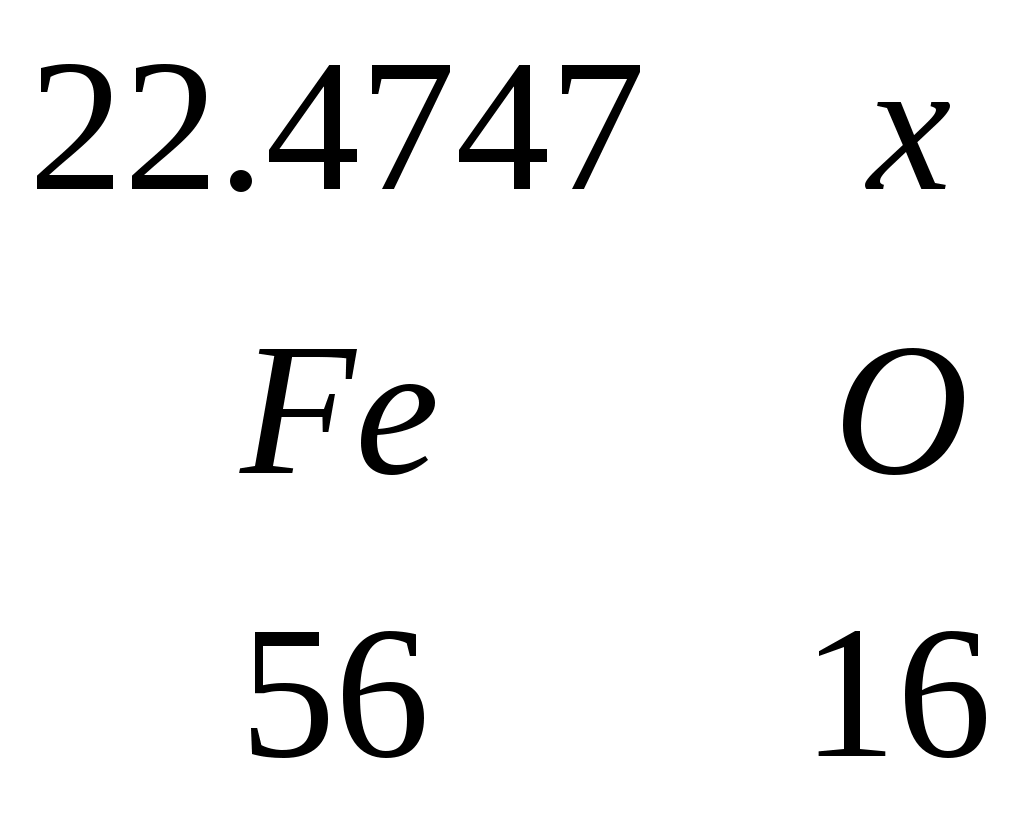 , , масса закиси: m(FeO) = 22,4747 + 6,4213 = 28,896кг, масса кремнезема в фаялите: 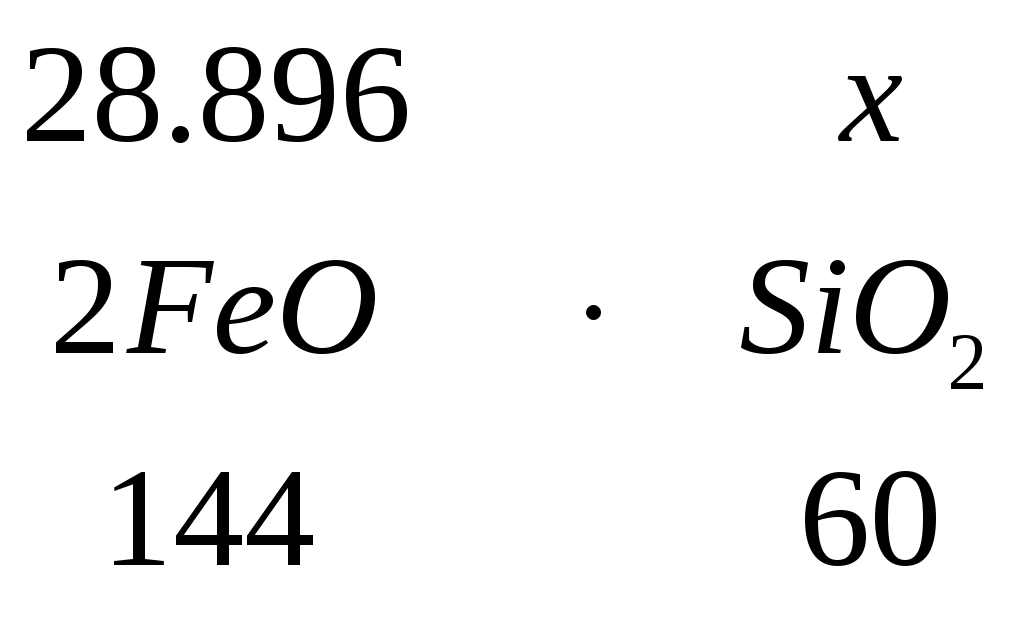 , , общая масса фаялита: m(2FeO*SiO2) = 28,896 + 12,04 = 40,936 кг. 3.9.2 Расчет остальных шлакообразующих В шлаке MgO находится в виде 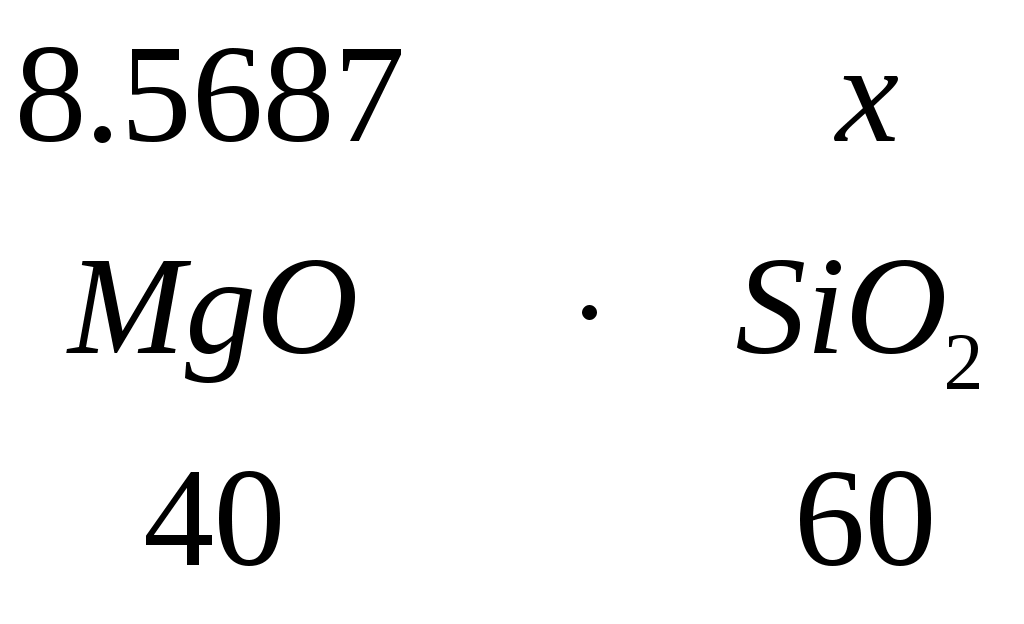 , , m(MgO*SiO2) = 8.5687 + 12,853 = 21,4217 кг. Al2O3 находится в виде 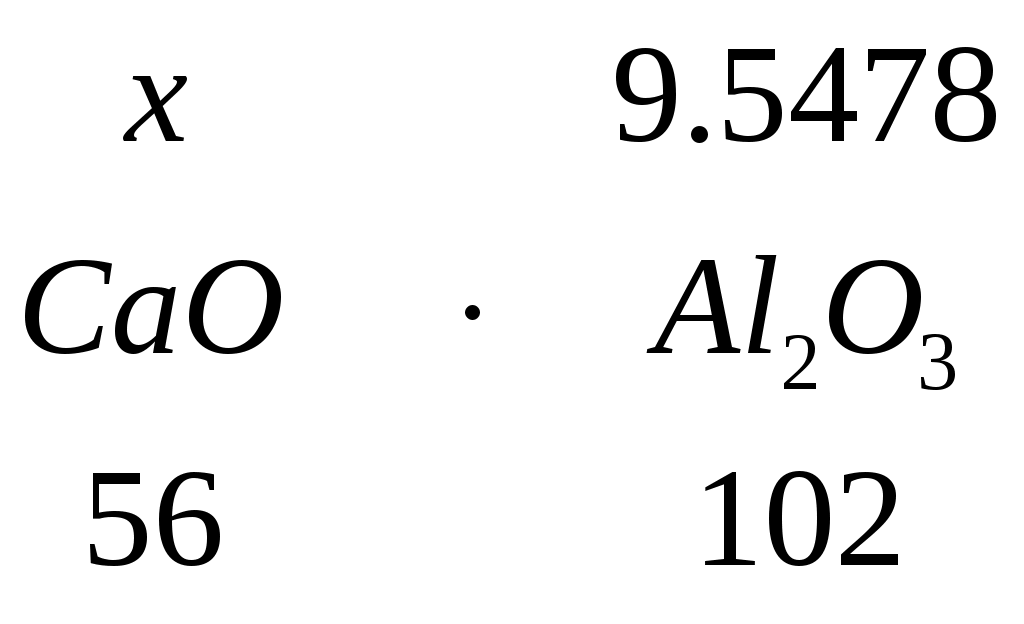 , , m(CaO*Al2O3) = 9,5478 + 5,2419 = 14,789кг. Остается CaO: 29,7419 – 5,2419=24,5кг. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
