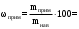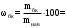оч. Работы по очистке веществ. Лабораторная работа 1 Очистка органических веществ возгонкой Цель
 Скачать 428.23 Kb. Скачать 428.23 Kb.
|
|
Лабораторная работа № 1 Очистка органических веществ возгонкой Цель: Ознакомиться с методом очистки органических веществ – возгонкой; Изучить методику очистки бензойной кислоты возгонкой, ознакомиться с лабораторным оборудованием; Рассчитать массовую долю чистой бензойной кислоты. Теоретическое обоснование Возгонка (сублимация) – процесс испарения твердого вещества с последующей конденсацией паров в твердую фазу, минуя жидкую фазу. Возгоняется вещество при температуре ниже температуры плавления. Этим способом хорошо очищаются вещества, если летучесть загрязнений отличается от летучести основного вещества. Таким способом можно очистить бензойную кислоту, антрацен, нафталин, йод, серу и др. Возгонку можно проводить при нормальном и пониженном давлении. Существует разное аппаратурное оформление процесса возгонки, рис. 6. 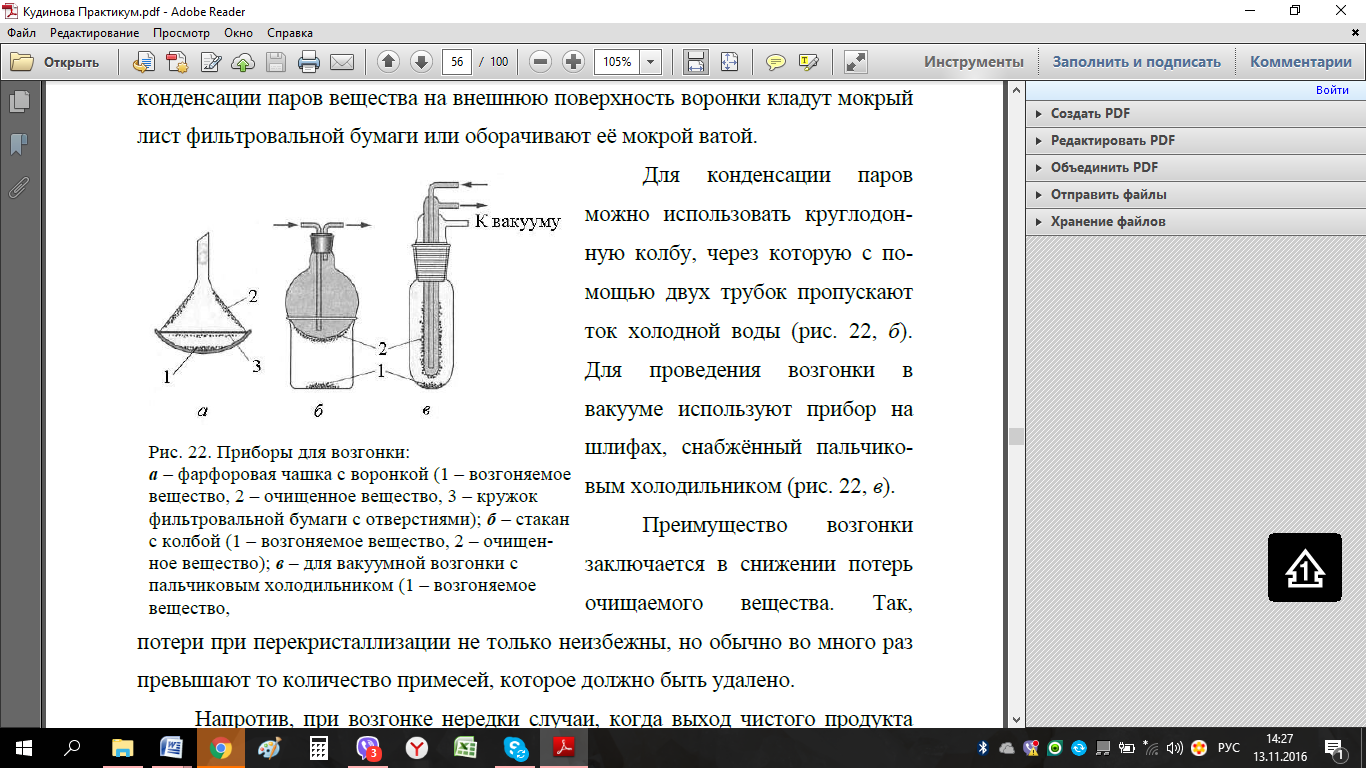 Рис. 6. Приборы для возгонки: а – фарфоровая чашка с воронкой, б – стакан с колбой, в – вакуумная возгонка с пальчиковым холодильником (1 – возгоняемое вещество, 2 – очищенное вещество, 3 – кружок фильтровальной бумаги с отверстиями). Преимущества метода возгонки: сразу получается чистый продукт, возгонку можно провести даже с небольшим количеством вещества, потери основного вещества минимальны (иногда выход чистого продукта достигает 98-99 %). Вопросы для повторения 1. Что называется процессом возгонки? 2. Приведите примеры веществ, которые могут быть очищены возгонкой. 3. Опишите схему прибора и принцип его работы. 4. В чем основные преимущества метода возгонки? Методика выполнения работы По краткому химическому справочнику В.А. Рабиновича изучите свойства очищаемого органического вещества - бензойной кислоты. Запишите его формулу, молярную массу, температуру плавления. Взвесьте на аналитических весах химический стакан (mст), поместите в стакан около 0,5 г очищаемого вещества и снова взвесьте на аналитических весах (mст+нав). Круглодонную колбу заполните ледяной водой (для лучшей конденсации паров вещества) и поместите на стакан, рис. 7. Отверстие носика стакана закройте ватой, чтобы предотвратить попадание возогнанного вещества в атмосферу. 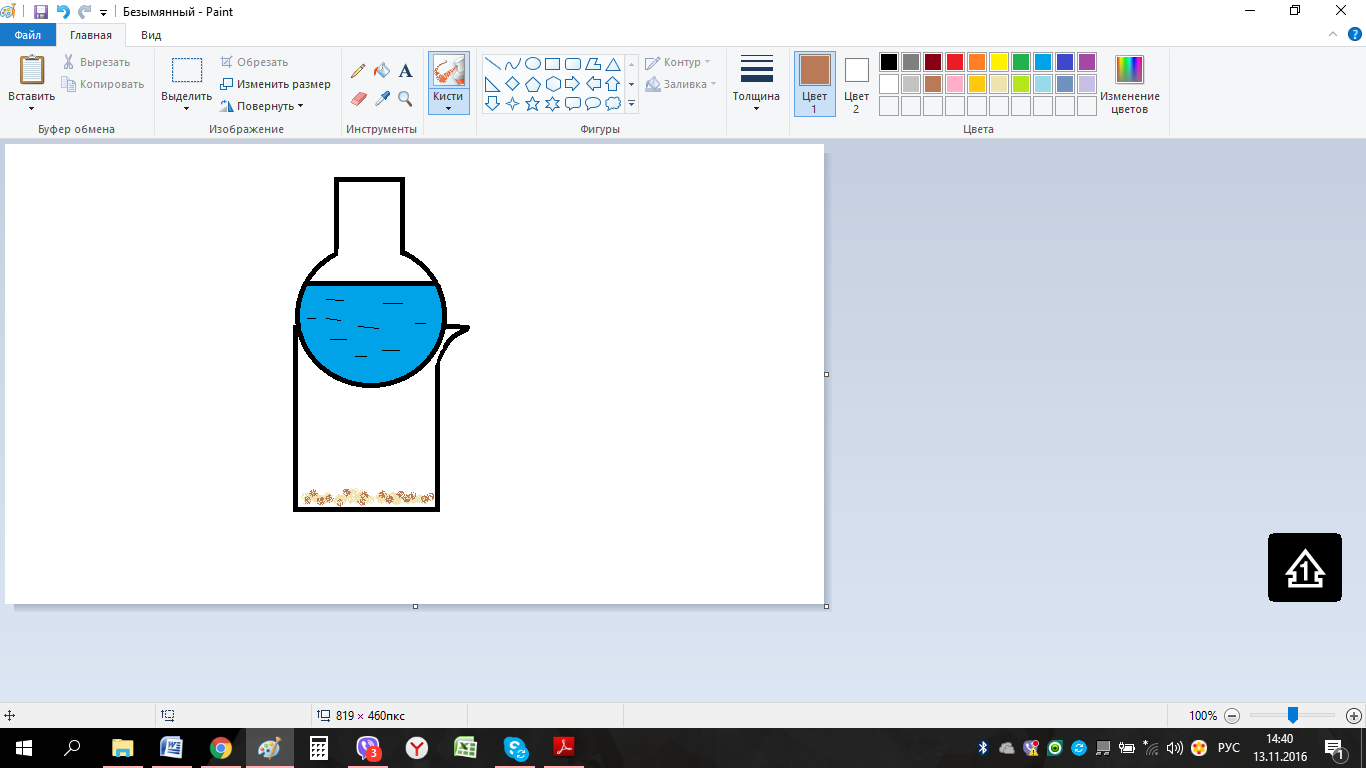 Рис. 7. Схема установки Стакан слабо нагревайте, не допуская плавления вещества. При этом бензойная кислота возгоняется и, охлаждаясь, оседает в виде игл на нижней части колбы, а нелетучие примеси остаются на дне стакана. После окончания процесса возгонки, очищенную бензойную кислоту поместите в специальную емкость. Стакан с примесями охладите в эксикаторе до комнатной температуры, после чего взвесьте на аналитических весах (mст+прим). Рассчитайте массовую долю чистой бензойной кислоты и примесей в исходном образце. Обработка результатов анализа
Выводы Лабораторная работа № 2 Очистка органических веществ методом перегонки Перегонкой называют процесс, в ходе которого вещество нагревается до температуры кипения, а образовавшиеся пары отводят и конденсируют. Перегонкой осуществляют очистку и разделение жидкостей, когда перегоняемые вещества устойчивы при температуре кипения. Простой перегонкой можно разделить вещества, если разница их температур кипения не менее 30 °С. Иначе используют процесс многократной перегонки – ректификацию. Для проведения перегонки собирают прибор из колбы Энглера (1), термометра (2), прямого нисходящего холодильника (3), аллонжа (4), приемника (5), нагревательного прибора, согласно рис. 9.  Рис. 9. Прибор для прямой перегонки жидкостей Прибор закрепляют в двух штативах при помощи необходимого количества лапок и муфт. При сборе прибора необходимо обратить внимание на следующее: Термометр в перегоняемой колбе помещают строго вертикально, и так, чтобы ртутный шарик термометра находился примерно на 0,5 см ниже отверстия отводной трубки и полностью омывался парами перегоняемой жидкости. Вода в холодильник поступает в нижний отвод, а выходит в верхний отвод. Прибор собирается слева направо, как показано на рисунке. Работу проводят следующим образом: Колбу Вюрца заполняют определенным объемом (но не более 2/3 емкости колбы) перегоняемой жидкости. Для равномерного кипения в колбу помещают несколько кипелок (кусочков неглазурованного фарфора). Включают воду и нагревательный прибор. Регулируют нагревание таким образом, чтобы в колбе было равномерное медленное кипение. При слишком быстром нагреве пары легко перегреваются. Температуру перегонки записывают. Заканчивают перегонку тогда, когда температура поднимется на 2-3 ºС выше той, при которой перегонялась основная масса жидкости. По окончании перегонки замеряют объем дистиллята. Вопросы для повторения 1. Что такое простая перегонка? 2. Какие вещества можно разделить перегонкой? 3. Что такое ректификация, когда ее применяют? 4. Опишите основное оборудование для проведения процесса перегонки. 4. Какие требования необходимо выполнять при сборке установки и самом процессе перегонки, почему? Методика выполнения работы Оборудование и материалы: – раствор перманганата калия; – штатив, колба Энглера, прямой холодильник, аллонж, приемник, термометр, цилиндр V=25 см3. Ход работы: По краткому химическому справочнику В.А. Рабиновича изучить свойства перманганата калия и воды (химическую формулу, молярную массу, температуры кипения). Отмерить цилиндром 100 см3 анализируемой смеси (водный раствор перманганата калия), перелить в колбу Энглера, закрепленную в штативе. Добавить «кипелки». Собрать прибор, установить термометр, приемник, подключить холодильник. Включить нагревательный прибор, основную выкипающую фракцию собирать в приемник, при этом зафиксировав температуру начала перегонки (падения первой капли в приемник). После окончания процесса перегонки замерить объем готового очищенного продукта (бидистиллята), перелить его в специальную емкость. Рассчитать выход продукта. Сделать выводы по работе. Обработка результатов: 1. Объем очищаемой смеси (см3): VСм=100 см3 2. Объем полученного бидистиллята (см3): Vбд= 3. Выход бидистиллята (%): 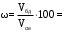 Выводы Лабораторная работа № 3 Очистка органических веществ кристаллизацией Цель: Ознакомиться с методом очистки органических веществ – кристаллизацией; Изучить методику очистки бензойной кислоты от посторонних примесей (сахарозы) кристаллизацией, ознакомиться с лабораторным оборудованием; Рассчитать массовую долю чистой бензойной кислоты и сахарозы в исследуемом веществе, сделать выводы. Теоретическое обоснование Кристаллизация (перекристаллизация) основана на различной растворимости веществ в одном и том же растворителе. Особенностью метода является то, что чаще всего понижение температуры приводит к уменьшению растворимости веществ. При выборе растворителя необходимо учитывать следующие требования: растворитель должен хорошо растворять вещество при нагревании и плохо – при охлаждении; растворитель не должен химически взаимодействовать с веществами; растворитель желательно применять в минимальных количествах, иначе очищаемое вещество не будет полностью выделяться при охлаждении. Очищаемое вещество может быть окрашено за счет присутствия примесей смолистых веществ. В этом случае при растворении вещества добавляют небольшое количество активированного угля (3-5 % по массе). Уголь можно помещать только в холодных раствор для предотвращения бурного вскипания раствора. Сущность процесса кристаллизации заключается в постепенном нагревании исследуемых веществ с небольшим количеством растворителя до кипения до полного растворения вещества. Если раствор содержит нерастворимые примеси, его фильтруют в горячем виде, после чего охлаждают в холодильнике или бане со льдом. За счет понижения растворимости выпадают кристаллы чистого вещества, которые отделяют от раствора фильтрованием при пониженном давлении (отсасыванием) на нутч-фильтре, рис. 10. На дно воронки Бюхнера укладывается бумажный фильтр и смачивают растворителем.  Рис. 10. Схема прибора для фильтрования при уменьшенном давлении (нутч-фильтр): 1 – воронка Бюхнера; 2 – колба Бунзена; 3 –водоструйный насос Выпавшие в растворе кристаллы очищаемого вещества вместе с раствором при помощи стеклянной палочки или узкого шпателя переносят на фильтр. После того как раствор отфильтруется, кристаллы промывают небольшим количеством холодного растворителя. На нутч-фильтр можно фильтровать органические вещества, находящиеся в осадке, при этом надо помнить, что фильтровать можно только холодные растворы. Методика выполнения работы Оборудование и материалы: – бензойная кислота загрязненная сахарозой, дистиллированная вода; – стаканчик, нутч-фильтр, эксикатор; – аналитические весы, электрическая плитка, сушильный шкаф. Ход работы: По краткому химическому справочнику В.А. Рабиновича изучите свойства бензойной кислоты и сахарозы (химическую формулу, молярную массу, температуры кипения и плавления, растворимость и нерастворимость в веществах). Определите, с помощью какого растворителя можно очистить бензойную кислоту от сахарозы кристаллизацией. Взвесьте около 1 г бензойной кислоты, загрязненной сахарозой. Добавьте к смеси небольшое количество горячего растворителя, перемешайте. Прокипятите полученный раствор пару минут до полного растворения смеси на электрической плитке. Интенсивным перемешиванием охлаждайте полученный раствор. Для ускорения охлаждения можно поместить стакан в ледяную баню. В результате охлаждения бензойная кислота выпадет в осадок в виде белых хлопьев, а сахароза останется в растворе. Вырежьте подходящий бумажный фильтр по размеру воронки Бюхнера, взвесьте его на аналитических весах, запишите массу. Поместите фильтр в воронку, включите водоструйный насос. Смочите фильтр дистиллированной водой так, чтобы он «прилип» ко дну воронки. После создания вакуума приступите к фильтрованию. Отфильтруйте осадок на нутч-фильтре. Фильтр с осадком поместите в сушильный шкаф на 30 минут при 30 ºС. Охладите просушенную кислоту пару минут на воздухе. Взвесьте фильтр с бензойной кислотой на аналитических весах. Произведите расчеты, сделайте выводы по работе. Обработка результатов: 1. Масса навески очищаемого вещества, взвешенная на аналитических весах (г): mН = 2. Масса взвешенного бумажного фильтра (г): mФ = 3. Масса взвешенного бумажного фильтра с бензойной кислотой после сушки (г): mФ+К = 4. Масса чистой бензойной кислоты (г): mК = mФ+К – mФ = 5. Массовая доля чистой бензойной кислоты (%): 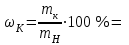 6. Массовая доля примеси – сахарозы (%): 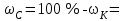 Выводы Вопросы для повторения 1. На чем основан метод кристаллизации (перекристаллизации)? 2. Перечислите основные требования при выборе растворителя. 3. Как необходимо дополнительно подготовить органическое вещество для очистки, если оно содержит примеси смолистых веществ? 4. Расскажите сущность процесса кристаллизации. 5. Опишите устройство нутч-фильтра и принцип его работы. 6. О какой особенности не следует забывать при фильтровании на нутч-фильтре? 7. Опишите кратко ход проведения лабораторной работы. 8. По каким признакам подбирают растворитель для очистки веществ кристаллизацией. Приведите пример. 9. Почему после фильтрования очищенную бензойную кислоту сушат при температуре 100 ºС, а не при 150 ºС, например? 10. По каким формулам рассчитывается содержание чистого вещества в очищаемом образце. |