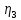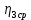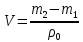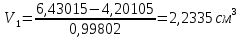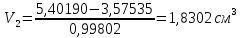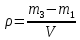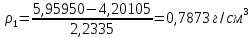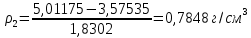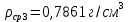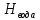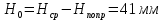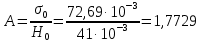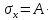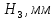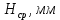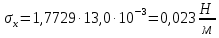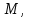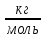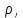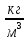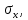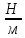ВЫДЕЛЕНИЕ ПЕКТИНА ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ И ОПРЕДЕЛЕНИЕ ЕГО РЕОЛОГИЧЕСКИХ ХАРАКТЕРИСТИК (ХАКАРТЕРИСТИЧЕСКОЙ ВЯЗКОСТИ МЕТОДОМ ВИСК. Лабораторная работа 3
 Скачать 317.75 Kb. Скачать 317.75 Kb.
|
|
ЛАБОРАТОРНАЯ РАБОТА №3 ВЫДЕЛЕНИЕ ПЕКТИНА ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ И ОПРЕДЕЛЕНИЕ ЕГО РЕОЛОГИЧЕСКИХ ХАРАКТЕРИСТИК (ХАКАРТЕРИСТИЧЕСКОЙ ВЯЗКОСТИ МЕТОДОМ ВИСКОЗИМЕТРИИ И МОЛЕКУЛЯРНОЙ МАССЫ) Задания: Выделить препарат пектина из растительного сырья. Определить вязкость водных растворов пектина различной концентрации. Определить характеристическую вязкость и средневязкостную молекулярную массу выделенного препарата пектина. Выполнение работы: Определение показателя преломления: Перед началом измерений проверяли нулевую точку прибора, используя дистиллированную воду; для этого 1-2 капли дистиллированной воды наносили на полированную поверхность измерительной призмы и устанавливали резкость по шкале и визирной линии в виде штрихов. Затем помещали окуляр при помощи рукоятки по шкале, до тех пор, пока визирная штриховая линия не совместится с границей светотени. Правильность произведенной установки проверяли 2-3 раза. После установки прибора на нулевую точку открывали верхнюю камеру Аббе, вытирали плоскость осветительной и измерительной призм досуха фильтровальной бумагой. На поверхность измерительной призы наносили 1-2 капли исследуемой жидкости и плавно опускали верхнюю камеру Аббе. Определяли показатель преломления жидкости. Измерения проводили несколько раз и вычисляли среднее арифметическое значение показателя преломления и среднюю квадратичную ошибку.
Определение плотности растворов: Сухой пикнометр, предварительно взвешенный на аналитических весах, заполняли дистиллированной водой и помещали в термостат. После 5-минутного выдерживания в термостате доводили уровень воды в пикнометре до метки. Затем заполненный водой пикнометр взвешивали на аналитических весах. Объем пикнометра, 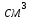 . .
где 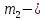 масса пикнометра с дистиллированной водой, г; масса пикнометра с дистиллированной водой, г; 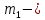 масса пустого пикнометра, г; масса пустого пикнометра, г; 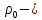 плотность воды при температуре опыта (21 плотность воды при температуре опыта (21 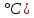 , 0,99802 г/ , 0,99802 г/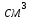 . .
Таким же образом заполняли сухой пикнометр исследуемой жидкостью, взвешивали и находили плотность жидкости по формуле:
где 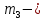 масса пикнометра с исследуемой жидкостью, г. масса пикнометра с исследуемой жидкостью, г.
Определение поверхностного натяжения: П 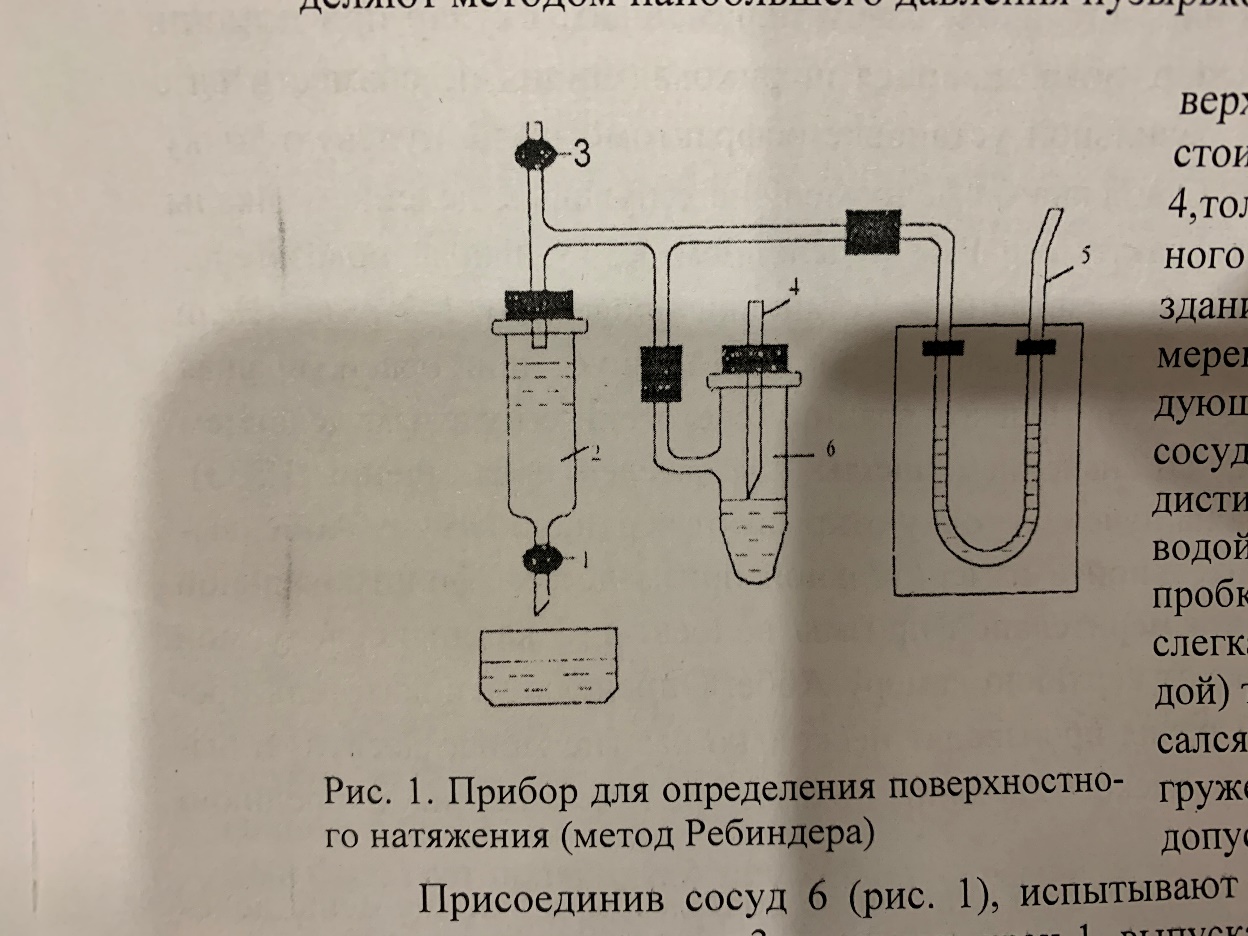 оверхностное натяжение для исследуемой органической жидкости определяли методом наибольшего давления пузырьков (метод Ребиндера). оверхностное натяжение для исследуемой органической жидкости определяли методом наибольшего давления пузырьков (метод Ребиндера).Прибор для определения поверхностного натяжения (рис. 1) состоит из сосуда 6, капилляра 4, толуольного манометра 5 и водяного эжектора 2, служащего для создания разрежения в системе. Измерения на приборе проводили следующим образом. В сухой и чистый сосуд 6 из бюретки наливали 10 мл дистиллированной воды. Сосед с водой плотно закрывали резиновой пробкой с капилляром так, чтобы капилляр только касался поверхности жидкости. Присоединив сосуд 6 (рис.1), испытывали систему на герметичность. Для этого закрывали кран 3 и, открыв кран 1, выпускали небольшое количество воды из эжектора 2, создавая в системе разряжение. Затем закрывали кран 1. Если разность уровней в манометре 5 не уменьшалась в течение 1-2 минут, то система достаточной герметична. Убедившись в герметичности прибора, определяли начальный уровень жидкости в манометре (поправку 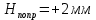 ), для этого открывали кран 3. ), для этого открывали кран 3.Затем определяли константу прибора, используя жидкость, поверхностной натяжение которой известно (обычно это вода). Для определения константы прибора измеряли высоту столбы жидкости в манометре в момент отрыва пузырька воздуха. С этой целью постепенно увеличивали разряжение в системе (при закрытом кране 3), по каплям выпуская воду из эжектора 2. Под влиянием разности давлений атмосферного и внутри системы на капиллярном кончике пипетки образовывался пузырек воздуха, который затем отрывался. Скорость образования и отрыва пузырька зависела от скорости вытекания воды из эжектора, она регулировалась краном 1 таким образом, чтобы образование пузырька происходило в течение 5-10 секунд. В момент отрыва пузырька создавалось некоторое максимальное разряжение в системе, которому соответствовала максимальная высота столба жидкости H в одном из колен манометра, измеряемая с точностью до 0,5 мм. Отмечали несколько значений максимальной высоты, находили среднюю величину 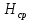 и рассчитывали высоту столба жидкости, учитывая поправку на начальный уровень жидкости в манометре: и рассчитывали высоту столба жидкости, учитывая поправку на начальный уровень жидкости в манометре:
Константу прибора А находили по формуле:
где 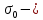 поверхностное натяжение воды при температуре 21 поверхностное натяжение воды при температуре 21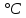 , Н\м. , Н\м.Далее сосуд 6 отсоединяли от системы, освобождали от воды, ополаскивали сосуд и пипетку небольшим количеством исследуемого раствора и наливали 10 мл данного раствора в сосуд 6. Плотно закрывали сосуд и проводили измерения, аналогичные вышеописанным. Таким образом, измеряли высоту 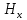 для исследуемой органической жидкости. для исследуемой органической жидкости.Вычисляли поверхностное натяжение для раствора по формуле:
Полученные результаты вносим в таблицу 1. В нее вносим также справочные значения для веществ с близкими экспериментальными значениями физических параметров. Таблица 1 – Физические свойства исследуемого органического соединения и веществ известного строения
По полученному опытным путем среднему значению показателя преломления и плотности вычисляют молекулярную рефракцию ( 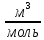 ) для предполагаемых веществ ) для предполагаемых веществ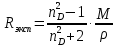 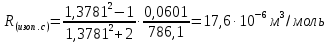 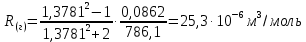 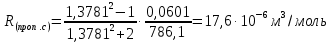
Сравнивают молекулярную рефракцию 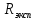 со значением рефракции, вычисленным по сумме атомных рефракций и инкрементов со значением рефракции, вычисленным по сумме атомных рефракций и инкрементов 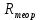 исходя из структурной формулы молекулы. исходя из структурной формулы молекулы.На основании молекулярной рефракции судят об объеме электронного облака молекулы, а по атомным рефракциям – об объеме, занимаемом электронным облаком атома. Объем молекулы близок к сумме объемов атомов, из которых она образована, поэтому молекулярная рефракция равна сумме соответствующих атомных рефракций: 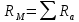 . .При наличии двойных и тройных связей в исследуемом соединении следует вводить поправки: 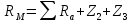 . .Рефракция атома зависит от соседних атомов, например, рефракция кислорода в гидроксильной группе имеет иное значение, чем его рефракция в карбонильной или эфирной группе. Поскольку рефракция зависит от строения молекул, то исходя из нее делают заключение о характере связей между атомами и определяю структуру молекулы. Затем устанавливали, какие из значений 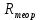 ближе к ближе к 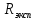 , они и определяю строение изучаемой молекулы: бутиловый или изобутиловый спирт. , они и определяю строение изучаемой молекулы: бутиловый или изобутиловый спирт.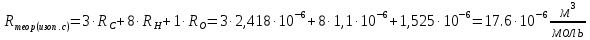 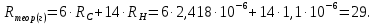 9 9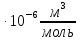  По полученному опытным путем значению поверхностного натяжения и плотности вычисляют молекулярный парахор для предполагаемых веществ: 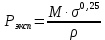 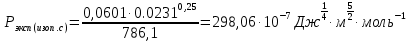 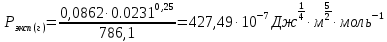 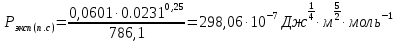 Сравнивают молекулярный парахор 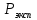 со значением парахора вычисленного по сумме атомных парахоров и инкрементов со значением парахора вычисленного по сумме атомных парахоров и инкрементов 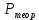 исходя из структурной формулы молекулы. исходя из структурной формулы молекулы.Парахор может быть вычислен как сумма парахоров отдельных атомов и инкрментов различных связей и инкрементов замкнутых циклов. 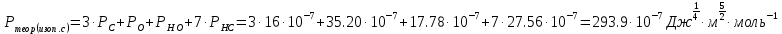 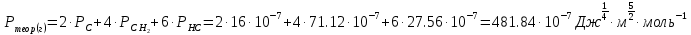 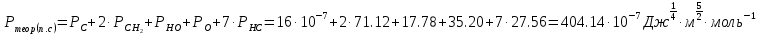 Парахор является удобной характеристикой, устанавливающей связь между химическим составом, строением молекул и физическими свойствами веществ. Сравнение значений парахора, вычисленного через определенное опытным путем значение поверхностного натяжения 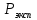 и по правилу аддитивности и по правилу аддитивности 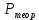 дает возможность сделать заключение о строении молекул. Расхождение между этими величинами не должен превышать 2-4 %. дает возможность сделать заключение о строении молекул. Расхождение между этими величинами не должен превышать 2-4 %. Вывод: на основании полученных расчетов можно сделать вывод о строение неизвестной органической жидкости: по рефракции не превышает 2% - пропиловый и изопропиловый спирт, по парахору не превышает 2 % - изопропиловый спирт. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||