Приготовление раствора и определение его концентрациии. Лабораторная работа 5 Отчет По дисциплине Химия (наименование учебной дисциплины согласно учебному плану) Тема Концентрация Автор студент гр. То21 Фролов Т. И. (Подпись) (Ф. И. О.) Дата 23. 05. 22. Проверил
 Скачать 0.69 Mb. Скачать 0.69 Mb.
|
|
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ   Федеральное государственное бюджетное образовательное учреждение высшего образования «САНКТ-ПЕТЕРБУРГСКИЙ ГОРНЫЙ УНИВЕРСИТЕТ» Кафедра общей химии Лабораторная работа №5 Отчет По дисциплине: Химия (наименование учебной дисциплины согласно учебному плану) Тема: Концентрация Автор: студент гр. ТО-21 Фролов Т.И. (Подпись) (Ф.И.О.) Дата: 23.05.22. ПРОВЕРИЛ: (Должность) (Подпись) (Ф.И.О) Санкт-Петербург 2022 Цель работы: ознакомиться с методами приготовления растворов заданной концентрации и анализом растворов заданной концентрации и анализом раствора при помощи титрования. Общие сведения Раствором называется гомогенная (однородная) система, состоящая из двух или более компонентов, состав которой может непрерывно изменяться в определенных пределах. Приём количественного анализа, при котором к раствору определяемого вещества по каплям приливают раствор реагента точно заданной концентрации, называют титрованием. Состояние системы, в котором аналитическая реакция прошла полностью в соответствии со стехиометрическими уравнениями при отсутствии избытка реагента, называют точкой эквивалентности. Задача титрования – определить эквивалентный объём добавляемого реагента – титранта, необходимый для установления точки эквивалентности, так как в ней числа эквивалентов определяемого вещества и титранта равны между собой. Из определения нормальной концентрации следует, что число эквивалентов вещества в растворе равно произведению нормальности на объём раствора. Следовательно: СN(x)Vx = CN(T)VT где индекс x относиться к пробе, а T- к титранту. Отобрав для титрования мерной пипеткой точный объём пробы Vx, зная нормальность титранта CN(T) и определив эквивалентный VT, по формуле можно вычислить концентрацию пробы CN(x). До эквивалентной точки в ходе титрования в растворе присутствует избыток определяемого вещества, а после – избыток титранта. Поэтому в эквивалентной точке свойства раствора резко изменяются, в частности, изменяется окраска специально подобранных цветных индикаторов, что позволяет определить эквивалентный объём титрата. Протокол лабораторной работы 1. 2. Объем аликвоты соляной кислоты, взятый для титрования, Vа =5 мл. 3. Концентрация раствора щелочи CNaOH = 0,2 экв/л. 4. Объем щелочи, пошедший на титрование пробы соляной кислоты: VNaOH, 1 = 2,5 мл; VNaOH,2 = 2,5 мл; VNaOH,ср = 2,5 мл. Обработка результатов эксперимента: 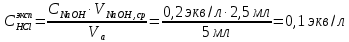 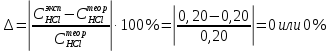 Вывод: ознакомился с методами приготовления растворов заданной концентрации и анализом растворов заданной концентрации и анализом раствора при помощи титрования. |
