Лабораторная работа Определение щелочности воды
 Скачать 17.91 Kb. Скачать 17.91 Kb.
|
|
Лабораторная работа «Определение щелочности воды» Щелочностью считается способность некоторых компонентов воды взаимодействовать с водородными ионами сильной кислоты. Общая щелочность природных вод обуславливается анионами слабы кислот НСО3–, СО32–, НSiО3–, Н2PО4– и другими анионами, гидролизующимися с образованием гидроксид–ионов. Та часть щелочности, которая соответствует количеству кислоты, необходимой для понижения рН до 8,3, называется свободной щелочностью. Количество кислоты необходимое для достижения рН=4,5, эквивалентно общей щелочности. Если рН воды меньше 4,5, то ее щелочность равна нулю. Показатель ПДК для водоемов хозяйственно-питьевого назначения составляет 0,5–6,5 ммоль/л МЕТОД ОПРЕДЕЛЕНИЯ Метод определения общей щелочности является титриметрическим (ГОСТ Р 52963, ПНД Ф 14.1:2.245–07, РД 52.24.493–2008) и пригоден для анализа питьевой, природной минеральной лечебно-столовой и т.п. вод, а также почвенных вытяжек. Определение основано на реакции карбонат– и гидрокарбонат–ионов с водородными ионами в присутствии, в качестве индикаторов, фенолфталеина и метилового оранжевого. РЕАКТИВЫ И ОБОРУДОВАНИЕ Раствор индикатора фенолфталеина; раствор индикатора метилового оранжевого; 0,1н раствор соляный кислоты. Пипетка-капельница полимерная; пипетка градуированная на 2 мл или на 5 мл для титрования с соединительной трубкой и шприцем-дозатором или титровальная установка; конические колбы на 100 и 250 мл; склянка с меткой «10 мл». ХОД ОПРЕДЕЛЕНИЯ СВОБОДНОЙ ЩЕЛОЧНОСТИ (КАРБОНАТ–ИОНА) В коническую колбу на 100 мл или мерную склянку отберите пробу анализируемой воды объемом 10 мл, добавьте в колбу пипеткой–капельницей 3–4 капли индикатора фенолфталеина. Содержимое колбы перемешайте. Проведите титрование пробы с помощью титровальной установки, либо градуированной пипеткой со шприцем-дозатором раствором соляной кислоты, до обесцвечивания, и определите объем раствора соляной кислоты, израсходованный на титрование по фенолфталеину (VК, мл). Раствор после титрования карбонат–иона оставьте для дальнейшего определения в нем массовой концентрации гидрокарбонат–иона. Рассчитайте содержание карбонат–иона (свободную щелочность – ЩСВ) в ммоль/л по формуле:  где VК – объем раствора соляной кислоты, израсходованного на титрование, мл; C – концентрация раствора соляной кислоты, моль/л экв; Vп – объем пробы воды взятой для анализа, мл; 1000 – коэффициент пересчета из моль в ммоль. ХОД ОПРЕДЕЛЕНИЯ ОБЩЕЙ ЩЕЛОЧНОСТИ (ГИДРОКАРБОНАТ–ИОНА) В ту же колбу, где проводили определение свободной щелочности, прибавьте 2–3 капли индикатора метилового оранжевого и титруйте раствором соляной кислоты до перехода от желтоватой до слабо–розовой окраски. Определите объем соляной кислоты, израсходованной на титрование общей щелочности (VО). Рассчитайте содержание гидрокарбонат–иона (общую щелочность – ЩО) в ммоль/л по формуле: 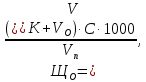 где VК и VО – объем раствора соляной кислоты, израсходованного на титрование по фенолфталеину и метиловому оранжевому, мл; C – концентрация раствора соляной кислоты, моль/л экв; Vп – объем пробы воды взятой для анализа, мл; 1000 – коэффициент пересчета из моль в ммоль. Для определения массовой концентрации карбонат– и гидрокарбонат–ионов используйте значения свободной щелочности (ЩСВ), ммоль/л, и общей щелочности (ЩО), ммоль/л (табл. 4). Таблица 4 Соотношение между щелочностью и молярной концентрацией карбонатов и гидрокарбонатов
Массовую концентрацию гидрокарбонатов (СГК масс), мг/л, и карбонатов (СК масс), мг/л в анализируемой пробе воды, рассчитывайте по формулам: СГК масс = СГК ·61, СК масс = СК ·60, где СГК и СК – молярная концентрация гидрокарбонатов и карбонатов соответственно, определенная по табл. 2 , ммоль/л; 61 и 60 – молярная концентрация эквивалента гидрокарбонат– и карбонат–иона соответственно в реакциях титрования, г/моль. Контрольные вопросы: 1. Что понимают под щелочностью воды? 2. Какие вещества обуславливают щелочность воды? 3. Что понимают под свободной щелочностью воды? 4. Что понимают под общей щелочностью воды? 5. Каким методом определяют данный показатель? Инструкция 1. Оформить теорию в виде ответов на контрольные вопросы. 2. Записать ход определения. 3. Произвести расчет по формулам Щсв и Що. Vk=0.1, Vo=0.1 4.Произвести расчеты по формулам СГК масс, СК, используя рассчитанные значения Щсв, Що и таблицу. 5. Сделать вывод по работе. |
