Термодинамические этюды. Общая неорганическая химия. Лекция Термодинамические этюды. Часть 2
 Скачать 1.1 Mb. Скачать 1.1 Mb.
|
Лекция № 7. Термодинамические этюды. Часть 2.Что значит – «процесс идет самопроизвольно?» Пример: таяние снега (льда) при температуре выше 0 по Цельсию. P(->) – Вероятность прямого процесса P(<-) – Верятность обратного процесса P(->)>P(<-) – Условие самопроизвольного протекания прямого процесса Самопроизвольные процессы сопровождаются ростом беспорядка (хаоса) Хаос- один из самых могущественных богов во многих мифах, основа сотворения мира. Интересный факт хаос не всегда имеет вероятную природу, он может возникнуть в системе описываемые системы жестко детерминированных линейных уравнений.  «Странный аттрактор» Хаос для нас важен, потому что это спутник, самопроизвольно протекающий процессов. Хаос связан с некоторыми вероятностями, что по природе своей явления вероятностное. Если есть некоторая система, которая описывается сложными уравнениями движения (не линейные), то тогда траектория движения частиц, которые входят в эту систему, она оказывается часто не устойчивой к начальному слою микроразличному возмущениям (Эти уравнения можно решать численно, потому что они сложны). Потому что, когда начинаешь решать уравнения, то возникают такие ситуации, что малейшее отклонение от начальных значений, когда погрешность приводит к появлению очень странных траекторий, которые никак не описывают привычные траектории движения(«Странный аттрактор»).  Закон сохранения энергии не нарушается. Один моль газа в цилиндре, разделенном перегородкой 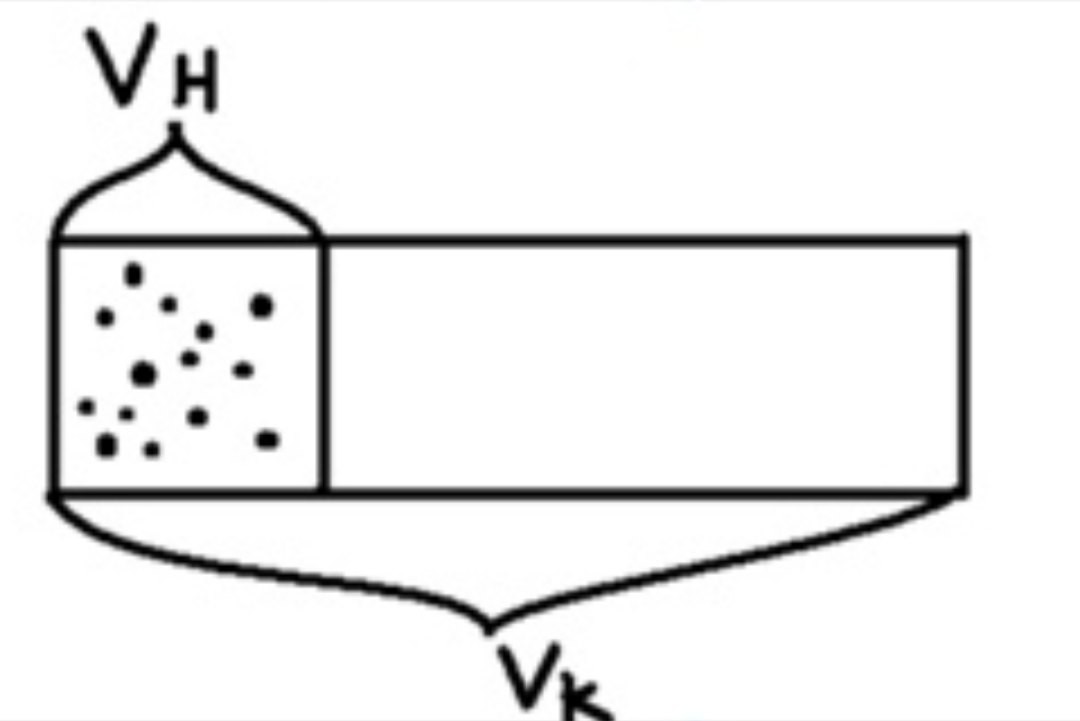 Vн и Vк – начальный и конечный объем системы   Вывод: экзотермический процесс приводит к росту энтропии окр. среды, а эндотермический – к её уменьшению! Связь энтропии с микроструктурой системы: важное следствие задачи об изотермическом расширении газа Sсист = kB In Vk/Vн = kB InW Где W – безразмерная величина, пропорциональная объему. Можно предположить, что W – число микросостояний системы, описывающих её макросостояние с данной энергией (W>= 1)   К  ак работает формула Больцмана: иллюстрация на простой модельной системе ак работает формула Больцмана: иллюстрация на простой модельной системеSсист = kB InW 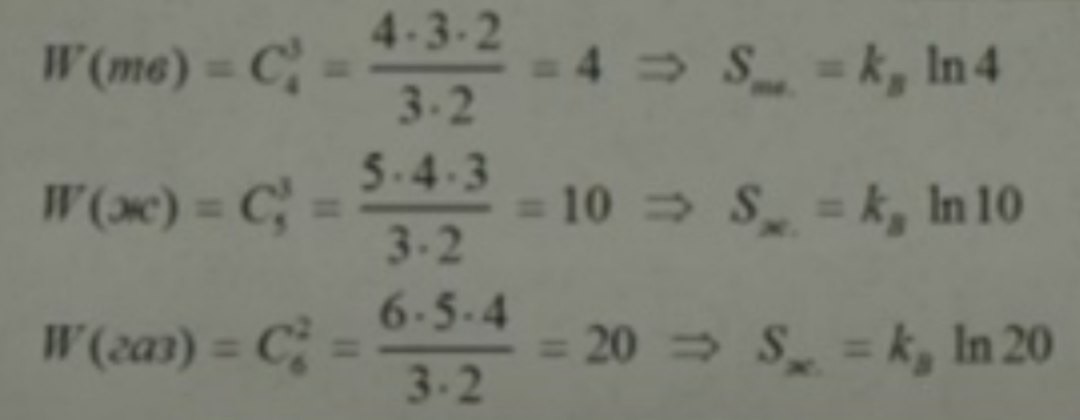 Вывод: энтропия системы зависит от её агрегатного состояния! Второй закон термодинамики Самопроизвольный процесс сопровождается ростом суммарной (полной) энтропии: Sполн = Sсист + Sср > 0 Другая формулировка: Sполн > 0 – условие термодинамической возможности (вероятности) процесса. «Энергия мира постоянна, а энтропия стремится к максимуму» -Rudolf Klausius Пример 1. Хорошо известная реакция – вулканчик   Энергия Гиббса процесса не содержит информации о его интенсивности (скорости протекания). Расчеты изменения энтропии и энергия Гиббса реакций, с использованием табличных данных основаны на правиле Гиббса.  Нет информации о скорости протекания. G может быть очень отрицательным, т.е. термодинамическая вероятность протекания может быть большая, а силу большого барьера может протекать очень медленно и без активации (при конкретных условиях) Немного истории науки Сади Карно сформулировал 2-ой закон термодинамики, не используя понятия энтропия. И. Р. Пригожин получил нобелевскую премию по химии в 1977 за работы по неравновесной термодинамики.  |
