лекция. Лекция 1+ (1). Лекция 1 Введение в курс Строение металлов и сплавов
 Скачать 385.67 Kb. Скачать 385.67 Kb.
|
|
Лекция 1 Введение в курс Строение металлов и сплавов Чтобы понимать, как подобрать подходящее для той или иной операции высокотемпературной обработки оборудование следует понимать базовые основы металловедения и теории термообработки. В данной статье мы расскажем о строении металлов и сплавов. Металловедение — прикладная наука, которая изучает строение, свойства металлов, устанавливает связь между химическим составом, структурой и свойствами металлов, а также закономерности изменения структуры и свойств под воздействием внешних факторов. Металловедение - это прикладная наука, изучающая связь между составом, строением и свойствами металлов и сплавов, а также их изменение при различных внешних воздействиях. К числу свойств металлов и сплавов, в частности, относятся: механические (прочность, пластичность, вязкость и твердость), химические (сопротивление действию агрессивной среды), физические (магнитные, электрические, объемные и тепловые), технологические (жидкотекучесть, штампуемость, об-рабатываемость режущим инструментом, прокаливаемость). Несмотря на то, что человек использовал металлы на протяжении почти всей своей истории, металловедению как науке сейчас около 200 лет. Для истории металловедения характерны следующие три периода. Первый период (до двадцатых годов ХХ века), во время которого были заложены основы металловедения и создано общее представление о металлах и сплавах. Это было сделано на основе исследования их строения как невооруженным глазом, так и под металлографическим микроскопом и путем обычных методов лабораторных испытаний их свойств. Во втором периоде (с двадцатых по пятидесятые годы ХХ века), удалось создать ясное представление о расположении атомов в идеальных кристаллах металлов и о процессах, происходящих в них, на основе результатов рентгеноструктурного анализа и более тонких и всесторонних методов лабораторных исследований. Однако оказалось, что наиболее важные свойства металлов определяются не идеальным расположением атомов в металлических кристаллах, а нарушениями такого расположения, т. е. дефектами их строения. Третий период (с пятидесятых годов ХХ века) связан с применением гораздо более эффективного, чем рентгеновские лучи, ядерного излучения (быстрые нейтроны, -частицы и т. д.), что наряду с применением электронной микроскопии и других совершенных методов лабораторного исследования обеспечило возможность более глубокого и всестороннего изучения строения реальных металлов. В кристаллах металлов удалось изменять расположение атомов, создавать там различные дефекты строения и изучать их взаимодействие, от которого зависят важнейшие свойства реальных металлов. Благодаря этому металловедение может не только объяснять строение и свойства металлов и сплавов, но и предвидеть их, а также изменять их в желательном для производства и эксплуатации направлении. Появление новых методов исследования обусловлено тем, что непрерывно развивается и совершенствуется теоретическая база науки о металлах – физика твердого тела, а практика требует получения новых металлов и сплавов. Современное металловедение все больше сближается с металлофизикой, и сейчас невозможно представить себе подлинно научных работ в этой области, в которых не использовались бы достижения современной физики твердого тела. Точно также ни одна рациональная технология термической обработки не может не опираться на основные положения научного металловедения. Хотя металловедение нашего времени не может быть отделено от физики и химии, но, как и в первый период своего развития, металловедение является, прежде всего, наукой о технических металлах и сплавах. Металловедение обычно подразделяют на 2 части: • теоретическое металловедение или теория сплавов; • практическое металловедение. Теоретическое металловедение рассматривает природу металлов и сплавов; методы их исследования; связь изменений в металлах и сплавах под влиянием температуры, давления и иных внешних воздействий, с законами, по которым строение и свойства сплавов изменяются в зависимости от их состава. В практическом металловедении даются необходимые сведения о физических, химических и технологических свойствах металлов и сплавов, применяющихся в технике, а также указываются пути рационального выбора металлических материалов для определенного назначения. В первый период развития металловедения наибольшее внимание уделялось железу и его сплавам с углеродом (стали и чугуну), но постепенно исследования охватили и другие металлы и сплавы, и сейчас металловедение занимается изучением практически всех металлических элементов и сплавов на их основе. Основными разделами классического металловедения являются: •Теория сплавов (кристаллическое строение, плавление и кристаллизация, механические свойства, процессы деформации и нагрева, строение сплавов, диаграммы состояния). • Металловедение черных металлов: железоуглеродистые сплавы (диаграмма состояния, классификация, структура, процессы термической обработки, легирование). Сюда также относят сплавы титана, тугоплавких металлов, сплавы с особыми свойствами, магнитные сплавы и сплавы атомной энергетики. • Цветные металлы и их сплавы (благородные металлы, алюминий, медь, цинк и др; подшипниковые и типографские сплавы, биметаллы и композиты). Основана на теоретическом и экспериментальном изучении физики металлов, химически-структурных методах анализа твёрдого тела, а также на термодинамических и кинетических концепциях. Строение металлов В твердом состоянии любой металл обладает кристаллическим строением. Для этого вида строения характерна упорядоченность расположения ионов (атомов). Элементарные ячейки периодически повторяются в пространстве, образуя кристаллическую решетку. Внутри кристаллической решетки располагаются положительно заряженные ионы, или как их называют по-другому – атомные ядра. Вокруг атомных ядер в постоянном движении находятся отрицательно заряженные частицы – электроны. Количество электронов, находящихся между ионами и определяет уровень теплопроводности металла. Ионы (атомы) внутри кристаллической решетки находятся в непрерывном тепловом колебании. Если температура повышается, то амплитуда колебаний атомов резко возрастает, если температура понижается, то амплитуда замедляется. Плавка металла разрушает кристаллическую решетку, выпуская ионы в беспорядочное движение в пространстве. Элементарная ячейка – это главный элемент кристаллической решетки. Увидеть ее вы можете на изображении 1. Изображена решетка в виде куба. Однако можно заметить, что каждый атом этой решетки одновременно принадлежит восьми соседним элементарным ячейкам. 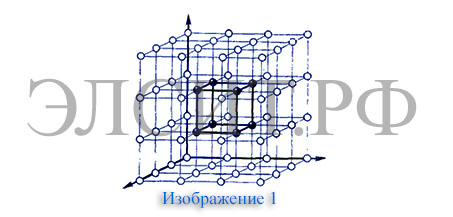 На изображении 2 вы можете увидеть наиболее распространенные типы кристаллических решеток. а) Объемно-центрированная решетка. Как видно из рисунка восемь атомов данного типа решетки располагается в углах куба, а один находится в центре. Данная кристаллическая решетка свойственна следующим металлами – натрий, литий, свинец, вольфрам и т.п.  б) Гранецентрированная решетка. Внимательно рассмотрев ее изображение, вы заметите, что восемь атомов данного типа решетки расположено в уголках куба, а в центре каждой из шести граней размещается еще по одному атому. Свойственна гранецентрированная кубическая решетка следующим металлам: медь, серебро, алюминий, золото и т.п.  в) Гексагональная решетка имеет расположение атомов в углах и центре основания призмы. При этом три атома располагаются в средней плоскости призмы. Характерен данный вид кристаллической решетки следующим металлам: титан, магний, цинк, бериллий и другие металлы.  Индукционный нагрев способен проникать в кристаллические решетки металла, равномерно распределяя тепло и не нарушая их структуру. Автоматизированное программное обеспечение, которым снабжена каждая установка ЭЛСИТ позволяет проконтролировать процесс обработки, чтобы та не нарушила структуру кристаллической решетки. Дефекты кристаллической решетки Ничто в нашем мире не идеально. Кристаллы металлов не обладают идеально правильным расположением атомов внутри кристаллической решетки. Практически всегда внутри кристаллов встречаются различные несовершенства (дефекты строения). В некоторой степени дефекты кристаллической решетки определяют физические и механические свойства металлов. Дефекты строения кристаллической решетки можно подразделить на три вида: точечные, поверхностные и линейные. Среди точечных дефектов наиболее распространенными являются – вакансии. На изображении 3 вы можете заметить вакансии. Вакансии представляет собой дефект кристалла с отсутствующим внутри кристаллической решетки атомом. Еще одним точечным дефектом является дислоцированный атом. Дислоцированный атом – это дефект кристаллической решетки, при котором один из атомов выходит из равновесия. Вы можете наблюдать данный дефект на изображении 4. 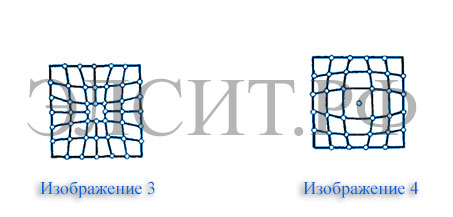 Ни вакансии, ни дислоцированный атом не остаются без движения. Их непрерывное перемещение внутри кристаллической решетки называется диффундированием. Так как энергия между атомами распределяется неравномерно, вакансия может передвигаться внутри атома до тех пор, пока не выйдет из него на поверхность кристалла. Дислоцированные атомы и вакансии искажают кристаллическую решетку, по этой причине свойства кристалла могут меняться. При проведении термообработки важно учитывать все эти факторы. Индукционный нагрев в некоторых случаях может помочь избавиться от дефекта кристаллической решетки, равномерно распределив тепло по всей поверхности кристалла. Наиболее распространенными линейным дефектом кристаллической решетки является дислокация. Дислокация – это нарушение правильного кристаллического строения металла. На изображении пять вы можете разглядеть дислокацию атомов. а) Дислокация расположена на левом краю кристалла. б) Центральное расположение дислокации. в) Дислокация расположена на правом краю кристалла. 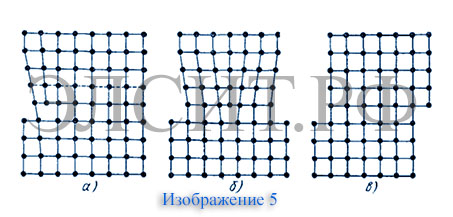 Поверхностные дефекты появляются на границе зерен или субзерен, если атомы обладают не таким правильным расположением, как внутри зерна. Как правило, по границам зерен скапливаются дислокации и вакансии. На изображении 6 вы можете разглядеть поверхностные дефекты кристаллической решетки, разделяющие зерно на блоки.  Сплавы металлов - структура На сегодняшний день производители все чаще стали использовать при создании металлических изделий не чистые металлы, а сплавы. Сплавы металла – это вещества, которые образовались в результате затвердения расплава, состоящего из нескольких компонентов. Компонентами формирования сплавов служат только металлы или металлы с небольшим количеством примесей. Металлические сплавы подразделяются на двойные, тройные и т.п. (по количеству входящих в них компонентов), а также на черные и цветные металлы (в зависимости от того, какой металл лежит в основе сплава). Если строение металлов понять проще, то строение сплавов существенно отличается. Строение металлического сплава довольно сложное. Существует несколько видов сплавов, в зависимости от характера взаимодействия его компонентов друг с другом. Химическое соединение – сплавы металлов, элементы которого могут вступать друг с другом в химическое взаимодействие, тем самым создавая новую кристаллическую решетку. Образовавшееся химическое соединение обладает уже совсем другими свойствами, чем компоненты, вошедшие в его состав. Механическая смесь – сплавы металла, компоненты которого не растворяются, находясь в твердом состоянии, а также не вступают друг с другом в химическое соединение. Как правило, механическая смесь не изменяет кристаллические решетки металлов, входящих в сплав. Твердый раствор – сплав, образовавшийся во время охлаждения жидкого раствора сплава, компоненты которого сохранили растворимость, а при кристаллизации смогли образовать единую кристаллическую решетку. Твердые растворы также подразделяются на два главных типа: внедрения и замещения. Если посмотреть на изображение 7, то вы отметите на первой картинке, как атомы растворимого компонента начали замещать атомы растворителя. При этом никогда не ясно, в каком соотношении атомы заменят друг друга. Однако важно отметить, что необходимо соблюдение двух главных условий, чтобы началась замена атомов. Первое – оба компонента должны иметь схожие кристаллические решетки. Второе – размеры атомов входящих в состав сплава компонентов должны различаться лишь незначительно (не более 8%). 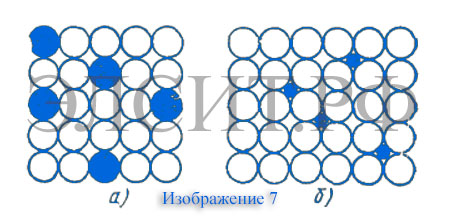 Атомы, входящие в состав твердых растворов внедрения, значительно отличаются друг от друга по размерам. Справа на изображении 7 вы можете заметить, как атомы одного компонента внедряются в пустоты кристаллической решетки другого. Во время формирования твердого раствора кристаллическая решетка искажается, а ее параметры меняются. В большинстве случаев атомы распределяются беспорядочно, однако бывают случаи, когда она размещаются внутри кристаллической решетки упорядоченно (при медленном охлаждении расплава меди и золота). Твердые растворы с равномерно распределенными атомами внутри кристаллической решетки называются сверхструктурными. |
