генетика. Лекция Введение. Молекулярные основы наследственности
 Скачать 238.64 Kb. Скачать 238.64 Kb.
|
|
4.5 Действие хромосомных мутаций на различные системы организма Степень изменения признаков организма при хромосомных мутациях зависит от величины дефектного участка и от содержания в нем важных для развития генов. Для определения последствий хромосомных мутаций у человека все аутосомные мутации и мутации, связанные с Х-хромосомой, разделили на следующие 4 группы.
Мутации, вызванные дефектами Х-хромосомы, вызывают поражения высших функций организма, связанных с нервной и сенсорными системами. А мутации аутосом чаще приводят к изменениям в строении тела и вегетативных функций. По статистике, около 15% всех беременностей у женщин прерываются спонтанными абортами. Из их числа примерно 40% выкидышей имеют хромосомные мутации. Чаще всего выкидыши наблюдаются в период между 8-й и 15-й неделями беременности. Около 50% всех зачатий у человека не реализуются и не обнаруживаются, так как из-за пороков развития гибель зародыша наступает уже в первые две недели развития. Этим способом природа защищает человечество от дефектных организмов. Лишь немногие мутанты доживают до момента рождения, поэтому частота хромосомных мутаций среди живорожденных младенцев по сравнению с эмбрионами оказывается гораздо ниже (около 0,5-0,6%). Особенно часто ранняя гибель плодов наблюдается при трисомии по 16 хромосоме. Эти трисомии полностью несовместимы с жизнью –они летальны. Меньше нарушается эмбриональное развитие при трисомии 8 хромосомы. Около 60% всех зигот с трисомией по 21 хромосоме абортируются. Этот дефект совместим с жизнью, но сопровождается выраженной патологией (синдром Дауна). Велико количество выкидышей и при моносомии по Х-хромосоме (ХО), когда в развивающемся женском организме вместо двух Х-хромосом обнаруживается лишь одна Х-хромосома. К гибели организма приводят не только дефекты белков, но и аномалии ферментов. У человека имеется около 10 тыс. ферментов. Для 200 ферментов из этого количества (2%) характерны различные дефекты. Они приводят к нарушениям обменных процессов, сниженному синтезу гормонов, недостаткам переноса веществ через клеточные мембраны, ошибкам при «ремонте» поврежденных участков ДНК и другим отклонениям от нормы. Но, для нормальной функции клеток достаточно 50 % нормального уровня активности ферментов. В этом случае возможно выживание целостного организма. Если же дефект фермента снижает его активность больше чем на 50%,то организм погибает. 4.6 Последствия мутации в половых и соматических клетках Результат действия мутации на фенотип человека может различаться в зависимости от типа клеток, в которых происходит изменение наследственных структур. Генеративные мутации или изменение наследственного материала в половых клетках происходит в периоде оогенеза или сперматогенеза, при репликации ДНК и расхождении хромосом в процессе мейоза. В результате может образоваться одна или несколько аномальных гамет. В большинстве случаев это только небольшая часть всех половых клеток организма, и она не влияет на фенотип человека, имеющего эти гаметы. Однако, если несущая мутацию половая клетка вступит в оплодотворение, то образовавшийся из такой зиготы организм может иметь определенные фенотипические особенности. В дальнейшем возможно наследование этой мутации в ряду поколений. Генеративные мутации часто осложняются гибелью зародыша. Рождением ребенка заканчивается только 30-40% зачатий. Иногда происходит спонтанный аборт или внутриутробная гибель плода, особенно в первые три месяца беременности. При этом 60-65% зародышей имеют изменения структуры или числа хромосом. Соматические мутации – это изменения наследственного материала в соматических клетках. Такая мутация передается только потомкам мутантной клетки в процессе митоза. В результате в организме человека могут оказаться клеточные популяции с разным набором наследственного материала. Если мутация происходит на ранних стадиях дробления зиготы, формируется мозаицизм. Мозаичный организм может иметь ткани как с нормальными, так и измененными геном или хромосомой. Мозаицизм – очень распространенное явление. Примерно 1 из 48 больных с синдромом Дауна является мозаиком. Доля клеток, несущих аномальный клон, зависит от стадии развития зародыша. Чем позднее происходит мутация, тем меньше клеток организма содержат эти изменения наследственного материала. При мозаицизме фенотипические нарушения у человека выражены слабее, чем, когда мутация содержится во всех клетках организма. Мозаицизм установлен для хромосомных и моногенных мутаций, хотя многие генные соматические мутации остаются недиагностированными. Подобное изменение наследственного материала было обнаружено примерно при 30 заболеваниях. Если соматическая мутация происходит после эмбрионального периода, то она приводит к образованию только небольшого количества аномальных клеток. Такое изменение наследственного материала может не иметь последствий для здоровья человека. Но иногда клетки, несущие мутацию, подвергаются злокачественному перерождению. Установлено, что для очень большого числа опухолевых заболеваний характерны специфические изменения наследственных структур в поврежденных клетках. Так, при хроническом миелолейкозе (злокачественное заболевание крови) у больных часто обнаруживается «филадельфийская» хромосома (делеция участка длинного плеча 22-й хромосомы). При этом утраченная часть обычно присоединена к 9-й хромосоме. Специфические хромосомные изменения выявлены и при других опухолевых заболеваниях человека (острых лейкозах, карциномах, нейробластоме, ретинобластоме). Одним из механизмов, приводящих к развитию злокачественных заболеваний, являются мутации онкогенов. Онкогены – это гены, участвующие в процессе опухолевого перерождения клеток. В норме они определяют различные стороны жизнедеятельности клетки. Так, некоторые из них контролируют факторы и рецепторы роста, активное деление клеток на ранних стадиях внутриутробного развития организма. Мутации таких генов приводят к перерождению клеток в опухолевые, которые способны к неограниченному делению. Соматические мутации онкогенов обнаружены при карциноме мочевого пузыря. Считают, что соматические мутации участвуют и в процессе нормального старения. Известно несколько моногенных наследственных заболеваний, характеризующихся преждевременным старением человека (например, синдром Вернера). 4.7 Устойчивость и репарация генетического материала Устойчивость генетического материала обеспечивается:
Репарация генетического материала– это внутриклеточный процесс, обеспечивающий восстановление поврежденной структуры молекулы ДНК. Нарушения могут быть вызваны повреждениями азотистых оснований, разрывом одной или двух нитей молекулы, вставками или выпадениями нуклеотидов, сшивками нитей ДНК. Различают репарацию: 1) дорепликативную (до удвоениямолекулы ДНК), 2) репликативную (в процессе удвоения), 3) пострепликативную (после удвоения). Впервые возможность репарации молекулы ДНК была установлена в 1948 г. А. Кельнером, К. Руперт (1962) описал один из способов репарации –фотореактивацию. Было выявлено, что при ультрафиолетовом облучении фагов, бактерий и протистов наблюдается резкое снижение их жизнеспособности. Однако выживаемость их значительно повышается, если на них дополнительно воздействовать видимым светом. Оказалось, что под действием ультрафиолета в молекуле ДНК образуются димеры (химические связи между двумя пиримидиновыми основаниями одной цепочки, чаще (Т-Т), что препятствует считыванию информации. Видимый свет активирует фермент фотолиазу, разрушающий димеры. Темновая (эксцизионная) репарация была изучена А. Герреном в 50-е годы. Она заключается в нахождении и удалении поврежденного участка нити ДНК путем его "вырезания", в синтезе и вставке нового фрагмента с участием ферментов. Темновая репарация протекает в 4 стадии (рис. 25): 1) эндонуклеаза "узнает" поврежденный участок и рядом с ним разрывает нить ДНК; 2) экзонуклеаза "вырезает" поврежденный участок; 3) ДНК-полимераза по принципу комплементарности синтезирует фрагмент ДНК на месте разрушенного; 4) лигаза "сшивает" концы ресинтезированного участка с основной нитью ДНК. Нарушение процессов репарации приводит к ряду заболеваний. У больных пигментной ксеродермой под действием солнечного света появляются веснушки, расширяются капилляры, ороговевает эпидермис, поражаются глаза, развиваются злокачественные опухоли кожи. При анемии Фанконинаблюдается недостаточность функций костного мозга, приводящая к снижению содержания всех клеток крови и гиперпигментации. Рис. 25.Схема темновой репарации молекулы ДНК: 1 - поврежденная молекула ДНК; 2 - эндонуклеаза разрывает поврежденную цепь ДНК; 3 - экзонуклеаза "вырезает" поврежденный участок; 4 - ДНК-полимераза синтезирует новый фрагмент ДНК; 5 - лигаза его "вшивает" 4.8 Антимутагены Мутационный процесс является источником изменений, приводящих к различным патологическим состояниям. Компенсационный принцип на современном этапе предполагает мероприятия по предотвращению генетических последствий загрязнения среды: предотвращение или снижение вероятности возникновения мутаций и устранение возникших в ДНК изменений путем репарации наследственного аппарата методами генетической инженерии. В начале 50-х годов была обнаружена возможность замедления или ослабления темпов мутирования с помощью некоторых веществ. Такие вещества назвали антимутагенами, а сам процесс антимутагенезом. Выделено около 200 природных и синтетических соединений, обладающих антимутагенной активностью:
Установлено, что антимутагены достаточно эффективны для человека. Наша пища является одним из поставщиков натуральных генотоксичных продуктов. С пищей человек получает несколько граммов в день веществ, способных вызвать генетические нарушения. Это в десять тысяч раз больше остатков синтетических пестицидов, содержащихся в различных продуктах. Такие количества мутагенов должны вызывать существенные поражения в наследственных структурах человека. Но этого не происходит, так как наряду с мутагенами пища содержит вещества, которые нейтрализуют их эффект. Соотношение тех и других веществ в различных продуктах питания неодинаково. Некоторые виды бобов, люпин, неочищенное хлопковое масло, черный перец, определенные виды съедобных грибов содержат больше мутагенов. Обнаружено, что потребление в пищу мяса животных, питавшихся растениями, поглотившими мутагенные вещества из окружающей среды, повышает мутационный уровень у человека. В 80-х годах был описан случай появления врожденных дефектов в одном хозяйстве у новорожденного ребенка, выводка щенят и козлят. Оказалось, что в период беременности женщина и собака употребляли молоко, полученное от домашних коз, которых кормили люпином. Генетический аппарат коз был непосредственно поражен генотоксическими компонентами люпина, а человека и собаки - через компоненты молока. Соотношение антимутагенов и мутагенов в продуктах зависит от сроков их хранения и консервирования, а также от способа их приготовления. Например, повреждающие ДНК-продукты образуются в гренках, мясе, рыбе при их интенсивном нагревании, т.к. жир в процессе кулинарной обработки окисляется с образованием множества токсических продуктов. Рационы традиционного питания не всегда отвечают демографическим (возрастная структура населения) и экологическим условиям. Защита наследственного аппарата от воздействия средовых токсинов предполагает увеличение в пользу антимутагенов баланса веществ в продуктах. Одна из наиболее изученных групп пищевых антимутагенов - витамины и провитамины. Это: ретинол (витамин А и его синтетические аналоги - ретиноиды) и его провитамин каротин, токоферол (витамин Е), фолиевая кислота (витамин В4), аскорбиновая кислота (витамин С), филлохинон (витамин К). Антимутагенные свойства витамина Е (а-токоферола) впервые были описаны в 70-х годах. Он содержится в растительных продуктах: маслах, семенах и проростках злаковых (облепихе, послене, семенах шиповника). Другой распространенный антимутаген – аскорбиновая кислота (витамин С). Для поддержания оптимального состояния здоровья ежедневная потребность в витамине С у разных людей варьируется в пределах от 250 мг до нескольких граммов. Аскорбиновая кислота активный антиканцероген. Отмечается высокое содержание аскорбиновой кислоты в зеленом и красном перце, черной смородине, петрушке, апельсиновом, лимонном, грейпфрутовом соках, помидорах, огурцах, клюкве, крыжовнике и др. Витамин В4 (фолиевая кислота) служит барьером для вирусов, провоцирующих раковые заболевания. Ежедневная доза витамина (около 800 мкг) значительно сокращает и даже прекращает развитие предраковых состояний у женщин, принимающих пероральные противозачаточные средства. Антимутагенами могут быть не только компоненты, но и пищевые продукты в целом. Экстракты крестоцветных растений, среди которых наиболее активны различные виды капусты, уменьшали уровень мутаций, более чем в 8-10 раз. Экспериментально определено, что токсический эффект снижается под действием экстракта яблок – в 8 раз, мятного листа - в 11 раз, зеленого перца – в 10, баклажана – в 7, винограда – в 4 раза. Рекордсменом оказался лопушник большой (семейство сложноцветных) - более чем в 20 раз. Среди лекарственных трав отмечают антимутагенное действие зверобоя. Правильное питание является одним из путей предотвращения действия генотоксических факторов среды. Экспертная группа Международной комиссии по защите окружающей среды от мутагенов и канцерогенов отмечает достоверное снижение риска у лиц, придерживающихся диеты, богатой хлебными злаками, овощами и фруктами при снижении потребления продуктов, богатых жирами, и алкоголя. Вопросы для аудиторного контроля по теме практической работы №1
Нервные клетки называют нейронами. В этой статье мы рассмотрим строение нейрона. Нейроны состоят: -из «стандартных» элементов присущих и другим клеткам нашего тела - (органелл), -из специфичных элементов и органелл, делающих их внешне и функционально непохожими на остальные клетки. В общем виде строение нейрона можно описать, пользуясь рисунком: 1 – дендриты, 2 – нейрит (аксон), 3 – концевые ответвления нейрита (аксона) - терминали. Каждая нервная клетка нейрон имеет тело (перикарион или сому) и отростки. Один из отростков – маловетвящийся и обычно самый длинный – аксон (нейрит). Дру гие, короткие, имеющие много ответвлений – дендриты, отличаются разветвленным (подобно корням дерева) строением. Именно наличие таких внешних признаков как отростки отличает нервные клетки от других клеток. С другими клетками человеческого организма нейроны роднит наличие клеточных органелл, таких как клеточное ядро, ядрышко, митохондрии, лизосомы, рибосомы, цитоплазма…и. т. п. Снаружи нейрон покрывает оболочка – плазматическая мембрана, или плазмалемма, а внутри помимо типичных клеточных органелл он имеет специфичные клеточные органеллы, такие как нейрофибриллы, опорные нити, тигроидное вещество - вещество Ниссля (см. рисунок): 1 — ядро; 2 — ядрышко; 3 — сателлит яд рышка; 4 — дендрит; 5 — эндоплазматическая сеть с гранулами РНК (вещество Ниссля); 6 — синапс; 7 — ножка астроцита; 8 — гра нулы ДНК; 9 — липофусцин; 10 — аппарат Гольджи; 11 — митохондрия; 12 — аксонный холмик; 13 — нейрофибриллы; 14 — аксон; 15 — миелиновая оболочка; 16 — перехват Ранвье; 17 — ядро леммоцита; 18 — леммоцит в области нервно-мышечного синапса; 19 — ядро мышечной клетки; 20 — нервно-мышеч ное соединение; 21 — мышца. Наличие у нейрона специфичных конструктивных элементов придает ему специфичные функциональные возможности. Основной функцией нейрона является генерирование и проведение нервных импульсов. Причем нейрон способен проводить нервный импульс лишь в одном направлении - от дендрита к терминали аксона. Иными словами нейрон способен как воспринимать раздражение и возбуждаться, так и передавать возбуждение в форме нервного импульса соседним нейронам. Последнее говорит о том, что строение нейрона позволяет ему создавать общую нейронную сеть с другими нейронами или так называемые рефлекторные дуги, проводящие нервные импульсы в определенном направлении. Каждый нейрон является патологической функциональной единицей. Это значит что при достаточно серьезном повреждении цитоплазмы нейрона или его отростков, он погибает. Погибшие нейроны не возмещаются, поэтому говорят о том, что «нервные клетки не восстанавливаются». Однако при повреждении отростков нейрона, возможно их последующее восстановление. Таким образом, наиболее характерной функциональной чертой нейронов является наличие у них отростков, с помощью которых они получают сенсорную информацию с периферии и генерируют и проводят управляющие нервные импульсы. Нервные отростки позволяют нейронам образовывать нейронные сети (посредством синаптических контактов), а так же соединяться с иннервируемыми структурами – мышечными волокнами, кровеносными сосудами и т. п. Длина отростков нейронов варьируется от назначения образуемой ими рефлекторной дуги и в отдельных случаях может составлять до 1 метра. А размер тела нейрона в зависимости от его назначения может различаться от 4 до 100 мкм в диаметре. Ученые полагают, что лишь в одном головном мозге человека содержится порядка 10 млрд нейронов. В связи с функциональным разнообразием нейронов в анатомии нервной системы присутствует классификация нейронов по видам. По форме тел нейроны делят: -звездчатые, -корзинчатые, -пирамидные и пр. По функции нейронов их подразделяют на следующие виды: -сенсорные, -моторные, -ассоциативные. Особенно значимой для неспециалиста может оказаться классификация нейронов по типу вырабатываемого ими нейромедиатора, то есть химического вещества, посредством которого осуществляется передача нервного импульса. По типу нейромедиатора нейроны подразделяют на следующие виды: -серотонинергические (нейромедиатор серотонин), -дофаминергические (нейромедиатор дофамин) -холинсргические, и т. д. -адреналинергические, -ГАМКергические, По длине форме и расположению отростков аксонов нейроны делят: -клетки с длинными аксонами, выходящими за пределы конкретного скопления клеток (ядра), называют клетками Гольджи I, -клетки с коротки ми аксонами - клетками Гольджи II; -биполярные нейроны, имеющие один дендрит и один аксон; -мультиполярные нейроны, имеющие множество отростков. Именно мультиполярные нейроны присутствуют в нашем организме в подавляющем большинстве, тогда как истинных однополярных (имеющих один отросток) нейронов в организме человека нет. Именно благодаря мультиполярности нейронов, возможно образование ими нейронных сетей, что создает условия для восприятия каждым нейроном различной информации. А это уже повышает эффективность нервной деятельности. Рис. Виды нейронов (из книги Никифорова и Гусева «Общая неврология): 1 — периферический чувствительный нейрон; 2 — короткоаксонный нейрон типа Гольджи II; 3 — периферический мотонейрон; 4 — обонятельный нейрон; 5 — клетка зер нистого слоя мозжечка; 6 — нейрон симпатического узла; 7 — клетка Пуркинье; 8 — пирамидная клетка Беца. Стрелки показывают направление перемещающихся по клетке нервных импульсов. Подводя итоги, отметим для себя основное, что необходимо знать неспециалисту о нервных клетках нейронах: 1.Генерирует и проводит управляющие нервные импульсы; 2.Син тезирует белки, липиды, углеводы, 3.Синтезирует нейромедиаторы или как их иначе называют нейротрансмиттеры; 4.Некоторые нейроны, в частности нейроны гипоталамуса, производят гормоны, например вазопрессин (антидиуретический горомон) или окситоцин, а так же рилизинг-факторы. 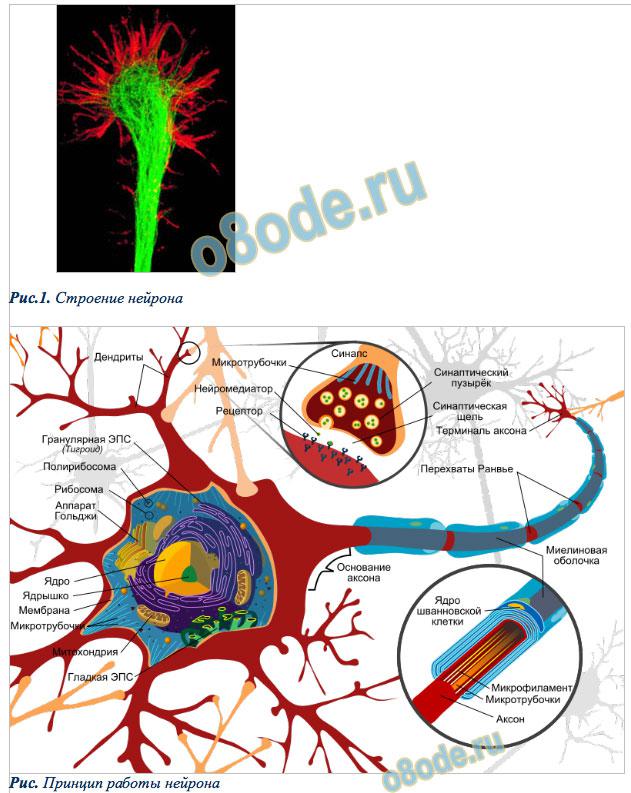 |
