курсовой проект. Литература 41 Введение
 Скачать 224.21 Kb. Скачать 224.21 Kb.
|
Физико-химические основы процесса.Перевод свободного азота воздуха в связанное состояние осуществляется главным образом путём синтеза аммиака: N2 + 3H2 ↔ 2NH3 + 92 кДж По принципу Ле-Шателье сдвигу равновесия такой реакции вправо, т. е. в сторону образования аммиака, способствует повышение давления и понижение температуры. Однако даже при 7000С скорость реакции настолько мала (и следовательно, равновесие устанавливается так медленно), что не может быть и речи о её практическом использовании. Напротив, при более высоких температурах, когда равновесное состояние устанавливается быстро, ничтожно малым становится содержание аммиака в системе. Таким образом, техническое проведение рассматриваемого процесса оказывается как будто невозможным, так как, ускоряя достижение равновесия при помощи нагревания, мы одновременно смещаем его положение в невыгодную сторону. Существует, однако, средство ускорить достижение равновесного состояния без одновременного смещения равновесия. Таким часто помогающим средством является подходящий катализатор. Подходящим катализатором является металлическое железо (с примесями Al2O3 и К2О). Процесс обычно ведут при температуре 400-600 0С (на катализаторе) и давлениях 100-1000 атм. После выделения аммиака из газовой смеси последняя вновь вводится в цикл. В процессе катализа азото-водородная смесь переходит в аммиак лишь частично. Для рекуперации азото-водородной смеси из неё нужно выделить аммиак. По технологии ГИАПАМ-76 выделение аммиака из газовой смеси происходит в двух ступенях: охлаждение газовой смеси воздухом в аппарате воздушного охлаждения и жидким аммиаком в испарители жидкого аммиака. Содержание аммиака в газовой смеси в зависимости от температуры и давления можно определить по формуле: lg C NH3 4,1856 5,987879 1099,544 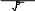 T Tгде Р – давление смеси, атм; Т – температура газовой смеси, К. Если свежая азото-водородная смесь вводится в цикл до колонны синтеза, то степень выделения аммиака из газа можно определить по формуле: 2 х Рх1 100 р х1 (Р р) где Р – общее давление в системе, атм; р – парциальное давление аммиака при данных условиях, атм; х1 – концентрация аммиака в газе, %. Если свежая азото-водородная смесь вводится в цикл после колонны синтеза, то формула принимает вид: 2 х Рх1 100 р х1 (Р р) Эти формулы показывают, что с повышением давления и понижением температуры степень конденсации аммиака возрастает, а количество его в циркуляционном газе падает. Степень выделения аммиака из газа в значительной степени влияет на производительность установки, так как количество образовавшегося в колонне синтеза аммиака соответствует разности его содержания в выходящем из колонны и поступающем в колонну газе. Процессы конденсации аммиака характеризуются резким снижением упругости газообразного аммиака и превращением его в жидкость. |
