реферат. масс-спектрометры. Методы определения состава газовой фазы массспектрометрия
 Скачать 1.31 Mb. Скачать 1.31 Mb.
|
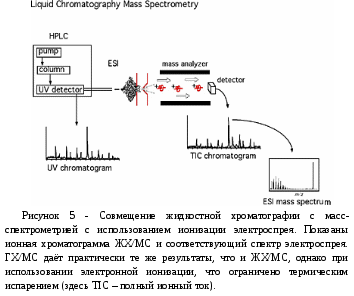
Реферат по дисциплине Инженерное обеспечение производства сварных конструкций Тема «Методы определения состава газовой фазы: масс-спектрометрия» Выполнил: Проверил: г. Пермь 2021 ОглавлениеВВЕДЕНИЕ 3 1.Устройство и принцип работы масс-спектрометров 5 2. Определение состава газовой фазы методом газовой хроматографии 16 В то же время масс-спектрометрия - один из самых дорогих методов анализа, наряду с ЯМР-спектрометрией, уступающий только структурному рентгеноструктурному анализу. В основном это связано с необходимостью создания высокого вакуума внутри устройства и связанными с этим трудностями при выборе оборудования. 20 Список использованной литературы 21 Электронные ресурсы: 21 ВВЕДЕНИЕ Масс-спектрометрия является мощным аналитическим методом, используемым для количественной оценки известных материалов, выявления неизвестных соединений в образце, а также для выяснения структуры и химических свойств различных молекул. Полный процесс включает в себя преобразование образца в газообразные ионы, с или без фрагментации, которые затем характеризуются их массы для зарядки отношения (м/з) и относительного изобилия. Этот метод в основном изучает влияние ионизирующего энергии на молекулы. Это зависит от химических реакций в газовой фазе, в которой молекулы образца потребляются во время формирования ионных и нейтральных видов. Масс-спектрометр генерирует несколько ионов из проб, которые исследуются, затем отделяет их в зависимости от их специфического соотношения массы к заряду (м/z), а затем записывает относительное процентное содержание каждого типа ионов. Первым шагом в масс-спектрометрическом анализе соединений является производство ионов газовой фазы соединения, в основном путем ионизации электронов. Этот молекулярный ион подвергается фрагментации. Каждый ион первичного продукта, полученный из молекулярного иона, в свою очередь, подвергается фрагментации и так далее. Ионы разделены в масс-спектрометре в соответствии с их соотношением массы к заряду и обнаруживаются пропорционально их наличию. Таким образом, вырабатывается массовый спектр молекулы. Он отображает результат в виде участка ионового изобилия по сравнению с соотношением массы к заряду. Ионы предоставляют информацию о природе и структуре их молекулы-предшественника. В спектре чистого соединения молекулярный ион, если он присутствует, оказывается на самом высоком значении м/з (после ионов, содержащих более тяжелые изотопы) и дает молекулярную массу соединения. Устройство и принцип работы масс-спектрометров Масс-спектрометры состоят из четырех основных частей; система обработки для внедрения неизвестного образца в оборудование; ионный источник, в котором производится пучок частиц, характерный для образца; анализатор, который отделяет частицы в зависимости от массы; и детектор, в котором собираются и характеризуются разделенные ионные компоненты. Спектрометр требует столкновения свободный путь для ионов и, следовательно, работает в вакууме или в приближенных к вакууму условиях. Система взвеси образца предназначена для минимальной потери вакуума. Источник ионов создает из образца фрагменты ионов. Существует два вида ионных источников; газо-фазных источников и источников излучения. Газо-фазные источники: образец сначала нагревается до ионизации. Переход в газовую фазу компонентов происходит различными способами. Образец испаряется за пределами источника ионов. Примерами методов ионизации являются химическая ионизация, ионизация электронов и пр. 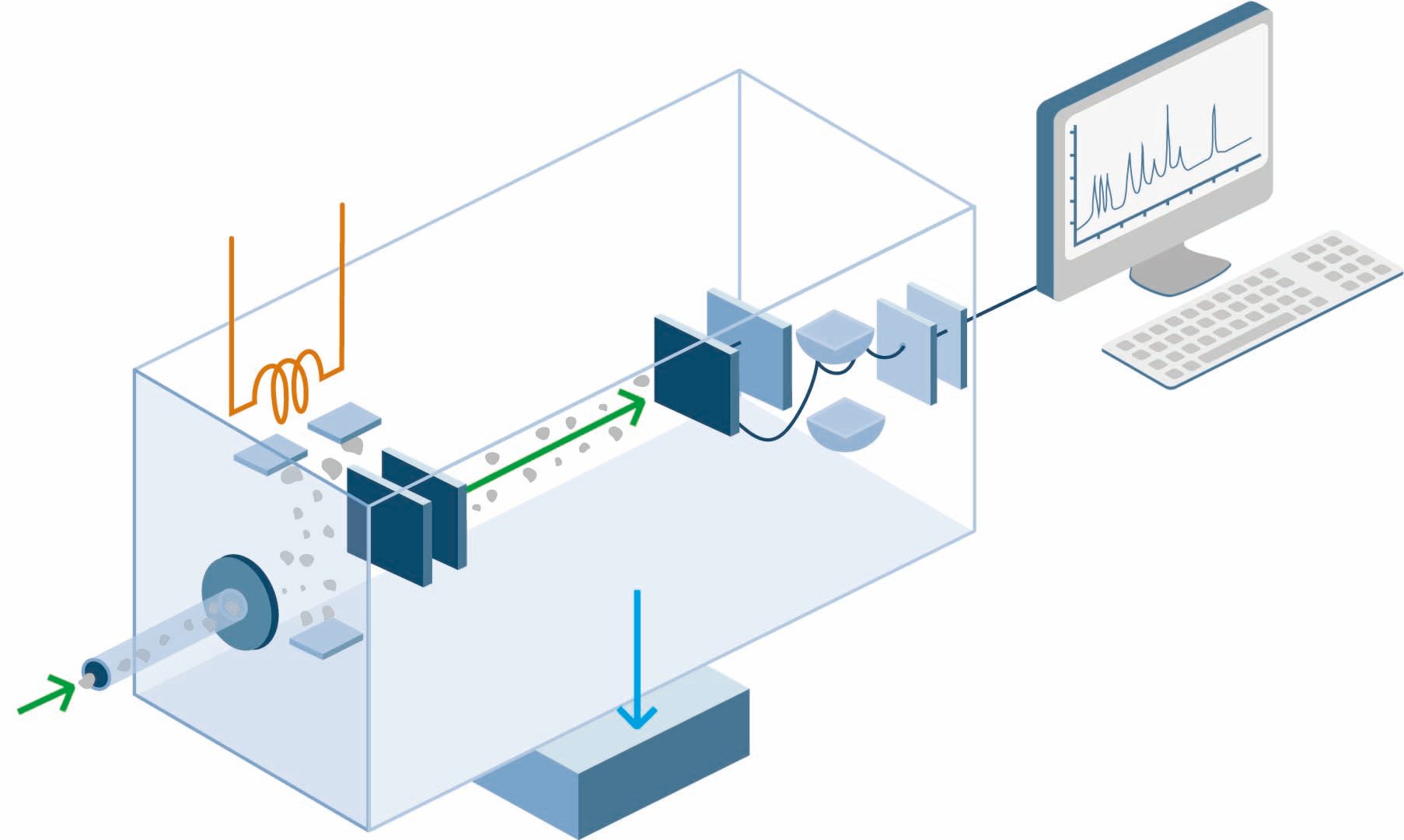 Рисунок 1. Устройство масс-спектрометра Масс-спектрометр определяет массу молекулы, измеряя отношение массы к заряду (m / z) ее иона. Ионы образуются, когда нейтральные частицы теряют или набирают заряд. После образования ионы электростатически отправляются в масс-анализатор, где они разделяются в соответствии с их m / z и, наконец, обнаруживаются. Результатом ионизации молекул, разделения ионов и обнаружения ионов является спектр, который можно использовать для определения молекулярной массы и даже некоторой информации о структуре вещества. Можно провести аналогию между масс-спектрометром и призмой, как показано на рис. 2. В призме свет делится на составляющие длины волны, которые затем обнаруживаются оптическим приемником. Аналогичным образом, в масс-спектрометре генерируемые ионы разделяются в масс-анализаторе, подсчитываются и определяются в детекторе ионов (таком как электронный умножитель). 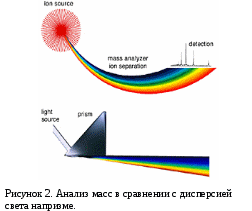 Принципиальное устройство масс-спектрометра Большинство масс-спектрометров стандартно состоят из четырех основных компонентов (рис. 3): системы ввода пробы, ионизационного устройства, масс-анализатора и ионного детектора. В некоторых приборах сочетаются инжекция пробы и ионизация, в других - масс-анализатор и детектор. Однако все молекулы в образце обрабатываются одинаково, независимо от конфигурации прибора. Частицы пробы вводятся через впускную систему. При входе в устройство молекулы преобразуются в ионы в устройстве ионизации, а затем электростатически переносятся на масс-анализатор. Затем ионы разделяются в соответствии с их m / z. Детектор преобразует энергию ионов в электрические сигналы, которые затем отправляются на компьютер.  Способы ввода образца Ввод образца был одной из первых проблем масс-спектрометрии. Для анализа массы образца, который изначально находится при атмосферном давлении (760 Торр), его необходимо ввести в прибор так, чтобы вакуум внутри последнего оставался практически неизменным ( |
| Механизм ионизации | Преимущества | Недостатки |
| Протонирование (положительные ионы) | многие соединения присоединяют протон с получением заряда многие способы ионизации, такие, как ESI, APCI, FAB, CI и MALDI производят такие частицы | многие соединения нестабильны в протонированной форме (например, углеводы) или с трудом присоединяют протон (например, углеводороды) |
| Катионизация (положительные ионы) | многие соединения присоединяют катион, такой как Na+ или K+ с получением заряда многие способы ионизации, такие, как ESI, APCI, FAB и MALDI производят такие частицы | опыты тандемной масс-спектрометрии на катионизированных молекулах часто дают очень ограниченную информацию по фрагментации |
| Депротонирование (отрицательные ионы) | многие полезные вещества в какой-то мере являются кислотами многие способы ионизации, такие, как ESI, APCI, FAB и MALDI производят такие частицы | применимо только для специфических соединений |
| Перенос заряженных молекул в газовую фазу (положительные и отрицательные ионы) | полезно для соединений, которые уже заряжены многие способы ионизации, такие, как ESI, APCI, FAB и MALDI производят такие частицы | применимо только для уже заряженных частиц |
| Отрыв электрона (положительные ионы) | наблюдается при электронной ионизации и даёт информацию не только о молекулярной массе, но и информацию о фрагментарных ионах | часто производит слишком сильную фрагментацию может быть непонятно, является ли ион с наибольшей массой молекулярным ионом или же фрагментом |
| Захват электрона (отрицательные ионы) | наблюдается при электронной ионизации и даёт информацию не только о молекулярной массе, но и информацию о фрагментарных ионах | часто производит слишком сильную фрагментацию может быть непонятно, является ли ион с наибольшей массой молекулярным ионом или же фрагментом |
Способы ионизации
Ионизация выбиванием электрона (ЭУ)
M + e-(70eV) --> M+ + 2e-
Метод ионизации (ЭУ) подходит для нетермолабильных соединений. Молекулы образца в парообразном состоянии бомбардируются быстро движущимися электронами, обычно с энергией 70 эВ. Это приводит к образованию ионов. Один электрон с самой высокой орбитальной энергией смещается, и, как следствие, образуются молекулярные ионы. Некоторые из этих молекулярных ионов разлагаются, и образуются фрагментарные ионы. Фрагментация данного иона происходит из-за избытка энергии, необходимой для ионизации. Фрагмент ионов может быть нечетным электроном или четным электроном. Молекулярные ионы, образующиеся при ионизации электронным ударом, являются нечетными электронными ионами. Ионы нечетных электронных фрагментов образуются прямым расщеплением (например, прямым расщеплением связи С-С). Даже ионы электронных фрагментов часто образуются путем перегруппировки (например, перенос протонов). Образец может быть введен в источник ЭУ с помощью устройства газовой хроматографии, например, в случае смесей, или непосредственно с помощью устройства для зондирования твердых частиц. Количество, необходимое для эксперимента, обычно меньше микрограмма материала.
Масс-спектры ЭУ в большинстве случаев содержат интенсивные пики ионов фрагментов и гораздо менее интенсивные пики молекулярных ионов. Когда пик молекулярных ионов не наблюдается в масс-спектре, для получения информации о молекулярных ионах можно использовать химическую ионизацию. Одним из полезных правил для определения того, является ли ион молекулярным ионом, является правило азота.
Правило азота: Как указано выше, молекулярные ионы, образующиеся при ионизации ЭУ, являются ионами нечетных электронов. Если их наблюдаемое отношение массы к заряду нечетно, исследуемая молекула содержит нечетное число атомов азота. Если отношение массы к заряду является четным числом, эта молекула не содержит атомов азота или даже атомов азота.
Химическая ионизация
Для химиков-органиков химическая ионизация (ХИ) является особенно полезным методом, когда в массовом спектре ХИ не наблюдается молекулярного иона, а также в случае подтверждения отношения массы к заряду молекулярного иона. Метод химической ионизации использует практически то же устройство источника ионов, что и при электронном ударе, за исключением того, что CI использует плотный источник ионов и газ-реагент. Газообразный реагент (например, аммиак) сначала подвергается электронному воздействию. Ионы образца образуются в результате взаимодействия ионов газа реагента и молекул образца. Это явление называется ионно-молекулярными реакциями. Молекулы газа-реагента присутствуют в соотношении около 100:1 по отношению к молекулам образца. В процессе КИ образуются положительные и отрицательные ионы. В зависимости от настройки прибора (напряжения источника, детектора и т. Д.) регистрируются только положительные ионы или только отрицательные ионы.
В ХИ реакции молекул ионов происходят между ионизированными молекулами газа реагента (Г) и летучими нейтральными молекулами (M) для получения ионов. Часто наблюдаются псевдомолекулярные ионы MH+ (режим положительных ионов) или [M-H]-(режим отрицательных ионов). В отличие от молекулярных ионов, полученных методом ЭУ, обнаружение MH+ и [M-H]- происходит с высоким выходом и наблюдается меньшее количество фрагментарных ионов.
Режим положительных ионов:
ГH+ + M -- > MH+ + Г
Режим отрицательных ионов:
[Г-H]- + M -- > [M-H]- + Г
Эти простые реакции переноса протонов являются истинными газофазными кислотно-щелочными процессами в смысле Бронстеда-Лоури. "Плотный" источник ионов (давление = 0,1-2 торр) используется для максимизации столкновений, что приводит к повышению чувствительности. Чтобы эти реакции молекул ионов происходили, они должны быть экзотермическими. Перенос протонов - один из простых процессов, наблюдаемых в положительных КИ:
RH+ + M -- > MH+ + R
Одним из решающих параметров в этой реакции является сродство к протону. Для протекания реакции сродство молекулы М к протону должно быть выше, чем у молекулы газа. Основными газами-реагентами, используемыми в КИ, являются: Аммиак, метан и изобутан. Преобладающие образующиеся ионы реагента приведены в механизмах, показанных ниже. Выбор газа-реагента влияет на степень фрагментации квазимолекулярного иона.
Метан (химическая ионизация положительных ионов):
CH4 + e -- > CH4+ + 2e -- > CH3+ + H.
СН4+ + CH4 -- > CH5+ +CH3.
СН4+ + CH4 -- > C2H5+ + H2 + H.
Изобутан (химическая ионизация положительных ионов):
i-C4H10 + e --> i-C4H10+. + 2e
i-C4H10+ + i-C4H10 -- > i-C4H9+ + C4H9 +H2
Аммиак (химическая ионизация положительных ионов):
NH3 + e - - - - - > NH3+ + 2e
NH3+ + NH3 - - - - - - > NH4+ + NH2.
NH4+ + NH3 --------->N2H7+
При химической ионизации в режиме положительных ионов метана соответствующие пики образца наблюдаются в MH+, [M+CH5]+ и [M+C2H5]+; но в основном MH+. Это соответствует массам M+1, M+29 и M+41.
При химической ионизации в режиме положительных ионов изобутана основным наблюдаемым пиком является MH+. При химической ионизации в режиме положительных ионов аммиака основными наблюдаемыми пиками являются MH+ и [M+NH4]+. Если присутствует более одного сайта протонирования, могут наблюдаться дополнительные NH3, соответствующие [M+NH3+NH4]+. Это соответствует массам M+1, M+18 и M+35.
В некоторых случаях могут наблюдаться протонированные димеры или другие аддукты; потеря H2O с последующим протонированием или образованием ионов аддукта наблюдается для некоторых классов соединений. Если спектр, который вы наблюдаете, кажется, не показывает правильных ионов аддукта или показывает обширную фрагментацию, будьте осторожны, когда вы пытаетесь интерпретировать результаты. В литературе имеется множество данных, обсуждающих механизмы химической ионизации, применимые к конкретным классам соединений.
Выбор используемого газа реагента определяется двумя факторами:
Сродство к протону PA
Передача энергии
NH3 (аммиак) является наиболее используемым газом-реагентом в CI из-за низкой передачи энергии NH4+ по сравнению, например, с CH5+. При использовании NH3 в качестве реагентного газа обычно наблюдаются MH+ и MNH4+ (разница в 17 единиц массы).
2. Определение состава газовой фазы методом газовой хроматографии
Газовая хроматография - масс-спектрометрия является общей комбинацией для специфического обнаружения и идентификации химических веществ. Техника газовой хроматографии используется для первоначального разделения компонентов образца, которые затем вводятся в масс-спектрометр для сортировки в соответствии с их соотношением массы к заряду. Анализ широко используется в фармацевтической и пищевой промышленности, но также используется для обнаружения неизвестных образцов, например, экологического анализа, судебно-медицинской экспертизы, обнаружения пожаров и взрывчатых веществ.

Рисунок 6. Устройство газового хроматографа
Метод анализа смесей газов и летучих веществ. Разделение основано на различии адсорбции на поверхности твердого носителя (адсорбента). Адсорбция может быть вызвана неспецифическим (ориентационным, индуктивным и дисперсионным) и специфическим (комплексообразование или образование водородной связи) взаимодействиями и зависит от природы адсорбента и сорбата.
В качестве адсорбентов используются пористые носители, которые являются химически, физически и термически стабильными; однородная поверхность, равномерное распределение пор по размеру и известная адсорбционная активность. Адсорбционная активность зависит от удельной поверхности (определяемой геометрической структурой носителя) и от удельной поверхностной энергии (определяемой химической структурой поверхности). Преимуществами адсорбентов как стационарных фаз являются способность выдерживать высокие температуры, отсутствие фонового сигнала при работе с ионизационными детекторами и высокая селективность. Адсорбенты делятся на неорганические, полимерные (органические) и модифицированные.
Среди неорганических адсорбентов особое место занимают сорбенты на основе углеродных материалов. Это неполярные сорбенты, для которых геометрические параметры поверхности играют особую роль в процессе разделения. Самая интересная особенность этих материалов - способность разделять структурные изомеры.
Широко используются полярные неорганические сорбенты на основе диоксида кремния. Сорбенты используются для отделения легких углеводородов. Наиболее разнообразны полимерные сорбенты на основе пористых полимеров стирола, дивинилбензола и дивинилбензола. Их можно синтезировать с желаемыми свойствами и очень чистой поверхностью. Это гидрофобные сорбенты, которые слабо удерживают полярные молекулы, содержащие гидроксиаминовые группы. Основная область применения полимерных сорбентов - разделение полярных и химически активных газов, а также высокополярных органических соединений; определение воды в органических растворителях и летучих органических загрязнителей в воде.
Масс-спектрометрия (МС) использует движение ионов в электрических и магнитных полях для их сортировки в соответствии с их соотношением массы к заряду. Таким образом, MS является аналитическим методом, с помощью которого химические вещества идентифицируются путем сортировки газовых ионов в электрических и магнитных полях. Инструменты, используемые в этих исследованиях, работают по принципу, что движущиеся ионы могут отклоняться электрическими и магнитными полями. Устройство, которое выполняет эту операцию и использует электрические средства для обнаружения отсортированных ионов, называется масс-спектрометром.
MS предоставляет качественную и количественную информацию об атомном и молекулярном составе неорганических и органических материалов.
ЗАКЛЮЧЕНИЕ
Масс-спектрометрия становится важным методом анализа биологических и небиологических макромолекул. Это один из самых чувствительных и точных методов, способный обнаруживать только сотни частиц, уступающий только методам радиационного анализа. Разрешение некоторых методов достигает 30 000, что означает точность в несколько десятков ppm. Эта точность позволяет проводить изотопный анализ макромолекул, таких как белки, а также определять дефект массы и вычислять общую формулу легких молекул и даже белков, основываясь исключительно на данных молекулярной массы и распределения изотопов.
Фрагментированная информация, особенно при использовании тандемной масс-спектрометрии, позволяет определить структуру молекулы, а также в ограниченном масштабе механизмы газофазных реакций и реакционные центры исследуемых молекул.
В то же время масс-спектрометрия - один из самых дорогих методов анализа, наряду с ЯМР-спектрометрией, уступающий только структурному рентгеноструктурному анализу. В основном это связано с необходимостью создания высокого вакуума внутри устройства и связанными с этим трудностями при выборе оборудования.
Список использованной литературы
Dole M, Mack LL, Hines RL, Mobley RC, Ferguson LD, Alice MB. Molecular beams of macroions. Journal of Chemical Physics. 1968, 49:5, 2240.
Whitehouse CM, Dreyer RN, Yanashita M, Fenn JB. Electrospray interface for liquid chromatographs and mass spectrometers. Anal. Chem. 1985, 57, 675-679.
Tanaka K, Waki H, Ido Y, Akita S, Yoshida Y, Yoshida T. Protein and polymer analysis up to m/z 100,000 by laser ionization time-of-flight mass spectrometry. Rapid Commun. Mass Spectrom. 1988, 2, 151.
Karas M & Hillenkamp F. Laser desorption ionization of proteins with molecular mass exceeding 10,000 Daltons. Anal. Chem. 1988, 60, 2299.
Bruins AP. Mechanistic aspects of electrospray ionization. J. Chromatogr. A, 1998, 795, 345-357.
McLafferty FW & Turecek F. Interpretation of Mass Spectra. 4th ed. Mill Valley, Calif. : University Science Books, 1993.
Cole R (Editor). Electrospray Ionization Mass Spectrometry: Fundamentals, Instrumentation, and Applications. New York: Wiley and Sons, 1997.
Cole RB. Some tenets pertaining to electrospray ionization mass spectrometry. J. Mass Spectrom. 2000, 35, 763-772.
Электронные ресурсы:
http://www.spectromass.ru/stati/metod-mass-spektrometricheskogo-issledovaniya-veshhestva/
https://mvdrb.ru/mass-spektrometriya-metody-ionizacii/
https://labinstruments.ru/stati/mass-spektrometriya#::text=Масс-спектрометрия%20—%20один%20из%20точнейших,азота%2C%20фосгена%20и%20углекислого%20газа