Горение 2. Курсовая работа Теория горения и взрыва++. Методические указания к курсовой работе Пермь ипц ПрокростЪ 2023 удк 621 148 ббк 79. 3 Рецензенты
 Скачать 0.58 Mb. Скачать 0.58 Mb.
|
3.2 Методические указания по расчету теплоты сгорания веществЦель работы: Усвоить основные понятия энергетического баланса процессов горения. Научиться делать расчет теплоты сгорания для разного типа горючего вещества (индивидуальные вещества, сложные вещества, газы) Расчетные формулыПри расчетах теплового баланса на пожаре определяют, как правило, низшую теплоту сгорания (таблица 3.1): QB-QH=QИС, (3.1) где QB - высшая теплота сгорания; QH - низшая теплота сгорания; QИС - теплота испарения воды, выделяющейся при сгорании вещества. Таблица 3.1 – Расчет теплоты сгорания
где 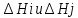 - соответственно теплоты образования одного кмоля i-го конечного продукта горения и - соответственно теплоты образования одного кмоля i-го конечного продукта горения и 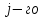 исходного вещества; исходного вещества;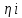 , , 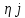 - соответственно количество кмолей - соответственно количество кмолей 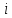 -го продукта реакции и -го продукта реакции и 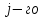 исходного вещества в уравнении реакции горения; исходного вещества в уравнении реакции горения;С,Н,S,W - соответственно содержание, % вес, углерода, серы, водорода, влаги в составе вещества; О - сумма кислорода и азота ,% вес QHi -низшая теплота сгорания 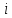 -го горючего компонента газовой смеси, кДж/моль; кДж/м3 -го горючего компонента газовой смеси, кДж/моль; кДж/м3φri- содержание 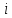 -го горючего компонента в газовой смеси ,% об. -го горючего компонента в газовой смеси ,% об.Расчет теплоты сгорания газовоздушных смесей проводят по формуле 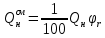 (3.5) (3.5)где Qсмн- теплота сгорания газовоздушной смеси, кДж/м3, кДж/м3; QH-низшая теплота сгорания горючего вещества, кДж/м3, кДж/м3; φri- концентрация горючего в смеси, % об. Удельная скорость (интенсивность) тепловыделения при горении: q=QH∙m, (3.6) где q- удельная интенсивность тепловыделения,кВт/м3; m- массовая скорость выгорания, кг/(м2∙с). Скорость тепловыделения при горении: Q= QH∙m, (3.7) где Q-интенсивность тепловыделения, кВт; F- площадь горения, м3. Примеры решения задачПример №1 Определить низшую теплоту сгорания уксусной кислоты, если теплота ее образования 485,6 кДж/моль; Решение: Для расчета по формуле (3.2) запишем уравнение горения уксусной кислоты в кислороде: 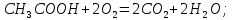 QH=(2∙396,9+2∙242,2-1∙485,6)=792,6 кДж/моль=792,6∙103 кДж/моль; Для расчета количества тепла, выделяющегося при горении 1кг горючего, необходимо полученную величину разделить на его молекулярную масса (64): QH=792,6∙103/64=12384кДж/кг. Пример № 2 Рассчитать низшую теплоту сгорания органической массы состава: С-62%, Н-8%, О-28%, S-2%. Решение: По формуле Д.И.Менделеева (2.3) QH=339,4∙62+1257∙8-108,9(28-2)-25,1∙9∙8=26460кДж/кг. Пример №3 Определить низшую теплоту сгорания газовой смеси, состоящей из СН4-40%, С4Н10-20%, О2-15%, Н2S-5%, NH3-10%, CO2-10% Решение: Для каждого горючего компонента смеси по формуле (3.2) находим теплоты сгорания (таблица 3.2) Таблица 3.2 – Теплота сгорания
По формуле (3.4) определим теплоту сгорания газовой смеси: QH=1/100∙(547.8∙40+2666,1∙20+338,6∙5+317,2∙10)103=1020∙103 кДж/кг. Для определения теплоты сгорания 1м3газовой смеси необходимо полученное значение разделить на объем, занимаемый 1 Кмолем газа при стандартных условиях (24,4м3): QH=1020∙10 3/24,4=41803 кДж/кг. Пример №4 Рассчитать теплоту сгорания 1м3 стехиометрической гексано-воздушной смеси. Решение: Находим стехиометрический состав горючей смеси по уравнению реакции горения: 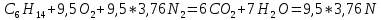 Весь объем вступивших в реакцию компонентов (1+9,5+9,5∙3,76) принимаем за 100%,а количество горючего (1 кмоль) будет соответствовать стехиометрической концентрации: 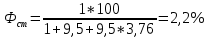 Теплоту сгорания 1м3 гексана определим по формуле (3.2) 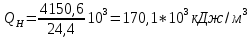 Теплоту сгорания 1 м3 стехиометрической гексано-воздушной смеси определим по формуле (3.5): 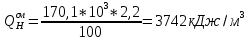 Пример №5 Определить интенсивность тепловыделения на пожаре органической массы (состав в примере 2), если скорость выгорания 0,015 кг/(м2/с), а площадь пожара 150 м2. Решение: согласно формуле (2.7): QH=26460,0∙0,15∙150=59,5∙103кВт |

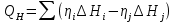 (3.2)
(3.2)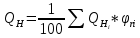 (3.4)
(3.4)