Методичка задачи по хроматографии. Методические указания к решению задач по хроматографии для студентов 4 курса химического факультета
 Скачать 79.96 Kb. Скачать 79.96 Kb.
|
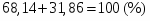 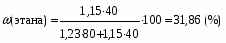 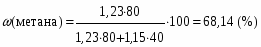 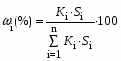  МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИ МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РОССИЙСКОЙ ФЕДЕРАЦИИФЕДЕРАЛЬНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ ВЫСШЕГО ПРОФЕССИОНАЛЬНОГО ОБРАЗОВАНИЯ Башкирский государственный университет МЕТОДИЧЕСКИЕ УКАЗАНИЯ к решению задач по хроматографии для студентов 4 курса химического факультета Уфа 2013 Печатается по решению кафедры аналитической химии (протокол № 18 от 4 апреля 2013 года) АННОТАЦИЯ Методические указания предназначены для самостоятельной работы по решению расчетных задач в хроматографии. Дается методика расчетов. Задачи охватывают все разделы курса «Хроматография», читаемого студентам химического факультета. Составители: к.х.н., ст.преп. Гуськов В.Ю., к.х.н., доцент Валинурова Э.Р., к.х.н., доцент Хатмуллина Р.М., д.х.н., профессор Кудашева Ф.Х. Введение Хроматография представляет собой самый распространённый метод химического анализа. Хроматографические и гибридные методы занимают лидирующие позиции в анализе органических соединений, и не имеют себе равных в аналитической химии сложных смесей токсичных веществ. Широкое применение хроматографии создаёт необходимость знания основ хроматографического метода любым дипломированным специалистом по химии. В рамках изучения дисциплины «Хроматография» студенты химического факультета должны освоить основные способы проведения качественного и количественного анализа, знать способы оценки эффективности применяемых для разделения хроматографических колонок, уметь пользоваться критериями разделения и индексами удерживания Ковача и правильно оценивать возможности детектора. Методические указания к решению задач по хроматографии охватывают все ключевые разделы хроматографической науки, и позволяют обучающемуся получить целостное представление о хроматографии и научиться решать аналитические задачи в её помощью. Задачи, представленные в настоящих методических указаниях, являются аналогами тех задач, которые даются на контрольных работах по курсу хроматографии. Параметры удерживания Примеры задач Задача 1. Была получена хроматограмма пропанаа на колонке с массой неподвижной фазы 3.829 г. Скорость газа-носителя, измеренная пенным расходометром, составила 60 мл/мин, скорость диаграммной ленты самописца 720 мм/час. Температура колонки 120 °С, температура окружающей среды 24 °С (парциальное давление паров воды при данной температуре составляет 23,1 мм.рт.ст.), атмосферное давление 762 мм.рт.ст. Расстояние от момента ввода пробы до выхода максимума пиков несорбирующегося компонента, и пропана составляет соответственно 0.8 и 3.4 мм. Найти значения удельных удерживаемых объёмов. Решение. Расчёт удельных удерживаемых объёмов производится по формуле: 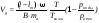 где l – расстояние от момента ввода пробы до максимума пика сорбата, мм; lm – расстояние от момента вводы пробы до максимума пика несорбирующегося компонента, мм; В – скорость диаграммной ленты самописца, мм/с; ω – скорость газа-носителя, мл/с; T – температура в термостате колонки, К; Ткомн – температура, при которой проводятся измерения скорости газа-носителя, К; рводы – давление паров воды при температуре измерения скорости газа-носителя, мм рт. ст.; pатм – атмосферное давление, мм рт. ст., ma – масса сорбента в колонке, г. Подставляя данные задачи в уравнение, получаем: 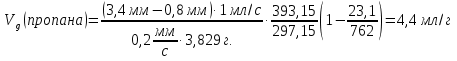 Ответ: 4,4 мл/г Задача 2. Удерживаемый объём несорбирующегося компонента составляет 5 мл. На данной колонке расстояние удерживания (lR) пропана при различных скоростях диаграммной ленты (q) составляет:
Погрешность определения lR составляет 1 мм. Другими погрешностями пренебречь. Определить, в каком случае возможен качественный анализ пропана. Решение: качественный анализ пропана возможен только при условии, что его удерживаемый объём на колонке отличается от удерживаемого объёма несорбирующегося компонента за пределами доверительного интервала. Если удерживаемый объём несорбирующегося компонента попадает в доверительный интервал, то удерживания искомого и несорбирующегося компонента будут различаться в пределах погрешности. Тогда искомый компонент не будет удерживаться на данной колонке и его качественный анализ будет невозможен. Рассмотрим влияние условий снятия хроматограмм: №1. Так как погрешность измерения lR составляет 1 мм, то lR будет меняться от 6 до 8. Нам нужно рассмотреть только нижнюю границу изменения lR, так как она может пересекаться с удерживанием несорбирующегося компонента. При lR=6 удерживаемый объём равен: 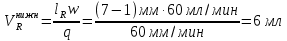 6 мл > 5 мл, следовательно, удерживаемый объём будет отличен от удерживаемого объёма несорбирующегося компонента, и для пропана будет возможно количественное определение. №2. Аналогично с №1: 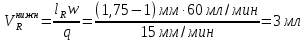 3 мл < 5 мл, следовательно, удерживаемый объём пропана, измеренный в данных условиях, будет в пределах ошибки равен удерживаемому объёму несорбирующегося компонента. Качественная идентификация невозможна. Ответ: в случае условий №1 качественная идентификация возможна; в случае условий №2 качественная идентификация невозможна. Задачи для самостоятельного решения Задача 3. Были получены хроматограммы этана, этилена и ацетилена на колонке с массой неподвижной фазы 4.267 г. Скорость газа-носителя, измеренная пенным расходометром, составила 30 мл/мин, скорость диаграммной ленты самописца 240 мм/час. Температура колонки 100 °С, температура окружающей среды 25 °С (парциальное давление паров воды при данной температуре составляет 24,5 мм.рт.ст.), атмосферное давление 758 мм.рт.ст. Расстояние от момента ввода пробы до выхода максимума пиков несорбирующегося компонента, этана, этилена и ацетилена составляет соответственно 1.2, 15.4, 13.9 и 17.2 мм. Найти значения удельных удерживаемых объёмов. Задача 4. Были получены хроматограммы пропана, н-бутана и бутена на колонке с массой неподвижной фазы 3.812 г. Скорость газа-носителя, измеренная пенным расходометром, составила 60 мл/мин, скорость диаграммной ленты самописца 60 мм/час. Температура колонки 120 °С, температура окружающей среды 24 °С (парциальное давление паров воды при данной температуре составляет 23,1 мм.рт.ст.), атмосферное давление 742 мм.рт.ст. Расстояние от момента ввода пробы до выхода максимума пиков несорбирующегося компонента, пропана, н-бутана и бутена составляет соответственно 2.4, 17.1, 32.1 и 29.7 мм. Найти значения удельных удерживаемых объёмов. Задача 5. Исправленное время удерживания о-ксилола при скорости газа-носителя 45 мл/мин составляет 12,9 с. На той же колонке расстояние от момента ввода пробы до выхода максимума пика п-ксилола равно 13 мм (расстояние удерживания несорбирующегося компонента 3 мм) на скорости диаграммной ленты 3 см/мин. Скорость газа-носителя составляла 30 мл/мин. Определить, какое вещество будет удерживаться сильнее. Задача 6. Исправленное время удерживания пиридина при скорости газа-носителя 60 мл/мин составляет 14,8 с. На той же колонке расстояние от момента ввода пробы до выхода максимума пика тиофена равно 11 мм (расстояние удерживания несорбирующегося компонента 2 мм) на скорости диаграммной ленты 1,5 см/мин. Скорость газа-носителя составляла 20 мл/мин. Определить, какое вещество будет удерживаться сильнее. Задача 7. Скорость потока несорбирующегося газа-носителя (аргона) 40 см3/мин. Время удерживания аргона 30 с. Время удерживания вещества Х – 4 мин. Вычислить удерживаемый объем и исправленный удерживаемый объем вещества Х. Задача 8. Расстояния, пройденные диаграммной лентой потенциометра-самописца от ввода пробы сивушного масла в хроматографическую колонку до появления максимумов хроматографических пиков №№1, 2 и 3, соответственно равны 2,16; 4,50 и 6,50 см. Скорость движения диаграммной ленты – 10 мм/мин. Времена удерживания (tR), установленные по препаратам спиртов квалификации «хроматографически чистые», в тех же условиях составляют:
Идентифицируйте спирты в сивушном масле. Задача 9. Удерживаемый объём несорбирующегося компонента составляет 5,5 мл. На данной колонке расстояние удерживания метана при различных скоростях газа-носителя (w) и диаграммной ленты (q) составляет:
Погрешность определения lR составляет 1 мм. Другими погрешностями пренебречь. Определить, в каком случае возможен качественный анализ. Задача 10. Удерживаемый объём несорбирующегося компонента составляет 3,8 мл. На данной колонке расстояние удерживания угарного газа при различных скоростях газа-носителя (w) и диаграммной ленты (q) составляет:
Погрешность определения lR составляет 0,5 мм. Другими погрешностями пренебречь. Определить, в каком случае возможен качественный анализ метана. Задача 11. Исправленный с учётом сжимаемости газа удерживаемый объём изооктана при скорости газа-носителя 30 мл/мин равен 110,4 мл. Расстояние от момента ввода пробы до выхода максимума пика составляет 21 мм, скорость диаграммной ленты 0,6 см/мин. Удерживаемый объём несорбирующегося газа-носителя составил 5 мл. Найти коэффициент Джеймса-Мартина. Задача 12. Исправленный удерживаемый объём н-нонана при скорости газа-носителя 45 мл/мин равен 118 мл. Расстояние от момента ввода пробы до выхода максимума пика составляет 36 мм, скорость диаграммной ленты 1,5 см/мин. Удерживаемый объём несорбирующегося газа-носителя составил 7 мл. Найти коэффициент Джеймса-Мартина. Задача 13. В гомологическом ряду н-алканов логарифм удерживаемого объёма зависит от количества атомов углерода (c) по следующему уравнению: lnVR=1,51*c+0,94. Скорость газа-носителя 45 мл/мин, время удерживания несорбирующегося компонента 2,3 с., коэффициент Джеймса-Мартина 1,021. Найти времена удерживания гексана и гептана. Задача 14. В гомологическом ряду н-спиртов логарифм удерживаемого объёма зависит от количества атомов углерода (c) по следующему уравнению: lnVR=1,19*c+0,78. Скорость газа-носителя 60 мл/мин, время удерживания несорбирующегося компонента 1,8 с., коэффициент Джеймса-Мартина 1,08. Найти времена удерживания н-бутанола и н-пентанола. Индексы Ковача Пример задачи Задача 15. Удерживаемые объёмы бутана, пентана и этанола соответственно равны 57, 152 и 78 мл. Рассчитать индекс Ковача для этанола. Решение. Расчёт индексов Ковача производится по формуле: 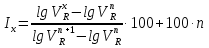 Тогда, подставляя параметры задачи в уравнение, получаем: 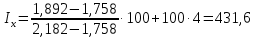 Ответ: 431,6 Задачи для самостоятельного решения Задача 16. Удерживаемые объёмы гептана, октана и бутилацетата соответственно равны 118, 204 и 173 мл. Рассчитать индекс Ковача для бутилацетата. Задача 17. На хроматограмме были обнаружены пики с временами удерживания 61.7, 66.3, 70.4, 73.8, 78.1, 84.3, 89.0, 93.7, 97.2 и 104.9 с. Пользуясь таблицей, проведите качественную идентификацию смеси. Времена удерживания пентана, гексана и гептана соответственно 55.4, 75.8 и 107.0 с.
Задача 18. Времена удерживания пентана, изо-бутанола и гексана соответственно равны 54, 67 и 89 с. Рассчитать индекс Ковача для изо-бутанола. Задача 19. На хроматограмме были обнаружены пики с временами удерживания 117.2, 124.8, 137.3, 142.9, 155.8, 162.5, 167.4, 178.0, 214.8 и 223.5 с. Пользуясь таблицей, проведите качественную идентификацию смеси. Времена удерживания гексана, гептана, октана и нонана соответственно 110.5, 145.4, 202.0 и 241.7 с.
Задача 20. При хроматографировании газа, содержащего вторичные амины, на хроматограмме получен пик с временем удерживания 381 с (жидкая неподвижная фаза сквалан, температура колонки 100 °С). В тех же условиях времена удерживания н-гептана и н-октана равны 348 и 372 с соответственно. В анализируемом газе могут находиться ди-изо-пропилаимн (индекс удерживания Ковача 644), ди-н-пропиламин (индекс удерживания Ковача 746), ди-втор-бутиламин (индекс удерживания Ковача 837). Какой амин содержится в анализируемой пробе? Задача 21. При разделении углеводородов в хроматографической колонке с жидкой неподвижной фазой (сквалан) при 80 °С индекс удерживания Ковача для 2-метилгексана равен 667. В тех же условиях времена удерживания н-гексана и н-гептана равны 143 и 285 с соответственно. Рассчитать время удерживания 2-метилгексана. Эффективность хроматографической колонки Пример задачи Задача 22. Расстояние от момента ввода пробы до выхода несорбирующегося компонента составляет 2,3 мм, до выхода 2-метилфенола 51 мм. Ширина пика 2-метилфенола у основания составляет 7 мм. Длина колонки 3 м. Вычислить высоту, эквивалентную теоретической тарелке. Решение: Найдём число теоретических тарелок колонки: 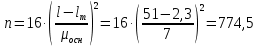 Найдём ВЭТТ: 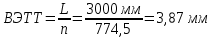 Ответ: 3,87 мм. Задачи для самостоятельного решения Задача 23. Расстояние от момента ввода пробы до выхода несорбирующегося компонента составляет 3 мм, до выхода бензола 26 мм, до выхода толуола 48 мм. Ширина пиков бензола и толуола у основания составляет соответственно 4 и 8 мм. Длина колонки 1,5 м. Вычислить высоту, эквивалентную теоретической тарелке. Задача 24. Расстояние от момента ввода пробы до выхода несорбирующегося компонента составляет 2,5 мм, до выхода гексана 38 мм, до выхода гептана 62 мм. Ширина пиков гексана и гептана у основания составляет соответственно 3 и 7 мм. Длина колонки 2,5 м. Вычислить высоту, эквивалентную теоретической тарелке. Задача 25. Время удерживания 2-метилгексана составляет 136 с. Ширина пика на половине высоты 6 мм. Найти время удерживания 3-метилгексана, если его ширина пика у основания равна 16 мм. Скорость диаграммной ленты 240 мм/ч. Задача 26. Удерживаемый объём 3-метилфенола равен 117 мл. Ширина пика у основания составила 36 с. Найти удерживаемый объём 2-метилфенола, если его ширина пика на половине высоты 8 мм. Скорость газа-носителя 30 мл/мин, скорость диаграммной ленты 3 см/мин. Задача № 27. При определении метана применена хроматографическая колонка с числом теоретических тарелок, равным 2000. Ширина основания хроматографического пика на диаграммной ленте составила 20 мм. Скорость диаграммной ленты хроматографа 600 мм/ч. Рассчитать время удерживания метана. Критерии разделения Пример задачи Задача 28. На хроматограмме пентана и гексана время удерживания соединений соответственно 37 и 54 с. Ширина пиков на половине высоты равнялась 4,7 с для пентана и 6,8 с для гексана. Рассчитать степень разделения компонентов К1. Решение: степень разделения рассчитывается по формуле: 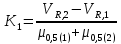 Подставляя в формулу данные из условия задачи, получаем: 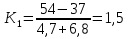 Ответ: степень разделения равна 1,5. Компоненты будут хорошо разделяться. Задачи для самостоятельного решения Задача 29. На хроматограмме 2-метилоктана и 2,3 – диметилгептана время удерживания соединений соответственно 37 и 34 с. Ширина пиков на половине высоты равнялась 3,2 мм для 2-метилоктана и 2,7 мм для 2,3-диметилгептана. Рассчитать степень разделения компонентов К1 если скорость диаграммной ленты 1,5 см/мин. Задача 30. На хроматограмме изопропилбензола и 1,2,3 – триметилбензола время удерживания соединений соответственно 112 и 84 с. Ширина пиков на половине высоты равнялась 2,1 мм для изопропилбензола и 2,3 мм для 1,2,3 – триметилбензола. Рассчитать степень разделения компонентов К1 если скорость диаграммной ленты 3 см/мин. Задача 31. На 1,5-метровой колонке с ВЭТТ = 3,4 мм предпринята попытка разделить этанол, ацетальдегид и пропанол-2. Времена удерживания компонентов смеси составляют соответственно 44, 56 и 48 с. Определить, какие из компонентов могут быть разделены на данной колонке. Задача 32. На хроматографической колонке с 2500 теоретических тарелок были разделены уксусная, щавелевая и валериановая кислоты. Времена удерживания компонентов смеси составляют соответственно 123, 138 и 194 с. Определить, какие из компонентов могут быть разделены на данной колонке. Задача 33. При разделения на хроматографической колонке (число теоретических тарелок N=256) объемы удерживания веществ А и В равны 5,0 и 6,2 см3 соответственно. Рассчитать ширину пика каждого вещества и их степень разделения. Количественный анализ Метод простой нормировки Пример задачи Задача 34. На хроматограмме обнаружены пики метанола, этанола и н-пропанола. Высота пиков равна соответственно 37, 184 и 17 мм. Ширина пиков на половине высоты 2.8, 10.2, и 2.4 мм соответственно. Рассчитать процентное содержание компонентов в смеси. Решение: Найдём площади пиков компонентов: 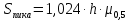 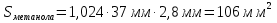 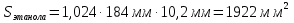 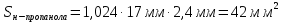 Процентное содержание компонентов рассчитывается по формуле: 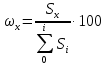 Тогда: 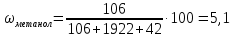 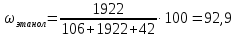 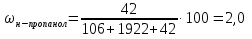 Ответ: 5,1% метанола, 92,9% этанола и 2,0% н-пропанола Задачи для самостоятельного решения Задача 35. На хроматограмме обнаружены пики о-ксилола, 1-этил-2-метилбензола, 1-изопропил-3-метилбензола, а также кумола. Высота пиков равна соответственно 128, 253, 27 и 58 мм. Ширина пиков на половине высоты 2.4, 5.8, 2.7 и 4.9 мм соответственно. Рассчитать процентное содержание компонентов в смеси. Задача 36. На хроматограмме обнаружены пики метиламина, диметиламина, пиридина, а также 6-метилурацила. Высота пиков равна соответственно 56, 72, 13 и 8 мм. Число теоретических тарелок равно 5000. Время удерживания компонентов равно 34, 42, 58 и 72 с. при скорости диаграммной ленты 3 см/мин. Рассчитать процентное содержание компонентов в смеси. Задача 37. Для вариантов 0-9 по известным площадям (мм2) хроматографических пиков методом простой нормализации рассчитать массовые доли спиртов в смеси:
Метод простой нормировки с введением поправочных коэффициентов Примеры задач Задача 38. Определить массовую долю (%) метана и этана в газовой смеси, если площади хроматографических пиков и поправочные коэффициенты этих компонентов равны, соответственно: 80 мм2 и 1.23 мм2, 40 мм2 и 1.15 мм2. Решение. Массовую долю компонента (%) в методе внутренней нормализации рассчитывают по формуле: Тогда, . . Следует заметить, что при правильном расчете суммарное содержание определяемых компонентов в газовой смеси составляет 100%: . Задача 39. Хроматографический анализ пропилбензола, изопропилбензола и толуола установил площади пиков этих соединений равными 118, 254 и 198 мм2 соответственно. Затем были введены стандартные смеси с концентрацией веществ 1 мг/л. Полученные пики имели площадь 123, 134 и 130 мм2 для пропилбензола, изопропилбензола и толуола соответственно. Рассчитать процентное содержание компонентов в пробе. За стандарт взять толуол. Решение: найдём поправочные коэффициенты f для пропилбензола и изопропилбензола: 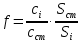 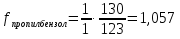 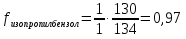 Проведём расчёт содержания компонентов по формуле: 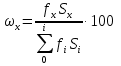 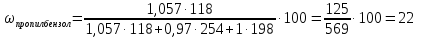 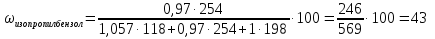 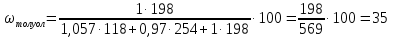 Ответ: 22% пропилбензола, 43% изопропилбензола и 35% толуола Задачи для самостоятельного решения Задача 40. Хроматографический анализ гексана, бензола и циклогексана установил площади пиков этих соединений равными 274, 112 и 328 мм2 соответственно. Затем были введены стандартные смеси с концентрацией веществ 1 мг/л. Полученные пики имели площадь 72, 74 и 66 мм2 для гексана, бензола и циклогексана соответственно. Рассчитать процентное содержание компонентов в пробе. За стандарт взять бензол. Задача 41. Хроматографический анализ показал, что в смеси содержится толуол, стирол и кумол с площадями пиков 151, 219 и 91 мм2 соответственно. Затем были введены стандартные смеси с концентрацией толуола 2 мг/л, стирола и кумола 3 мг/л, а также бензола 1 мг/л. Полученные пики имели площадь 63, 94 88 и 37 мм2 для толуола, стирола, кумола и бензола соответственно. Рассчитать процентное содержание компонентов в пробе. За стандарт взять бензол. Метод абсолютной градуировки Пример задачи Задача 42. Для построения калибровочного графика ацетилсалициловой кислоты были взяты его стандартные растворы с концентрациями 0.1, 0.2, 0.3, 0.4 и 0.5 мг/л. Хроматографический анализ данных проб показал, что площади пиков стандартных растворов будут равны соответственно 10, 21, 32, 41 и 49 мм2. Далее была взята проба неизвестной концентрации, площадь пика которой составила 37 мм2. Установить концентрацию ацетилсалициловой кислоты в неизвестной пробе. Решение: необходимо построить градуировочный график. Для этого воспользуемся любой программой, способной проводить расчёт методом наименьших квадратов (МНК, Advanced Grapher, SigmaPlot, Excel и т. д.) Построим в программе график зависимости площади пиков от концентраций в растворе (см. рисунок). 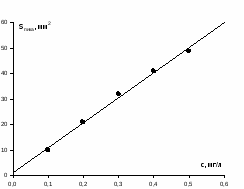 Уравнением, описывающим данную зависимость, является 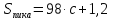 Подставляя в это уравнение площадь пика пробы, получаем с=0,37 мг/л Ответ: 0,37 мг/л Задачи для самостоятельного решения Задача 43. Для построения калибровочного графика гидрохинона были взяты его стандартные растворы с концентрациями 0.1, 0.2, 0.5, 1 и 2 мг/л. Хроматографический анализ данных проб показал, что площади пиков стандартных растворов будут равны соответственно 15, 31, 74, 146 и 287 мм2. Далее была взята проба неизвестной концентрации, площадь пика которой составила 43 мм2. Установить концентрацию гидрохинона в неизвестной пробе. Задача 44. Калибровочный график фенола был построен по стандартным растворам с концентрациями 0.05, 0.1, 0.2, 0.3 и 0.5 мг/л. Хроматографический анализ показал, что площади пиков стандартных растворов будут равны соответственно 35, 72, 143, 212 и 358 мм2. Из отходов лакокрасочных производств была отобрана проба массой 1 г., и растворена в 1 л. воды. После растворения полученный раствор подвергся хроматографическому анализу, который показал наличие пика фенола площадью 182 мм2. Определить содержание фенола в отходах. Задача 45. Для контроля содержания канцерогена бензапирен в воде 100 л речной воды пропустили через картридж для микроконцентрирования со степенью извлечения 97%. Далее, бензапирен был десорбирован 10 мкл гексана. Из полученного раствора отбиралась проба объёмом 1 мкл и вводилась в хроматограф. Был обнаружен пик бензапирена с площадью 190 мм2. Калибровочный график бензапирена строился из стандартных растворов с концентрациями 0.01, 0.02, 0.05, 0.1 и 0.2 мг/л, с объёмом вводимой пробы 1 мкл. Площади их пиков будут равны соответственно 46, 93, 234, 470 и 931 мм2. Определить содержание бензапирена в речной воде. Задача 46. Для построения градуировочного графика при определении этанола в кумысе приготовили стандартные растворы спирта с концентрациями 0,05; 0,1; 0,3; 0,5 и 0,7 г/дм3. В испаритель газового хроматографа послед
овательно ввели стандартные растворы, измерили площади хроматографических пиков: В колбе для перегонки взвесили 100 г кумыса, после удаления СО2 этанол отогнали в мерную колбу вместимостью 50,0 см3. Хроматографирование дистиллята провели в тех же условиях, что и стандартные растворы. Площадь пика составила 40,0 мм2. Вычислить массовую долю этанола в кумысе. Задача 47. Для контроля содержания формальдегида в воздухе 10000 л воздуха пропустили через 1 л. абсорбера со степенью извлечения 80%. Из полученного раствора отбиралась проба объёмом 1 мкл и вводилась в хроматограф. Был обнаружен пик формальдегида с площадью 234 мм2. Калибровочный график формальдегида строился из стандартных растворов с концентрациями 0.1, 0.2, 0.3, 0.4 и 0.5 мг/л, с объёмом вводимой пробы 0.1 мкл. Площади их пиков будут равны соответственно 13, 27, 38, 50 и 67 мм2. Определить содержание формальдегида в воздухе. Метод внутреннего стандарта Пример задачи Задача 48. При анализе сточных вод были обнаружены диметиламин, бензиламин и бензиловый спирт. Площадь их пиков на хроматограмме составила 180, 261, и 203 мм2 соответственно. В смесь заранее был добавлен этиламин в качестве вещества-стандарта с концентрацией 5 мг/л. Площадь пика этиламина составила 214 мм2. Рассчитать концентрацию компонентов в пробе, учитывая, что fi будет равен 1.09, 1.18 и 0.98 соответственно. Решение: Рассчитаем скорректированные площади пиков с учётом f: 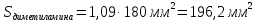 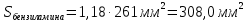 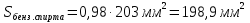 Учитывая: 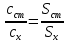 Получаем: 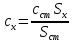 Подставляя значения в уравнение, получаем: 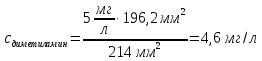 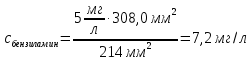 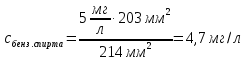 Ответ: концентрации диметиламина, бензиламина и бензилового спирта равны 4.6, 7.2 и 4.7 мг/л Задачи для самостоятельного решения Задача 49. При анализе смеси газов были обнаружены 2-метилпентан, метиламин, 2-метилбутан и пропан. Площадь их пиков на хроматограмме составила 132, 84, 219 и 114 мм2 соответственно. В смесь был добавлен гексан в качестве вещества-стандарта с концентрацией 10 мг/л. Площадь пика гексана составила 126 мм2. Рассчитать концентрацию компонентов в пробе, учитывая, что fi будет равен 1.13, 1.26, 1.32 и 1.48 соответственно. Задача 50. К 10 мл анализируемой смеси было добавлено вещество-стандарт н-бутанол в количестве 1 мл с концентрацией 20 мг/л. На хроматограмме полученной смеси были обнаружены пики изо-пропанола, н-бутанола, изо-пентанола, пропилацетата и метилметакрилата, имеющих площадь 92, 48, 15, 22 и 34 мм2 соответственно. fi будет равен 0.87, 1.04, 1.17 и 1.22 для изо-пропанола, изо-пентанола, пропилацетете и метилметакрилата соответственно. Найти концентрацию компонентов в смеси. Задача 51. Были введены стандартные смеси 2-метилпентана, 3-метилгексана, 2-метилгексана, 3-этилгексана и гептана с концентрацией 10, 15, 20, 10 и 5 мг/л. Получены пики площадью соответственно 105, 144, 197, 99 и 50 мм2. Далее, в неизвестную смесь был введён гептан в качестве стандарта в количестве 115 мкмоль. На хроматограмме были обнаружены пики с площадями 218, 33, 20, 116 и 47 мм2 для 2-метилпентана, 3-метилгексана, 2-метилгексана, 3-этилгексана и гептана соответственно. Найти количество вещества компонентов смеси. Задача 52. При анализе воздуха на предмет содержания полиароматических соединений 1000 л воздуха было пропущено через 1 л абсорбера (степень поглощения 82%), который, в свою очередь, был пропущен через картридж с адсорбентом (степень извлечения 94%), и далее десорбирован с поверхности адсорбента 10 мл пентана. К полученном раствору был добавлен 1 мл стандартного раствора нафталина (вещество-стандарт) с концентрацией 10 мг/л. На хроматограмме обнаружены пики 1,4-дигидронафталина, индола, аценафтена, фенантрена, антрацена, нафталина, флуорантена и бензофенантрена с площадями 13, 18, 54, 162, 178, 74, 102 и 42 ед. Определить концентрацию полиароматических соединений в воздухе, если fi для обнаруженных соединений соответственно 1.01, 1.17, 1.28, 1.34, 1.32, 1.0, 1.46 и 1.58 соответственно. Задача 53. Для анализа воды реки Рейн на предмет наличия пестицидов проба объёмом в 100 л была прокачена через форколонку, набитую сорбентом (степень извлечения 97%), а затем элюирована с поверхности сорбента 10 мл растворителя. В полученный раствор был добавлен 1 мл стандартного раствора анилина с концентрацией 0,1 мг/л. Смесь анализировали методом ВЭЖХ с детектором на диодной матрице. Были обнаружены пики следующих веществ:
Анализ стандартных образцов пестицидов с концентрацией 0,1 мг/л дал следующие результаты:
Рассчитать содержание пестицидов в воде Рейна, мг/л. Чувствительность детектора Пример задачи Задача 54. Площадь пика хризена, полученного на хроматографе с детектором по теплопроводности, составляет 117 мм2. Скорость газа-носителя 60 мл/мин, чувствительность самописца 10 mV при скорости диаграммной ленты 0,2 мм/с. Рассчитать чувствительность прибора по отношению к хризену, если количество вводимой пробы составило 1 мкл раствора хризена с концентрацией 1 моль/л. Решение: чувствительность концентрационного детектора, которым является детектор по теплопроводности, рассчитывается по формуле: 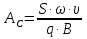 где ν – чувствительность самописца, q – количество вещества Количество вещества будет равно: 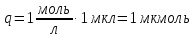 Подставляя в формулу, получаем: 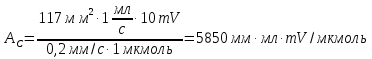 Ответ: 5850 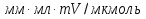 Задачи для самостоятельного решения Задача 55. Чувствительность детектора по теплопроводности в пересчете на н-пропан равна 103 мВ∙см3/мг. В детектор поступает газ, содержащий: 1) 10-2 масс.% метана; 2) 10 мг н-пропана в 1 м3 газовой смеси; 3) 20 мкг н-бутана в 1 дм3 газовой смеси; 4) 10-3 моль н-пропана в 1 м3 газовой смеси. Какие сигналы зафиксирует потенциометр хроматографа? Задача 56. Площадь пика 2-метилфенола, полученного на хроматографе с детектором по теплопроводности, составляет 135 мм2. Скорость газа-носителя 30 мл/мин, чувствительность самописца 50 mV при скорости диаграммной ленты 240 мм/час. Рассчитать чувствительность прибора по отношению к 2-метилфенолу, если количество вводимой пробы составило 1 мкл раствора 2-метилфенола с концентрацией 0,1 моль/л. Задача 57. Площадь пика бензола, полученного на хроматографе с детектором по теплопроводности, составляет 221 мм2. Скорость газа-носителя 60 мл/мин, чувствительность самописца 10 mV при скорости диаграммной ленты 1,5 см/мин. Рассчитать чувствительность прибора по отношению к бензолу, если количество вводимой пробы составило 0,5 мкл. Задача 58. На хроматографе с пламенно-ионизационным детектором получен пик 2,3-диметилоктана площадью 120 мм2. Чувствительность детектора по отношению к веществу составляет 84 mV. Чувствительность самописца 5 mV, скорость диаграммной ленты 0,25 мм/с. Какова будет площадь пика в случае использования в качестве детектора катарометра, если скорость газа-носителя 45 мл/мин, а чувствительность катарометра к 2,3-диметилоктану составляет 340 mV? Задача 59. На хроматографе с детектором по теплопроводности получен пик пирролидона площадью 264 мм2. Чувствительность катарометра по отношению к веществу составляет 290 mV. Какова будет площадь пика в случае использования пламенно-ионизационного детектора, если скорость газа-носителя 30 мл/мин, а чувствительность ПИД к пирролидону составляет 113 mV? Задача 60. Возможно ли хроматографическое определение дивинилхлорида, если площадь пика при использовании пламенно-ионизационного детектора составила 13 мм2, отклик самописца 10 mV при скорости диаграммной ленты 1,5 см/мин, концентрации вещества 10 мг/л, уровня шума 4,5 mV и скорости газа-носителя 20 мл/мин? Задача 61. Возможно ли хроматографическое определение фенантрена, если площадь пика при использовании детектора по теплопроводности составила 16 мм2, отклик самописца 1 mV при скорости диаграммной ленты 3 см/мин, концентрация вещества 30 мг/л, уровень шума 512 mV, а скорость газа-носителя 30 мл/мин? РЕКОМЕНДУЕМАЯ ЛИТЕРАТУРА 1. Основы аналитической химии. 2 кн. / Под ред. Ю. А. Золотова.– М.: Высшая школа, 2004. –359 с. (кн.1), 503 с. (кн.2) 2. Айвазов Б.В. Введение в хроматографию. – М.: Высшая школа, 1983. – 250с. 3. Гольдберт К.А., Вигдергауз М.С. Введение в газовую хроматографию. М.: Химия, 1990, 352 с. 4. Хефтман Э. Хроматография. Практическое приложение метода. М.: Мир, 1986, 336 с. 5. Айвазов Б.В. Практическое руководство по хроматографии. М.: Высшая школа, 1968, 280 с. 6. Столяров Б.В., Савинов И.М., Витенберг А.Г. и др. Практическая газовая и жидкостная хроматография. СПб: Изд-во С.-Петербург. ун-та, 2002, 616 с. 7. Яшин Я.И., Яшин Е.Я., Яшин А.Я. Газовая хроматография. М.: ТрансЛит. 2009. 512 с. 8. Москвин Л.М. Аналитическая химия в 3 томах. Т.2. Методы разделения веществ и гибридные методы анализа. М.: Академия. 2008г. 304 с. |
