Итоговый. Методические указания по решению задач Омск 2004 Составители Ласица Александр Михайлович Кондратьева Тамара Николаевна
 Скачать 2.6 Mb. Скачать 2.6 Mb.
|
|
| Дано: a = 0,5 м. p0= 105 Па. Т=300 К. |
| p -? |
 ешение:
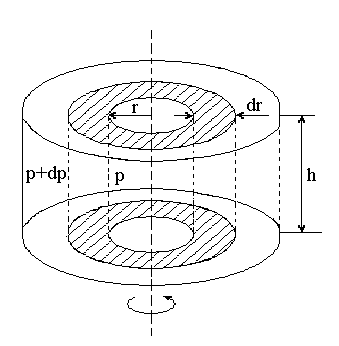
ешение: Рассмотрим находящийся в центрифуге цилиндрический слой воздуха бесконечно малой толщины dr, такой, что можно считать, что все молекулы данного слоя находятся на одинаковом расстоянии r от оси вращения.
Запишем для данного слоя второй закон Ньютона :
F = ma
Под силой F в данном случае нужно понимать разность сил давления действующих с внешней и внутренней стороны слоя
F = ((p+dp)-p)2
где произведение 2
dp =
(в правой и левой части сокращён одинаковый множитель 2
Проинтегрируем полученное уравнение:
где А - некоторая постоянная интегрирования. Представим её в виде натурального логарифма от некоторой другой постоянной С:A = ln C. Тогда
или
По условию задачи на оси центрифуги давление должно быть p0, это возможно только в случае, когда C= p0. Заменяя C на p0, определим давление как функцию расстояния до оси вращения:
Вспоминая, что
Подставляя в последнюю формулу r = a = 0,5 м и молярную массу радона
Ответ: давление на стенку ротора p0 =3 105 Па.
Задача № 4
Стальной стержень длиной ℓ = 20 см с площадью поперечного сечения S = 3 см2 нагревается с одного конца до температуры t1 = 3000С, а другим концом упирается в лёд. Предполагая, что передача тепла происходит исключительно вдоль стержня (без потерь через стенки), подсчитать массу льда, растаявшего за время t = 10 мин. Теплопроводность стали = 60 Вт/(м∙К).
| Дано: t1 = 3000С S = 3см2 t2 = 00С ℓ = 20см. = 60 Вт/м∙К |
| m -? |
Найдём количество теплоты полученное льдом. Для этого запишем уравнение теплопроводности.
Считая, что поток тепла не изменяется со временем и постоянен в пределах сечения стержня, данную формулу можно записать в виде
Производная
Так как всё это количество теплоты идёт на плавление льда, Q = m ( = 3,3105 Дж/кг – удельная теплота плавления льда). Объединяя выражения и производя расчеты получим
Ответ: масса растаявшего льда m = 0,049 кг = 49 г.
Задача № 5
В результате некоторого процесса вязкость некоторого идеального газа увеличилась в
| Дано: |
| |
Согласно молекулярно кинетической теории,
где
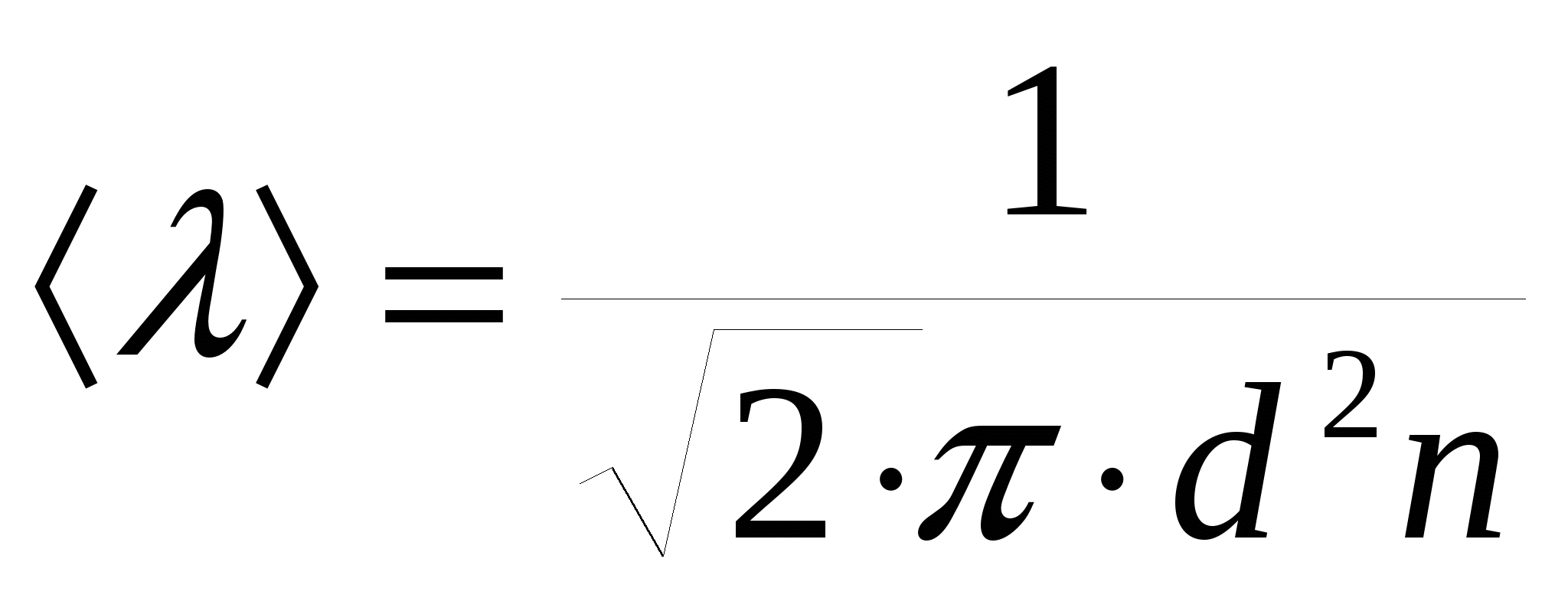 средняя длина свободного пробега,
средняя длина свободного пробега, По основному уравнению МКТ
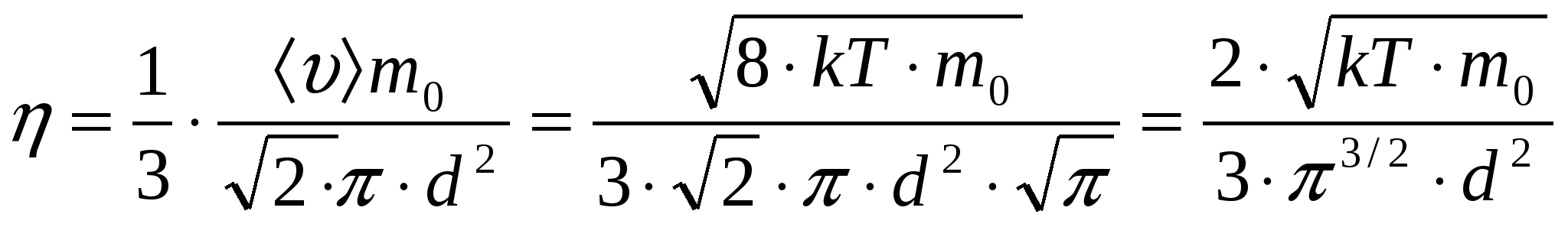 ;
;Из формул видно, что
Ответ: давление возрастет в два раза.
Задачи, рекомендуемые для аудиторных занятий
1. 12 г газа занимают объем 4 дм3 при температуре 70С. После нагревания газа при постоянном давлении его плотность стала равна 0,6 мг/см3. До какой температуры нагрели газ?
Ответ: до 1400 К.
2. В сосуде находится 14 г азота и 9 г водорода при температуре 100С и давлении 1 МПа. Найти молярную массу смеси и объем сосуда.
Ответ: 4,6 г/моль; 12 дм3.
3. В двух сосудах емкостями 3 и 4 л находится газ под давлениями 0,2 и 0,1 МПа соответственно. Температура в обоих сосудах одинакова. Под каким давлением будет находиться газ, если соединить сосуды трубкой?
Ответ: 140 кПа.
4. В баллоне емкостью 150 см3 содержится газ при температуре 30 0С. Вследствие утечки из колбы вышло 4∙1018 молекул. Определить, на сколько понизилось при этом давление газа?
Ответ: 112 Па.
5. Плотность некоторого газа равна 6∙10-2 кг/м3, средняя квадратичная скорость молекул этого газа равна 500 м/с. Найти давление, которое газ оказывает на стенки сосуда.
Ответ: 5 кПа.
6. В баллоне емкостью 5 л находится 25∙1021 молекул азота. Найти среднюю квадратичную скорость его молекул, если давление в баллоне P = 720 мм рт.ст.
Ответ: 1100 м/с.
7. Найти число молекул азота в 1 см3 при нормальных условиях и обладающих скоростью: а) между 99 м/с и 101 м/с; б) между 499 м/с и 501 м/с.
Ответ: 8,6∙1018; 4,9∙1019.
8. Найти для газообразного азота температуру, при которой скоростям молекул υ1 = 300 и υ2 = 600 м/с соответствуют одинаковые значения функции распределения Максвелла.
Ответ: 330 К.
9. Полагая температуру воздуха и ускорение свободного падения не зависящими от высоты, определить, на какой высоте h над уровнем моря плотность воздуха меньше своего значения на уровне моря в 2 раза. Температура воздуха t= 00С.
Ответ: 5,5 км.
10. Вычислить среднюю длину свободного пробега молекул воздуха при температуре 17 0С и нормальном давлении. Эффективный диаметр молекул воздуха принять равным 3∙10-8 см.
Ответ: 10-7 м.
11. Определить среднее число всех столкновений между молекулами, которые происходят в течение 1 с в 1 см3 кислорода при температуре 17 0С и давлении 5 мм рт. ст. Эффективный диаметр молекулы кислорода 2,9∙10-8 см.
Ответ: 2,27∙1024.
12. Найти среднюю длину свободного пробега азота, если его динамическая вязкость 17 мкПас, d = 0,3 нм.
Ответ: 0,09 нм.
13. Найти коэффициент теплопроводности воздуха при температуре 10 0С и давлении 100 кПа, если диаметр молекулы воздуха принять равным 0,3 нм.
Ответ: 13 мВт/(мּК).
14. Вычислить коэффициент диффузии и динамическую вязкость азота при давлении 0,1 МПа и температуре 7 0С.
Ответ:14ּ10-6 м2/с и 17ּ10-6 Паּс.
Задачи для самостоятельного решения
Сколько молекул содержится в 2 л кислорода, находившегося при температуре 170С и давлении 0,2 МПа?
Сосуд емкостью 1 л содержит 1,5 г некоторого газа под давлением 0,25 МПа. Определить среднюю квадратичную скорость молекул газа.
Среднеквадратичная скорость молекул газа при давлении 0,1 МПа составляет 500 м/с. Определить плотность газа при этих условиях.
При какой температуре средняя квадратичная скорость атомов гелия станет равной второй космической скорости (11,2 км/с)?
Определить массу одной молекулы углекислого газа.
В сосуде емкостью 5 л находится 0,2 моля некоторого газа. Определить, какой это газ, если его плотность 1,12 кг/м3.
Газ при температуре 309 К и давлении 0,7 МПа имеет плотность 12 кг/м3. Определить молярную массу этого газа.
Сколько молекул газа содержится в баллоне вместимостью 30 л при температуре 300 К и давлении 5 МПа?
Плотность некоторого газа 0,06 кг/м3, средняя квадратичная скорость молекул этого газа 500 м/с. Найти давление, которое газ оказывает на стенки сосуда.
Давление газа 1 МПа; концентрация молекул 1010 см-1. Найти температуру газа и среднюю кинетическую энергию поступательного движения одной молекулы.
Плотность воздуха при температуре 0 0С и давлении 760 мм рт. ст. равна 0,001293 г/см3. Сколько весит литр воздуха при температуре 27,3 0С и давлении 750 мм рт. ст.?
Баллон содержит газ при t1 = 500С и давлении 30 атм. Каково давление, когда из баллона будет выпущена половина массы газа, а температура понизится до t2 = 10 0С?
Сосуд ёмкостью V = 0,01 м3 содержит азот массой m1 = 7 г и водород массой m2 = 1 г при температуре Т = 280 К. Определить давление P смеси газов.
Найти плотность ρ газовой смеси, состоящей по массе из одной части водорода и восьми частей кислорода, при давлении P = 0,1 МПа и температуре Т = 290 К.
Баллон емкостью V = 15 л содержит смесь водорода и азота при температуре Т = 300 К и давлении P = 1,23 МПа. Масса смеси m = 145 г. Определить массу m1 водорода и массу m2 азота.
Газовая смесь, состоящая из кислорода и азота, находится в баллоне под давлением P = 1 МПа. Считая, что масса кислорода составляет 20% от массы смеси, определить парциальные давления P1иP2от дельных газов.
Два сосуда с объемами V1 = 1 л и V2 = 3 л соединены трубкой с краном. До открытия крана в первом сосуде содержался азот под давлением P1 = 0,5 атм и при температуре t1 = 0 0С, а во втором - аргон под давлением P2 = 1,5 атм и при температуре t2 = 100 0С. Определить, какое давление установится в смеси газов, если открыть кран. Температура смеси 79 0С.
Плотность газа ρ при давлении P = 720 мм рт. ст. и температуре t2 = 0 0С равна 1,3 г/л. Найти массу моля μ газа.
Сколько молекул водорода находится в объеме 1,55 л при температуре 270С и давлении 750 мм рт. ст.?
Найти число молекул Nв 1 см3 и плотность ρ азота при давлении 1,0010-11 мм рт. ст. и температуре 15 0С.
Два баллона соединены трубкой с краном. В первом находится газ под давлением 105 Н/м2, во втором – при 6ּ104 Н/м2. Емкость первого баллона 1 л, второго – 3 л. Какое давление установится в баллонах (в мм рт. ст.), если открыть кран? Температуре постоянна. Объемом трубки можно пренебречь.
Найти число ν молей и число N молекул, содержащихся в объеме V = 1см3 водяного пара при температуре t = 4 0С.
В баллоне емкостью V = 20 л находится аргон под давлениемP1 = 800 кПа и температуре Т1 = 325 К. когда из баллона было взято некоторое количество аргона, давление в баллоне снизилось до P2 = 600 кПа, а температура установилась Т2 = 300 К. Определить массу mаргона, взятого из баллона.
Баллон емкостью V = 40 л заполнен азотом. Температура азота Т = 300 К. Когда часть азота израсходовали, давление в баллоне понизилось на ∆P = 400 кПа. Определить массу израсходованного азота. Процесс считать изотермическим.
В баллоне находился идеальный газ при давлении 4ּ107 Па и температуре 300 К. Затем 3/5 содержащегося в баллоне газа выпустили, а температура понизилась до 240 К. Под каким давлением находится оставшийся в баллоне газ?
Какой объем
