Методические указания в сжатой форме знакомят студентов с основными теоретическими положениями, относящимися к данной лабораторной работе или группе лабораторных работ со схожей тематикой,
 Скачать 1.55 Mb. Скачать 1.55 Mb.
|
Содержание протокола лабораторной работыМасса навески угля g = __________ г Концентрация раствора щелочи С(NaOH) = ________ экв/л. Слабый электролит (название и химическая формула). Ориентировочная концентрация слабого электролита (указана на емкости с кислотой). Объем аликвоты Va = ________ мл. Результаты анализа проб кислоты
Обработка результатов эксперимента1. Рассчитать значение концентрации раствора кислоты, взятого на приготовление растворов и проведение адсорбции по формуле: где V0 – средний объем гидроксида натрия, затраченный на титрование пробы исходной кислоты, мл, (см. табл. «Результаты анализа проб кислоты»). Полученное значение занести в строку 1 графы «С0» таблицы (п. 6). 2. Вычислить концентрации растворов, полученных согласно п. 3 раздела «Выполнение работы» и занести их в строки 2-4 графы «С0» таблицы (п. 6). 3. По результатам титрования проб после адсорбции вычислить значения равновесных концентраций кислоты по формуле где Vi – средний объем гидроксида натрия, затраченный на титрование пробы кислоты после адсорбции, мл, (см. табл. 6). Полученные значения занести в графу «С*» таблицы (п. 6). 4. Вычислить изменение концентрации кислоты в процессе адсорбции по формуле: 5. Вычслить значения удельной адсорбции растворенного вещества Г по формуле где V – объем кислоты, взятый на адсорбцию, л; ms – навеска адсорбента (активированного угля), кг. 6. Заполнить таблицу. Данные для построения изотерм адсорбции
7. Построить изотерму удельной адсорбции кислоты в координатах Г = f(C) (рис. 8). 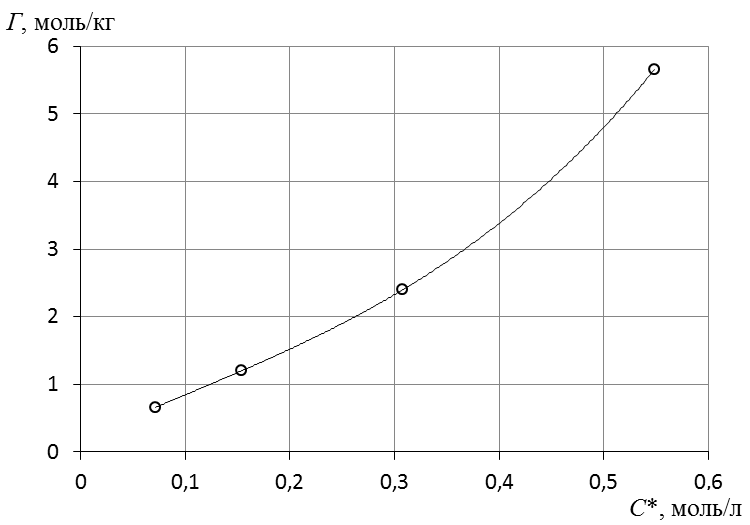 Изотерма удельной адсорбции.8. Построить изотерму адсорбции Фрейндлиха в координатах lgГ = f(lgC) и вычислить коэффициенты уравнения Фрейндлиха по уравнению линии тренда (рис. 9). 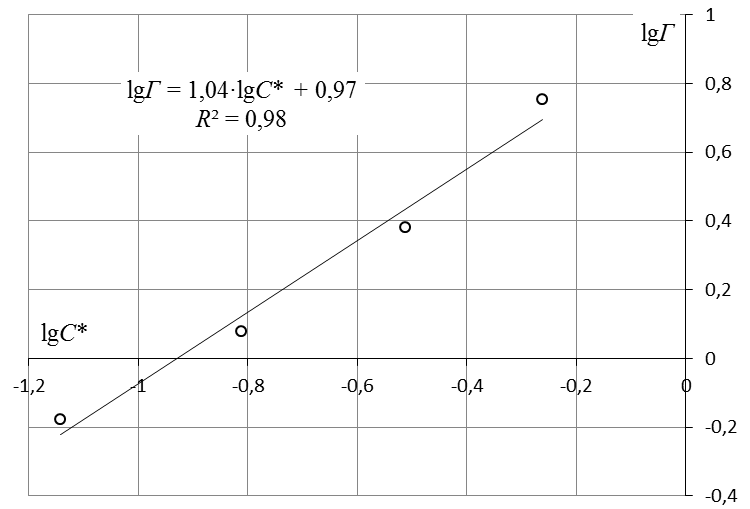 Линейная форма уравнения адсорбции Фрейндлиха. lgK = 0,97; 1/n = 1,04.9. Построить график линейной формы изотермы адсорбции Ленгмюра в координатах 1/Г = f(1/C). 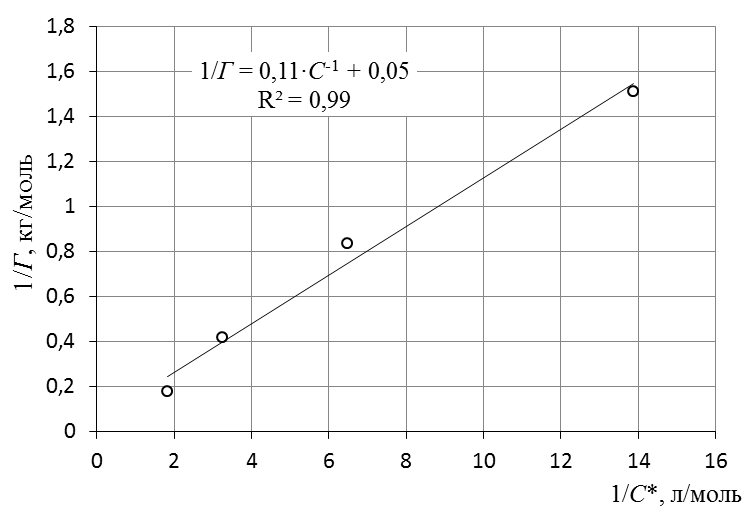 Линейная форма уравнения адсорбции Ленгмюра в координатах 1/Г = f(1/C). 10. По уравнению линии тренда определить константы уравнения Ленгмюра Г∞ и K. 11. Оценить удельную поверхность активированного угля по уравнению где NA – число Авогадро; SM – площадь поперечного сечения молекулы адсорбата, равная для карбоновых кислот 20,51020 м2. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
