Материал по микробиологии. Теоретический материал по микробиологии. Микробиология пищевых производств
 Скачать 0.61 Mb. Скачать 0.61 Mb.
|
|
Тема: «Превращение микроорганизмами соединений углерода и азота». 3.1. Круговорот углерода в природе и участие в нём микроорганизмов. Углерод (С) является важнейшим элементом органических веществ. Органические вещества, в свою очередь, обладают огромным запасом скрытой солнечной энергии, которая обеспечивает жизнью всё живое на земле. Микроорганизмы играют главную роль в круговороте всех биологически важных элементов, в том числе и О2. В круговороте С различают два процесса , связанные с выделением и поглощением 02: Фиксация С02 в процессе фотосинтеза Минерализация органических веществ с выделением С02. Фотосинтез - осуществляется как высшими, так и низшими растениями, в том числе и микроорганизмами из числа водорослей и цианобактерий. При этом окисленная форма углерода (С02) переводится в восстановленную форму органических веществ; восстановленный 02 (в форме Н20) окисляется до молекулярного 02, поступающего в атмосферу. Минерализацию органических веществ совершают разнообразные микроорганизмы. При этом 02 расходуется на распад сложных органических соединений с выделением С02 и Н20. Установлено, что содержание С02 в атмосфере составляет 0,03%, а растения ежегодно поглощают 19 млрд. тонн С02. Схема круговорота углерода включает в себя следующие звенья: Органические вещества растительного происхождения. Органические вещества животного происхождения. Минерализация органических веществ микроорганизмами в процессе брожения, гниения, окисления, происходящих в почве и водоёмах. При этом идёт выделение С02, который направляется на фотосинтез и замыкает цепь круговорота С в природе. В природе наблюдается два типа распада отмерших растительных и животных остатков: фитогенный распад - осуществляется при участии существ растительного происхождения (высшими и низшими грибами, бактериями актиномицетами и т.д.) и зоогенный распад - идёт при участии беспозвоночных животных (простейшие, черви, моллюски, насекомые). Установлено что оба процесса идут параллельно, но преобладает фитогенный распад. Медленно разлагаются: полисахариды, клетчатка, крахмал, пектиновые вещества. Наиболее устойчивым является лигнин, который служит ядром молекул гумусовых (перегнойных) веществ. Большей скоростью разложения обладают дисахариды. 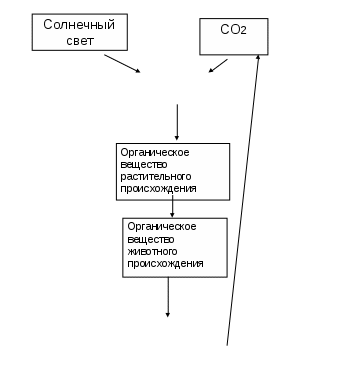 фотосинтез Минерализация с участием микроорганизмов  3.2. Брожение, его сущность и значение. Виды брожений. Брожение - это анаэробное превращение углеводов. При этом идёт неполное расщепление органических веществ с освобождением незначительного количества энергии и накоплением богатых конечных продуктов (спиртов, органических кислот). Процессы дыхания и брожения генетически связаны между собой, т.к. их исходным веществом является глюкоза (С6Н1206). Г  люкоза (С6Н1206) люкоза (С6Н1206)П  ировиноградная кислота (СНЗСОСООН) ировиноградная кислота (СНЗСОСООН) +02 без 02 —С02+Н20 СНЗСHОH (спирт, кислоты) (дыхание) (брожение) Гликолиз - это превращение глюкозы до ПВК под действием специфических ферментов. Химизм брожения. Брожение как химический процесс состоит из 2х стадий: 1) Окислительная (гликолиз) - это превращение глюкозы до ПВК под действием специфических ферментов. 2) Восстановительная - ПВК в зависимости от вида микроорганизмов под действием ферментов превращаются в конечный продукт. Виды брожений. Молочно-кислое брожение - это процесс разложения углеводов до молочной кислоты в анаэробных условиях. Молочно-кислые бактерии находятся в кормах, растениях, в кишечнике животных и человека; почти не встречаются в воде и почве. Молочно-кислый стрептококк обладает антимикробным действием, образует антибиотики. Используется для приготовления молочно-кислых продуктов, при квашении овощей. Болгарская палочка - используется в Южных широтах для скисания молока. Силосная палочка - для силосования кормов. Спиртовое брожение - это анаэробное превращение углеводов под действием микроорганизмов с образованием спирта и С02. Если процесс идёт при кислой реакции среды (рН=3-5), то в качестве основного продукта образуется этиловый спирт и С02; если рН=8-9 (щелочная реакция), то образуется еще глицерин, уксусная кислота, а этиловый спирт является побочным продуктом. Брожение сопровождается бурным газообразованием, помутнением раствора, выпадением осадка. Впервые биологическую природу спиртового брожения подчеркнул Луи Пастер. Он доказал, что м/орг-мы участвуют в процессе брожения. Однако немецкий ученый Либих утверждал, что спиртовое брожение является чисто химическим процессом и связано с изменением веществ, находящихся в бродильной жидкости. Братья Бухлера установили, что в процессе брожения участвуют ферменты, выделяемые м/орг-ми. Химизм спиртового брожения: протекает по типу гликолиза с дальнейшим превращением ПВК в уксусный альдегид, который восстанавливается в этиловый спирт. Кроме этилового спирта и глицерина образуются сивушные масла - это бутиловый, амиловый, изобутиловый и др. спирты. Спирты получают из отходов различных производств - паточной, нефтяной, но сначала отходы подвергаются гидролизу. Наиболее подходящая концентрация сахара в бродящей жидкости - 10-15%. Концентрация 10% нежелательна, а при 30-35% приостанавливается деятельность дрожжей и сам процесс брожения. Брожение должно идти при анаэробных условиях. При обильном доступе воздуха бродящие дрожжи окисляют углеводы и процесс брожения переходит в процесс дыхания. Возбудители спиртового брожения – различные расы дрожжей: пивные, хлебные, винокуренные, винные, жировые, дикие. Дрожжи требовательны к источникам азота (белки, АМК, пептоны); являются продуцентами многих витаминов. В бродильной практике различают 2 расы дрожжей: дрожжи верхового брожения - развиваются при t = 25-28C и доступе кислорода. По окончании брожения дрожжи поднимаются наверх (используются в хлебопечении, спиртовой практике). дрожжи низового брожения - сбраживают углеводы при t = 4-1ОС без бурного газообразования, а по окончании брожения оседают на дно (используются в пивоварении). По происхождению различают: Дикие дрожжи - обитают в естественной среде на листьях, плодах, ягодах. Обладают слабой бродильной способностью, образуют побочные продукты разложения, имеют неприятный привкус и запах. Культурные дрожжи - выведены на основе диких путём селекции, генной инженерии, гибридизации и представляют собой чистую культуру с положительными производственными качествами: они быстро размножаются и выделяют большее количество С02; полученный продукт обладает приятным запахом и вкусом. Культурные дрожжи широко используются для приготовления марочных вин из винограда. Винокуренные дрожжи дают высокий выход спирта. Жировые дрожжи получены селекционным путём и используются для выработки большого количества жира для технических целей. Пектиновое брожение. Скорость минерализации растительных остатков в большей степени зависит от разрушения пектиновых веществ бактериями, грибами. Пектиновые вещества склеивают серединные пластинки растительных клеток между собой . Наибольшим содержанием пектиновых веществ характеризуется прядильные культуры: лён, конопля. Бактерии расщепляющие пектиновые вещества высвобождают растительные волокна , которые идут в ткацкое производство. Пектин добываемый из кожуры фруктов (в части яблоко), используется в кондидерской пр-ти для приготовления мармелада и пастилы . Пектиновые в-в относятся к полисахаридам, состоящим из частиц галактуроновой к-ты. Различают 3 типа пектиновых в-в : 1)Протопектин - водорастворимая часть клеточной стенки. 2)Пектин — межклеточное водорастворимое вещество. 3)Пектиновая кислота - водорастворимая часть, полимер галактуроновой кислоты. Эти вещества расщепляются специфическими экзоферментами, выделяемыми м/орг-ми. Микробы участвующие в брожении пектиновых веществ, являются самыми кислотоустойчивыми. Окисление жира. Жир попадает в почву вместе с животными и растительными остатками и подвергаются гидролитическому распаду с участием экзоферментов. Возбудители: Psevdomones fluorensis -палочковидный ,на питательной среде образует колонии зеленоватого цвета светящиеся в темноте . Chromobacter prodeginosum - палочковидные, образует колонии красного цвета. Окисление жира могут вызывать грибы родов: Aspergillus и Реnicillium. Важным моментом этого процеccа является то, что глицерин и жирные кислоты, постепенно окисляясь, дают перегнойные вещества почвы (образование гумуса). Окисление этилового спирта в уксусную кислоту. Впервые этот процесс был обнаружен Луи Пастером в 1882 г. Химизм процесса происходит в анаэробных условиях. С2Н50Н+02 -> СНЗСООН+Н20 Вызывается бактериями рода Acetobacter и Cluconobacter . Это хемоорганотрофные палочковидные бактерии, не образуют спор, строгие анаэробы. Бактерии из рода Acetobacter - перитрихи ; они накапливают уксусную к-ту как промежуточный продукт и могут дальше её окислять. Бактерии из рода Cluconobacter - лофотрихи ; накапливают уксусную к-ту как конечный продукт, который не подвергается дальнейшему окислению. Эти бактерии обитают на растениях, цветах, иногда на плодах, иногда на отмерших растительных остатках. Окисление углеводов до лимонной кислоты. Лимонная кислота получается при участии плесневых грибов из родов Aspergillus и Реnicillium. Процесс наблюдается в почве, в стоячих водоёмах, на различных продуктах (варенье, томате, плодах). Лимонную к-ту в практических условиях получают по методу Косточева и Буткевича, которые разработали методику ещё в 1924г. Сначала выращивают плёнку гриба на 5% р-ре сахара, затем жидкость сливают и заменяют её 20-25% р-ром сахара. В этой фазе происходит быстрое накопление к-ты .При хорошей аэрации в спец камере при t=30C процесс продолжается 6-8 дней . Выход лимонной кислоты составляет 50-60% от израсходованного сахара. При отсутствии сахара к-та потребляется грибом как питательный материал. В лимонах содержится 7-9%) лимонной кислоты. Разложение целлюлозы. Целлюлоза представляет собой сложный полисахорид, к-рый является главной составной частью клеточных стенок . В воде она не растворима и трудно растворима в кислотах. Попадая в почву целлюлоза подвергается воздействию различных м/орг-в (бактерий, грибов), к-рые которые выделяют специфический фермент. Постепенно полисахариды переходят в моносахариды . Из аэробных бактерий наибольшей активностью обладают микробы рода Cutophaga, к-рые преобладают на увлажненных плодородных почвах. Из анаэробных бактерий выделяется род Celvibrio они предпочитают почвы с минеральным составом, бедные органикой. 3.3. Круговорот азота в природе. Азот наряду с такими минеральными элементами, как сера, фосфор, железо, калий и др., является составной частью живой материи. Большой запас на нашей планете составляет атмосферный молекулярный азот. Массовая доля свободного азота в сухом воздухе 0,755 (75,5 %), а его объемная доля — 0,781 (78,1 %). Над каждым гектаром почвы поднимается столб воздуха, в котором сосредоточено 80000 т молекулярного азота. Растения не могут усваивать этот азот, однако некоторые почвенные микроорганизмы обладают способностью с помощью ферментов фиксировать атмосферный азот и синтезировать белок. Главный поставщик связанного азота в природе — бактерии: благодаря им связывается приблизительно от 90 до 140 миллионов тонн азота (точных цифр, к сожалению, нет). Самые известные бактерии, связывающие азот, находятся в клубеньках бобовых растений. На их использовании основан традиционный метод повышения плодородия почвы: на поле сначала выращивают горох или другие бобовые культуры, потом их запахивают в землю, и накопленный в их клубеньках связанный азот переходит в почву. Затем поле засевают другими культурами, которые этот азот уже могут использовать для своего роста. Таким образом, первый этап превращения азота в природе заключается в его фиксации микроорганизмами. Белковый азот микроорганизмов, так же как и азот растений и животных, после их гибели минерализуется в почве большой группой аммонифицирующих бактерий до аммиака. Поэтому второй этап превращения азота носит название аммонификации. На третьем этапе аммонийный азот нитрифицирующими бактериями частично окисляется в нитраты, этот процесс получил название нитрификации. Наконец, на четвертом этапе нитратный азот некоторыми видами бактерий при определенных условиях частично восстанавливается до молекулярного азота — происходит процесс денитрификации. Общая схема круговорота азота представлена на таблице (по А. А. Имшенецкому). 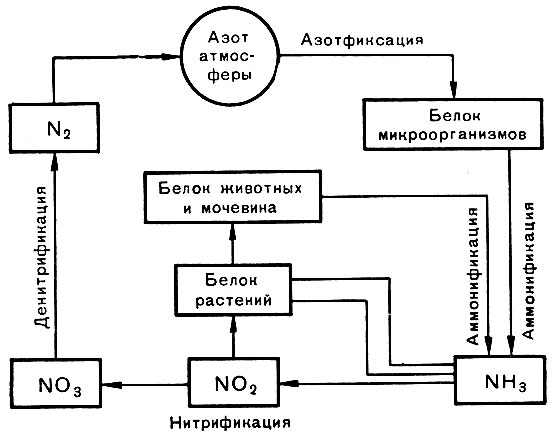 3.4. Аммонификация, нитрификация, денитрификация. Аммонификация белковых веществ Почти весь азот, попадающий в почву с растительными и животными остатками, а также азот гумуса находится в виде органических соединений. В пахотном слое 1га различных типов почв связанный азот в виде биомассы бактерий, грибов, водорослей, насекомых, червей и др. и составляет от 6 до 18 т. Однако растения могут усваивать только минеральные соединения азота. Азот органических веществ должен быть предварительно превращен в основном в нитратную и аммиачную формы и только затем его смогут использовать растения. В теле их из азота вновь образуются сложные белковые соединения. Гниение, или аммонификация белков — микробиологический процесс, при котором под воздействием гнилостных микроорганизмов происходит гидролитическое расщепление белков, поступающих в почву с трупами животных и отмирающими растениями, с образованием промежуточных продуктов (альбумоз, пептонов, амино- и амидокислот), а также дурно пахнущих веществ — индола, сероводорода, меркаптана, летучих жирных кислот. Превращение азота из органических соединений (белков) в минеральные называется аммонификацией. Этот процесс осуществляется различными бактериями, актиномицетами и плесневыми грибами. Аммонификации подвергаются азотсодержащие соединения самой разнообразной структуры: белки, аминокислоты, аминосахара, нуклеиновые кислоты, амиды, почвенный гумус, фосфатиды, алкалоиды, амины, мочевая кислота и мочевина. Первым продуктом минерализации органического азота в почве является аммиак. Разложение белковых веществ широко распространено в природе и постоянно протекает в воздухе, воде, земле, а также в органах живых существ. Оно связано с использованием микроорганизмами белков в качестве азотного или углеродного питания, а также энергетического материала. Некоторые микробы продуцируют ферменты эктопротеазы, способные разрушать белки, в то время как микроорганизмы, не выделяющие их, могут воздействовать лишь на продукты распада, например на пептоны, аминокислоты. Если аммонификация протекает в аэробных условиях, то конечными продуктами этого процесса будут аммиак, углекислый газ, вода, сероводород и соли фосфорной кислоты. В анаэробных условиях не происходит полного окисления промежуточных продуктов распада аминокислот, поэтому, кроме NH3 и СО2, накапливаются различные органические соединения, в том числе и ядовитые — диамины или птомаины. При аммонификации белка наряду с процессами окисления происходят восстановительные реакции с образованием иногда фенола, индола и скатола, которые обладают очень неприятным запахом. При бактериальном разложении аминокислот, содержащих серу, выделяется сероводород и редко его производные — меркаптаны— вещества с отвратительным запахом. Если расщепляются белки, в состав которых входит фосфор, то среди продуктов распада обнаруживается фосфорная кислота. Аммонифицирующие бактерии могут быть, спорообразующие и неспорообразующие, аэробные и анаэробные. Среди аэробных микробов, способных разлагать белки, наиболее распространены и активны следующие: Bacteriafluorescens— небольшая подвижная палочка, образует желто-зеленый флуоресцирующий пигмент; Bad. prodigiosum— «чудесная палочка», вырабатывает красный пигмент; Bacillussubtilis— сенная палочка; В В. mesentericus— картофельная палочка. Из группы факультативно анаэробных микроорганизмов чаще всего встречается Proteusvulgaris, очень полиморфная палочка; на питательных средах она меняет форму и размеры, откуда и получила название Proteus(мифический бог Протей, сказочные превращения которого были описаны Гомером в «Одиссее»); B. coli(кишечная палочка), а из анаэробных — В. putrificus, В. sporogenesи ряд других бактерий. Особенно много в почве аэробных и факультативно-анаэробных микробов. Аммонификация мочевины и цианамида Мочевина — продукт распада белков в организме животных и человека, выделяющаяся во внешнюю среду с мочой. В моче человека содержится около 2 %мочевины, лошадей — около 3, коров — до 5 %. До 11 % мочевины встречается в продуктах обмена некоторых высших грибов. Она содержит 47 % азота. Однако азот мочевины становится доступным для растений только после разложения ее уробактериями и гнилостными бактериями. Распад мочевины происходит под влиянием экзофермента уреазы, выделяемого уробактериями. Под его влиянием азот мочевины освобождается в виде неустойчивой углеаммиачной соли, разрушающейся до аммиака: уреаза CO(NH2)2 + 2H2О → (NH4)2CО3; мочевина углеаммиачная соль (NH4)2СО3 → 2NH3 + СО2 + Н2О Уробактерии относятся к аэробным микроорганизмам. Они хорошо развиваются в щелочной среде (рН 8,0). По форме эти бактерии бывают шаровидные и палочковидные. Типичным представителем шаровидных форм является Planosarcinaureae — подвижная, спорообразующая сарцина с множеством, жгутиков. Наиболее активно разлагают мочевину палочковидные бактерии. Из них заслуживает внимания Urobacilluspasteuri— длинная подвижная спорообразующая палочка. Расщеплять мочевину способны в небольшом количестве и многие гнилостные бактерии, например B. fluorescens(рис. 20). Под действием уробактерий цианамид кальция (CaCN2) в почве превращается в форму, доступную для растений. Разложение проходит в три этапа: первый гидролиз цианамида, второй — превращение его в мочевину и третий — распад мочевины до аммиака и углекислого газа: CaCN2 + 2H2О → H2CN2 + Ca(OH)2 ; H2CN2 + H2О → CO(NH2)2; CO(NH2)2 + H2О → 2NH3 + CO2 Накопление аммиака в почве возможно только в том случае, когда углерод и азот находятся в разрушаемом (минерализующемся) веществе в определенном соотношении. Если в отмерших органических остатках соотношение С:N больше 25, то весь азот будет использован микроорганизмами и вновь превратится в белок бактерий в результате их интенсивного размножения, а следовательно, NH3 накапливаться в почве не будет. Быстрое размножение микробов обусловлено высоким содержанием энергии в углеродистых соединениях. И только при отношении углерода к азоту меньше, чем 25:1, микроорганизмы не используют весь азот органических веществ, поэтому аммиак остается в свободном состоянии в почве. Таким образом, чем больше органические вещества содержат азота, тем больше аммиака будет накапливаться в почве. Аммонификация гумуса (технологам кратко) Значительное количество связанного азота содержится в почве в виде гумусовых веществ (перегной). В пахотном слое 1 га дерново-подзолистой почвы они составляют 70—90 т, чернозема — от 90 до 300 т, а иногда и больше. Для использования растениями азота из гумуса необходима аммонификация гумуса. Минерализация перегнойных веществ происходит медленно, тогда как свежие органические остатки разрушаются во много раз быстрее. По данным многих авторов, в зоне умеренного климата за год микробы разлагают не более 1—3 % общего запаса почвенного гумуса. Активность микроорганизмов при минерализации гумусовых веществ в почве в значительной степени зависит от температуры, аэрации, рН, концентрации почвенного раствора, влажности и других свойств. Оптимальной для разложения гумусовых веществ является температура 30—35° С и влажность 60—70 % полевой влагоемкости. Аэрация должна быть достаточной, иначе из всей микрофлоры почвы будут активными лишь анаэробы. Хорошая аэрация способствует усиленному разрушению органических веществ и обеспечивает господство окислительных процессов. Минерализация органических соединений почвы успешно проходит в условиях нейтральной и слабокислой реакции при рН 5,0—7,5. Внесение свежих органических или минеральных удобрений активизирует деятельность микробов, а это приводит к усилению интенсивности разложения органических веществ почвы и накоплению перегноя. Нитрификация. Окисление аммиачного азота, освободившегося в результате процесса аммонификации, в нитраты называется нитрификацией. Это процесс проходит в два этапа: 1) окисление аммиака в нитриты и 2) окисление нитритов в нитраты. Впервые С. Н. Виноградским в 1890 г. была получена чистая культура, бактерий, обусловливающих эти превращения. Микроорганизмы, вызывающие эти два этапа, принадлежат к различным родам и относятся к автотрофам. На первом этапе аммиак окисляется до азотистой кислоты по следующему уравнению: 2NH3+3O2 = 2HNO2 + 2H2O + 663600 Дж. В этом процессе участвуют нитрозные бактерии, объединенные С. Н. Виноградским в три рода: Nitrosomonas, Nitrosocystis, Nitrosospira. Nitrosomonas(типичный род) — бактерии овальной формы размером 1,0—1,5 мкм, подвижные, не образуют спор, грамотрицательные; они широко распространены в почве (рис. 21). С. Н. Виноградский различает пять разновидностей Nitrosomonas (a, b, с, d, e) по форме и отношению к среде. К роду Nitrosocystisпринадлежат шарообразные бактерии, образующие крупные зооглеи, окруженные общей капсулой, внутри которой находятся кокки величиной 1,5—2,0 мкм в диаметре (рис. 22). Род Nitrosospiraвключает бактерий спиральной формы, достигающих в длину 15—20 мкм. В старых культурах нити распадаются на гранулы кокковидной формы. По данным М. В. Федорова, представители рода Nitrosospiraразвиваются преимущественно в необрабатываемых почвах. На втором этапе нитрификации азотистая кислота окисляется в азотную: 2HNO2 + O2 = 2HNO3 + 201600 Дж. В этом процессе участвуют бактерии рода Nitrobacter— мелкие палочки длиной 1 мкм, неподвижные, грамотрицательные, спор не образуют. В качестве источника углерода нитрифицирующие бактерии используют углерод углекислого газа, а азот — в виде аммиака и нитратов. Нормальная нитрификация протекает при влажности 40—60 % полной влагоемкости почвы, достаточном снабжении ее кислородом воздуха, в слабокислой или щелочной среде (рН 6,2—9,2). Оптимальная температура для развития нитрифицирующих, бактерий 30—37◦ С. Нитрифицирующие бактерии распространены почти повсеместно. Они отсутствуют лишь в очень кислых почвах. Встречаются в изобилии в хорошо обработанных плодородных почвах. Значение для земледелия. 1.Нитраты являются необходимым элементом азотного питания растений. Процессу нитрификации способствует нейтральная реакция среды (рН = 7),влажность. 2. Отрицательным является то, что нитраты и нитриты - это подвижные соли, способные вымываться на глубину, где корневая система не в состоянии их усваивать. Денитрификация. Значительное количество нитратов почвы используется зелеными растениями, частично вымывается водой, частично усваивается почвенными микроорганизмами, превращающими их в белок цитоплазмы. Многие бактерии способны восстанавливать соли азотной кислоты и аммиак до свободного азота. Этот процесс, противоположный нитрификации, называется денитрификацией. Денитрификация приводит к снижению содержания азота в почве: NaNО3 → NaNО2 ® NH3 → N2 Процесс денитрификации обусловлен не только деятельностью, микроорганизмов, но также чисто химической реакцией между аминокислотами и, азотной кислотой, в результате чего также выделяется азот. Денитрификация, связанная с жизнедеятельностью бактерий, называется прямой денитрификацией, а связанная с чисто химической реакцией — косвенной. Прямая денитрификация вызывается факультативными анаэробами, которые, для питания не нуждаются в готовых азотистых органических веществах. Переводя нитраты в нитриты, факультативные анаэробы поглощают из этих соединений азот для синтеза белка тела, а углерод усваивают из безазотистых органических веществ. Для дыхания эти бактерии используют кислород нитратов вместо молекулярного кислорода. По типу питания денитрифицирующие бактерии принадлежат к гетеротрофам. Наиболее активны из этих бактерий следующие: 1. Bacteriumdeniirificans— маленькая (1,5—3,0 мкм), подвижная, не образующая спор почвенная палочка, способная восстанавливать только нитриты до молекулярного азота. 2. B. stutzeri— небольшая (2—4 мкм) бесспоровая, грамотрицательная, подвижная, постоянно встречающаяся в почве палочка. В анаэробных условиях она восстанавливает нитраты. 3. B. ftuorescens— подвижная, грамотрицательная, не образующая спор палочка. При низкой температуре вырабатывает и выделяет во внешнюю среду желто-зеленый пигмент. Способна восстанавливать нитраты до молекулярного азота. В природе денитрификаторы распространены очень широко: они постоянно встречаются в почве, навозе, сточных и загрязненных водах, реках, морях и океанах, в кале животных. Восстановление нитратов до молекулярного азота легко осуществляется только в анаэробных условиях, поэтому обработка почвы должна создать благоприятный водно-воздушный режим, который позволяет заглушать процессы денитрификации. Как уже было сказано, косвенная денитрификация— это результат химического взаимодействия между азотистой кислотой и аминокислотами. Поэтому все микроорганизмы, разлагающие белковые вещества до аминокислот и нитратов, способствуют этому процессу. Косвенная денитрификация проходит обычно в кислой среде, в связи с этим в хорошо окультуренных почвах с реакцией, близкой к нейтральной, она не имеет существенного значения. Значение: 1. Для агрономии – отрицательное, так как навоз обедняется доступным азотом. 2. Планетарное - способствует поддержанию баланса в природе его круговорот. 3. Очищает почву от скопления биологических масс, проводя их минерализацию. 3.5. Биологическая фиксация молекулярного азота. Биологическая фиксация азота имеет большое значение в повышении плодородия почвы и урожайности сельскохозяйственных культур, а также в экономии минеральных удобрений. Впервые азотфиксирующий микроорганизм был выделен в чистую культуру Н. С. Виноградским (1893). Это был анаэробный, спорообразующий, палочковидный азотфиксатор — C. pasteurianum. Позже, в 1901г., голландский микробиолог М. Бейеринк открыл аэробную азотфиксирующую бактерию рода Azotobacter . За последнее время способность фиксировать молекулярный азот выявлена у многих других видов бактерий, многочисленных водорослей и ряда почвенных грибов. Известны две основные группы азотфиксирующих бактерий: свободноживущие в почве и симбиотические. Из свободноживущих в почве азотфиксирующих бактерий наибольший интерес представляют бактерии рода Clostridiumи Azotobacter. C. pasteurianum— крупные толстые палочки длиной 1,5—8,0 мкм с перитрихально расположенными жгутиками, облигатные анаэробы. После образования спор клетка утолщается в середине или на конце клетки и принимает форму веретена. В качестве источника углеродного питания C. pasteurianumможет использовать моносахариды, дисахариды, некоторые полисахариды и органические кислоты. На 1 г сброженного сахара этот микроб может связывать до 10—12 мг азота. Бактерии этого рода для азотного питания могут использовать соли аммония, нитраты, а при дефиците азота усваивают молекулярный азот. Способностью фиксировать атмосферный азот обладают и другие виды рода Clostridium (C. pectinovorum, C. felsineum, C. butyricum). После открытия М. Бейеринком аэробного азотфиксатора — Azotobacterchroococcum, связывающего молекулярный азот, был описан ряд других видов из рода Azotobacter:A. beierinckii, A. agile. Размеры клеток азотобактера колеблются в пределах 2,0—7,0 × 1.0—2,5 мкм, в молодом возрасте они палочковидные, подвижные, а затем превращаются в крупные кокки-, покрываются капсулой и продуцируют пигмент. Все виды азотобактера — аэробы, гетеротрофы. Они могут ассимилировать азот из солей аммония, нитритов, нитратов и аминокислот, а при отсутствии связанных форм азота фиксируют молекулярный азот. В качестве источника углерода азотобактер использует различные сахара (гексозы, пентозы), одноатомные и многоатомные спирты (метиловый, этиловый, бутиловый, глицерин) и органические кислоты (уксусную, масляную и др.). Встречается азотобактер лишь в почвах с рН от 5,8 до 8,5. Оптимальная температура для его развития 28°С. По данным М. В. Федорова, усвоение свободного азота азотобактером осуществляется при участии фермента нитрогеноксидазы. Для нормального роста клеток и фиксации молекулярного азота азотобактер нуждается в фосфоре, кальции, сере, железе, калии и некоторых микроэлементах, особенно в молибдене или боре. В теле азотобактера фиксированный молекулярный азот аккумулируется в виде белковых соединений. Отмирая в почве, клетки минерализуются, и накопленный в них азот становится доступным растениям. Азотобактер синтезирует также ростовые вещества (типа ауксинов), стимулирующие рост и развитие растений витамины (биотин, инозит, тиамин, пиридоксин и др.). Особенно активно азотобактер размножается в высокоплодородных влажных почвах, а при дефиците увлажнения большинство клеток отмирает. В последнее время установлено, что многие почвенные микроорганизмы также обладают способностью связывать атмосферный азот. Так, описаны азотфиксаторы из семейств Pseudomonadaceae, Spirilaceae, Rhizobiaceae,Enterobacteriaceae и др. Азотфиксирующая способность установлена и у некоторых ми- кробактерий, актиномицетов, проактиномицетов и у отдельных грибов. Функция азотоусвоения широко распространена и среди сине-зеленых водорослей. К настоящему времени такая способность зарегистрирована почти у 40 видов этих организмов. Это различные виды родов Anabaena, Nostos, Calothrixи др. Симбиотическая фиксация азота. Свободный азот атмосферы связывается и накапливается в почве также особыми бактериями, представленными их симбиотическими ассоциациями с высшими растениями. На корнях бобовых растений можно увидеть бородавчатые круглые вздутия, наполненные белым мутным соком — клубеньки. У гороха, клевера, вики клубеньки образуются на мелких разветвлениях корней, у люпинов они находятся на главном корне. М. С. Ворониным (1865) и М. Бейеринком (1888) было установлено, что молекулярный азот усваивается живущими в клубеньках бактериями. Отсюда их и называют клубеньковыми Rhizobium. Молодые клубеньковые бактерии имеют форму палочек размером примерно 0,5—0,9 × 1,2—3,0 мкм, подвижны. Бактерии как в средах, так и в клубеньках формируют утолщения, разветвленные, грушевидные или сферические образования, которые значительно крупнее обычных клеток клубеньковых бактерий (1,2—1,6 × 2,0—4,0 мкм). Такие формы бактерий получили название бактероидов. Оптимальная температура для роста клубеньковых бактерий 24—26 °С. Все клубеньковые бактерии грамотрицательные, гетеротрофы, энергетическими источниками для них служат углеводы растений. Азот они фиксируют из атмосферы. Легко усваивают моносахариды и дисахариды, хуже — полисахариды. Кроме того, эти бактерии могут использовать в пищу и многоатомные спирты. Некоторые представители клубеньковых бактерий при использовании углеводов образуют слизистые вещества, содержащие стимуляторы роста (биотин). Эти слизистые вещества защищают бактерии от поражения бактериофагами и служат источниками углерода для некоторых рас клубеньковых бактерий. Клубеньковые бактерии могут использовать и различные соединения азота. Очень благоприятно влияет на их рост нитратный азот, хотя они способны усваивать аммиачный азот, пептоны и аминокислоты. Кроме необходимых макроэлементов (фосфор, калий, кальций) клубеньковые бактерии нуждаются в микроэлементах (железо, молибден, бор и др.). У клубеньковых бактерий резко выражена видовая специфичность (избирательность) по отношению к различным бобовым растениям. Каждому виду бобовых растений соответствует своя, особая раса бактерий. Микроб, выделенный из гороха, не приживается на корнях клевера или люцерны, и наоборот. В практике заслуживают внимания шесть разновидностей клубеньковых бактерий, специфичных для определенных растений: 1)Rhizobiumtrifoli — образуют клубеньки на корнях белого, красного и других видов клевера; 2)R. japonicutn— формирует клубеньки на корнях сои; 3)R. phaseoli— образует клубеньки на корнях фасоли; 4)R. meliloti— живет на корнях люцерны и донника; 5)R. leguminosarum— характерная культура клубеньков корней гороха, вики, чины и нута; 6)R. lupine— образует клубеньки на корнях люпинов. Клубеньковые бактерии проникают в ткань корня бобовых растений через корневые волоски. По мере продвижения по корневому волоску бактерии окутываются выделяемой ими слизью, образуют длинные слизи-стые нити или тяжи, напоминающие мицелий гриба. Эти образования получили название инфекционных нитей. Они глубоко проникают в корни растений, где бактерии интенсивно размножаются и стимулируют быстрое деление клеток вокруг бактериального очага, что и приводит к образованию клубенька. В тканях бобовых растений клубеньковые бактерии размножаются разными способами: в инфекционных нитях — делением: перегородкой, в цитоплазме растений— как изоморфным (сходное по форме), так и гете-роморфным (разноформенность) делением и почкованием (В. К. Шильникова, А. А. Авакян, Н. И. Коркина, 1969). Клубеньковые бактерии могут жить не только в клубеньках бобовых растений, но и самостоятельно в почве. Иногда удавалось выделить различные расы этих бактерий из почвы, на которой много лет не выращивали бобовые растения (М. В. Федоров). На развитие клубеньковых бактерий оказывает влияние реакция почвы. Так, почвы с рН ниже 6,0 содержат меньше бактерий, чем почвы, близкие к нейтральным или щелочным. Значительное снижение численности Rhizobiumв почве наблюдается зимой. Весной с повышением температуры почвы начинается быстрое размножение клубеньковых бактерий. Многочисленными исследованиями доказано, что у клубеньковых бактерий биохимические реакции фиксации азота аналогичны азотобактеру. Клубеньковые бактерии могут накопить за период вегетации 100—200 кг азота на 1 га. Фиксировать атмосферный азот могут также бактерии, живущие в клубеньках на корнях лоха, облепихи, сосны, лучистой ольхи и ряда других растений. Способны к фиксации азота и бактерии, живущие в узлах листьев некоторых тропических кустарников. Тема: «Влияние агроприёмов на почвенные микроорганизмы». 3.1. Возникновение и развитие почвенной микробиологии. Почвенная микробиология традиционно является областью интересов отечественной микробиологии. Начало ее лежит в трудах С.Н. Виноградского, особенно относящихся ко второму этапу его деятельности, основанному на применении прямых методов. Затем последовали работы ряда исследователей, из которых особенно нужно отметить Н.А. Красильникова, рассматривавшего почвенную микробиологию как синтетическую дисциплину "биология почв" с особенным вниманием к взаимодействию микроорганизмов с корневой системой растений, но так же учитывавшего роль грибов, почвенных водорослей, простейших. Однако впоследствии доминирование получила почвенная бактериология, особенно распространившаяся благодаря работам Е.Н. Мишустина. В развитии почвенной микробиологии огромное значение имели труды выдающихся русских микробиологов: В. В. Докучаева, П. А. Костычеаа, Д И, Ивановского, С. Н. Виноградского, В. Л. Омелянского, В Л, Исаченко, Н. Г. Холодного, Б. В. Перфильева, Н, А, Красильникова, Н. Н. Худякова, В. С. Буткевича и других исследователей. Почва как среда обитания микроорганизмов имеет ряд характерных особенностей: путь углерода ведет к образованию резервуара гумуса как стойкого органического вещества, доминирующей группой являются мицелиальные организмы - грибы и актиномицеты. 3.2. Микроорганизмы почвы, методы определения их состава и активности. Количество организмов в почве огромно. Растения, животные и микроорганизмы, обитающие в почве, находятся в постоянном взаимодействии друг с другом и со средой обитания. Данные взаимоотношения сложны и многообразны. Животные и бактерии потребляют растительные углеводы, жиры и белки. Благодаря этим взаимоотношениям и в результате коренных изменений физических, химических и биохимических свойств горной породы в природе постоянно происходят почвообразовательные процессы. В среднем почва содержит 2 — 3 кг/м2 живых растений и животных, или 20 — 30 т/га. При этом в умеренном климатическом поясе корни растений составляют 15 т/га, насекомые — 1 т, дождевые черви — 500 кг, нематоды —50, ракообразные — 40, улитки, слизни — 20, змеи, грызуны —20кг, бактерии — 3т, грибы — 3т, актиномицеты — 1,5 т, простейшие — 100 кг, водоросли — 100 кг на 1 гектар. Несмотря на неоднородность экологических условий в почве, она выступает как достаточно стабильная среда, особенно для подвижных организмов. Крутой градиент температур и влажности в почвенном профиле позволяет почвенным животными путем незначительных перемещений обеспечить себе подходящую экологическую обстановку. Неоднородность почвы приводит к тому, что для организмов разных размеров она выступает как разная среда. Для микроорганизмов особое значение имеет огромная суммарная поверхность почвенных частиц, потому что на них адсорбируется подавляющая часть микроорганизмов. Сложность почвенной среды создает большое разнообразие условий для самых разных функциональных групп: аэробов, анаэробов, потребителей органических и минеральных соединений. Для распределения микроорганизмов в почве характерна мелкая очаговость, поскольку на протяжении нескольких миллиметров могут сменяться разные экологические зоны. По степени связи с почвой как средой обитания животных объединяют в три экологические группы: геобионты геофилы и геоксены. Геобионты — животные, постоянно обитающие в почве. Весь цикл их развития протекает в почвенной среде. Геобионтами являются дождевые черви (Lymbricidae), многие первично-бескрылые насекомые (Apterydota). Геофилы — животные, часть цикла развития которых (чаще одна из фаз) обязательно проходит в почве. К этой группе принадлежит большинство насекомых: саранчовые (Acridoidea), ряд жуков (Staphylinidae, Carabidae, Elateridae), комары-долгоножки (Tipulidae). Их личинки развиваются в почве. Во взрослом же состоянии это типичные наземные обитатели. К геофилам принадлежат и насекомые, которые в почве находятся в фазе куколки. Геоксены — животные, иногда посещающие почву для временного укрытия или убежища. К геоксенам из насекомых относятся таракановые (Blattodea), многие полужесткокрылые (Hemiptera), некоторые развивающиеся вне почвы жуки. Сюда же относятся грызуны и другие млекопитающие, живущие в норах. Вместе с тем приведенная классификация не отражает роли животных в почвообразовательных процессах, так как в каждой группе есть организмы, активно передвигающиеся и питающиеся в почве и пассивные, которые пребывают в почве в период отдельных фаз развития (личинки, куколки или яйца насекомых). Почвенных обитателей в зависимости от их размеров и степени подвижности можно разделить на несколько групп. Микробиотип, микробиота — это почвенные микроорганизмы, составляющие основное звено детритной пищевой цепи, представляют собой как бы промежуточное звено между растительными остатками и почвенными животными. Сюда относятся, прежде всего, зеленые (Chlorophyta) и сине-зеленые (Cyanophyta) водоросли, бактерии (Bacteria), грибы (Fungi) и простейшие (Protozoa). По существу можно сказать, что это водные организмы, а почва для них — это система микроводоемов. Они живут в почвенных порах, заполненных гравитационной или капиллярной водой, как и микроорганизмы, часть жизни могут находиться в адсорбированном состоянии на поверхности частиц в тонких прослойках пленочной влаги. Многие из этих видов обитают и в обычных водоемах. Вместе с тем почвенные формы обычно мельче пресноводных и, кроме того, отличаются способностью значительное время находиться в инцистированном состоянии, пережидая неблагоприятные периоды. Так, пресноводные амебы имеют размеры 50—100 мкм, почвенные — 10—15 мкм. Жгутиковые не превышают 2—5 мкм. Почвенные инфузории также имеют мелкие размеры и могут в значительной степени менять форму тела. Мезобиотип, мезобиота — это совокупность сравнительно мелких, легко извлекающихся из почвы, подвижных животных. Сюда относятся почвенные нематоды (Nematoda), мелкие личинки насекомых, клещи (Oribatee), ногохвостки (Collembola) и др. Эта группа весьма многочисленна — от десятков и сотен тысяч до миллионов особей на 1м2 почвы. Питаются в основном детритом и бактериями. Клещи и насекомые нередко являются хищниками. Отдельные виды нематод паразитируют в корнях растений, зачастую сильно их повреждая. Для данной группы животных почва представляется как система мелких пещер. У них нет специальных приспособлений к рытью. Они ползают по стенкам почвенных полостей при помощи конечностей или червеобразно извиваясь. Насыщенный водяными парами почвенный воздух позволяет им дышать через покровы тела. Многие виды животных этой группы не имеют трахейной системы и весьма чувствительны к высыханию. Средством спасения от колебаний влажности воздуха для них является передвижение вглубь. Более крупные животные имеют некоторые приспособления, которые позволяют переносить временное снижение влажности почвенного воздуха: защитные чешуйки на теле, частичную непроницаемость покровов, сплошной толстенный панцирь. Периоды затопления почвы водой животные переживают, как правило, в пузырьках воздуха. Воздух задерживается вокруг их тела из-за несмачиваемости покровов, снабженных у большинства из них волосками, чешуйками и т. д. Пузырек воздуха служит для мелкого животного своеобразной «физической жаброй». Дыхание осуществляется за счет кислорода, диффундирующего в воздушную прослойку из окружающей среды. Животные мезо- и микробиотипов способны переносить зимнее промерзание почвы, что особенно является важным, так как большинство из них не может уходить вниз из слоев, подвергающихся воздействию отрицательных температур. Макробиотип, макробиота — это крупные почвенные животные, с размерами тела от 2 до 20 мм. К данной группе относятся личинки насекомых, многоножки, энхитреиды, дождевые черви и др. Почва для них является плотной средой, оказывающей значительное механическое сопротивление при движении. Они передвигаются в почве, расширяя естественные скважины путем раздвижения почвенных частиц либо роя новые ходы. Оба способа передвижения накладывают отпечаток на внешнее строение животных. У многих видов развиты приспособления к экологически более выгодному типу передвижения в почве — рытью с закупориванием за собой хода. Газообмен большинства видов данной группы осуществляется при помощи специализированных органов дыхания, но наряду с этим дополняется газообменом через покровы. У дождевых червей и энхитреид отмечается исключительно кожное дыхание. Роющие животные могут уходить из слоев, где возникает неблагоприятная обстановка. К зиме и в засуху они концентрируются в более глубоких слоях, большей частью в нескольких десятках сантиметров от поверхности. Мегабиотип, мегабиота — это крупные землерои, главным образом из числа млекопитающих. Многие из них проводят в почве всю жизнь (златокроты в Африке, слепушонки, цокоры, кроты Евразии, сумчатые кроты Австралии, слепыши и т.п.). Они прокладывают в почве целые системы ходов и нор. Приспособленность к роющему подземному образу жизни находит отражение во внешнем облике и анатомических особенностях этих животных: у них недоразвиты глаза, компактное вальковатое тело с короткой шеей, короткий густой мех, сильные компактные конечности с крепкими когтями. Помимо постоянных обитателей почвы среди крупных животных нередко выделяют отдельную экологическую группу обитателей нор. К данной группе животных относятся барсуки, сурки, суслики, тушканчики и др. Они кормятся на поверхности, однако размножаются, зимуют, отдыхают, спасаются от опасности в почве. Ряд других животных использует их норы, находя в них благоприятный микроклимат и укрытие от врагов. Обитатели нор, или норники, имеют черты строения, характерные для наземных животных, но в то же время обладают рядом приспособлений, связанных с роющим образом жизни. Так, для барсуков характерными чертами являются длинные когти и сильная мускулатура на передних конечностях, узкая голова, небольшие ушные раковины. К особой группе псаммофилов относят животных, заселяющих сыпучие подвижные пески. К типичным псаммофилам относятся мраморные хрущи из рода Polyphylla, личинки муравьиных львов (Myrmeleonida) и скакунов (Cicindelinae), большое количество перепончатокрылых (Hymenoptera). Почвенные животные, обитающие в подвижных песках, имеют специфические приспособления, которые обеспечивают им передвижение в рыхлом грунте. Как правило, это «минирующие» животные, раздвигающие частицы песка. У позвоночных псаммофилов конечности нередко устроены в форме своеобразных «песчаных лыж», облегчающих передвижение по рыхлому грунту. Например, у тонкопалого суслика и гребнепалого тушканчика пальцы покрыты длинными волосами и роговыми выростами. Как уже было отмечено выше, 25% всех почв нашей планеты засолено. Животных, приспособившихся к жизни на засоленных почвах, называют галофилами. Обычно в засоленных почвах фауна в количественном и качественном отношении сильно обедняется. Например, исчезают личинки щелкунов (Elateridae), хрущей (Melolonthinae), а вместе с тем появляются специфические галофилы, которые не встречаются в почвах обычной засоленности. Среди них можно отметить личинки некоторых пустынных жуков-чернотелок (Tenebrionidae). Представление о микробиологическом составе почв дают различные методы исследования (микроскопирование, посев на питательные среды, стекла обрастания, использование педоскопа и т. п.), позволяющие учесть численность, видовое разнообразие или суммарную активность отдельных микробиологических процессов (нитрификационную способность, дыхание, ферментативную активность и др.). При анализе почв устанавливают не только состав их микронаселения, но и суммарную биохимическую активность почв. Одним из показателей такой активности служит нитрификационная способность почвы, характеризующая мобилизуемость азотного запаса почвы в результате деятельности микроорганизмов. Нитрификационную способность устанавливают по нарастанию в почве количества нитратов после выдерживания при определенных условиях в термостате. По результатам такого анализа можно судить о потенциальной способности почвы накапливать то или иное количество минерального азота. Если в начале опыта в почву внести соль аммония, то по накоплению нитратов можно получить дополнительное представление об энергии работы нитрифицирующих бактерий. |
