физика. СРСП №6 физика. Молекулярная физика. Реальные газы. Явления переноса
 Скачать 19.88 Kb. Скачать 19.88 Kb.
|
|
МИНИСТЕРСТВО СЕЛЬСКОГО ХОЗЯЙСТВА РЕСПУБЛИКИ КАЗАХСТАН КАЗАХСКИЙ АГРОТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ ИМ. С.СЕЙФУЛЛИНА СРСП №6 Тема: Молекулярная физика. Реальные газы. Явления переноса. Выполнила: студентка группы БТ 18-15 Курганбаева А.Д. Астана 2018 Содержание: Молекулярная физика. Реальный газ. Молекулярная физика Молекулярная физика – раздел физики, в котором свойства вещества изучаются на основе его молекулярного (микроскопического) строения. Молекулярно-кинетической теорией (МКТ) называется теория, объясняющая строение и свойства тел движением и взаимодействием частиц, из которых состоят тела. В основе МКТ лежат следующие основные положения: все тела состоят из частиц, разделенных промежутками; частицы вещества находятся в непрерывном хаотическом движении; частицы взаимодействуют между собой. Атомом называется мельчайшая частица химического элемента. Атом электрически нейтрален. Размеры атома порядка 10-10 м. Атомы одного и того же химического элемента одинаковы. Атом состоит из положительно заряженного ядра и отрицательно заряженных электронов. В состав атомного ядра входят протоны и нейтроны. Атомы соединяются в молекулы. Молекула – наименьшая устойчивая частица данного вещества, обладающая его химическими свойствами. Размеры молекул 10-10–10-7 м. Молекулы одного вещества одинаковы. Молекулы электрически нейтральны. Реальный газ Реальным называется газ, между молекулами которого действуют силы межмолекулярного взаимодействия, состоящие из сил притяжения и сил отталкивания. Это уравнение может получено путем соответствующего изменения уравнения Менделеева-Клапейрона путем внесения в него поправок. Уравнение состояния реального газа (уравнение Ван-дер-Ваальса) для одного моля имеет вид: 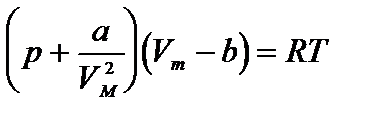 , ,где р - давление, оказываемое на стенки сосуда, VМ – объем одного моля газа, а и b - постоянные Ван-дер-Ваальса, имеющие для разных газов различные значения, определяемые опытным путем. |
