Название метода
 Скачать 340.68 Kb. Скачать 340.68 Kb.
|
|
Оптические методы. Название метода : Рефрактометрия С 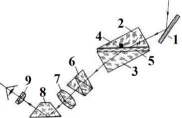 хема прибора : 1 – зеркало; хема прибора : 1 – зеркало; 2 – вспомогательная откидная призма; 3 – основная измерительная призма; 4 – матированная грань откидной призмы; 5 – исследуемая жидкость; 6 – призмы Амичи компенсатора; 7 – объектив зрительной трубы; 8 –поворотная призма; 9 – окуляр зрительной трубы. Условия проведения анализа : При стабильной температуре (20 ±0,3ºС) и длине волны линии D спектра натрия 589,3 нм. Основан на определении показателя преломления исслед вещества Определяемые вещества : Неорганические и органические ЛВ. Область применения : Определение концентраций ЛВ в растворах, для ряда веществ – установление подлинности и чистоты (эфирные масла). Измеряемая величина : Показатель преломления Расчеты : Концентрация раствора в процентах (С): 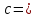 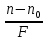 где n – показатель преломления раствора; n0 – показатель преломления растворителя; F – фактор, равный величине прироста показателя преломления при увеличении концентрации на 1%. Для количественного анализа лекарственной смеси, состоящей из двух или более компонентов, концентрация компонента: где C1, C2, Сn-1 – процентное содержание ЛВ, найденных химическим методом; F1, F2 – факторы растворов ЛВ, определяемых химическим Оптические методы. Н 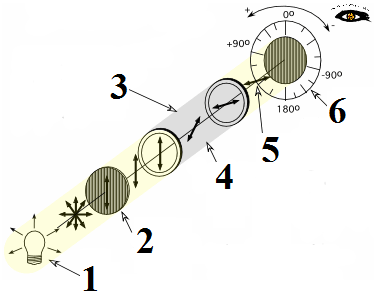 азвание метода : Поляриметрия азвание метода : ПоляриметрияСхема прибора 1 – источник света; 2 – неподвижный поляризатор; 3 – раствор оптически активного вещества; 4 – поляриметрическая трубка; 5 – плоскость поляризации света изменяется при прохождении через раствор; 6 – анализатор. Метод основан на способности веществ вращать плоскость поляризованного света Условия проведения анализа: При стабильной температуре (20 ±0,3ºС) и длине волны линии D спектра натрия 589,3 нм Определяемые вещества: Оптически активные вещества: антибиотики, алкалоиды, эфирные масла, белки, нуклеиновые кислоты, морфин, никотин, кислота винная и др. Область применения: Установление подлинности ЛВ;оценка чистоты ЛВ; определение концентраций ЛВ в растворах. Измеряемая величина: Угол вращения плоскости поляризации света Расчеты: Для растворов вращение удельное определяют по формуле где α – угол вращения; С – концентрация раствора, %; ℓ – толщина трубки, дм. Концентрация вещества в растворе: Спектральные методы. Н 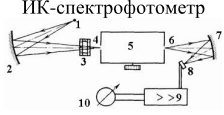 азвание метода : ИК-спектроскопия азвание метода : ИК-спектроскопияСхема прибора : 1 – источник непрерывного ИК- спектра; 2 – зеркало осветителя; 3 – кювета с исследуемым веществом; 4 – входная щель монохроматора;5 – монохроматор;6 – выходная щель монохроматора 7 – зеркало конденсора;8 – приёмник излучения; 9 – усилитель;10 – измерительный или регистрирующий прибор. Метод основан на поглощении энергии электромагнитного излучения по сопряженным системам ( двойные связи, неподеленные электр пары) Условия проведения анализа : Средняя ИК- область(4000 до 400 см-1) Определяемые вещества: Неорганические и органические ЛВ, биологически активные вещества растений и др Область применения: Установление подлинности ЛВ; оценка чистоты ЛВ, количествен ное определение ЛВ. Измеряемая величина: Пропускание (Т), оптическая плотность Расчеты: Расчет количественного содержания индивидуального вещества (Х): в субстанциях: 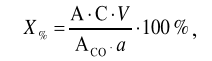 где Х – содержание индивидуального вещества, %; A и AСО оптическая плотность растворов исследуемого и стандартного образца соответственно; С – концентрация раствора стандартного образца, г/мл; а – точная масса лекарственного вещества, г; V – разведение, согласно НД, мл. Спектральные методы. Название метода: УФ-спектрофотометрия 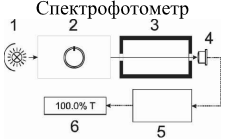 1 – источник излучения; 2 – монохроматор; 3 – кюветы с исследуемым раствором и растворителем; 4 – детектор (фотоэлемент); 5 – электронная схема; 6 – цифровой индикатор. 1 – источник излучения; 2 – монохроматор; 3 – кюветы с исследуемым раствором и растворителем; 4 – детектор (фотоэлемент); 5 – электронная схема; 6 – цифровой индикатор.Метод основан на поглощение монохроматического света, описываемого законом Бугера –Ламберта Бера. Условия определения анализа: Аналитическая область: УФ-(190-380нм),видимая область (380-800 нм) Определяемые вещества: Вещества способные поглощать монохроматическое излучение ЛВ, имеющие в структуре хромофорные группы (группы,содержащие в составе сопряженные двойные связи и неподеленные пары электронов). Область применения: Установление подлинности ЛВ; оценка чистоты ЛВ; определение количественного содержания ЛВ. Измеряемая величина: Оптическая плотность Расчеты: Расчет количественного содержания индивидуального вещества (Х): г 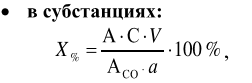 де Х – содержание индивидуального вещества, %; де Х – содержание индивидуального вещества, %;A и AСО - оптическая плотность растворов исследуемого и стандартного образца соответственно; С – концентрация раствора стандартного образца, г/мл; а – точная масса лекарственного вещества, г; V – разведение, согласно НД,мл. В твердых лек.формах г 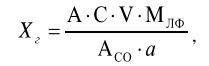 де Х – содержание индивидуального вещества, г; де Х – содержание индивидуального вещества, г; MЛФ – средняя масса таблеток, драже и др.; а – точная масса порошка растертых таблеток, драже и др., г. г 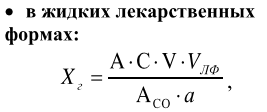 де Х – содержание индивидуального вещества, г; де Х – содержание индивидуального вещества, г; а – аликвота лекарственной формы; VЛФ – объем лекарственной формы по прописи. Расчет количественного содержания индивидуального вещества (Х) с учетом величины удельного коэффициента светопоглощения ( ): см Е 1% 1 В субстанциях г 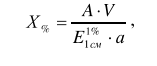 де, Х – содержание индивидуального вещества, %;см де, Х – содержание индивидуального вещества, %;смЕ1 1% - величина удельногокоэффициентасветопоглощения. В 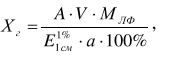 твердых лек.формах твердых лек.формах где Х – содержание индивидуального вещества, г; MЛФ – средняя масса таблеток, драже и др. В жидких лекарственных формах: 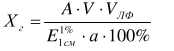 где Х – содержание индивидуального вещества, г; а – аликвота лекарственной формы; VЛФ – объем лекарственной формы по прописи . Спектральные методы. Название метода: Фотоэлектрокалориметрия Фотоэлектроколориметр 1 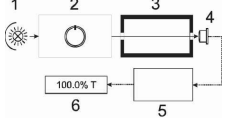 – источник излучения (лампа накаливания); 2 – светофильтр; 3 – кюветы с исследуемым раствором и растворителем; 4 – детектор (фотоэлемент); 5 – электронная схема; 6 – цифровой индикатор. – источник излучения (лампа накаливания); 2 – светофильтр; 3 – кюветы с исследуемым раствором и растворителем; 4 – детектор (фотоэлемент); 5 – электронная схема; 6 – цифровой индикатор. Метод основан на измерении степени поглощения немонохроматического света веществом с помощью фотолектрокалориметра Условия определения анализа: Видимая область спектра (360-780 нм). Определяемые вещества: Поглощают окрашенные вещества вещества: за счёт собственной окраски (рибофлавин) или за счёт окрашенных продуктов реакции определяемых веществ с реагентами (диазосоединения, гидроксаматы меди и пр.). Область применения: Определение количественного содержания ЛВ. Измеряемая величина: Оптическая плотность Расчеты: Расчет количественного содержания индивидуального вещества (Х): г 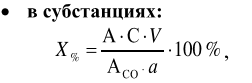 де Х – содержание индивидуального вещества, %; де Х – содержание индивидуального вещества, %;A и AСО - оптическая плотность растворов исследуемого и стандартного образца соответственно; С – концентрация раствора стандартного образца, г/мл; а – точная масса лекарственного вещества, г; V – разведение, согласно НД,мл. В твердых лек.формах г 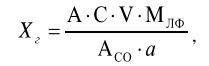 де Х – содержание индивидуального вещества, г; де Х – содержание индивидуального вещества, г; MЛФ – средняя масса таблеток, драже и др.; а – точная масса порошка растертых таблеток, драже и др., г. г 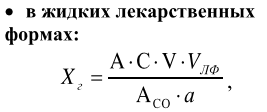 де Х – содержание индивидуального вещества, г; де Х – содержание индивидуального вещества, г; а – аликвота лекарственной формы; VЛФ – объем лекарственной формы по прописи. Расчет количественного содержания индивидуального вещества (Х) с учетом величины удельного коэффициента светопоглощения ( ): см Е 1% 1 В субстанциях г 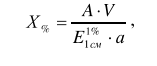 де, Х – содержание индивидуального вещества, %;см де, Х – содержание индивидуального вещества, %;смЕ1 1% - величина удельногокоэффициентасветопоглощения. В 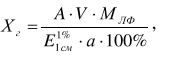 твердых лек.формах твердых лек.формах где Х – содержание индивидуального вещества, г; MЛФ – средняя масса таблеток, драже и др. В жидких лекарственных формах: 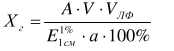 где Х – содержание индивидуального вещества, г; а – аликвота лекарственной формы; VЛФ – объем лекарственной формы по прописи . Спектральные методы. Название метода: Флуориметрия 1 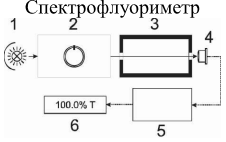 – источник излучения (лампа накаливания); 2 – светофильтр; 3 – кюветы с исследуемым раствором и растворителем; 4 – детектор (фотоэлемент); 5 – электронная схема; 6 – цифровой индикатор. – источник излучения (лампа накаливания); 2 – светофильтр; 3 – кюветы с исследуемым раствором и растворителем; 4 – детектор (фотоэлемент); 5 – электронная схема; 6 – цифровой индикатор. Метод основан на измерении флуоресценции - испускание света хим веществом Приборы 2х типов : 1) фильтрационный флуориметр. 2) спектрофлуориметр Условия определения анализа: Спектральная область от 250 до 800 нм, т.е. области: УФ (частично), видимую и начало ближнего ИК. Определяемые вещества: Органические ЛВ, имеющее собственное свечение или приобретающие его в результате химических реакций: адреналин, метилтио-урацил, папаверина гидрохлорид, прогестерон, производные α-бензопирона и др. Область применения: Установление подлинности ЛВ; определение количественного содержания ЛВ. Измеряемая величина: Интенсивность испускаемого излучения Расчеты: Расчетные формулы как в спектрофотометрии. Расчеты: Расчет количественного содержания индивидуального вещества (Х): г 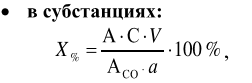 де Х – содержание индивидуального вещества, %; де Х – содержание индивидуального вещества, %;A и AСО - оптическая плотность растворов исследуемого и стандартного образца соответственно; С – концентрация раствора стандартного образца, г/мл; а – точная масса лекарственного вещества, г; V – разведение, согласно НД,мл. В твердых лек.формах г 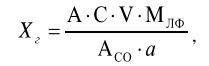 де Х – содержание индивидуального вещества, г; де Х – содержание индивидуального вещества, г; MЛФ – средняя масса таблеток, драже и др.; а – точная масса порошка растертых таблеток, драже и др., г. г 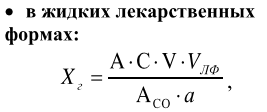 де Х – содержание индивидуального вещества, г; де Х – содержание индивидуального вещества, г; а – аликвота лекарственной формы; VЛФ – объем лекарственной формы по прописи. Расчет количественного содержания индивидуального вещества (Х) с учетом величины удельного коэффициента светопоглощения ( ): см Е 1% 1 В субстанциях г 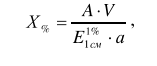 де, Х – содержание индивидуального вещества, %;см де, Х – содержание индивидуального вещества, %;смЕ1 1% - величина удельногокоэффициентасветопоглощения. В 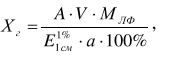 твердых лек.формах твердых лек.формах где Х – содержание индивидуального вещества, г; MЛФ – средняя масса таблеток, драже и др. В жидких лекарственных формах: 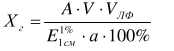 где Х – содержание индивидуального вещества, г; а – аликвота лекарственной формы; VЛФ – объем лекарственной формы по прописи . Хроматографические методы Название метода: Бумажная хроматография 1 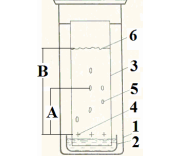 – хроматографическая камера; 2 – резервуар с растворителем; 3 – хроматографическая бумага; 4 – стартовые точки; 5 – разделенные компоненты; 6 – фронт растворителя. – хроматографическая камера; 2 – резервуар с растворителем; 3 – хроматографическая бумага; 4 – стартовые точки; 5 – разделенные компоненты; 6 – фронт растворителя. А – расстояние старт – пятно определяемого вещества; В – расстояние старт – фронт. Метод основан на разделении веществ Условия определения анализа: 1. Пробы наносят специальной микропипеткой, диаметр пятна 3-4 мм; 2. использовать смесь нескольких растворителей с разной полярностью; 3. хроматографирование проводят в камерах с герметично закрытой крышкой и насыщенных парами растворителей; 4. хроматографирование заканчивается, когда фронт растворителя почти достигнет края бумаги. Определяемые вещества: Неорганические и органические ЛВ, биологически активные вещества растений (флавоноиды, сахара и др.) Область применения: Установление подлинности ЛВ; оценка чистоты ЛВ; определение количественного содержания ЛВ. Измеряемая величина: Величина Rf (Rate fraction – скорость фракции), Rs. Расчеты: Качественный анализ: 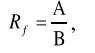 где A – расстояния от центра пятна на пластинке до линии старта; B – расстояние, пройденное растворителем от линии старта до финиша. 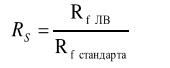 Количественный анализ: 1. Непрямое определение: вещество сначала элюируют из бумаги, а затем определяют спектрофотометрическим, люминесцентным, полярографическим м др. методами анализа. 2. Прямое определение: 2.1. сравнивают площадь пятен анализируемых веществ со стандартом (полуколичественный анализ); 2.2. используют денситометрию, основанную на измерении оптической плотности разделенных зон. Хроматографические методы Название метода: Хроматография в тонком слое сорбента 1 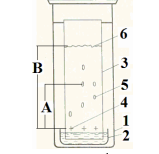 – хроматографическая камера; 2 – резервуар с растворителем; 3 – хроматографическая пластина; 4 – стартовые точки; 5 – разделенные компоненты; 6 – фронт растворителя. А – расстояние старт – пятно определяемого вещества; В – расстояние старт – фронт. – хроматографическая камера; 2 – резервуар с растворителем; 3 – хроматографическая пластина; 4 – стартовые точки; 5 – разделенные компоненты; 6 – фронт растворителя. А – расстояние старт – пятно определяемого вещества; В – расстояние старт – фронт. Условия определения анализа: Как в бумажной хроматографии. Определяемые вещества: Неорганические и органические ЛВ, биологически активные вещества растений. Область применения: Установление подлинности ЛВ; оценка чистоты ЛВ; определение количественного содержания ЛВ. Измеряемая величина: Величина Rf (Rate fraction – скорость фракции), Rs Расчеты: Качественный анализ: 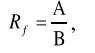 где A – расстояния от центра пятна на пластинке до линии старта; B – расстояние, пройденное растворителем от линии старта до финиша. 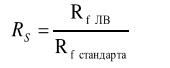 Количественный анализ: 1. Непрямое определение: вещество сначала элюируют из бумаги, а затем определяют спектрофотометрическим, люминесцентным, полярографическим м др. методами анализа. 2. Прямое определение: 2.1. сравнивают площадь пятен анализируемых веществ со стандартом (полуколичественный анализ); 2.2. используют денситометрию, основанную на измерении оптической плотности разделенных зон. Хроматографические методы Название метода: Газожидкостная хроматография 1 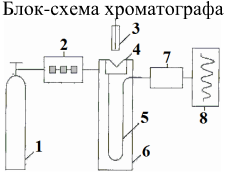 – баллон с сжатым газом; 2 – блок подготовки газа- носителя (регулятор, измеритель, фильтр); 3 – микрошприц для введения пробы; 4 – испаритель; 5 – хроматографическая колонка; 6 – термостат; 7 – детектор; 8 – регистратор. – баллон с сжатым газом; 2 – блок подготовки газа- носителя (регулятор, измеритель, фильтр); 3 – микрошприц для введения пробы; 4 – испаритель; 5 – хроматографическая колонка; 6 – термостат; 7 – детектор; 8 – регистратор. Условия определения анализа: 1. Неподвижная фаза – высококипящая жидкость, нанесенная в виде тонкой пленки на твердый носитель, подвижная фаза – газ; 2. газ-носитель должен быть инертным, чистым, иметь как можно меньшую вязкость, обеспечивать высокую чувствительность детектора, взрывобезопасным, доступным (гелий, азот, аргон); 3. летучесть компонентов анализируемой смеси и их устойчивость при повышенной температуре разделительной колонки. Определяемые вещества: Лекарственные средства, биологически активные вещества растений, пищевые продукты, белки и др. Область применения: Установление подлинности ЛВ; оценка чистоты ЛВ; определение количественного содержания ЛВ. Измеряемая величина: Время удерживания (tR) Расчеты: Качественный анализ: г tR0 – время пребывания вещества в подвижной фазе; tRs – время пребывания вещества в неподвижной фазе. Количественный анализ: 1. Метод абсолютной градуировки используют при определении не всех компонентов анализируемой смеси, а только одного или двух, (анализ примесей). г 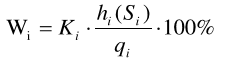 де Wi – массовая доля определяемого компонента, %; де Wi – массовая доля определяемого компонента, %; qi – величина пробы, мкл или мкг; Ki – градуировочный множитель; hi(Si) – высота (площадь) пика, мм (мм2). 2. Метод внутренней нормализации основан на том предположении, что вещества, взятые в одинаковом количестве, дают одну и ту же площадь пика, независимо от их строения. Это приближенно выполняется, если вещества химически сходны. г 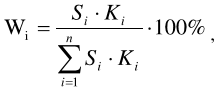 де Ki – градуировочный коэффициент i-го компонента, который определяют экспериментально или используют литературные данные. де Ki – градуировочный коэффициент i-го компонента, который определяют экспериментально или используют литературные данные. 3. Метод внутреннего стандарта используют, если при анализе многокомпонентной смеси необходимо определить содержание одного или двух компонентов. о 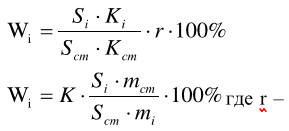 тношение массы внутреннего стандарта в смеси к массе анализируемого вещества; тношение массы внутреннего стандарта в смеси к массе анализируемого вещества; Кi, Kст, Si, Sст – градуировочные коэффициенты, площади анализируемого компонента и стандартного вещества. Хроматографические методы Название метода: Высокоэффективная жидкостная хроматография 1 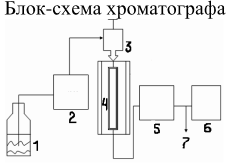 – сосуд для элюента; 2 – насос высокого давления; 3 – устройство для ввода пробы; 4 – хроматографическая колонка; 5 – детектор; – сосуд для элюента; 2 – насос высокого давления; 3 – устройство для ввода пробы; 4 – хроматографическая колонка; 5 – детектор; 6 – система обработки результатов, самописец; 7 – слив. Метод основан на разделении веществ Условия определения анализа: 1.Подвижная фаза (ПФ) – жидкость, неподвижная фаза (НФ) – тонко измельченная твердая основа, либо жидкость, нанесенная на твердую подложку; 2. исследуемые вещества должны растворяться в ПФ, удерживаться НФ. 3. выполняется под повышенным давлением. Определяемые вещества: Неорганические и органические ЛВ, смесь аминокислот и белков, биологически активные вещества растений и др Область применения: Установление подлинности ЛВ; оценка чистоты ЛВ; определение количественного содержания ЛВ. Измеряемая величина: Время удерживания (tR) Расчеты: Качественный анализ: г tR0 – время пребывания вещества в подвижной фазе; tRs – время пребывания вещества в неподвижной фазе. Количественный анализ: 1. Метод абсолютной градуировки используют при определении не всех компонентов анализируемой смеси, а только одного или двух, (анализ примесей). г 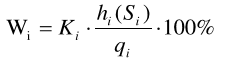 де Wi – массовая доля определяемого компонента, %; де Wi – массовая доля определяемого компонента, %; qi – величина пробы, мкл или мкг; Ki – градуировочный множитель; hi(Si) – высота (площадь) пика, мм (мм2). 2. Метод внутренней нормализации основан на том предположении, что вещества, взятые в одинаковом количестве, дают одну и ту же площадь пика, независимо от их строения. Это приближенно выполняется, если вещества химически сходны. г 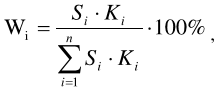 де Ki – градуировочный коэффициент i-го компонента, который определяют экспериментально или используют литературные данные. де Ki – градуировочный коэффициент i-го компонента, который определяют экспериментально или используют литературные данные. 3. Метод внутреннего стандарта используют, если при анализе многокомпонентной смеси необходимо определить содержание одного или двух компонентов. о 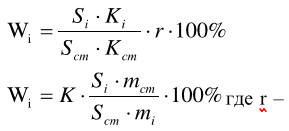 тношение массы внутреннего стандарта в смеси к массе анализируемого вещества; тношение массы внутреннего стандарта в смеси к массе анализируемого вещества; Кi, Kст, Si, Sст – градуировочные коэффициенты, площади анализируемого компонента и стандартного вещества Хроматографические методы Название метода: Ионообменная хроматография 1 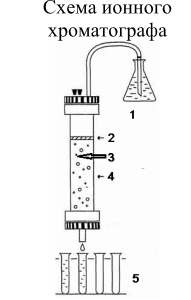 – элюент; 2 – исследуемый раствор; 3 – катионобменник; 4 – хроматографическая колонка; 5 – коллектор для сбора фракций. – элюент; 2 – исследуемый раствор; 3 – катионобменник; 4 – хроматографическая колонка; 5 – коллектор для сбора фракций. Условия определения анализа: 1. Подвижная фаза – ионные растворы (соли, кислоты и основания, буферы); 2. Неподвижная фаза – аниониты, которые имеют на поверхности положительно заряженные группы; катиониты содержат группы с отрицательным зарядом. Метод основан на разделении веществ Определяемые вещества: Соли органических и минеральных кислот, соли алкалоидов и азотистых оснований. Область применения: Разделение и выделение ЛВ с последующим количественным определением продуктов ионного обмена физическим, физико-химическим или химическим методом анализа. Измеряемая величина: Объем титранта, который пойдет на титрование продуктов ионного обмена. Расчеты: Количественное содержание ЛВ вычисляют по формуле прямого титрования (в случае определения продуктов ионного обмена химическим методом). Электрохимические методы Название метода: Потенциометрия 1  – блок потенциометрической ячейки; 2 – блок автоматического титрования; 3 – бюретка с титрованным раствором; 4 – потенциометр (рН- метр, иономер); 5 – самописец; 6 – мешалка. – блок потенциометрической ячейки; 2 – блок автоматического титрования; 3 – бюретка с титрованным раствором; 4 – потенциометр (рН- метр, иономер); 5 – самописец; 6 – мешалка. Метод основан на разделении веществ Условия определения анализа: 1. Электрохимическая ячейка с индикаторным электродом и электродом сравнения, 2. Потенциал индикаторного электрода должен зависеть от концентрации определяемых ионов. 3. Потенциал электрода сравнения должен быть постоянным. Определяемые вещества: Неорганические и органические кислоты, основания и соли (галогениды, роданиды, сульфиды), соли Mg2+, Сa2+, Al3+ , Bi3+. Область применения: Определение рН; установление концентрации отдельных ионов Измеряемая величина: Электродвижущая сила (ЭДС) электродной пары в точке эквисалентности. Расчеты: Строится интегральная кривая потенциометрического титрования в координатах: потенциал индикаторного электрода (Е) - объем титранта (V). Точка перегиба на кривой отвечает точке эквивалентности. Концентрацию определяемого иона рассчитывают по формуле: 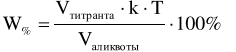 где W – концентрация определяемого иона, %; Vаликвоты – объем аликвоты для анализа. Электрохимические методы Название метода: Полярография Полярографическая установка 1 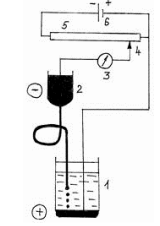 - электролизёр; 2 - сосуд с ртутью; 3 - гальванометр; 4 - передвижной контакт; 5 - реохорд; 6 - аккумулятор. - электролизёр; 2 - сосуд с ртутью; 3 - гальванометр; 4 - передвижной контакт; 5 - реохорд; 6 - аккумулятор. Метод основан на получении вольтамперных кривых, проводят электролиз раствора получают зависимость силы тока от приложенного к электролитической ячейке ( напряжение) Условия определения анализа: В исследуемый раствор погружаются 2 электрода: поляризующий – капельный ртутный электрод, не поляризующийся ртутный электрод. Определяемые вещества: Соли Cd, Pb, Cu, Zn, Sn, Hg, As, Ni, Co, Cr, Fe, Se, Mn, Mo Область применения: Установление подлинности ЛВ; определение количественного содержания ЛВ Измеряемая величина: Сила диффузионного тока (высота волны) Расчеты: 1. Метод стандартных растворов: 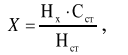 где Сст – концентрация раствора стандартного образца; Hx – высота волны исследуемого раствора; где Сст – концентрация раствора стандартного образца; Hx – высота волны исследуемого раствора; Hст – высота волны стандартного образца. 2. Метод добавок: 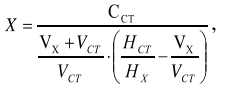 где Сст – концентрация раствора добавляемого стандартного образца; Hx – высота волны исследуемого раствора; Hст – высота волны, полученная после прибавления стандартно- го раствора. Vx – объем исследуемого раствора; Vст – объем прибавлен-ного стандартного раствора. где Сст – концентрация раствора добавляемого стандартного образца; Hx – высота волны исследуемого раствора; Hст – высота волны, полученная после прибавления стандартно- го раствора. Vx – объем исследуемого раствора; Vст – объем прибавлен-ного стандартного раствора. |
