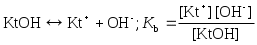
Значения Кb приведены для температуры 298,15 К
Название
|
Формула
|
Кb
|
рК=-lgКb
|
Алюминия гидроксид
|
Al(OH)3
|
|
|
К3
|
|
1,38 10-9
|
8,86
|
Аммиака раствор
|
H3N+H2O
|
1,76 10-5
|
4,76
|
Бария гидроксид
|
Ba(OH)2
|
|
|
К2
|
|
2,3 10-1
|
0,64
| Бериллия гидроксид |
Be(OH)2
|
|
|
K2
|
|
5,0 10–11
|
10,30
|
Вода
|
H2O
|
1,8 10-16
|
15,76
|
Ванадия (III) гидроксид
|
V(OH)3
|
|
|
K3
|
|
8,3 · 10-12
|
11,08
|
Гидразина раствор
|
N2H4 + H2O
|
9,3 10-7
|
6,03
|
Гидроксиламина
раствор
|
NH2OH + H2O
|
8,9 10-9
|
8,05
|
Галлия (III) гидроксид
|
Ga(OH)3
|
|
|
K2
|
|
1,6 10-11
|
10,80
|
K3
|
|
4,0 10-12
|
11,40
|
Железа (II) гидроксид
|
Fe(OH)2
|
|
|
К2
|
|
1,3 10-4
|
3,89
|
Железа (III) гидроксид
|
Fe(OH)3
|
|
|
К2
|
|
1,82 10-11
|
10,74
|
К3
|
|
1,35 10-12
|
11,87
|
Кадмия (II) гидроксид
|
Cd(OH)2
|
|
|
К2
|
|
5,0 10-3
|
2,30
|
Кальция гидроксид
|
Ca(OH)2
|
|
|
К2
|
|
4,0 10-2
|
1,40
|
Кобальта (II) гидроксид
|
Co(OH)2
|
|
|
К2
|
|
4,0 10-5
|
4,40
|
Кобальта (III) гидроксид
|
Со(ОН)3
|
|
|
К3
|
|
7,0 10–13
|
12,15
|
Лития гидроксид
|
LiOH
|
6,8 10-1
|
0,17
|
Название
|
Формула
|
Кb
|
рК=-lgКb
|
Магния гидроксид
|
Mg(OH)2
|
|
|
К2
|
|
2,5 10-3
|
2,60
|
Марганца (II) гидроксид
|
Mn(OH)2
|
|
|
К2
|
|
5,0 10-4
|
3,30
|
Меди (II) гидроксид
|
Cu(OH)2
|
|
|
К2
|
|
3,4 10-7
|
6,47
|
Натрия гидроксид
|
NaOH
|
5,9
|
0,77
|
Никеля гидроксид
|
Ni(OH)2
|
|
|
К2
|
|
1,0 10-4
|
4,00
|
Свинца (II) гидроксид
|
Pb(OH)2
|
|
|
К1
|
|
9,6 10-4
|
3,02
|
К2
|
|
3,0 10-8
|
7,52
|
Серебра гидроксид
|
AgOH
|
5,0 10-3
|
2,30
|
Стронция гидроксид
|
Sr(OH)2
|
|
|
К2
|
|
1,5 10-1
|
0,82
|
Хрома (III) гидроксид
|
Cr(OH)3
|
|
|
К3
|
|
1,02 10-10
|
9,99
|
Цинка гидроксид
|
Zn(OH)2
|
|
|
К1
|
|
4,0 10-5
|
4,40
|
К2
|
|
2,0 10–9
|
8,70
|
Значение ионного произведения воды (Кw)
при различных температурах
-
Температура, °С
|
Ионное произведение воды Кw
|
рН
|
0
|
0,11 · 10–14
|
7,48
|
20
|
0,69 · 10–14
|
|
25
|
1,00 · 10–14
|
7,00
|
40
|
2,95 · 10–14
|
|
60
|
9,55 · 10–14
|
|
80
|
25,10 · 10–14
|
|
100
|
55,00 · 10–14
|
6,13
|
Степень гидролиза солей в 0,1 М растворах при 25 °С
Соль |
Степень гидролиза, %
| Соль |
Степень гидролиза, %
|
NH4Cl
|
0,007
|
NaH2PO4
|
0,0004
|
NH4CH3COO
|
0,5
|
Na2CO3
|
4,0
|
(NH4)2S
|
99,0
|
NaHCO3
|
0,005
|
NH4HS
|
7,0
|
Na2S
|
99,0
|
Na2B4O7
|
0,5
|
NaHS
|
0,10
|
Na2SO3
|
0,13
|
NaClO
|
0,18
|
Na
|
0,0002
|
KCN
|
1,2
|
NaCH3COO
|
0,007
|
Al2(SO4)3
|
3,5
|
Na3PO4
|
34,0
|
Al(CH3COO)3
|
40,0
|
Na2HPO4
|
0,13
|
Fe(CH3COO)3
|
32,0
|
|
 Скачать 1.91 Mb.
Скачать 1.91 Mb.