Sn (г)
302,1
|
267,3
|
168,4
|
Sn (к, белое)
|
0
|
0
|
51,6
|
Sn (к, серое)
|
–2,1
|
–0,13
|
44,2
|
Sn2+ (р)
|
–10,5
|
–27,3
|
–22,7
|
Sn4+ (р)
|
–2,43
|
–2,4
|
–226,1
|
SnCl4 (ж)
|
–528,9
|
–457,7
|
299,6
|
SnH4 (г)
|
162,3
|
187,8
|
228,7
|
SnO (к)
|
–286,0
|
–256,9
|
56,5
|
SnO2 (к)
|
–580,8
|
–519,9
|
52,3
|
Sn(OH)2 (к)
|
–506,3
|
–491,6
|
87,7
|
Sn(OH)4 (к)
|
-
|
-946
|
155
|
SnS (к)
|
–110,2
|
–108,3
|
77,0
|
SnS2 (к)
|
–82,5
|
–74,1
|
87,5
|
SnSO4 (к)
|
–887
|
-
|
-
|
Sn(SO4)2 (к)
|
–1650
|
–1451
|
155,2
|
Sr (г)
|
164
|
130,9
|
135,1
|
Sr (к)
|
0
|
0
|
53,1
|
Sr2+ (р)
|
–545,5
|
–557,3
|
–26,3
|
SrCO3 (к)
|
–1218,4
|
–1137,6
|
97,1
|
SrCl2 (к)
|
–828,4
|
–781,2
|
117
|
SrF2 (к)
|
–1209,2
|
–1160,6
|
81,6
|
SrI2 (к)
|
–566,9
|
–559,8
|
159
|
Sr(NO3)2 (к)
|
–975,9
|
–778,2
|
195,5
|
Вещество
|
 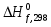 , кДж/моль , кДж/моль
|
Gf,298, кДж/моль
|
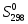 , ,
Дж/(моль К)
|
SrO (к)
|
–590,4
|
–559,8
|
54,4
|
Sr(OH)2 (к)
|
–959,4
|
–870,3
|
86,6
|
SrS (к)
|
–452,3
|
–447,7
|
68,2
|
SrSO4 (к)
|
–1451,0
|
–1334,3
|
119,7
|
Ta (г)
|
781,99
|
739,2
|
185,1
|
Ta (к)
|
0
|
0
|
41,5
|
TaCl5 (к)
|
–857,9
|
–750,5
|
238
|
TaF5 (к)
|
–1903,6
|
–1790,8
|
170
|
Ta2O5 (к)
|
–2045,14
|
–1909,99
|
143,01
|
Tc (г)
|
648,52
|
604,55
|
180,96
|
Tc (к)
|
0
|
0
|
33,5
|
Tc2O7 (к)
|
–1114,6
|
–937,8
|
191,5
|
TcO4– (р)
|
–723,8
|
–630,24
|
313,8
|
HTcO4 (к)
|
–700,49
|
–591,07
|
139,33
|
Te (г)
|
191,7
|
152,0
|
182,4
|
Te (к)
|
0
|
0
|
49,56
|
TeF6 (к)
|
–1323,0
|
–1226,4
|
337,26
|
TeO2 (г)
|
–51,9
|
–57,3
|
271,9
|
TeO2 (к)
|
–322,6
|
–270,2
|
79,8
|
H2Te (г)
|
99,7
|
85,16
|
228,8
|
Ti (г)
|
–471,12
|
426,53
|
180,2
|
Ti (к)
|
0
|
0
|
30,6
|
TiBr4 (к)
|
–619,2
|
–592
|
243,5
|
TiC (к)
|
–209
|
–205,7
|
24,7
|
TiCl2 (к)
|
–516,7
|
–472,67
|
105,85
|
TiCl3 (к)
|
–719,6
|
–653,96
|
130,12
|
TiCl4 (г)
|
–763,2
|
–726,12
|
352,23
|
TiCl4 (ж)
|
–804,2
|
–737,4
|
252,4
|
TiF4 (аморф.)
|
–1646,3
|
–1559,2
|
133,95
|
TiH2 (к)
|
–144,35
|
–105,13
|
29,71
|
TiI4 (г)
|
–287
|
–337,7
|
432,97
|
TiI4 (к)
|
–386,6
|
–381,6
|
246
|
TiN (к)
|
–336,81
|
–308,1
|
30,1
|
Вещество
|
 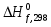 , кДж/моль , кДж/моль
|
Gf,298, кДж/моль
|
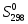 , ,
Дж/(моль К)
|
TiO (к)
|
–526,3
|
–496,93
|
34,79
|
TiO2 (к, рутил)
|
–943,9
|
–888,6
|
50,33
|
Ti2O3 (к)
|
–1518
|
–1431,0
|
77,3
|
H2TiO3 (к)
|
-
|
–1058,55
|
-
|
Ti(OH)3 (к)
|
–1188,26
|
-
|
-
|
Tl (к)
|
0
|
0
|
64,18
|
TlBr (к)
|
–172,7
|
–167,4
|
122,6
|
TlCl (к)
|
–204,1
|
–185,0
|
111,5
|
TlCl3 (к)
|
–311,3
|
–290,8
|
-
|
Tl2O (к)
|
–167,4
|
–153,1
|
161,1
|
Tl2O3 (к)
|
–390,4
|
–321,4
|
148,1
|
TlOH (к)
|
–233,5
|
–190,6
|
255,2
|
Tl(OH)3 (к)
|
–516,6
|
-
|
102,1
|
V (г)
|
515,34
|
469,49
|
182,2
|
V (к)
|
0
|
0
|
28,9
|
V2+ (р)
|
–221,9
|
–218,1
|
–114,32
|
V3+ (р)
|
–257,9
|
–242,8
|
–217,53
|
VCl2 (к)
|
–452,17
|
–406,12
|
97,1
|
VCl3 (к)
|
–582,41
|
–516,52
|
130,96
|
VCl4 (ж)
|
–569,8
|
–505,6
|
259
|
VF2 (к)
|
–837,4
|
–791,3
|
77,5
|
VF5 (ж)
|
–1480,9
|
–1378,4
|
191,9
|
VN (к)
|
–217,15
|
–191,21
|
37,28
|
VO (к)
|
–431,8
|
–402,6
|
33,6
|
VO2+ (р)
|
-
|
–456,06
|
–108,78
|
VO2 (к)
|
–720
|
–665
|
51,57
|
V2O3 (к)
|
–1219,1
|
–1139,4
|
98,3
|
V2O5 (к)
|
–1552
|
–1421,2
|
131
|
W (г)
|
844,33
|
802,26
|
173,85
|
W (к)
|
0
|
0
|
32,7
|
WC (к)
|
–41,0
|
–39,5
|
35
|
W(CO)6 (г)
|
–876,96
|
–825,9
|
4,184
|
WF6 (г)
|
–1721,5
|
–1635,9
|
353,5
|
Вещество
|
 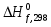 , кДж/моль , кДж/моль
|
Gf,298, кДж/моль
|
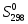 , ,
Дж/(моль К)
|
WO2 (к)
|
–589,63
|
–533,87
|
50,55
|
WO3 (к)
|
–842,7
|
–763,9
|
75,94
|
WO2Cl2 (к)
|
–835,54
|
–753,8
|
186,61
|
WO42– (р)
|
–1115,45
|
–920,48
|
62,76
|
H2WO4 (к)
|
–1132
|
–1036,4
|
117,2
|
Y (г)
|
426,77
|
384,9
|
-
|
Y (к)
|
0
|
0
|
46,0
|
YCl3 (к)
|
–982,4
|
–900
|
136,8
|
Y2O3 (к)
|
–1904
|
–1800
|
99,2
|
Y(OH)3 (к)
|
–1412,5
|
–1290,0
|
96,3
|
Zn (г)
|
130,73
|
95,19
|
160,87
|
Zn (к)
|
0
|
0
|
41,63
|
Zn2+ (р)
|
–153,74
|
–147,26
|
–110,67
|
ZnBr2 (к)
|
–329,7
|
–312,4
|
136
|
ZnCO3 (к)
|
–810,74
|
–732,48
|
92,47
|
ZnCl2 (к)
|
–415,05
|
–369,4
|
111,5
|
ZnF2 (к)
|
–764,4
|
–713,5
|
73,68
|
ZnI2 (к)
|
–208,2
|
–209,3
|
161,5
|
Zn(NH3)42+ (р)
|
–67,7
|
–53,64
|
-
|
Zn(NO3)2 (к)
|
–514,63
|
–298,82
|
193,72
|
Zn(NO3)2 2H2O (к)
|
–1111,05
|
–795,9
|
258,21
|
Zn(NO3)2 6H2O (к)
|
–2306,8
|
–1174,9
|
462,3
|
ZnO (к)
|
–350,6
|
–320,7
|
43,64
|
Zn(OH)2 (к, ромб)
|
–645,4
|
–555,9
|
76,99
|
Zn(OH)42– (р)
|
-
|
–905,42
|
-
|
ZnS (к)
|
–205,4
|
–200,7
|
57,74
|
ZnSO4 6H2O (к)
|
–2780,83
|
–2325,56
|
363,8
|
ZnSO4 7H2O
|
–3078,5
|
–2563,9
|
388,7
|
Zr (г)
|
608,42
|
565,97
|
181,24
|
Zr (к)
|
0
|
0
|
39,0
|
ZrC (к)
|
–206,7
|
–197,4
|
33,3
|
ZrCl4 (к)
|
–979,8
|
–889,3
|
181,4
|
Вещество
|
 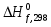 , кДж/моль , кДж/моль
|
Gf,298, кДж/моль
|
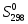 , ,
Дж/(моль К)
|
ZrF4 (к)
|
–1911,3
|
–1809,9
|
104,6
|
ZrO2 (к)
|
–1100,6
|
–1042,8
|
50,38
|
ZrOCl2 (к)
|
–986,6
|
–992,4
|
-
|
ZrOCl2 8H2O (к)
|
–3468
|
–2988,96
|
-
|
Константы ионизации кислот
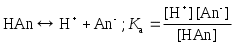
Значения Ka приведены для температуры 298,15 К
-
Название
|
Формула
|
Ка
|
рК=-lg Ка
|
Азотистая
|
HNO2
|
6,9 10-4
|
3,16
|
Борная
|
H3BO3
|
7,1 10-10
|
9,15
|
Бромноватая
|
HBrO3
|
2,0 10-1
|
0,70
|
Бромноватистая
|
HBrO
|
2,2 10-9
|
8,66
|
Вода
|
H2O
|
1,8 10-16
|
15,76
|
Германиевая
|
H4GeO4
|
|
|
К1
|
|
7,9 10-10
|
9,10
|
К2
|
|
2,0 10-13
|
12,7
|
Иодная
|
H5IO6
|
|
|
К1
|
|
2,5 10-2
|
1,61
|
К2
|
|
4,3 10-9
|
8,33
|
К3
|
|
1,0 10-15
|
15,0
|
Иодноватая
|
HIO3
|
1,7 10-1
|
0,77
|
Иодноватистая
|
HIO
|
2,3 10-11
|
10,64
|
Кремневая
|
H4SiO4
|
|
|
К1
|
|
1,3 10-10
|
9,9
|
К2
|
|
1,6 10-12
|
11,8
|
К3
|
|
2,0 10-14
|
13,7
|
Лимонная
|
(СН2СООН)2–С(ОН)СООН
|
|
|
К1
|
|
7,4 10-4
|
3,13
|
К2
|
|
2,2 10-5
|
4,66
|
К3
|
|
4,0 10-7
|
6,40
|
Название
|
Формула
|
Ка
|
рК=-lg Ка
|
Марганцовистая
|
H2MnO4
|
|
|
К1
|
|
10-1
|
1
|
К2
|
|
7,1 10-11
|
10,15
|
Мышьяковая
|
H3AsO4
|
|
|
К1
|
|
5,6 10-3
|
2,25
|
К2
|
|
1,7 10-7
|
6,77
|
К3
|
|
2,9 10-12
|
11,53
|
Мышьяковистая
|
H3AsO3
|
5,9 10-10
|
9,23
|
Надпероксид водорода
|
H2O4
|
6,3 10-3
|
2,2
|
Пероксид водорода
|
H2O2
|
2,0 10-12
|
11,70
|
Роданисто-водородная
|
HSNC
|
10
|
-1
|
Селенистая
|
H2SeO3
|
|
|
К1
|
|
1,8 10-3
|
2,75
|
К2
|
|
3,2 10-9
|
8,50
|
Селенисто-водородная
|
H2Se
|
|
|
К1
|
|
1,3 10-4
|
3,89
|
К2
|
|
1,0 10-11
|
11,0
|
Сернистая
|
H2SO3
|
|
|
К1
|
|
1,4 10-2
|
1,85
|
К2
|
|
6,2 10-8
|
7,20
|
Сероводородная
|
H2S
|
|
|
К1
|
|
1,0 10-7
|
6,99
|
К2
|
|
2,5 10-13
|
12,60
|
Теллуристая
|
H2TeO3
|
|
|
К1
|
|
2,7 10-3
|
2,57
|
К2
|
|
1,8 10-8
|
7,74
|
Теллуро-водородная
|
H2Te
|
|
|
К1
|
|
2,3 10-3
|
2,64
|
К2
|
|
6,9 10-13
|
12,16
|
Теллуровая
|
H6TeO6
|
|
|
К1
|
|
2,5 10-8
|
7,61
|
К2
|
|
1,1 10-11
|
10,95
|
Название
|
Формула
|
Ка
|
рК=-lg Ка
|
Тиосерная
|
H2SO3S
|
|
|
К1
|
|
2,5 10-1
|
0,60
|
К2
|
|
1,9 10-2
|
1,72
|
Угольная
|
CO2(р) + H2O
|
|
|
К1
|
|
4,5 10-7
|
6,35
|
К2
|
|
4,8 10-11
|
10,32
|
Уксусная
|
CH3COOH
|
1,8 10-5
|
4,76
|
Фосфористая
|
H3PO3
|
|
|
К1
|
|
3,1 10-12
|
1,51
|
К2
|
|
1,6 10-7
|
6,79
|
Фосфорная, орто
|
H3PO4
|
|
|
К1
|
|
7,1 10-3
|
2,15
|
К2
|
|
6,2 10-8
|
7,21
|
К3
|
|
5,0 10-13
|
12,0
|
Фосфорная, пиро
|
H4P2O7
|
|
|
К1
|
|
1,2 10-1
|
0,91
|
К2
|
|
7,9 10-3
|
2,10
|
Фосфорноватистая
|
HPO2H2
|
5,9 10-2
|
1,23
|
Фтористо-водородная
|
HF
|
6,2 10-4
|
3,21
|
Фторфосфорная
|
H2PO3F
|
|
|
К1
|
|
2,8 10-1
|
0,55
|
К2
|
|
1,6 10-5
|
4,80
|
Хлористая
|
HClO2
|
1,1 10-2
|
1,97
|
Хлорноватистая
|
HClO
|
2,9 10-8
|
7,53
|
Хромовая
|
H2CrO4
|
|
|
К1
|
|
1,6 10-1
|
0,80
|
К2
|
|
3,2 10-7
|
6,50
|
Циановодородная
|
HCN
|
5,0 10-10
|
9,30
|
Щавелевая
|
Н2С2О4
|
|
|
К1
|
|
5,6 10-2
|
1,25
|
К2
|
|
5,4 10-5
|
4,27
|
|
 Скачать 1.91 Mb.
Скачать 1.91 Mb.