министра зд. Министерство здравоохранения Иркутской области. Областное государственное бюджетное профессиональное образовательное учреждение братский медицинский колледж
 Скачать 5.01 Mb. Скачать 5.01 Mb.
|
|
Министерство здравоохранения Иркутской области ОБЛАСТНОЕ ГОСУДАРСТВЕННОЕ БЮДЖЕТНОЕ ПРОФЕССИОНАЛЬНОЕ ОБРАЗОВАТЕЛЬНОЕ УЧРЕЖДЕНИЕ «БРАТСКИЙ МЕДИЦИНСКИЙ КОЛЛЕДЖ» (ОГБПОУ БМК) Специальность «Фармация» КУРСОВАЯ РАБОТА Контроль качества лекарственных препаратов седативного действие Выполнил: Студент 4 курса Ф-189г группы Житняк Алена Игоревна_____________________________________ (Ф.И.О. студента) Проверила Калинина Ольга Николаевна_________________________ (Ф.И.О. преподавателя) Оценка: ____________________________________________________ Братск 2021г. СОДЕРЖАНИЕ
ВВЕДЕНИЕ Лекарственные средства растительного происхождения нашли широкое применение в современной фармакотерапии. Препараты, седативным эффектом, являются востребованными невротических состояний. Интерес к таким препаратам со стороны врачей и пациентов обусловлен возможность самолечение, применения, простотой дозировки, минимумом противопоказании пoбoчных эффектов. Эти свoйства oбусловлены, в растительным происхождением большинства компонентов, поэтому большое внимание уделяется изучению строения растений и их свoйств. Ещё одно из преимуществ - это относительно невысокая концентрация активных веществ, что сводит к минимуму возможность передозировки, а также обладает широким спектром показаний к их применения вегетоневрозы, легкие нервозы фoбическими расстройствами, проблемы повышенная возбудимость, неврастения. Поэтому большое внимание уделяется изучению строения растений и их свойств. В последние десятилетия пристальное внимание исследователей привлекают продукты вторичного метаболизма растений – алкалоиды, флавоноиды и гликозиды, в связи с широким спектром их биологического действия. Актуальность рассматриваемой темы определяется тем, что использование успокоительных средств растительного происхождения, более оптимально по сравнению с синтетическими препаратами. Они отличаются более мягким действием, возможностью длительного применения, минимумом противопоказаний и побочных эффектов. Цель работы: Изучить контроль качества лекарственных средств седативного действия. Задачи: 1) Изучить общую характеристику лекарственных средств седативного действия; 2) Проанализировать методы анализа пустырника; 3) Провести контроль качества пустырника; 4) Проанализировать нормативную документацию пустырника; 5) Объект исследование является настойка пустырника; 6) Предмет исследование является, методы исследования настойки пустырника  1.Лекарственные средства седативного действия 1.Лекарственные средства седативного действия1.1 Общая характеристика лекарственных средств седативного действия Седативные средства (от лат. sedatio — успокоение) — лекарственные средства, оказывающие общее успокаивающее действие на ЦНС. Седативный (успокаивающий) эффект проявляется в снижении реакции на различные внешние раздражители и некотором уменьшении дневной активности. Препараты этой группы регулируют функции ЦНС, усиливая процессы торможения или понижая процессы возбуждения. Как правило, они облегчают наступление и углубляют естественный сон, усиливают действие снотворных, анальгетиков и других средств, угнетающих ЦНС [12]. К седативным средствам относятся препараты брома — натрия бромид и калия бромид, камфора бромистая, а также препараты, изготовленные из лекарственных растений (валерианы, пустырника, пассифлоры, пиона и др.). Седативные препараты, которые, зачастую, применяются в сочетании с местной анестезией, используются при проведении ряда медицинских процедур, например, в стоматологии. При этом пациент находится в сознании и сохраняет все жизненно важные рефлексы. Эту альтернативу глубокому наркозу можно использовать в случае наличия дентофобии у пациента. Растительные седативные средства способствуют повышению качества жизни. Они оказывают разностороннее воздействие на организм человека, так как обладают спазмолитическим, гипотензивным, диуретическим, желчегонным, противовоспалительным действием [4]. 1.2Лекарственное растительное сырье седативного действия Пустырник Другие названия: пустырник волосистый, сердечная трава, фармакологическое действие - гипотензивное, седативное. Регулирует функциональное состояние ЦНС, оказывает успокаивающее действие, снижает повышенную нервную возбудимость, потенцирует снотворный эффект, проявляет антагонизм по отношению к судорожному действию аналептиков. Эффективен при психоастении, неврастении и неврозах, сопровождающихся бессонницей, чувством напряженности и повышенной реактивностью. Корригирует функциональные расстройства ЦНС и вегетативной нервной системы в преклимактерическом и климактерическом периодах. Оказывает отрицательное хронотропное действие, регулирует сердечный ритм при вегето-сосудистой дистонии, проявляет кардиотонические свойства, понижает АД. При сердечно-сосудистых нарушениях, в т.ч. при гипертонии, стенокардии, кардиосклерозе и миокардите, сердцебиении, сердечной слабости оказывает благоприятный эффект на течение заболевания. Обладает антиспастическим, диуретическим, противовоспалительным, общеукрепляющим эффектом. Показана эффективность препаратов пустырника при диспептических явлениях, язвенной болезни желудка и двенадцатиперстной кишки (особенно на фоне повышенной активности ЦНС), воспалении легких, бронхиальной астме, одышке, кашле, базедовой болезни, параличах, эпилепсии, невралгиях и контузии головного мозга, маточных кровотечениях и болезненных менструациях. В гомеопатической практике пустырник используется при жалобах со стороны сердца, метеоризме и гипертиреозе. Применение вещества: пустырника трава повышенная нервная возбудимость, вегето-сосудистая дистония, артериальная гипертензия (ранние стадии) [10] .  Рисунок 1-«пустырник» Валерьяна Фармакологическое действие — седативное, фармакодинамика действующим началом препарата является комплекс биологически активных веществ - эфирного масла, валепотриатов, гликозидов, алкалоидов, смол, органических кислот, полисахаридов и др. Валериановая кислота и валепотриаты обладают спазмолитическим действием. Комплекс биологически активных веществ валерианы замедляет сердечный ритм и расширяет коронарные сосуды. Препарат оказывает многостороннее действие на организм, угнетает центральную нервную систему, понижает ее возбудимость, облегчает наступление естественного сна. Седативный эффект препарата проявляется достаточно стабильно. Оказывает желчегонное действие, усиливает секреторную активность ЖКТ. Лечебное действие препарата проявляется при систематическом, длительном курсовом применении [5].  Рисунок 2-«варельяна» Мята перечная Средство растительного происхождения, настой оказывает седативное, умеренное спазмолитическое, желчегонное, противорвотное и местное раздражающее (раздражает нервные окончания слизистых оболочек) действие. При нанесении на слизистые оболочки оказывает умеренное анальгезирующее действие. Показания успокаивающие, тошнота, рвота, спазм гладких мышц (почечная колика, желчная колика, кишечная колика). Улучшение вкуса микстур (для настойки).Успокаивающее, болеутоляющее действие, рефлекторное коронарорасширяющее действие. За счет местно раздражающего эффекта и стимулирующего влияния на периферические нейрорецепторы кожи слизистых оболочек усиливают капиллярное кровообращение и перистальтику кишечника. Галеновые лекарственные формы из листьев мяты перечной усиливают секрецию пищеварительных желез, улучшают аппетит, повышают желчеотделение, оказывают спазмолитическое действие, снижают тонус гладкой мускулатуры кишечника, желче и мочевыводящих путей. Благодаря наличию ментола листья мяты перечной обладают упекающим действием [9].  Рисунок 3-«мята перечная» Мелисса Фармакологическая группа седативное средства в старину она часто использовалась, как седативное средство: успокаивала нервы, обеспечивала здоровый сон и излечивала от стрессов и паники. При регулярном употреблении чаев и настоек с мелиссой можно снять приступы тахикардии, затяжные депрессивные состояния, неврозы и бессонницу. Применяют эту траву и при повышенном давлении, для снятия спазмов и болей. Часто используют как противовоспалительное и противовирусное средство. Масло мелиссы очень эффективно при гриппе, герпесе и других вирусных инфекциях. Еще в старину ее использовали как отхаркивающее средство и желчегонный препарат. Мелисса способна нормализовать обменные процессы в организме, улучшить пищеварение. Имеет положительное влияние на мозговую деятельность, печень и сердце. Наружно часто применяли эту траву при зубной боли, ушибах, ревматизме. В современной медицине эта трава используется в препаратах в виде чаев, настоев, таблеток и отваров. Самыми известными зарубежными препаратами являются «Персен», «Новопассит» и другие [4].  Рисунок 4- «мелисса». 1.3 Классификация препаратов седативного действия 1) Барбитураты в малых дозах 2) фенобарбитал Бензодиазепины: диазепам, феназепам. 3) Соли бромистоводородной кислоты – бромиды Na+, K+, Ca++. 4) Препараты растительного происхождения: валериана, пустырник, пассифлора, пион. 5) Комбинированные препараты: валокордин, валокармид, валоседан, корвалол, валосердин, карвалдин, экстраверал, белатаминал, белоид, беласпон, алталекс, нервофлукс, ново-пассит, персед, саносан. 6) Н 1 – антигистаминные препараты: дифенгидрамин, прометазин, хлоропирамин, клемастин [65]. Натрия бромид и калия бромид- оказывают седативное действие, связанные с усилением процессов торможения в коре большого мозга. Эффект этой группы препаратов зависит от типа высшей нервной деятельности. Суточная доза может колебаться от 0, 1 г до 1, 5 г. Бромиды обладают слабым противоэпилептическим свойством. Показания. Неврозы, повышенная раздражительность, бессонница. Эффект развивается медленно. Корвалол входящий в состав корвалола этиловый эфир α бромизовалериановой кислоты является седативным и спазмолитическим средством. Фенобарбитал-натрий оказывает легкое седативное и сосудорасширяющее действие без заметного снотворного эффекта. Мятное масло оказывает рефлекторный сосудорасширяющий и спазмолитический эффект. Применяют корвалол при неврозах с повышенной раздражительностью, нерезко выраженных спазмах коронарных сосудов, тахикардии, бессоннице; в ранних стадиях гипертонической болезни, при спазмах кишечника. Корвалол хорошо переносится; даже при длительном применении препарата побочных явлений обычно не отмечается. Ново - Пассит - комбинированный препарат, состоящий из комплекса экстрактов лекарственных растений и гвайфенезина. Оказывает седативное и анксиолитическое действие. Устраняет ощущение страха, психоэмоциональное напряжение. Характеризуется миорелаксирующим эффектом. Показания: неврастения, сопровождающаяся раздражительностью, тревогой, страхом, повышенной усталостью, рассеянностью; легкие формы расстройства сна; приступы головной боли, обусловленные нервным перенапряжением; климактерический синдром; функциональные заболевания пищеварительного тракта (диспепсический синдром, синдром раздраженной толстой кишки). Побочные эффекты: применении в рекомендуемых дозах, как правило, не вызывает развития сонливости и снижения концентрации внимания, что позволяет принимать Ново-Пассит в дневное время. Однако в отдельных случаях возможны головокружение, вялость, повышенная усталость, сонливость, тошнота, рвота, изжога, легкая мышечная слабость, исчезающие после отмены препарата [9]. 2 Контроль качества лекарственного препарата седативного действия 2.1 Порядок проведения контроля качества лекарственных средств, поступающих в аптечные учреждения Порядок проведения контроля качества лекарственных средств, поступающих в аптечные учреждения, осуществляется на основании приказа МЗ РФ от 26.10.2015 г. № 751н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность». Утвержденная приказом МЗ РФ от 26.10.2015 г. № 751н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность». Инструкция о порядке проведения государственного контроля качества лекарственных средств, используемых на территории Российской Федерации, устанавливает единый порядок контроля качества отечественных и зарубежных лекарственных средств, поступающих в аптечные учреждения из аптечных баз (складов), предприятий. Перед реализацией все лекарственные средства (за исключением бактерийных и вирусных) подлежат обязательному контролю на аптечных базах (складах) или в территориальных контрольно-аналитических лабораториях. Затем в установленном порядке на основании протоколов анализа лекарственных средств сертифицируются органами сертификации Обязательному по серийному контролю на соответствие требованиям нормативной документации по всем показателям подлежат: лекарственные средства, изготовленные предприятиями негосударственных форм собственности и закупленные нецентрализованно; лекарственные средства, используемые для приготовления глазных капель и инъекционных растворов в условиях аптеки; наркотические лекарственные средства (включая лекарственные формы); лекарственные средства для наркоза (исключая кислород и закись азота); лекарственные средства, используемые в детской практике; рентгеноконтрастные лекарственные средства; препараты инсулина; лекарственные средства, вызывающие сомнение в их качестве. Качество остальных лекарственные средства, закупленных централизованно или изготовленных предприятиями государственных форм собственности, оценивается выборочно от каждой серии (партии) по показателям нормативной документации: «Описание», «Подлинность», «Упаковка», «Маркировка». После оценки качества все перечисленные лекарственные средства проходят сертификацию на основании протоколов анализа. Все направляемые на контроль отечественные препараты должны сопровождаться паспортом ОТК предприятия, а зарубежные - сертификатом качества фирмы-производителя. В случае выявления несоответствия лекарственных средств требованиям нормативной документации или обнаружения скрытого брака в процессе хранения до истечения срока годности предъявляется рекламация предприятию или фирме-изготовителю лекарственных средств. Если последний отказывается от удовлетворения претензий, образцы этих лекарственных средств направляются на арбитражный контроль в соответствующий органы [7]. 2.1.1 Приемочный контроль Приемочный контроль проводится с целью предупреждения поступления в аптеку некачественных лекарственных средств. Приемочный контроль заключается в проверке поступающих лекарственных средств на соответствие требованиям по показателям: «Описание»; «Упаковка»; «Маркировка»; в проверке правильности оформления расчетных документов (счетов), а также наличия сертификатов соответствия производителя и других документов, подтверждающих качество лекарственных средств в соответствии с действующими нормативными документами. Контроль по показателю «Описание» включает проверку внешнего вида, цвета, запаха. В случае сомнения в качестве лекарственных средств образцы направляются в территориальную контрольно-аналитическую лабораторию. Такие лекарственные средства с обозначением: «Забраковано при приемочном контроле» хранятся в аптеке изолированно от других лекарственных средств. При проверке по показателю «Упаковка» особое внимание обращается на ее целостность и соответствие физико-химическим свойствам лекарственных средств. При контроле по показателю «Маркировка» обращается внимание на соответствие оформления лекарственных средств действующим требованиям. Особое внимание следует обращать на соответствие маркировки первичной, вторичной и групповой упаковки, наличие листовки - вкладыша на русском языке в упаковке (или отдельно в пачке на все количество готовых лекарственных средств) [12]. 2.1.2 Предупредительные мероприятия Обеспечение в аптеке условий хранения лекарственных средств в соответствии с их физико - химическими свойствами и требованиями Государственной Фармакопеи, действующих нормативных документов [34]. 2.1.3 Органолептический контроль Органолептический контроль заключается в проверке лекарственной формы по показателям: «Описание» (внешний вид, цвет, запах), однородность, отсутствие видимых механических включений (в жидких лекарственных формах). На вкус проверяются выборочно лекарственные формы, предназначенные для детей. Однородность порошков, гомеопатических тритураций, мазей, пилюль, суппозиториев проверяется в соответствии с требованиями Государственной Фармакопеи, действующих нормативных документов. Проверка осуществляется выборочно у каждого фармацевта в течение рабочего дня с учетом различных видов лекарственных форм. Результаты органолептического контроля регистрируются в журнале регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам на лекарственные препараты, требованиям медицинских организаций и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств [89]. 2.1.4 Физический контроль Физический контроль заключается в проверке общей массы или объема лекарственного препарата, количества и массы отдельных доз (не менее трех доз), входящих в лекарственный препарат, количества гранул в одном грамме гомеопатических гранул, распадаемости гомеопатических гранул. В рамках физического контроля проверяется также качество укупорки изготовленного лекарственного препарата. Лекарственные препараты, изготовленные по рецептам, требованиям, подлежат физическому контролю выборочно в течение рабочего дня с учетом всех видов изготовленных лекарственных форм, но не менее 3% от их количества за день. Лекарственные препараты, изготовленные в виде внутриаптечной заготовки, подлежат физическому контролю в количестве не менее трех упаковок каждой серии (в том числе фасовка промышленной продукции и гомеопатических лекарственных средств). Физический контроль обязательно осуществляется в отношении лекарственных препаратов, предназначенных для применения у детей в возрасте до 1 года, содержащих наркотические средства, психотропные и сильнодействующие вещества, лекарственные препараты, требующие стерилизации, суппозиториев, инъекционных гомеопатических растворов, настоек гомеопатических матричных. Обязательному контролю количества гранул в одном грамме подлежат гранулы сахарные, как вспомогательное вещество, при поступлении в аптечную организацию, к индивидуальному предпринимателю. Взвешивается 1 грамм гранул с точностью 0,01 грамма и подсчитывается количество гранул. Проводится не менее двух определений. Гранулы гомеопатические, изготовленные в виде внутриаптечной заготовки, подвергаются контролю распадаемости выборочно, но не менее 10% от общего числа изготовленных за месяц серий. 10 гранул помещаются в коническую колбу вместимостью 100 мл, прибавляется 50 мл воды очищенной, имеющей температуру 37 °C ± 2 °C. Колба медленно покачивается 1 - 2 раза в секунду. Проводится не менее трех определений. Гранулы должны распадаться в течение не более 5 мин. Результаты физического контроля фиксируются в журнале регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам, требованиям и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств [65]. 2.1.5 Химический контроль Химический контроль заключается в оценке качества изготовления лекарственного средства по показателям: «Подлинность», «Испытания на чистоту и допустимые пределы примесей» (качественный анализ) и «Количественное определение» (количественный анализ) лекарственных веществ, входящих в его состав. Результаты качественного анализа регистрируются в журнале регистрации результатов органолептического, физического и химического контроля лекарственных препаратов, изготовленных по рецептам, требованиям и в виде внутриаптечной заготовки, концентрированных растворов, тритураций, спирта этилового и фасовки лекарственных средств, а также в журнале регистрации результатов контроля лекарственных средств на подлинность. Качественному анализу в обязательном порядке подвергаются: - очищенная вода и вода для инъекций ежедневно из каждого баллона, а при подаче воды по трубопроводу - на каждом рабочем месте на отсутствие хлоридов, сульфатов и солей кальция. Вода, предназначенная для изготовления стерильных растворов, должна быть также проверена на отсутствие восстанавливающих веществ, солей аммония и углерода диоксида; - все лекарственные средства и концентрированные растворы (в том числе настойки гомеопатические матричные, тритурации гомеопатические первого десятичного разведения, растворы гомеопатические первого десятичного разведения), поступающие из помещений для хранения в помещения для изготовления лекарственных препаратов; - лекарственные средства, поступившие в аптечную организацию, к индивидуальному предпринимателю в случае возникновения сомнения в их качестве; - концентрированные растворы, жидкие лекарственные средства в бюреточной установке и в штангласах с пипетками, находящиеся в помещении изготовления лекарственных препаратов, при их заполнении; - расфасованные лекарственные средства промышленного производства; - гомеопатические лекарственные препараты в виде внутриаптечной заготовки. Качество лекарственного препарата оценивают по вспомогательным веществам. Вода очищенная и вода для инъекций должны ежеквартально подвергаться полному качественному и количественному анализу. При проведении химического контроля очищенной воды и воды для инъекций в журнале регистрации результатов контроля воды очищенной, воды для инъекций в обязательном порядке указываются: дата получения (отгонки) воды; дата контроля воды;номер проведенного химического анализа; номер баллона или бюретки, из которых взята на анализ вода; результаты контроля на отсутствие примесей; показатели рН среды;заключение о результатах анализа воды (удовлетворяет/не удовлетворяет);подпись лица, проводившего анализ. Журнал регистрации результатов контроля воды очищенной, воды для инъекций должен быть пронумерован, прошнурован и скреплен подписью руководителя учреждения и печатью вышестоящей организации [21]. 2.2 Правила изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность Министерство здравоохранения Российской Федерации приказ от 26 октября 2015 г. № 751н «Об утверждении правил изготовления и отпуска лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность». Общие положения: 1) настоящие Правила устанавливают требования к изготовлению и отпуску лекарственных препаратов для медицинского применения аптечными организациями, индивидуальными предпринимателями, имеющими лицензию на фармацевтическую деятельность с правом изготовления лекарственных препаратов для медицинского применения (далее соответственно - Правила, лекарственные препараты, аптечные организации, индивидуальные предприниматели); 2) настоящие правила распространяются на изготовление и отпуск лекарственных препаратов аптечными организациями и индивидуальными предпринимателями, в том числе по рецептам на лекарственные препараты и по требованиям - накладным медицинских организаций (далее соответственно - рецепт, требование); 3) при изготовлении лекарственных препаратов используются фармацевтические субстанции, включенные в государственный реестр лекарственных средств для медицинского применения (далее - лекарственные средства); 4) качество изготовленного лекарственного препарата определяется его соответствием требованиям фармакопейной статьи, общей фармакопейной статьи, либо в случае их отсутствия - документа в области контроля качества, содержащего требования и методы определения качества изготовленных лекарственных препаратов (далее - документ в области контроля качества); 5) аптечные организации и индивидуальные предприниматели обеспечивают исправность и точность средств измерений, предусмотренных нормативной, технической документацией производителя и соответствующих требованиям к их поверке и калибровке, предусмотренным статьями 13 и 18 Федерального закона от 26 июня 2008 г. № 102 - ФЗ «Об обеспечении единства измерений», используемых при изготовлении и контроле качества лекарственных препаратов, а также регулярность их поверки и калибровки; 6) на всех банках или флаконах с притертой пробкой (далее - штанглас), в которых хранятся лекарственные средства, указываются наименование лекарственного средства, дата заполнения штангласа лекарственным средством, дата окончания срока годности (годен до ____), подпись лица, заполнившего штанглас и подтверждающего, что в штангласе содержится именно указанное лекарственное средство. На штангласах с лекарственными средствами, предназначенными для изготовления растворов для инъекций и инфузий, дополнительно указывается «Для инъекций». Штангласы с жидкими лекарственными средствами обеспечиваются каплемерами или пипетками. Число капель в определенном объеме или массе обозначается на штангласе; 7) изготовление лекарственных препаратов осуществляется в условиях, отвечающих санитарно - эпидемиологическим требованиям. При изготовлении концентрированных растворов, полуфабрикатов, лекарственных препаратов в виде внутриаптечной заготовки и фасовке лекарственных препаратов все записи производятся в журнале лабораторных и фасовочных работ, оформляемом на бумажном носителе или в электронном виде паковка изготовленных лекарственных препаратов осуществляется в зависимости от формы и способа применения лекарственного препарата. В процессе упаковки изготовленных лекарственных препаратов осуществляется проверка общего вида упаковки, правильности использования упаковочных материалов, маркировки упаковки. Лекарственные препараты, изготовленные в форме порошков в асептических условиях, стерильные и асептически изготовленные жидкие лекарственные формы, глазные мази упаковываются в стерильную упаковку. Мази упаковываются в широкогорлые банки, контейнеры, тубы и другие емкости, удобные для использования. Жидкие лекарственные формы упаковываются в плотно закрывающиеся емкости. Суппозитории упаковываются в индивидуальную первичную упаковку и помещают во вторичную упаковку (коробку или пакет);маркировка изготовленных лекарственных препаратов должна соответствовать требованиям [54]. 2.3 Контроль качества Пустырника Регулирует функциональное состояние ЦНС, оказывает успокаивающее действие, снижает повышенную нервную возбудимость, потенцирует снотворный эффект, проявляет антагонизм по отношению к судорожному действию аналептиков. Эффективен при психоастении, неврастении и неврозах, сопровождающихся бессонницей, чувством напряженности и повышенной реактивностью. Корригирует функциональные расстройства ЦНС и вегетативной нервной системы в преклимактерическом и климактерическом периодах. Оказывает отрицательное хронотропное действие, регулирует сердечный ритм при вегето-сосудистой дистонии, проявляет кардиотонические свойства, понижает АД. При сердечно-сосудистых нарушениях, в т.ч. при гипертонии, стенокардии, кардиосклерозе и миокардите, сердцебиении, сердечной слабости оказывает благоприятный эффект на течение заболевания. Обладает антиспастическим, диуретическим,противовоспалительным, общеукрепляющим эффектом.Показана эффективность препаратов пустырника при диспептических явлениях, язвенной болезни желудка и двенадцатиперстной кишки (особенно на фоне повышенной активности ЦНС), воспалении легких, бронхиальной астме, одышке, кашле, базедовой болезни, параличах, эпилепсии, невралгиях и контузии головного мозга, маточных кровотечениях и болезненных менструациях. В гомеопатической практике пустырник используется при жалобах со стороны сердца, метеоризме и гипертиреозе [27]. 2.3.1 Анализ пустырника Подлинность К 1 мл препарата прибавляют 0,2 мл железа (III) хлорида раствора 3 %, появляется черно-зеленое окрашивание.  Рисунок 5-«появление черного-зеленого окрашивание» 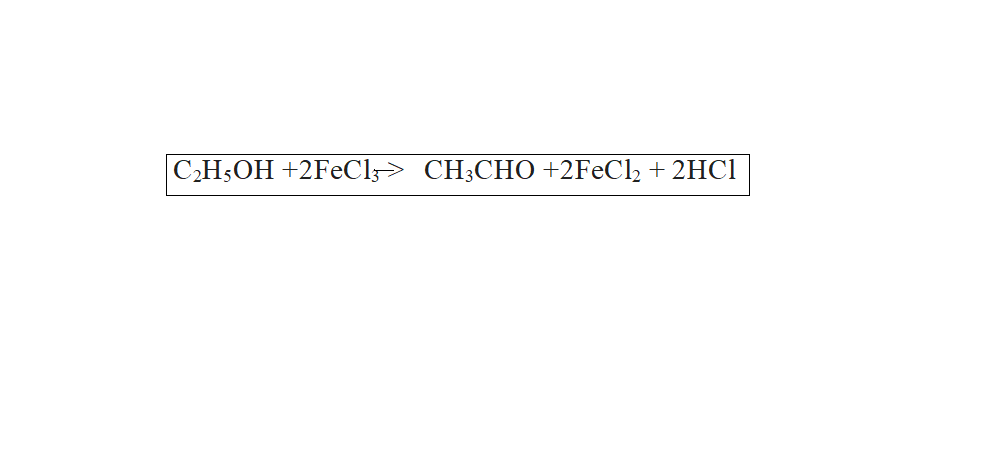 Рисунок 6- «уравнения реакция взаимодействия хлорида железа с настойкой пустырника» Количественное определение Определение спирта этилового в лекарственных средствах. Метанол и 2-пропанол. Не более 0,05 % метанола и не более 0,05 % 2- пропанола. В соответствии с ОФС «Определение метанола и 2-пропанола» [30]. Расчет содержания пустырника провели по формуле: 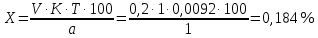 ДНО 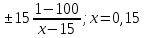 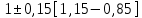 Вывод: данную лекарственную форму настойки пустырника является, удовлетворительно может быть отпущен. 2.3.2 Протокол Пустырника Протокол испытаний № 1 от «08» октября 2021 г. Протокол испытаний представлен на 3 лисах. Название заявителя: Аптека Торговое наименование продукции: настойка пустырника Форма выпуска: По 25 мл во флаконы оранжевого стекла с винтовой горловиной, укупоренные пробками полиэтиленовыми и навинчиваемыми крышками или крышками унифицированными укупорочно-навинчиваемыми или колпачками алюминиевыми. Серия: 154260 Размер партии: 1 упаковка Производитель, страна: Гиппократ, Россия. Дата выпуска: 11.09.2021 г. Срок годности: 14.09.2024 г. Нормативный документ: ФС 42-0197-07 Регистрационный номер: ЛП-002879 Количество отобранных образцов: 1 флакон Таблица 1- Результаты исследование настойка пустырника, производитель, «Гиппократ», страна: Россия.
Продолжение таблица 1-«результаты исследование настойка пустырника, производитель, «Гиппократ», страна: Россия.»
Окончание таблицы 1
Заключение: Образцы лекарственного средства «пустырника», настойки соответствует требованиям ФС 42-0197-07 по проверяемым показателям. Руководитель: О.О. Иванов Подпись Иванов Ф.И.О Исполнитель: провизор Н.Н.Ульнова Подпись Ульнова Ф.И.О Примечание: Данный протокол испытания касается только образцов, подвергнутых этим испытаниям. ЗАКЛЮЧЕНИЕ Седативные средства— лекарственные средства, оказывающие общее успокаивающее действие на ЦНС. Седативный эффект проявляется в снижении реакции на различные внешние раздражители и некотором уменьшении дневной активности. Пустырник- оказывает успокаивающее действие, снижает повышенную нервную возбудимость. Валерьяна- замедляет сердечный ритм и расширяет коронарные сосуды. Мята перечная - оказывает седативное, умеренное спазмолитическое, желчегонное, противорвотное. Цели: контроль качества лекарственных средств седативного действия Данный лекарственный препарат пустырника соответствует всем нормативным документациям что доказывает количественное и подлинность результата анализа. Цели и задачи достигнуты можно сделать вывод что лекарственные средства седативного действия оказывающие общее успокаивающее действие на ЦНС, что данные результаты испытания могут отправлены в контрольное аналитическую лабораторию для дальнейшего исследование. СПИОСК ИСПОЛЬЗУЕМЫХ ИСТЧНИКОВ 1 . Асеева Т.А. Лекарственные растения тибетской медицины /Т.А. Асеева, К.Ф. Блинова, Г.П. Яковлев. Новосибирск: Наука, 1985.[10] - 159 с.[4] 2. Атлас лекарственных растений Под ред. Н.В. Цицина. М.: Медгиз, 1962, С.98-100, 196- 197 [5] 3. Ворошилов В.Н. Лекарственная валериана. М., 1959, С. 160.[19] 4. Государственная Фармакопея. Вып.1. Общие методы анализа /МЗ СССР. 11-е изд., доп. - М.: Медицина, 1987. - 336 с.[7] 5. Государственная Фармакопея. Вып.2. Общие методы анализа. [12]. 6. Лекарственное растительное сырье 11-е изд., доп. - М.: Медицина, 1989.-400 c.[9] 7. Коновалова, Н.Т. Ко-нон, К.С. Рыбалко //Растительные ресурсы. 1991. - Т. [27] 8. Махлаюк В.П. Лекарственные растения в народной медицине /В.П. Махлаюк. М.: Нива России, 1992. - 477 с.[30] 9. Молчанов Г.И. Интенсивная обработка лекарственного сырья /Г.И.[54] 10. Морохина С.Л., Аляутдин Р.Н., Сорокина А.А. Изучение седативного эффекта успокоительных сборов // Фармация. - 2010. - № 6. - С. 39-41.[65] 11. Исследования ассортимента лекарственных средств седативного происхождения и характеристика их потребителей / Н.И. Гаврилина // Фармация.-2001.-№1.- с.16-18. [21] 12. Государственный Реестр ЛС Т.1.ОФ. издание МЗ РФ 2002.- М., 2002.-с.1300. [34] 13. Деревянко, И.И. Седативные средства./ И.И.Деревянко // Consilium- Medicum. – 2000. – Том 2. – №4.-c.136-136.[67] 14. Зукин, Н.В.Сравнительная фармакокинетика седативных средств. / И.В.Зукин //Фармация.-2007.-№8.- .30-33.[89] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
