Окислительные свойства азотной кислоты. Окислительные свойства азотной кислоты Азотная кислота
 Скачать 76.46 Kb. Скачать 76.46 Kb.
|
|
Окислительные свойства азотной кислоты Азотная кислота – в любом виде (и разбавленная, и концентрированная) является сильным окислителем. Причем, разбавленная восстанавливается глубже, чем концентрированная. Окислительные свойства обеспечиваются азотом в высшей степени окисления +5 Какая валентность у азота в этом соединении? Вопрос очень хитрый, многие отвечают на него корректно. У азота в азотной кислоте валентность IV. Три связи с каждым атомом кислорода, и четвертая как бы распределяется, образуется полуторная связь. Таким образом, валентность азота IV, а степень окисления +5  Первое самое интересное свойство: взаимодействие с металлами. Водород при взаимодействии с металлами никогда не выделяется Схема реакции азотной кислоты (и разбавленной, и концентрированной) с металлами: HNO3 + Ме → нитрат + H2O + продукт восстановленного азота Два нюанса: 1. Алюминий, железо и хром с концентрированной азотной кислотой в нормальных условиях не реагируют, из-за пассивации. Нужно нагреть. 2. С платиной и золотом концентрированная азотная кислота не реагирует вообще. Чтобы понять до чего вообще может восстанавливаться азот, посмотрим на диаграмму его степеней окисления: 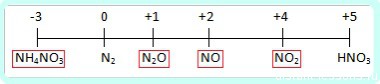 Азот +5 – окислитель, будет восстанавливаться, то есть понижать степень окисления. Все возможные продукты восстановления азотной на диаграмме обведены красным. Определить какой именно продукт будет образовываться можно чисто логически: до таких низких степеней окисления как -3 или +1, с образованием продуктовNH4NO3 или N2O соответственно, азот восстанавливают только достаточно сильные, активные металлы: щелочные — 1-я группа главная подгруппа, щелочноземельные, а так же Al и Zn. Как ранее уже было сказано, разбавленная кислота восстанавливается глубже, поэтому при взаимодействии активных металлов с конц. азотной кислотой образуется N2O, а при взаимодействии с разб. азотной кислотой NH4NO3. 4Ba + 10HNO3(конц.) → 4Ba(NO3)2 + 5H2O + N2O↑ 4Ba + 10HNO3(разб.) → 4Ba(NO3)2 + 3H2O + NH4NO3 8Li + 10HNO3(конц.) → 8LiNO3 + 5H2O + N2O↑ 8Li + 10HNO3(разб.) → 8LiNO3 + 3H2O + NH4NO3 8Al + 30HNO3(конц.) (t)→ 8Al(NO3)3 + 15H2O + 3N2O↑ 8Al + 30HNO3(разб.) → 8Al(NO3)3 + 9H2O + 3NH4NO3 Остальные металлы восстанавливают азотную кислоту до +2 или +4, с образованием продуктов соответственно: NO или O2. Разбавленная кислота восстанавливается глубже при взаимодействии с ней металлов, не отличающихся особой активностью, будет образовываться NO. Ну а с конц. азотной NO2: Cu + 4HNO3(конц.) → Cu(NO3)2 + 2H2O + 2NO2↑ 3Cu + 8HNO3(разб.) → 3Cu(NO3)2 + 4H2O + 2NO↑ Fe + 6HNO3(конц.) (t)→ Fe(NO3)3 + 3H2O + 3NO2↑ Fe + 4HNO3(разб.) → Fe(NO3)3 + 2H2O + NO↑ (обратите внимание, что железо окисляется до высшей степени окисления) Ag + 2HNO3(конц.) → AgNO3 + H2O + NO2↑ 3Ag + 4HNO3(разб.) → 3AgNO3 + 2H2O + NO↑ Если тяжело сразу понять всю логичность выбора, вот таблица: 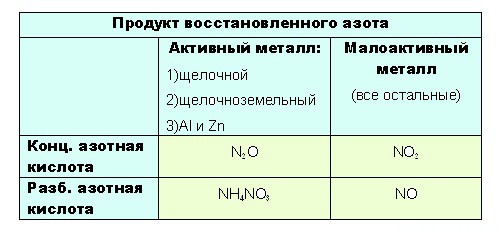 Азотная кислота окисляет неметаллы до высших оксидов. Так как неметаллы – не такие сильные восстановители, как активные металлы, азот может восстановиться только до +4, образовав NO2 или NO соответственно. При окислении неметаллов концентрированной азотной кислотой образуется бурый газ (NO2), а если кислота разбавленная, то образуется NO. Схемы реакций следующие: неметалл + HNO3(разб.) → соединение неметалла в высшей степени окисления +NO неметалл + HNO3(конц.) → соединение неметалла в высшей степени окисления +NO2 C + 4HNO3(конц.) → CO2↑ + 2H2O + 4NO2↑ 3C + 4HNO3(разб.) → 3CO2↑ + 2H2O + 4NO↑ (угольная кислота не образуется, так как она не стабильна) P + 5HNO3(конц.) → H3PO4 + H2O + 5NO2↑ 3P + 5HNO3(разб.) + 2H2O → 3H3PO4 + 5NO↑ B + 3HNO3(конц.) → H3BO3 + 3NO2↑ B + HNO3(разб.) + H2O → H3BO3 + NO↑ S + 6HNO3(конц.) → H2SO4 + 2H2O + 6NO2↑ S + 2HNO3(разб.)→ H2SO4 + 2NO↑ концентрированная азотная кислота окисляет сероводород. Окисление идет глубже при нагревании: 2HNO3(конц.) + H2S → S↓ + 2NO2 + 2H2O H2S + 8HNO3(конц.) → H2SO4 + 8NO2↑ + 4H2O концентрированная азотная кислота окисляет сульфиды до сульфатов: CuS + 8HNO3(конц.) → CuSO4 + 4H2O + 8NO2↑ азотная кислота настолько сурова, что может окислить даже ГАЛОГЕН. Только один – иод. Разбавленная восстанавливается глубже: до +2, концентрированная до +4. А вот иод окисляется не до высшей степени окисления +7 (слишком круто), а до +6, образуя иодноватую кислоту HIO3: 10HNO3(конц.) + I2 (t)→ 2HIO3 + 10NO2↑ + 4H2O 10HNO3(разб.) + 3I2 (t)→ 6HIO3 + 10NO↑ + 2H2O концентрированная азотная кислота реагирует с хлоридами и фторидами. Только следует понимать, что с фторидами и хлоридами протекает обычная реакция ионного обмена с вытеснением галогеноводорода и образованием нитрата: NaCl(тв.) + HNO3(конц.) → HCl↑ + NaNO3 NaF(тв.) + HNO3(конц.) → HF↑ + NaNO3 А вот с бромидами и иодидами (и с бромоводородами, и с иодоводородами) протекает ОВР. В обоих случаях образуется свободный галоген, а азот восстанавливается до NO2: 8HNO3(конц.) + 6KBr(тв.) → 3Br2 + 4H2O + 6KNO3 + 2NO2↑ 4HNO3(конц.) + 2NaI(тв.) → 2NaNO3 + 2NO2↑ + 2H2O + I2↓ Образовавшийся иод окисляется дальше до иодноватой кислоты, поэтому реакцию можно записать сразу: 7HNO3(конц.) + NaI → NaNO3 + 6NO2↑ + 3H2O + HIO3 То же самое происходит при взаимодействии с иодо- и бромоводородами: 2HNO3(конц.) + 2HBr → Br2 + 2NO2↑ + 2H2O 6HNO3(конц.) + HI → HIO3 + 6NO2↑ + 3H2O |
