Онкология
 Скачать 386.5 Kb. Скачать 386.5 Kb.
|
1 2 Клиника и диагностика опухолей Клиника и диагностика доброкачественных и злокачественных новообразований различна, что связано с их влиянием на окружающие органы и ткани, да и организм больного в целом. Особенности диагностики доброкачественных опухолей Диагностика доброкачественных образований основана на местных симптомах, признаках наличия самой опухоли. Часто больные обращают внимание на появление какого-то образования сами. При этом опухоли обычно медленно увеличиваются в размерах, не причиняют боли, имеют округлую форму, чёткую границу с окружающими тканями, гладкую поверхность. Беспокоит в основном наличие самого образования. Лишь иногда возникают признаки нарушения функции органа (полип кишки приводит к обтурационной кишечной непроходимости; доброкачественная опухоль головного мозга, сдавливая окружающие отделы, приводит к появлению неврологической симптоматики; аденома надпочечника за счёт выброса в кровь гормонов приводит к артериальной гипертензии и т.д.). Следует отметить, что диагностика доброкачественных опухолей не представляет особых трудностей. Сами по себе они не могут угрожать жизни пациента. Возможную опасность представляет лишь нарушение функции органов, но это, в свою очередь, довольно ярко манифестирует заболевание. Диагностика злокачественных опухолей Диагностика злокачественных новообразований достаточно трудна, что связано с разнообразными клиническими проявлениями этих заболеваний. В клинике злокачественных опухолей можно выделить четыре основных синдрома: • синдром «плюс-ткань»; • синдром патологических выделений; • синдром нарушения функции органа; • синдром малых признаков. Синдром «плюс-ткань» Новообразование можно обнаружить непосредственно в зоне расположения как новую дополнительную ткань - «плюс-ткань». Этот симптом просто выявить при поверхностной локализации опухоли (в коже, подкожной клетчатке или мышцах), а также на конечностях. Иногда можно прощупать опухоль в брюшной полости. Кроме того, признак «плюс-ткань» может быть определён с помощью специальных методов исследования: эндоскопии (лапароскопия, гастроскопия, колоноскопия, бронхоскопия, цистоскопия и др.), рентгеновского исследования или УЗИ и т.д. При этом можно обнаружить саму опухоль или определяить характерные для «плюс-ткани» симптомы (дефект наполнения при рентгеновском исследовании желудка с контрастированием сульфатом бария и др.). Синдром патологических выделений При наличии злокачественной опухоли вследствие прорастания ею кровеносных сосудов довольно часто имеют место кровянистые выделения или кровотечения. Так, рак желудка может вызвать желудочное кровотечение, опухоль матки - маточное кровотечение или мажущие кровянистые выделения из влагалища, для рака молочной железы характерным признаком является серозно-геморрагическое отделяемое из соска, для рака лёгкого характерно кровохарканье, а при прорастании плевры - появление геморрагического выпота в плевральной полости, при раке прямой кишки возможны прямокишечные кровотечения, при опухоли почки - гематурия. При развитии вокруг опухоли воспаления, а также при слизеобразующей форме рака возникают слизистые или слизисто-гнойные выделения (например, при раке ободочной кишки). Подобные симптомы получили общее название синдрома патологических выделений. В ряде случаев эти признаки помогают дифференцировать злокачественную опухоль от доброкачественной. Например, если при новообразовании молочной железы есть кровянистые выделения из соска - опухоль злокачественная. Синдром нарушения функции органа Само название синдрома говорит о том, что его проявления весьма разнообразны и определяются локализацией опухоли и функцией органа, в котором она находится. Для злокачественных образований кишечника характерны признаки кишечной непроходимости. Для опухоли желудка - диспептические расстройства (тошнота, изжога, рвота и др.). У больных раком пищевода ведущий симптом - нарушение акта глотания пищи - дисфагия и т.д. Указанные симптомы не специфичны, но часто возникают у больных со злокачественными новообразованиями. Синдром малых признаков Больные со злокачественными новообразованиями часто предъявляют, казалось бы, не совсем объяснимые жалобы. Отмечают: слабость, утомляемость, повышение температуры тела, похудание, плохой аппетит (характерно отвращение к мясной пищи, особенно при раке желудка), анемия, повышение СОЭ. Перечисленные симптомы объединены в синдром малых признаков (описан впервые А.И. Савицким). В некоторых случаях этот синдром возникает на довольно ранних стадиях заболевания и может быть даже единственным его проявлением. Иногда он может быть позже, являясь по существу проявлением явной раковой интоксикации. При этом больные имеют характерный, «онкологический» вид: они пониженного питания, тургор тканей снижен, кожа бледная с иктеричным оттенком, ввалившиеся глаза. Обычно такой внешний вид больных свидетельствует о наличии у них запущенного онкологического процесса. Клинические отличия доброкачественной и злокачественной опухоли При определении синдрома «плюс-ткань» возникает вопрос, сформирована ли эта лишняя ткань за счёт развития доброкачественной или злокачественной опухоли. Существует ряд различий в местных изменениях (status localis), которые прежде всего имеют значение при доступных для пальпации образованиях (опухоль молочной железы, щитовидной железы, прямой кишки). Различия в местных проявлениях злокачественных и доброкачественных опухолей представлены в табл. 16-2. Общие принципы диагностики злокачественных новообразований Учитывая выраженную зависимость результатов лечения злокачественных опухолей от стадии заболевания, а также довольно высокий риск развития рецидивов и прогрессирования процесса, в диагностике этих процессов следует обратить внимание на следующие принципы: • ранняя диагностика; • онкологическая преднастороженность; • гипердиагностика. Таблица 16-2. Местные различия злокачественной и доброкачественной опухоли 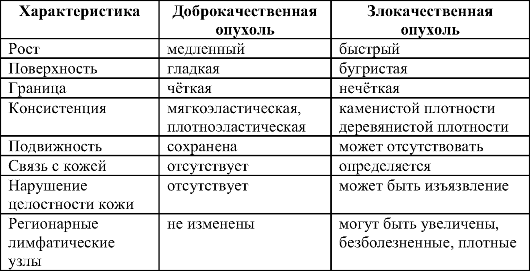 Ранняя диагностика Выяснение клинических симптомов опухоли и применение специальных диагностических методов важны для постановки в кратчайшие сроки диагноза злокачественного новообразования и выбора оптимального пути лечения. В онкологии существует понятие о своевременности диагностики. В связи с этим выделяют следующие её виды: • ранняя; • своевременная; • поздняя. О ранней диагностике говорят в тех случаях, когда диагноз злокачественного новообразования установлен на стадии рак in situ или на I клинической стадии заболевания. При этом подразумевают, что адекватное лечение должно привести к выздоровлению пациента. Своевременным считают диагноз, поставленный на II и в некоторых случаях на III стадии процесса. При этом предпринятое лечение позволяет полностью излечить пациента от онкологического заболевания, но возможно это только у части больных, тогда как другие в ближайшие месяцы или годы погибнут от прогрессирования процесса. Поздняя диагностика (установление диагноза на III-IV стадии онкологического заболевания) свидетельствует о малой вероятности или принципиальной невозможности излечения пациента и по существу предопределяет его дальнейшую судьбу. Из сказанного ясно, что нужно стараться диагностировать злокачественную опухоль как можно быстрее, так как ранняя диагностика позволяет добиться значительно лучших результатов лечения. Целенаправленное лечение при онкологическом заболевании необходимо начинать в течение двух недель с момента постановки диагноза. Значение ранней диагностики наглядно показывают следующие цифры: пятилетняя выживаемость при хирургическом лечении рака желудка на стадии in situ составляет 90-97%, а при раке III стадии - 25-30%. Онкологическая настороженность При обследовании пациента и выяснении любых клинических симптомов врач любой специальности должен задавать себе вопрос: не могут ли эти симптомы быть проявлением злокачественной опухоли? Задав этот вопрос, врач должен предпринять все усилия для того, чтобы либо подтвердить, либо исключить возникшие подозрения. При обследовании и лечении любого больного у врача должна быть онкологическая настороженность. Принцип гипердиагностики При диагностике злокачественных новообразований во всех сомнительных случаях принято выставлять более грозный диагноз и предпринимать более радикальные способы лечения. Такой подход получил название гипердиагностики. Так, например, если при обследовании выявлен большой язвенный дефект в слизистой оболочке желудка и применение всех доступных методов исследования не позволяет ответить на вопрос, хроническая ли это язва или язвенная форма рака, считают, что у пациента рак, и лечат его как онкологического больного. Принцип гипердиагностики, безусловно, нужно применять в разумных пределах. Но если существует вероятность ошибки, всегда правильнее думать о более злокачественной опухоли, большей стадии заболевания и на основании этого использовать более радикальные средства лечения, чем просмотреть рак или назначить неадекватное лечение, в результате чего процесс будет прогрессировать и неминуемо приведёт к летальному исходу. Предраковые заболевания Для ранней диагностики злокачественных заболеваний необходимо проводить профилактическое обследование, так как постановка диагноза рака in situ, например, на основании клинических симптомов крайне затруднительна. Да и на более поздних стадиях атипичная картина течения заболевания может препятствовать его своевременному обнаружению. Профилактическому обследованию подлежат люди из двух групп риска: • лица, по роду деятельности связанные с воздействием канцерогенных факторов (работа с асбестом, ионизирующим излучением и т.д.); • лица с так называемыми предраковыми заболеваниями, которые требуют особого внимания. Предраковыми называют хронические заболевания, на фоне которых резко возрастает частота развития злокачественных опухолей. Так, для молочной железы предраковое заболевание - дисгормональная мастопатия; для желудка - хроническая язва, полипы, хронический атрофический гастрит; для матки - эрозия и лейкоплакия шейки матки и т.д. Пациенты с предраковыми заболеваниями подлежат диспансерному наблюдению с ежегодным осмотром онкологом и проведением специальных исследований (маммография, фиброгастродуоденоскопия). Специальные методы диагностики В диагностике злокачественных новообразований наряду с общепринятыми методами (эндоскопия, рентгенография, УЗИ) особое, иногда решающее значение имеют различные виды биопсии с последующим гистологическим и цитологическим исследованием. При этом обнаружение в препарате злокачественных клеток достоверно подтверждает диагноз, в то время как отрицательный ответ не позволяет его снять - в таких случаях ориентируются на клинические данные и результаты других методов исследования. Опухолевые маркёры Как известно, в настоящее время специфических для онкологических процессов изменений клинических и биохимических параметров крови не существует. Однако в последнее время в диагностике злокачественных опухолей всё большее значение приобретают опухолевые маркёры (ОМ). ОМ в большинстве случаев представляют собой сложные белки с углеводным либо липидным компонентом, синтезирующиеся в опухолевых клетках в больших концентрациях. Эти белки могут быть связанными с клеточными структурами и тогда их обнаруживают при иммуногистохимических исследованиях. Большая группа ОМ секретируется опухолевыми клетками и накапливается в биологических жидкостях онкологических больных. В этом случае их можно использовать для серологической диагностики. Концентрация ОМ (прежде всего в крови) в определённой степени может коррелировать с возникновением и динамикой злокачественного процесса. В клинике широко применяют около 15-20 ОМ. Основные методы определения уровня ОМ в сыворотке крови - радиоиммунологический и иммуноферментный. Наиболее распространены в клинической практике следующие опухолевые маркёры: осфетопротеин (для рака печени), карциноэмбриональный антиген (для аденокарциномы желудка, толстой кишки и др.), простатспецифический антиген (для рака предстательной железы) и др. Известные в настоящее время ОМ, за небольшим исключением, ограниченно пригодны для диагностики или скрининга опухолей, так как повышение их уровня наблюдают у 10-30% больных с доброкачественными и воспалительными процессами. Тем не менее ОМ нашли широкое применение при динамическом наблюдении за онкологическими больными, для раннего выявления субклинических рецидивов и контроля за эффективностью противоопухолевой терапии. Исключение составляет лишь простатоспецифический антиген, используемый для прямой диагностики рака предстательной железы. Общие принципы лечения Лечебная тактика доброкачественных и злокачественных опухолей различна, что прежде всего зависит от инфильтрирующего роста, склонности к рецидивированию и метастазированию последних. Лечение доброкачественных опухолей Основной и в подавляющем большинстве случаев единственный способ лечения доброкачественных новообразований - хирургический. Лишь в лечении опухолей гормонозависимых органов вместо или вместе с хирургическим методом применяют гормональную терапию. Показания к операции При лечении доброкачественных новообразований важен вопрос о показаниях к операции, так как эти опухоли, не несущие угрозы для жизни пациента, не всегда должны быть обязательно удалены. Если у пациента длительное время существует доброкачественная опухоль, не причиняющая ему никакого вреда, и в то же время есть противопоказания к хирургическому лечению (тяжёлые сопутствующие заболевания), то оперировать больного вряд ли целесообразно. При доброкачественных новообразованиях операция необходима при наличии определённых показаний: • Постоянная травматизация опухоли. Например, опухоль волосистой части головы, повреждаемая при расчёсывании; образование на шее в области ворота; опухоль в области пояса, особенно у мужчин (трение брючным ремнём). • Нарушение функции органа. Лейомиома может нарушать эвакуацию из желудка, доброкачественная опухоль бронха может полностью закрыть его просвет, феохромоцитома за счёт выброса катехоламинов приводит к высокой артериальной гипертензии и т.д. • До операции нет абсолютной уверенности в том, что опухоль имеет злокачественный характер. В этих случаях операция, кроме лечебной функции, выполняет ещё и роль эксцизионной биопсии. Так, например, при новообразованиях щитовидной или молочной железы больных в ряде случаев оперируют потому, что при такой локализации вопрос о злокачественности опухоли может быть решён только после срочного гистологического исследования. Результат исследования становится известен хирургам в то время, когда пациент ещё находится под наркозом на операционном столе, что помогает им выбрать правильные вид и объём операции. • Косметические дефекты. Это прежде всего характерно для опухолей на лице и шее, особенно у женщин, и не требует особых комментариев. Принципы хирургического лечения Под хирургическим лечением доброкачественной опухоли понимают полное её удаление в пределах здоровых тканей. При этом образование должно быть удалено целиком, а не по частям, и вместе с капсулой, при наличии таковой. Иссечённое новообразование обязательно подлежит гистологическому исследованию (срочному или плановому), учитывая, что после удаления доброкачественной опухоли рецидивы и метастазы не возникают; после операции пациенты полностью выздоравливают. Лечение злокачественных опухолей Лечение злокачественных опухолей - более сложная задача. Существуют три способа лечения злокачественных новообразований: хирургический, лучевая терапия и химиотерапия. При этом основным, безусловно, является хирургический метод. Принципы хирургического лечения Удаление злокачественного новообразования - наиболее радикальный, а при некоторых локализациях и единственный метод лечения. В отличие от операций при доброкачественных опухолях здесь недостаточно просто удалить образование. При удалении злокачественного новообразования необходимо соблюдать так называемые онкологические принципы: абластика, антибластика, зональность, футлярность. Абластика Абластика - комплекс мер по предупреждению распространения во время операции опухолевых клеток. При этом необходимо: • выполнять разрезы только в пределах заведомо здоровых тканей; • избегать механического травмирования ткани опухоли; • как можно быстрее перевязать венозные сосуды, отходящие от образования; • перевязать тесёмкой полый орган выше и ниже опухоли (предупреждение миграции клеток по просвету); • удалить опухоль единым блоком с клетчаткой и регионарными лимфатическими узлами; • перед манипуляциями с опухолью ограничить рану салфетками; • после удаления опухоли поменять (обработать) инструменты и перчатки, сменить ограничивающие салфетки. Антибластика Антибластика - комплекс мер по уничтожению во время операции отдельных клеток опухоли, оторвавшихся от основной её массы (могут лежать на дне и стенках раны, попадать в лимфатические или венозные сосуды и в дальнейшем быть источником развития рецидива опухоли или метастазов). Выделяют физическую и химическую антибластику. Физическая антибластика: • использование электроножа; • использование лазера; • использование криодеструкции; • облучение опухоли перед операцией и в раннем послеоперационном периоде. Химическая антибластика: • обработка раневой поверхности после удаления опухоли 70° спиртом; • внутривенное введение противоопухолевых химиопрепаратов на операционном столе; • регионарная перфузия противоопухолевыми химиотерапевтическими препаратами. Зональность При операции по поводу злокачественного новообразования нужно не только удалить его, но и убрать всю зону, в которой могут быть отдельные раковые клетки, - принцип зональности. При этом учитывают, что злокачественные клетки могут находиться в тканях вблизи опухоли, а также в отходящих от неё лимфатических сосудах и регионарных лимфатических узлах. При экзофитном росте (опухоль на узком основании, а большая её масса обращена к внешней среде или к внутреннему просвету - полиповидная, грибовидная форма) нужно отступить от видимой границы образования на 5-6 см. При эндофитном росте (распространение опухоли по стенке органа) от видимой границы следует отступить не менее 8-10 см. Вместе с органом или его частью единым блоком необходимо удалить все лимфатические сосуды и узлы, собирающие лимфу из этой зоны (при раке желудка, например, следует удалить весь большой и малый сальник). Некоторые подобные операции получили название «лимфодисекция». В соответствии с принципом зональности при большей части онкологических операций удаляют весь орган или большую его часть (при раке желудка, например, возможно выполнение лишь субтотальной резекции желудка [оставление 1/7-1/8 его части] или экстирпации желудка [полное его удаление]). Радикальные хирургические вмешательства, выполненные с соблюдением всех онкологических принципов, отличаются сложностью, большим объёмом и травматичностью. Даже при небольшой по размерам эндофитно растущей опухоли тела желудка производят экстирпацию желудка с наложением эзофагоэнтероанастомоза. При этом единым блоком вместе с желудком удаляют малый и большой сальник, а в некоторых случаях и селезёнку. При раке молочной железы единым блоком удаляют молочную железу, большую грудную мышцу и подкожную жировую клетчатку с подмышечными, над- и подключичными лимфатическими узлами. Наиболее злокачественная из всех известных опухолей меланома требует широкого иссечения кожи, подкожно-жировой клетчатки и фасции, а также полного удаления регионарных лимфатических узлов (при локализации меланомы на нижней конечности, например, паховых и подвздошных). При этом размеры первичной опухоли обычно не превышают 1-2 см. Футлярность Лимфатические сосуды и узлы, по которым возможно распространение опухолевых клеток, обычно расположены в клетчаточных пространствах, разделённых фасциальными перегородками. В связи с этим для большей радикальности необходимо удаление клетчатки всего фасциального футляра, желательно вместе с фасцией. Яркий пример соблюдения принципа футлярности - операция по поводу рака щитовидной железы. Последнюю удаляют экстракапсулярно (вместе с капсулой, образованной висцеральным листком IV фасции шеи), при том что из-за опасности повреждения п. laryngeus recurrens и околощитовидных желёз удаление ткани щитовидной железы при доброкачественном её поражении обычно выполняют интракапсулярно. При злокачественных новообразованиях наряду с радикальными применяют паллиативные и симптоматические хирургические вмешательства. При их выполнении онкологические принципы либо не соблюдают, либо выполняют не в полном объёме. Подобные вмешательства производят для улучшения состояния и продления жизни пациента в тех случаях, когда радикальное удаление опухоли невозможно из-за запущенности процесса или тяжёлого состояния больного. Например, при распадающейся кровоточивой опухоли желудка с отдалёнными метастазами выполняют паллиативную резекцию желудка, достигая улучшения состояния больного за счёт прекращения кровотечения и уменьшения интоксикации. При раке поджелудочной железы с механической желтухой и печёночной недостаточностью накладывают обходной билиодигестивный анастомоз, ликвидирующий нарушение оттока желчи и т.д. В некоторых случаях после паллиативных операций на оставшуюся массу опухолевых клеток воздействуют лучевой или химиотерапией, достигая излечения пациента. Основы лучевой терапии Применение лучевой энергии для лечения онкологических больных основано на том, что быстро размножающиеся клетки опухоли с большой интенсивностью обменных процессов более чувствительны к воздействию ионизирующего излучения. Задача лучевого лечения - уничтожение опухолевого очага с восстановлением на его месте тканей, обладающих нормальными свойствами обмена и роста. При этом действие лучевой энергии, приводящее к необратимому нарушению жизнеспособности клеток опухоли, не должно достигать такой же степени влияния на окружающие её нормальные ткани и организм больного в целом. Чувствительность опухолей к облучению Различные виды новообразований по-разному чувствительны к лучевой терапии. Наиболее чувствительны к облучению соединительнотканные опухоли с круглоклеточными структурами: лимфосаркомы, миеломы, эндотелиомы. Высокочувствительны отдельные виды эпителиальных новообразований: семинома, хорионэпителиома, лимфоэпителиальные опухоли глоточного кольца. Локальные изменения при таких видах опухолей довольно быстро исчезают под воздействием лучевой терапии, но это, однако, не означает полного излечения, так как указанные новообразования обладают высокой способностью к рецидивированию и метастазированию. В достаточной степени реагируют на облучение опухоли с гистологическим субстратом покровного эпителия: рак кожи, губы, гортани и бронхов, пищевода, плоскоклеточный рак шейки матки. Если облучение применяют при небольших размерах опухоли, то с уничтожением первичного очага может быть достигнуто стойкое излечение пациента. В меньшей степени подвержены лучевому воздействию различные формы железистого рака (аденокарциномы желудка, почки, поджелудочной железы, кишечника), высокодифференцированные саркомы (фибро-, мио-, остео-, хондросаркомы), а также меланобластомы. В таких случаях облучение может быть лишь вспомогательным способом лечения, дополняющим хирургическое вмешательство. Основные способы лучевой терапии В зависимости от места нахождения источника излучении выделяют три основных вида лучевой терапии: внешнее, внутриполостное и внутритканевое облучение. При внешнем облучении используют установки для рентгенотерапии и телегамматерапии (специальные аппараты, заряжённые радиоактивными Со60, Cs137). Лучевую терапию применяют курсами, выбирая соответствующие поля и дозу облучения. Метод наиболее эффективен при поверхностно расположенных новообразованиях (возможна большая доза облучения опухоли при минимальном повреждении здоровых тканей). В настоящее время внешняя рентгенотерапия и телегамматерапия - наиболее распространённые методы лучевого лечения злокачественных новообразований. Внутриполостное облучение позволяет приблизить источник излучения к месту расположения опухоли. Источник излучения через естественные отверстия вводят в мочевой пузырь, полость матки, полость рта, добиваясь максимальной дозы облучения опухолевой ткани. Для внутритканевого облучения применяют специальные иглы и трубочки с радиоизотопными препаратами, которые хирургическим путём устанавливают в тканях. Иногда радиоактивные капсулы или иглы оставляют в операционной ране после удаления злокачественной опухоли. Своеобразным методом внутритканевой терапии является лечение рака щитовидной железы препаратами I131: после поступления в организм больного йод кумулируется в щитовидной железе, а также в метастазах её опухоли (при высокой степени дифференцировки), таким образом, излучение оказывает губительное действие на клетки первичной опухоли и метастазы. Возможные осложнения лучевой терапии Лучевая терапия - далеко не безобидный метод. Все его осложнения можно разделить на местные и общие. Местные осложнения Развитие местных осложнений связано с неблагоприятным влиянием облучения на здоровые ткани вокруг новообразования и прежде всего на кожу, являющейся первым барьером на пути лучевой энергии. В зависимости от степени повреждения кожи выделяют следующие осложнения: • Реактивный эпидермит (временное и обратимое повреждение эпителиальных структур - умеренный отёк, гиперемия, кожный зуд). • Лучевой дерматит (гиперемия, отёк тканей, иногда с образованием пузырей, выпадение волос, гиперпигментация с последующей атрофией кожи, нарушением распределения пигмента и телеангиоэктазией - расширением внутрикожных сосудов). • Лучевой индуративный отёк (специфическое уплотнение тканей, связанное с повреждением кожи и подкожной клетчатки, а также с явлениями облитерирующего лучевого лимфангита и склерозом лимфатических узлов). • Лучевые некротические язвы (дефекты кожи, отличающиеся выраженной болезненностью и отсутствием какой-либо тенденции к заживлению). Профилактика указанных осложнений включает в себя прежде всего правильный выбор полей и дозы облучения. Общие осложнения Применение лучевого лечения может вызывать общие расстройства (проявления лучевой болезни). Её клинические симптомы - слабость, потеря аппетита, тошнота, рвота, нарушения сна, тахикардия и одышка. В большей степени к лучевым методам чувствительны органы кроветворения, прежде всего костный мозг. При этом в периферической крови возникает лейкопения, тромбоцитопения и анемия. Поэтому на фоне лучевой терапии необходимо не реже 1 раза в неделю выполнять клинический анализ крови. В некоторых случаях неуправляемая лейкопения служит причиной уменьшения дозы облучения или вообще прекращения лучевой терапии. Для уменьшения указанных общих расстройств применяют стимуляторы лейкопоэза, переливание крови и её компонентов, витамины, высококалорийное питание. Основы химиотерапии Химиотерапия - воздействие на опухоль различными фармакологическими средствами. По своей эффективности она уступает хирургическому и лучевому методу. Исключение составляют системные онкологические заболевания (лейкоз, лимфогранулематоз) и опухоли гормонозависимых органов (рак молочной железы, яичника, предстательной железы), при которых химиотерапия высокоэффективна. Химиотерапию обычно применяют курсами в течение длительного времени (иногда в течение многих лет). Различают следующие группы химиотерапевтических средств: • цитостатики, • антиметаболиты, • противоопухолевые антибиотики, • иммуномодуляторы, • гормональные препараты. Цитостатики Цитостатики тормозят размножение опухолевых клеток, угнетая их митотическую активность. Основные препараты: алкилирующие средства (циклофосфамид), препараты растительного происхождения (винбластин, винкристин). Антиметаболиты Лекарственные вещества действуют на обменные процессы в опухолевых клетках. Основные препараты: метотрексат (антагонист фолиевой кислоты), фторурацил, тегафур (антагонисты пиримидина), меркаптопурин (антагонист пурина). Антиметаболиты вместе с цитостатиками широко применяют при лечении лейкозов и низкодифференцированных опухолей соединительнотканного происхождения. При этом используют специальные схемы с применением различных препаратов. Широкое распространение, в частности, получила схема Купера при лечении рака молочной железы. Ниже представлена схема Купера в модификации НИИ онкологии им. Н.Н. Петрова - схема CMFVP (по первым буквам препаратов). На операционном столе: • 200 мг циклофосфамида. В послеоперационном периоде: • в 1-14 сут ежедневно 200 мг циклофосфамида; • 1, 8 и 15-е сут: метотрексат (25-50 мг); фторурацил (500 мг); винкристин (1 мг); • в 1 - 15-е сут - преднизолон (15-25 мг/сут внутрь с постепенной отменой к 26-м сут). Курсы повторяют 3-4 раза с интервалом 4-6 нед. Противоопухолевые антибиотики Некоторые вещества, вырабатываемые микроорганизмами, прежде всего актиномицетами, обладают противоопухолевым действием. Основные противоопухолевые антибиотики: дактиномицин, сарколизин, доксорубицин, карубицин, митомицин. Применение цитостатиков, антиметаболитов и противоопухолевых антибиотиков оказывает токсическое действие на организм пациента. В первую очередь страдают органы кроветворения, печень и почки. Возникают лейкопения, тромбоцитопения и анемия, токсический гепатит, почечная недостаточность. В связи с этим при проведении курсов химиотерапии необходимо контролировать общее состояние пациента, а также клинический и биохимический анализы крови. В связи с высокой токсичностью препаратов у больных старше 70 лет химиотерапию обычно не назначают. Иммуномодуляторы Иммунотерапию стали применять для лечения злокачественных новообразований лишь в последнее время. Хорошие результаты получены при лечении рака почки, в том числе на стадии метастазирования, рекомбинантным интерлейкином-2 в сочетании с интерферонами. Гормональные препараты Гормональную терапию используют для лечения гормонозависимых опухолей. При лечении рака предстательной железы с успехом применяют синтетические эстрагены (гексэстрол, диэтилстильбэстрол, фосфэстрол). При раке молочной железы, особенно у молодых женщин, применяют андрогены (метилтестостерон, тестостерон), а у пожилых в последнее время - препараты с антиэстрогенной активностью (тамоксифен, торемифен). Комбинированное и комплексное лечение В процессе лечения больного можно сочетать основные методы лечения злокачественных опухолей. Если у одного пациента применяют два метода, говорят о комбинированном лечении, если все три - о комплексном. Показания к тому или иному способу лечения или их комбинации устанавливают в зависимости от стадии опухоли, её локализации и гистологической структуры. Примером может служить лечение различных стадий рака молочной железы: • I стадия (и рак in situ) - достаточно адекватного хирургического лечения; • II стадия - комбинированное лечение: необходимо выполнить радикальную хирургическую операцию (радикальная мастэктомия с удалением подмышечных, над- и подключичных лимфатических узлов) и провести химиотерапевтическое лечение; • III стадия - комплексное лечение: вначале применяют облучение, затем выполняют радикальную операцию с последующей химиотерапией; • IV стадия - мощная лучевая терапия с последующей операцией по определённым показаниям. Организация помощи онкологическим больным Применение сложных методов диагностики и лечения, а также необходимость диспансерного наблюдения и длительность лечения обусловили создание специальной онкологической службы. Помощь пациентам со злокачественными новообразованиями оказывают в специализированных лечебно-профилактических учреждениях: онкологических диспансерах, больницах и институтах. В онкологических диспансерах осуществляют профилактические осмотры, диспансерное наблюдение за пациентами с предраковыми заболеваниями, первичный осмотр и обследование больных с подозрением на опухоль, проводят амбулаторные курсы лучевой и химиотерапии, контролируют состояние пациентов, ведут статистический учёт. В онкологических стационарах осуществляют все способы лечения злокачественных новообразований. Во главе онкологической службы России стоит Российский онкологический научный центр РАМН, Онкологический институт им. П.А. Герцена в Москве и Научно-исследовательский институт онкологии им. Н.Н. Петрова в Санкт-Петербурге. Здесь осуществляют координацию научных исследований по онкологии, организационно-методическое руководство другими онкологическими учреждениями, разрабатывают проблемы теоретической и практической онкологии, применяют наиболее современные методы диагностики и лечения. Оценка эффективности лечения Многие годы единственным показателем эффективности лечения злокачественных новообразований была 5-летняя выживаемость. Полагают, что если в течение 5 лет после лечения пациент жив, рецидива и метастазирования не наступило, прогрессирование процесса в дальнейшем уже крайне маловероятно. Поэтому пациентов, проживших 5 лет и более после операции (лучевой или химиотерапии), считают выздоровевшими от рака. Оценка результатов по 5-летней выживаемости и в настоящее время остаётся основной, но в последние годы в связи с широким внедрением новых методов химиотерапии появились и другие показатели эффективности лечения. Они отражают длительность ремиссии, количество случаев регресса опухоли, улучшение качества жизни пациента и позволяют оценить эффект лечения уже в ближайшие сроки. 1 2 |
