Определение показателя адиабаты при адиабатическом расширении газа
 Скачать 240.97 Kb. Скачать 240.97 Kb.
|
 Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования Санкт-Петербургский государственный горный университет  Кафедра общей и технической физикиОтчёт по лабораторной работе № 1По дисциплине: ФизикаТема: Определение показателя адиабаты при адиабатическом расширении газа Выполнил: студент ГНГ-14 ______________ /Блоцкий Максим Александрович/ (подпись) (Ф.И.О.) Проверил: доцент ____________ /Егоров Сергей Валентинович /(должность) (подпись) (Ф.И.О.) Санкт-Петербург 2014 Цель работы: – изучить законы идеального газа и основные положения классической теории теплоёмкости; определить коэффициент Пуассона g - отношение теплоёмкости при постоянном давлении Cp к теплоемкости при постоянном объеме Cv методом адиабатического расширения (методом Клемана - Дезорма). Краткие теоретические сведения Основное явление изучаемое в работе- теплообмен Основные определения физических величин Показатель адиабаты- (коэффициент Пуассона) — отношение теплоёмкости при постоянном давлении (Cp) к теплоёмкости при постоянном объёме (Сv). Молярная теплоемкость-Количество тепла, которое необходимо сообщить одному молю вещества, чтобы повысить его температуру на 1 К Адиабатический процесс- термодинамический процесс в макроскопической системе, при котором система не обменивается тепловой энергией с окружающим пространством Изобарный процесс - термодинамический процесс, происходящий в системе при постоянном давлении. Изохорный процесс - термодинамический процесс, происходящий в системе при постоянном объеме. Количество теплоты – энергия, которую получает или теряет тело при теплопередаче. Теплоемкость – физическая величина, определяющая отношение количества теплоты, полученного телом, к соответствующему изменению его температуры. Законы и соотношения: Первый закон термодинамики: Q=∆U+A, Теплота, сообщаемая системе, расходуется на изменение внутренней энергии системы и на совершение системой работы против внешних сил. Q – количество теплоты подводимое системе ∆U – изменение внутренней энергии системы A – работа, которую совершает система. Соотношение Р.Майера: Cp = CV + R Cp – теплоемкость газа при постоянном давлении Cv – теплоемкость газа при постоянном объеме R – универсальная газовая постоянная Уравнение Бойля-Мариотта: p1V1=p2V2 V2 – объем газа во втором состоянии V1 – объем газа в первом состоянии p1 – давление газа в пером состоянии p2 – давление газа в 2-ом состоянии Уравнение Пуассона: 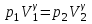 p1 – давление газа в пером состоянии p2 – давление газа во 2-м состоянии V2 – объем газа во втором состоянии V1 – объем газа в первом состоянии y - коэффициент Пуассона. Схема установки (рис.1) 1- Стеклянный сосуд 2,4 - Магистраль 3,10 - Кран 5,6 - Табло 7 - U-образный жидкостный манометр 8 - Баллон с газом 9  - Редуктор - РедукторРасчетные формулы: g=h1/h1-h2 g - коэффициент Пуассона h1 - разность уровней манометра в первом состоянии h2 - разность уровней манометра в третьем состоянии gср= g1+g2+g3+...+gn/n gср - средний коэффициент Пуассона n - количество опытов Формула для расчета погрешностей: X  = h*100/gср = h*100/gсрX - погрешность измерений коэффициента Пуассона Прямые погрешности: ∆h = 1 мм – абсолютная погрешность измерений манометра. Таблица 1. Результаты измерений.
Вычисление значений: gср = 1,39+1,36+1,4+1,37+1,36+1,41+1,45+1,36+1,46+1,43/10=1,4 Расчет погрешности: Х = 1мм/1,4=0,7 Вывод: В результате эксперимента был обнаружен коэффициент Пуассона(отношение теплоемкости при постоянном давлении Cр к теплоемкости при постоянном объеме Cv), по данным его давления после адиабатического расширения и изохорного нагревания. Среднее значение коэффициента Пуассона равно gср = 1,4. |
