Лабораторная работа: определение загрязняющих веществ. Лаб_определение загрязняющих веществ. Определение содержания загрязняющих веществ в воздухе
 Скачать 141.14 Kb. Скачать 141.14 Kb.
|
|
Министерство науки и высшего образования Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего образования Санкт-Петербургский Горный Университет  Кафедра геоэкологии Отчёт по лабораторной работе №2 По дисциплине: Экология Тема: Определение содержания загрязняющих веществ в воздухе Выполнили: студенты группы РТ-17 Королев Н.С. (подпись) (Ф.И.О.) Верещагин И.И. (подпись) (Ф.И.О.) Филинов В.А. (подпись) (Ф.И.О.) Проверил: ассистент Мысин А.В. (подпись) (Ф.И.О.) Санкт-Петербург 2020 Цель работы: изучить методику измерения содержания веществ в воздухе с помощью прибора «ГАНК-4» Краткое теоретическое содержание Углекислый газ (двуокись углерода, диоксид углерода) занимает важнейшее место среди технических газов, он широко используется практически во всех отраслях промышленности и агропромышленного комплекса. На долю СО2 приходится 10% всего рынка технических газов, что ставит этот продукт в один ряд с основными продуктами разделения воздуха. Направления использования углекислого газа в различных агрегатных состояниях многообразны – пищевая промышленность, сварочные газы и смеси, пожаротушение и т.д. Всё больше находит применение и его твердая фаза – сухой лёд, от заморозки, сухих брикетов до очистки поверхностей (бластинга). Получение Извне углекислоту получить нельзя по причине того, что в атмосфере ее почти не содержится. Животные и человек получают её при полном расщеплении пищи, поскольку белки, жиры, углеводы, построенные на углеродной основе, при сжигании с помощью кислорода в тканях образуют углекислый газ (СО2). В промышленности углекислый газ получают из печных газов, из продуктов разложения природных карбонатов (известняк, доломит). В пищевых целях используется газ, образующийся при спиртовом брожении. Также углекислый газ получают на установках разделения воздуха, как побочный продукт получения чистого кислорода, азота и аргона. В лабораторных условиях небольшие количества СО2 получают взаимодействием карбонатов и гидрокарбонатов с кислотами, например, мрамора, мела или соды с соляной кислотой. Побочные источники производства СО2 - продукты горения; брожение; производство жидкого аммиака; установки риформинга; производство этанола; природные источники. Применение По ряду оценок, потребление СО2 на мировом рынке превышает 20 млн. метрических тонн в год. Столь высокий уровень потребления формируется под влиянием требований пищевой промышленности и нефтепромысловых предприятий, технологий газирования напитков и других промышленных нужд, например, снижения показателя ph установок водоочистки, проблем металлургии (в том числе использования сварочного газа) и т.д. Потребление углекислого газа неуклонно растет, поскольку расширяются сферы его применения, которые охватывают задачи от промышленного назначения до пищевого производства – консервация продуктов, в машиностроении от сварочного производства и приготовления защитных сварочных смесей до очистки поверхностей деталей гранулами «сухого льда», в сельском хозяйстве для подкормки растений, в газовой и нефтяной промышленности при пожаротушении. Основные области применения СО2: в машиностроении и строительстве (для сварки и прочее); для холодной посадки частей машин; в процессах тонкой заточки; для электросварки, основанной на принципе защиты расплавленного металла от вредного воздействия атмосферного воздуха; в металлургии; продувка углекислым газом литейных форм; при производстве алюминия и других легкоокисляющихся металлов; в сельском хозяйстве для создания искусственного дождя; в экологии заменяет сильнодействующие минеральные кислоты для нейтрализации щелочной отбросной воды; в изготовлении противопожарных средств; применяется в углекислотных огнетушителях в качестве огнетушащего вещества, эффективно останавливает процесс горения; в парфюмерии при изготовлении духов; в горнодобывающей промышленности; при методе беспламенного взрыва горных пород; в пищевой промышленности; используется как консервант и обозначается на упаковке кодом Е290; в качестве разрыхлителя теста; для производства газированных напитков; Меры борьбы c CO2 в горном деле Основным способом борьбы с поступлением углекислого газа в выработки является деятельное проветривание. При выборе способа вентиляции на углекислотообильных шахтах учитывают порядок отработки шахтного поля, глубину разработки, депрессию выемочных участках, склонность углей пластов к самовозгоранию, утечки воздуха через выработанное пространство и вентиляционные сооружения, интенсивность газо-выделения, места установки регуляторов воздуха, соотношение аэродинамических сопротивлений вентиляционных участков шахты, схемы проветривания участков и шахты в целом, технико-экономическая целесообразность. Применяют также различные средства и способы управления углекислотовыделением, которые позволяют регулировать поступление газа в вентиляционные струи. Их условно делят на две группы: способы, локализующие углекислый газ в источниках его выделения и, способы, изолирующие источники выделения. К первой группе относят поглощение газа щелочными растворами или твердыми адсорбентами, искусственное повышение давления воздуха в периоды падения атмосферного давления, удаление газа из источника газовыделения на поверхность. Вторая группа включает покрытие газоотдающих поверхностей слабопроницаемыми материалами (глина, бетон, пластмассы), сооружение газопроницаемых перемычек и др. Физиологическое воздействие Растворенный в крови углекислый газ активирует дыхательный центр мозга в физиологических и несколько повышенных концентрациях. Незначительные повышения концентрации, вплоть до 0,2−0,4 % (2000−4000 ppm) partspermillion - миллионная доля — единица измерения каких-либо относительных величин, равная 1⋅10^−6 от базового показателя), в помещениях приводят к развитию у людей сонливости и слабости. В значительно более высоких концентрациях он приводит к снижению или устранению рефлекторного респираторного раздражителя, сначала к угнетению дыхания и, наконец, к остановке дыхания. От 5 % углекислого газа во вдыхаемом воздухе возникают головные боли и головокружение, при более высоких концентрациях учащенное сердцебиение (тахикардия), повышение артериального давления, одышка и потеря сознания, так называемая углекислотная анестезия. Концентрация углекислого газа 8 % приводит к смерти в течение 30-60 минут. Накопление углекислого газа в крови называется гиперкапнией. Для помещений нормальным является уровень CO₂ около 600 ppm. Повышенные концентрации углекислого газа снижают когнитивные способности людей. Уже при 1200 ppm расширяются кровеносные сосуды в мозге, снижается активность нейронов и уменьшается объём коммуникации между регионами мозга. В школьных классах типичной является концентрация 2000−2500, а общий разброс значений — от 1000 до 6000, это вызывает обеспокоенность у исследователей, поскольку выявлено снижение результатов учеников, выполняющих тестовые задания в душных помещениях. Монооксид углерода или угарный газ — бесцветный чрезвычайно токсичный газ без вкуса и запаха, легче воздуха (при нормальных условиях). Химическая формула — CO. Получение В лаборатории угарный газ можно получить действием концентрированной серной кислоты на муравьиную или щавелевую кислоты. В промышленности угарный газ получают в газогенераторах при пропускании воздуха через раскаленный уголь. Еще один важный промышленный способ получения угарного газа — паровая конверсия метана. При взаимодействии перегретого водяного пара с метаном образуется угарный газ и водород. Применение Химическая промышленность Окись углерода представляет собой промышленный газ, который имеет множество применений в производстве сыпучих химических веществ. Большие количества альдегидов получают путем реакции гидроформилирования алкенов, окиси углерода и Н2. Гидроформилирование в процессе Шелла дает возможность создавать предшественники моющих средств. Фосген, пригодный для получения изоцианатов, поликарбонатов и полиуретанов, производится путем пропускания очищенного монооксида углерода и газообразного хлора через слой пористого активированного угля, который служит в качестве катализатора. Мировое производство этого соединения в 1989 году оценивалось в 2,74 млн тонн. Металлургия и топливо Угарный газ используют при выплавке чугуна и стали для восстановления железа из оксидов, он находит широкое применение и в органическом синтезе. При взаимодействии смеси оксида углерода (II) с водородом в зависимости от условий (температуры, давления) образуются различные продукты — спирты, карбонильные соединения, карбоновые кислоты. Особенно большое значение имеет реакция синтеза метанола, являющегося одним из основных продуктов органического синтеза. Энергетика Угарный газ используют для синтеза фосгена, муравьиной кислоты, в качестве высококалорийного топлива. Благодаря такой хорошей теплотворной способности, CO является компонентом разных технических газовых смесей (см., например генераторный газ), используемых, в том числе, для отопления. Физиологическое воздействие Угарный газ чрезвычайно опасен для человека. Он вызывает сильное отравление, нередко может стать причиной смерти. Все дело в том, что окись углерода обладает способностью реагировать с гемоглобином крови, выполняющим перенос кислорода всем клеткам тела. В результате такой реакции образуется карбогемоглобин. Из-за недостатка кислорода клетки испытывают голодание. Можно выделить следующие симптомы отравления: тошнота, рвота, головная боль, потеря цветоощущения, расстройство дыхания и другие. Человеку, отравившемуся угарным газом, необходимо как можно скорее оказать первую помощь. Сначала его нужно вытащить на свежий воздух и приставить к носу ватку, смоченную в нашатырном спирте. Далее растереть грудь пострадавшего и приложить к его ногам грелки. Рекомендуется обильное теплое питье. Нужно сразу же после обнаружения симптомов вызвать врача. Описание прибора «ГАНК-4» Многокомпонентный переносной газоанализатор ГАНК-4 (А), (Р), (АР) используется для непрерывного автоматического или периодического контроля концентрации одного из 25 вредных веществ в одном приборе без пробоподготовки в атмосферном воздухе (А), в воздухе рабочей зоны (Р) и в расширенном диапазоне (атмосферный воздух и воздух рабочей зоны) (АР) в целях охраны окружающей среды, обеспечения безопасности труда работников и оптимизации технологических процессов. Измерения концентраций вредных веществ являются последовательными и осуществляются на встроенных датчиках (до 10 датчиков в одном газоанализаторе) и на сменных химкассетах (до 15 химкассет в одном газоанализаторе). Области применения многокомпонентного газоанализатора ГАНК-4 (А), (Р), (АР): лаборатории охраны труда промышленных предприятий; центры оценки условий труда; центры эпидемиологии и гигиены; службы производственного экологического контроля предприятий; региональные экологические службы Минприроды, МЧС, Министерства Обороны нефтехимическая и химическая промышленность; службы экологии железнодорожного и автомобильного транспорта чёрная и цветная металлургия. Газоанализатор включает в себя: электронную схему с микропроцессором, памятью и программным управлением; систему пропуска анализируемого воздуха с малогабаритным насосом; систему газовых коммуникаций; систему встроенных датчиков; сменные химкассеты с миниблоком памяти «TouchMemory» и реактивной лентой на определяемые вещества; фотоголовку с оптронной парой (светодиод-фотодиод); аккумулятор, встроенный в корпус; зарядное устройство для Li-Ion аккумуляторов жидкокристаллический дисплей (ЖКИ); тактовые кнопки управления; разъём RS-232 для подключения персонального компьютера к COM порту. Принцип действия газоанализатора ГАНК-4 (А), (Р), (АР) комбинированный и основан на следующих методах измерений: со встроенными датчиками: электрохимический (СО, О2, и другие), термокаталитический (СН4, C6H14 и другие) или полупроводниковый (C8H8, C6H6 и другие) со сменной химкассетой: оптронноспектрофотометрический с дожигателем и химкассетой: конверсионный оптронноспектрофотометрический (CCL4 и другие). Работа многокомпонентного газоанализатора ГАНК-4 (А), (Р), (АР) Работа газоанализатора осуществляется в автоматическом режиме. Насос подаёт через входной штуцер газоанализатора ГАНК-4 (А), (Р), (АР) анализируемый воздух на датчик или ленту химкассеты. При измерении с помощью электрохимического датчика измеряется величина тока, пропорциональная концентрации определяемого вещества. При измерении с помощью термокаталитического датчика измеряется изменение проводимости на платино-палладиевом электроде при термокаталитической реакции, пропорциональной концентрации определяемого вещества. При измерении с помощью полупроводникового датчика измеряется изменение электропроводимости полупроводникового газочувствительного слоя при химической адсорбции газа на его поверхности, пропорциональной концентрации определяемого вещества. При измерении с помощью химкассеты измеряется скорость изменения потемнения (окраски) ленты, пропорциональная концентрации определяемого вещества. При измерении концентраций анализируемый воздух поступает через входной штуцер на датчик или химкассету. Через время, не более 20 с (при измерении датчиком), или время, не более 30 с (при измерении химкассетой), сигнал поступает в вычислительное устройство, которое преобразовывает его и выдаёт на дисплей в виде значения текущей и средней концентраций в мгм3. Измеренные значения текущей концентрации могут быть записаны пользователем в память газоанализатора ГАНК-4 (А), (Р), (АР) вручную. Интервал выдачи значений усреднённой величины на дисплей осуществляется в зависимости от режима работы газоанализатора и записывается в память автоматически. Текущие и средние значения могут быть просмотрены после измерения в режиме «Просмотр памяти» и выведены на персональный компьютер. При работе в режиме «Непрерывные измерения» измеренные значения текущей концентрации и средняя концентрация вычисляются и выдаются на дисплей от момента включения газоанализатора до момента его выключения (остановки измерений). При превышении уровня предельно допустимой концентрации (ПДК), установленного предприятием-изготовителем, срабатывает звуковая и световая сигнализации. При падении напряжения на аккумуляторе менее 10,2 В на экране высвечивается индикация разрядки аккумулятора и выдаётся звуковой сигнал. При подключении кабеля питания к разъёму и включении в сеть, а также во время работы от сети автоматически производится подзарядка аккумулятора. Таблица с результатами измерений и вычислений. Таблица 1.Определение содержания CO2 в воздухе с помощью анализатора.
Диаграмма 1. Средние значения показателей анализатора 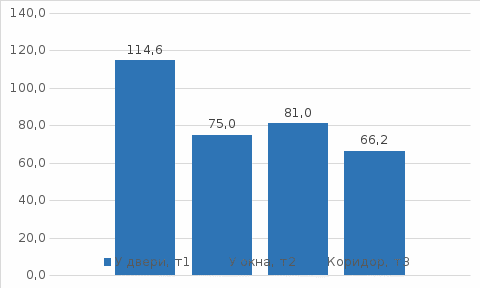 Таблица 2.Определение содержания CO в воздухе с помощью анализатора.
Диаграмма 2. Средние значения показателей анализатора 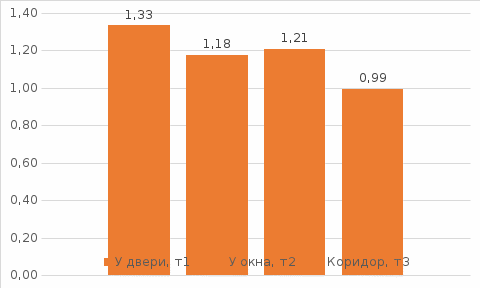 Вывод В результате лабораторной работы изучена методика измерения содержания ртути в воздухе. Получены результаты опытов в виде таблицы 1, 2 и диаграммы 1, 2. При измерении содержания CO2 и СO в коридоре относительно аудитории были примерно на 22% и 12% меньше. Связан такой результат с тем, что пространство имеет больший объем, а газы постоянно подвергаются перемещению. Поэтому мерой для снижения концентрации газов в аудитории следует проводить проветривания. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
