Экзамен перечень 77. Основные исторические этапы развития микробиологии, вклад отечественных и зарубежных ученых. Разделы микробиологии
 Скачать 1.87 Mb. Скачать 1.87 Mb.
|
|
К принципам вакцинопрофилактики относятся: безопасность вакцин информированность: доступность (бесплатно) Аутовакцины - вакцины, изготовляемые из выделенных от б-ного патогенных или условно-патогенных микробов и используемые для его лечения. Могут содержать Аг одного или нескольких видов микроорганизмов в виде: а) живых или инактивированных бактерий, выращенных на жидких или плотных средах; б) комплексных препаратов, содержащих культуры бактерий и их метаболиты; в) хим. препаратов, состоящих из соматических и (или) поверхностных Аг возбудителей заболевания; г) лизатов бактер. к-р или инфицированных тканей. Применяют для лечения хронических, рецидивирующих, локальных или генерализованных заболеваний у лиц с приобретенной недостаточностью иммунной системы (бруцеллез, брюшной тиф, гонорея, склерома, озена, пневмонии, бронхиты, отиты, фурункулез, пиодермии, циститы, пиелиты, уретриты, колиты и др.). Противопоказания к применению такие же, как при использовании вакцин из экзогенных штаммов. Приготовление аутовакцины состоит из: 1) выделения чистой культурры микроба, этиол. или патогенетическая роль к-рого при данном заболевании доказана; 2) идентификации к-ры; 3) стандартизации и обработки к-ры; 4) контроля за стерильностью и безопасностью вакцины. Оценка эффективности А. опирается на динамику клин, картины, элиминацию возбудителя из организма б-ного, нарастание титра Ат Живые вакцины, методы аттенуации вакцинных штаммов и особенности их применения. Живые вакцины - препараты, действующим началом в которых являются ослабленные тем или иным способом, потерявшие свою вирулентность, но сохранившие специфическую антигенность штаммы патогенных бактерий. Примером таких вакцин являются БЦЖ и вакцина против натуральной оспы человека, в качестве которой используется непатогенный для человека вирус оспы коров. Живые вакцины - препараты, действующим началом в которых являются ослабленные тем или иным способом, потерявшие свою вирулентность, но сохранившие специфическую антигенность штаммы патогенных бактерий. Аттенуация (ослабление) возможна путём воздействия на штамм химических (мутагены) и физических (температура) факторов или посредством длительных пассажей через невосприимчивый организм. Так же в качестве живых вакцин используются дивергентные штаммы (непатогенные для человека), имеющие общие протективные антигены с патогенными для человека микробами. Примером такой вакцины является БЦЖ и вакцина против натуральной оспы. Возможно получение живых вакцин генно-инженерным способом. Принцип получения таких вакцин сводится к созданию непатогенных для человека рекмбинантных штаммов, несущих протективные антигены патогенных микробов и способных при введении в орг. человека размножаться и создавать иммунитет. Такие вакцины называют векторными. Вне зависимости от того, какие штаммы включены в вакцины, бактерии получают путём выращивания на искусственных питательных средах, культурах клеток или куриных эмбрионах. В живую вакцину, как правило, добавляют стабилизатор, после чего подвергают лиофильному высушиванию. В связи с тем, что живые вакцины способны вызывать вакцинную инфекцию (живые аттенуированные микробы размножаются в организме, вызывая воспалительный процесс проходящий без клинических проявлений), они всегда вызывают перестройку иммунобиологического статуса организма и образование специфических антител. Это так же может являться недостатком, т. к. живые вакцины чаще вызывают аллергические реакции. Вакцины данного типа, как правило, вводятся однократно. Примеры: сибиреязвенная вакцина, чумная вакцина, бруцеллёзная вакцина, БЦЖ вакцина, оспенная дермальная вакцина. Убитые вакцины и техника их приготовления; контроль. Определение. Применение Инактивированные (убитые) вакцины – препараты, в качестве действующего начала включающие убитые химическим или физическим способом культуры патогенных вирусов или бактерий, (клеточные, вирионные) или же извлечённые из патогенных микробов комплексы антигенов, содержащие в своём составе проективные антигены (субклеточные, субвирионные вакцины). В препараты иногда добавляют консерванты и адьюванты. Молекулярные вакцины – в них антиген находится в молекулярной форме или даже в виде фрагментов его молекул, определяющих специфичность т. е. в виде эпитопов, детерминант. Корпускулярные вакцины – содержащие в своем составе протективный антиген. Инактивированные (убитые, корпускулярные или молекулярные) вакцины – препараты, в качестве действующего начала включающие убитые химическим или физическим способом культуры патогенных вирусов или бактерий, (клеточные, вирионные) или же извлечённые из патогенных микробов комплексы антигенов, содержащие в своём составе проективные антигены (субклеточные, субвирионные вакцины). Для выделения из бактерий и вирусов антигенных комплексов (гликопротеинов, ЛПС, белков) применяют трихлоруксусную кислоту, фенол, ферменты, изоэлектрическое осаждение. Их получают путем выращивания патогенных бактерий и вирусов на искусственных питательных средах, инактивируют, выделяют антигенные комплексы, очищают, конструируют в виде жидкого или лиофильного препарата. Преимуществом данного типа вакцин является относительная простота получения (не требуется длительного изучения и выделения штаммов). К недостаткам же относятся низкая иммуногенность, потребность в трехкратном применении и высокая реактогенность формализированных вакцин. Так же, по сравнению с живыми вакцинами, иммунитет, вызываемый ими, непродолжителен. В настоящее время применяются следующие убитые вакцины: брюшнотифозная, обогащенная Vi антигеном; холерная вакцина, коклюшная вакцина Реакции агглютинации, сущность, техника, варианты, применение. Реакция агглютинации — простая по постановке реакция, при которой происходит связывание антителами корпускулярных антигенов (бактерий, эритроцитов или других клеток, нерастворимых частиц с адсорбированными на них антигенами, а также макромолекулярных агрегатов). Она протекает при наличии электролитов, например при добавлении изотонического раствора натрия хлорида. Применяются различные варианты реакции агглютинации: развернутая, ориентировочная, непрямая и др. Реакция агглютинации проявляется образованием хлопьев или осад¬ка (клетки, «склеенные» антителами, име ющими два или более антигенсвязывающих центра). РА используют для: 1) определения антител в сыворотке крови боль¬ных, например, при бруцеллезе (реакции Райта, Хеддельсона), брюшном тифе и паратифах (реак¬ция Видаля) и других инфекционных болезнях; 2) определения возбудителя, выделенного от больного; 3) определения групп крови с использованием моноклональных антител против алло-антигенов эритроцитов. Для определения у больного антител ставят развернутую реакцию агглютинации: к разведениям сыворотки крови больного добавляют диагностикум (взвесь убитых микробов,) и через несколько часов инкубации при 37 ˚С отмечают наибольшее разведение сыворотки (титр сыворотки), при котором произошла агглютинация, т. е. образовался осадок. Характер и скорость агглютинации зависят от вида антигена и антител. Примером являются особенности взаимодействия диагностикумов (О- и H-антигенов) со специфическими антителами. Реакция агглютинации с О-диагностикумом (бактерии, убитые нагреванием, сохранившие термостабильный О-антиген) происходит в виде мелкозернистой агглютинации. Реакция агглютинации с Н-диагностикумом (бактерии, убитые формалином, сохранившие термолабильный жгутиковый Н-антиген) — крупнохлопчатая и протекает быстрее. Если необходимо определить возбудитель, выделенный от больного, ставят ориентировочную реакцию агглютинации, применяя диагностические антитела (агглютинирующую сыворотку), т. е. проводят серотипирование возбудителя. Ориентировочную реакцию проводят на предметном стекле. К капле диагностической агглютинирующей сыворотки в разведении 1:10 или 1:20 добавляют чистую культуру возбудителя, выделенного от больного. Рядом ставят контроль: вместо сыворотки наносят каплю раствора натрия хлорида. При появлении в капле с сывороткой и микробами хлопьевидного осадка ставят развернутую реакцию агглютинации в пробирках с увели-чивающимися разведениями агглютинирующей сыворотки, к которым добавляют по 2—3 капли взвеси возбудителя. Агглютинацию учитывают по количеству осадка и степени просветления жидкости. Реакцию считают положительной, если агглютинация отмечается в разведении, близком к титру диагностической сыворотки. Одновременно учитывают контроли: сыворотка, разведенная изотоническим раствором натрия хлорида, должна быть прозрачной, взвесь микробов в том же растворе — равномерно мутной, без осадка. Разные родственные бактерии могут агглютинироваться одной и той же диагностической агглютинирующей сывороткой, что затрудняет их идентификацию. Поэтому пользуются адсорбированными агглютинирующими сыворотками, из которых удалены перекрестно реагирующие антитела путем адсорбции их родственными бактериями. В таких сыворотках сохраняются антитела, специфичные только к данной бактерии. Реакции гемагглютинации (прямая, непрямая), реакция торможения гемагглютинации, их диагностическое значение при инфекциях. В основе реакции прямой гемагглютинации лежит способность эритроцитов склеиваться при адсорбции на них определенных антигенов. Поскольку это происходит без участия иммунной сыворотки, реакция не является серологической. В серологических исследованиях реакцию прямой гемагглютинации применяют для выбора рабочего разведения антигена, используемого в реакции торможения гемагглютинации. В основе последней лежит задержка гемагглютинирующего действия антигена специфической сывороткой. Реакция прямой гемагглютинации (РПГА) используется для выявления поверхностных антигенов микроорганизмов и эритроцитов, а также антител к ним. К стандартным сывороткам, содержащим антитела, добавляют исследуемый материал (кровь). Скорость прямой реакции агглютинации связана с количеством исследуемого материала, количеством и концентрацией сыворотки, температурой окружающей среды. Реакция непрямой (пассивной) гемагглютинации (РНГА, РПГА) основана на использовании эритроцитов (или латекса) с адсорбированными на их поверхности антигенами или антителами, взаимодействие которых с соответствующими антителами или антигенами сыворотки крови больных вызывает склеивание и выпадение эритроцитов на дно пробирки или ячейки в виде фестончатого осадка. Компоненты. Для постановки РНГА могут быть использованы эритроциты барана, лошади, кролика, курицы, мыши, человека и другие, которые заготавливают впрок, обрабатывая формалином или глютаральдегидом. Адсорбционная емкость эритроцитов увеличивается при обработке их растворами танина или хлорида хрома. Антигенами в РНГА могут служить полисахаридные АГ микроорганизмов, экстракты бактериальных вакцин, АГ вирусов и риккетсий, а также другие вещества. Эритроциты, сенсибилизированные АГ, называются эритроцитарными диагностикумами. Для приготовления эритроцитарного диагностикума чаще всего используют эритроциты барана, обладающие высокой адсорбирующей активностью. Применение. РНГА применяют для диагностики инфекционных болезней, определения гонадотропного гормона в моче при установлении беременности, для выявления повышенной чувствительности к лекарственным препаратам, гормонам и в некоторых других случаях. Механизм. Реакция непрямой гемагглютинации (РНГА) отличается значительно более высокой чувствительностью и специфичностью, чем реакция агглютинации. Ее используют для идентификации возбудителя по его антигенной структуре или для индикации и идентификации бактериальных продуктов — токсинов в исследуемом патологическом материале. Соответственно используют стандартные (коммерческие) эритроцитарные антительные диагностикумы, полученные путем адсорбции специфических антител на поверхности танизированных (обработанных танином) эритроцитов. В лунках пластмассовых пластин готовят последовательные разведения исследуемого материала. Затем в каждую лунку вносят одинаковый объем 3 % суспензии нагруженных антителами эритроцитов. При необходимости реакцию ставят параллельно в нескольких рядах лунок с эритроцитами, нагруженными антителами разной групповой специфичности. Через 2 ч инкубации при 37 °С учитывают результаты, оценивая внешний вид осадка эритроцитов (без встряхивания): при отрицательной реакции появляется осадок в виде компактного.диска или кольца на дне лунки, при положительной реакции — характерный кружевной осадок эритроцитов, тонкая пленка с неровными краями. 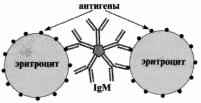 Реакция торможения гемагглютинации (РТГА) - метод идентификации вируса или выявления противовирусных антител в сыворотке крови больного, основанный на феномене отсутствия агглютинации эритроцитов препаратом, содержащим вирус, в присутствии иммунной к нему сыворотки крови. Реакция торможения гемагглютинации (РТГА) основана на блокаде, подавлении антигенов вирусов антителами иммунной сыворотки, в результате чего вирусы теряют свойство агглютинировать эритроциты. РТГА применяют для диагностики многих вирусных болезней, возбудители которых (вирусы гриппа, кори, краснухи, клещевого энцефалита и др.) могут агглютинировать эритроциты различных животных. Механизм. Типирование вируса проводят в реакции торможения гемаг-глютинации (РТГА) с набором типоспецифических сывороток. Результаты реакции учитывают по отсутствию гемагглютинации. Подтипы вируса А с антигенами H0N1, H1N1, Н2N2, H3N2 и др. могут быть дифференцированы в РТГА с набором гомологичных типоспецифических сывороток. 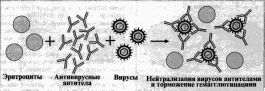 Реакция гемадсорбции и реакция торможения гемадсорбции, их диагностическое значение при вирусных инфекциях. Гемадсорбция - процесс адсорбции эритроцитов на поверхности инфицированных вирусами клеток. Наблюдается в основном у вирусов, вирионы к-рых после образования выходят из клетки путем почкования, напр., у орто- и парамиксовирусов. Проводят для индикации вируса на чувствительной к нему к-ре клеток. Наблюдаются различия в типе адсорбции (диффузный, очаговый), виде сорбируемых эритроцитов (человека, обезьян, морской свинки и др.), температуре, при к-рой протекает реакция (37°С , 0°С), наличии элюции (есть, нет). Г. может быть заторможена предварительной инкубацией инфицированной вирусом к-ры клеток со специфической к вирусу антисывороткой. Реакцию торможения Г. используют для идентификации вирусов. Реакция связывания комплемента, сущность, техника, варианты, применение. Специфичность РСК при вирусных инфекциях. Примеры. Реакция связывания комплемента (РСК) за¬ключается в том, что при соответствии друг другу антигены и антитела образуют иммун¬ный комплекс, к которому через Fc-фрагмент антител присоединяется комплемент (С), т. е. происходит связывание комплемента комп¬лексом антиген—антитело. Если же комплекс антиген—антитело не образуется, то комп¬лемент остается свободным. Специфическое взаимодействие АГ и AT сопровождается адсорб¬цией (связыванием) комплемента. Поскольку процесс связыва¬ния комплемента не проявляется визуально, Ж. Борде и О.Жангу предложили использовать в качестве индикатора гемолитическую систему (эритроциты барана + гемолитическая сыворотка), кото¬рая показывает, фиксирован ли комплемент комплексом АГ-АТ. Если АГ и AT соответствуют друг другу, т. е. образовался иммунный комплекс, то комплемент связывается этим комплексом и гемоли¬за не происходит. Если AT не соответствует АГ, то комплекс не образуется и комплемент, оставаясь свободным, соединяется со второй системой и вызывает гемолиз. Компоненты. Реакция связывания комплемента (РСК) относится к слож¬ным серологическим реакциям. Для ее проведения необходимы 5 ингредиентов, а именно: АГ, AT и комплемент (первая система), эритроциты барана и гемолитическая сыворотка (вторая система). Антигеном для РСК могут быть культуры различных убитых микроорганизмов, их лизаты, компоненты бактерий, патологи¬чески измененных и нормальных органов, тканевых липидов, ви-русы и вирусосодержащие материалы. В качестве комплемента используют свежую или сухую сыво¬ротку морской свинки. Механизм. РСК проводят в две фазы: 1-я фаза — инкубация смеси, содержащей три компонента антиген + антитело + комплемент; 2-я фаза (инди¬каторная) — выявление в смеси свободного комплемента путем добавления к ней гемоли¬тической системы, состоящей из эритроцитов барана, и гемолитической сыворотки, содер¬жащей антитела к ним. В 1-й фазе реакции при образовании комплекса антиген—антите¬ло происходит связывание им комплемента, и тогда во 2-й фазе гемолиз сенсибилизирован¬ных антителами эритроцитов не произойдет; реакция положительная. Если антиген и ан¬титело не соответствуют друг другу (в иссле¬дуемом образце нет антигена или антитела), комплемент остается свободным и во 2-й фазе присоединится к комплексу эритроцит — ан-тиэритроцитарное антитело, вызывая гемо¬лиз; реакция отрицательная. Применение. РСК применяют для диагностики многих инфекционных болезней, в частности сифи-лиса (реакция Вассермана). Реакция преципитации, сущность, техника, варианты, применение. Реакция преципитации (РП) - это формирование и осаждение комплекса растворимого молекулярного антигена с антителами в виде помутнения, называемого преципитатом. Он образуется при смешивании антигенов и антител в эквивалентных количествах; избыток одного из них снижает уровень образования иммунного комплекса. |
