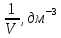Лабораторная физика. Лаба II-4. Отчет по Лабораторной работе ii4 Состояние уравнения ВандерВаальса
 Скачать 0.57 Mb. Скачать 0.57 Mb.
|
Кафедра гуманитарных и естественно-научных дисциплин Дисциплина: Физика Отчет по Лабораторной работе № II-4 «Состояние уравнения Ван-дер-Ваальса» Выполнили: Нургалин Ринат Фоменко Иван студенты группы ГД-21104 Проверила: доцент кафедры ГЕНД Коржавина Наталья Валерьевна г. Верхняя Пышма 2022 Цель работы: Ознакомиться с поведением вещества, находящегося в газообразном состоянии и переходящего в жидкое состояние. Экспериментально подтвердить закономерности поведения реального газа. Оборудование: Компьютерная модель. Ход работы: Эксперимент 1. Определение критических параметров. 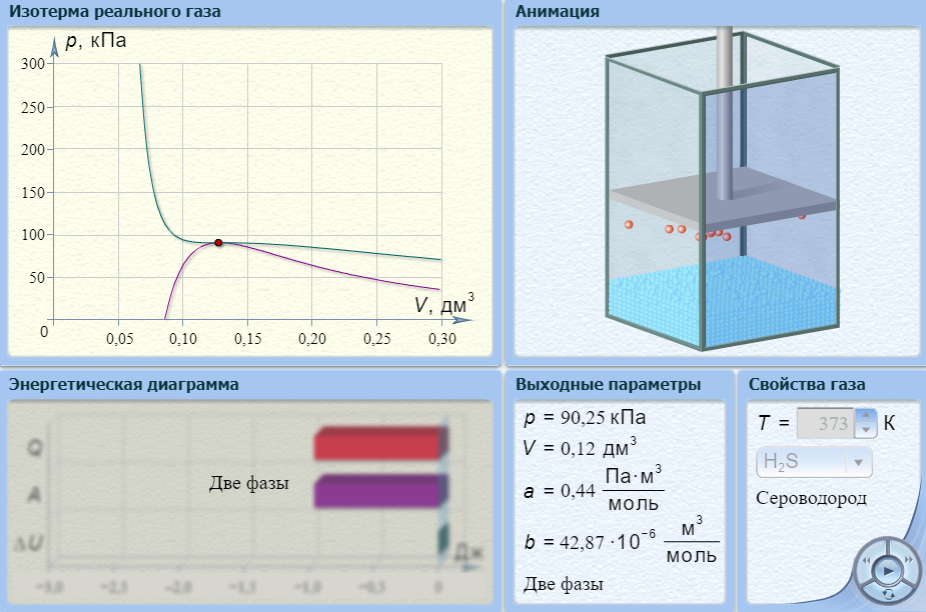 Подвели маркер курсора на регулятор температуры и нажали левую кнопку мыши. Удерживая кнопку в нажатом положении, пытались добиться состояния, когда появится критическая изотерма. Температура критической изотермы называется критической температурой. 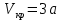 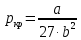 Следовательно, исходя из данных: 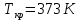 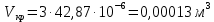 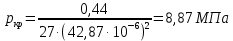 Эксперимент 2. Исследование изотерм газа ВдВ. Таблица 1. Результаты измерений при температуре Т= 450 К.
Таблица 2. Результаты измерений при температуре Т= 500 К.
Таблица 3. Результаты измерений при температуре Т= 550 К.
Таблица 4. Результаты измерений при температуре Т= 600 К.
По измеренным значения критических параметров, вычислили константу 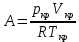 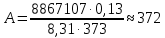 Построили на одном рисунке графики экспериментальных зависимостей давления pот обратного объема 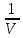 для начальных точек всех изотермических процессов. для начальных точек всех изотермических процессов.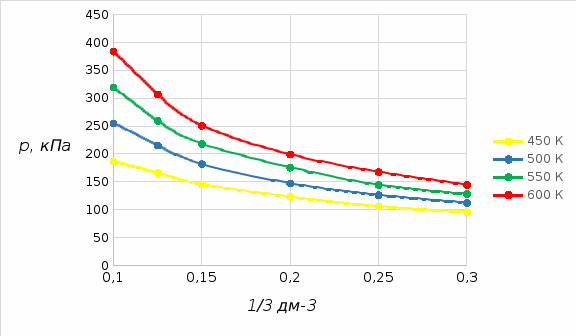 Для каждой изотермы определили значение количества вещества, используя формулу 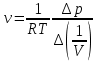 v1= 0,12 моль v2= 0,17 моль v3= 0,21 моль v4= 0,24 моль Вычислим среднее значение vи величину константы A’ по формуле A’=0,375v. 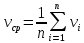 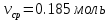 A’=0,06938 Вывод:В данной лабораторной работе мы нашли критические данные по H2S – Tкр= 373 K, Vкр= 0,13 дм3, pкр= 8,87 МПа. Нашли давление и обратный объем от разных значений температур. Сделали график, по которому мы увидели, что при повышении температуры (V=const), давление возрастает. И при возрастании обратного объема, давление снижается. |