Отчет. Отчет по нирс за I семестр 20172018 г. Анодное оксидирование металлического Al для мембранных технологий
 Скачать 0.64 Mb. Скачать 0.64 Mb.
|
|
Министерство образования и науки Российской Федерации Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТОМСКИЙ ПОЛИТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ» Институт физики высоких технологий Направление подготовки 22.04.01 Материаловедение и технология материалов Кафедра Наноматериалов и нанотехнологий Отчет по НИРС за I семестр 2017/2018 г. «Анодное оксидирование металлического Al для мембранных технологий» Выполнил: студент гр. 4БМ72 кафедры НМНТ Тилеуберди Т. Научный руководитель: доц.каф. НМНТ к.х.н. Воронова Г.А. Проверил: доц.каф. НМНТ к.х.н. Лямина Г.В. Оценка научного руководителя___________ Томск 2018 Реферат В отчете представлен обзор литературных данных на тему «Анодное оксидирование металлического Al для мембранных технологий». Ключевые слова: мембрана, анодирование, высокоупорядоченного роста, самоорганизованный, анодирование, оксид алюминия, нанопористый, наночастицы, структура, морфология. Сокращения и обозначения: АОП- анодными оксидными пленками AOA- анодные оксиды алюминия АСМ-атомно силовой микроскоп Анодными оксидами или анодными пленками (АОП) принято называть, прежде всего, оксидные слои, которые образуются на поверхности металлов и полупроводников при их анодной поляризации в растворах электролитов [1]. Применение различных электролитов позволяет варьировать структуру и морфологию пленок и как следствие, их свойства. Так в умеренно растворяющих оксид электролитах например, водных растворах серной, ортофосфорной, щавелевой и других кислот при анодировании алюминия образуются оксидные пленки с регулярно- пористым строением, иначе пористые анодные оксиды алюминия (AOA). Пористые AOA могут иметь толщину В десятки и сотни микрометров и состоят из тонкого плотного. барьерного. примыкающего к поверхности металла, и пористого слоев [1-211]. 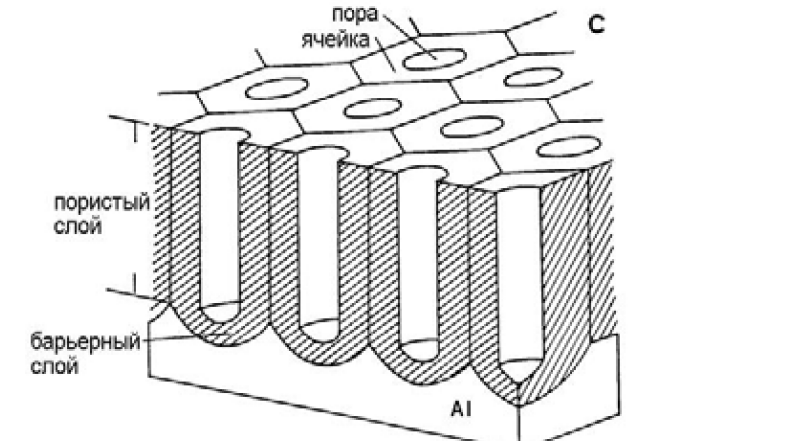 Рис.1.1. Схематическое изображение идеального строения пористого AOA. Согласно идеальной модели (рис,1.1), поры в таком оксиде представляют собой цилиндрические каналы одинакового диаметра. изменяющегося в зависимости от условий формирования от 10 до 250 нм нормальные к поверхности метали и находящиеся в центрах гексагональных ячеек [14, 17-211]. В конце 20 века были установлены условия формирования пористых АОП на алюминии с высокой степенью порядка в расположении пор, так называемых самоорганизованных АОП, в водных электролитах на основе щавелевой, серной, ортофосфорной кислот [24]. С применением этих условий получены высокоупорядоченные АОП на алюминии с диаметром пор: (20-25) нм, (40-80) нм и (160-180) нм, соответственно. Представляет интерес расширение размерного ряда пор, а также поиск условий ускоренного формирования высоко упорядоченных АОП. В связи с этим, актуально изучение процесса анодирования в органических электролитах. Известно [50,51], что анодирование в водных растворах малиновой кислоты позволяет достичь напряжений Ua = 100-125 В и получить АОП с размерами пор 70-130 нм в зависимости от выбранного напряжения. В данном разделе представлены результаты параллельного изучения кинетики роста АОП, формируемых в водном растворе 20% H4C3O4 при различных значениях I,А и температуры электролита, и строения поверхности барьерного и пористого слоев методом АСМ. В качестве подложек использовался предварительно отожженный алюминий А99. Перед анодированием образцы подвергались химической очистке в щелочи и электрохимической полировке. Анодирование проводилось в ГСР. Анодирование при комнатной температуре приводило к сильному разогреву электролита, поэтому была использована двухэлектродная электрохимической ячейка с охлаждающим модулем на основе элементов Пельтье. Температура процесса поддерживалась Та 283-287К. Сравнение кинетических зависимостей показывает, что увеличение ja в два раза приводит к увеличению скорости роста Ua на начальном участке (от 1,2 В/с до 2,8 В/с) и более быстрому зарождению и развитию пор. Однако величина Ua, соответствующего процессу стационарного роста пор для всех значений ja практически не меняется и составляет Uaст=(100±3)В. Оценка толщины полученных АОП, сформированных при j=0.5 А/дм2 в течение 30 минут, дала значение = 15 мкм. Как следует из АСМ-изображения, на поверхности пористого слоя, наблюдаются выходы пор (диаметр порядка 60-80 нм), т.е. отмечается неполная их открытость, поскольку оценка размера основных пор с помощью универсального эмпирического соотношения, связывающего размер ячейки с величиной напряжения стационарного роста Uaст [23], дает величину dп 100 нм. Скорее всего, на поверхности пористого массива присутствует «дефектный» слой, отражающий состояние барьерного слоя АОП на стадии зарождения пор, что является характерным для ГСР-анодирования. Таким образом, ГСР-анодирование алюминия в водном растворе 20% H4C3O4 при Та=283К позволяет получить на его поверхности самоорганизованные пористые АОП с размером пор порядка 100 нм. Формирование АОП в данном электролите является мало энергозатратным, поскольку скорость роста толщины пористых АОП в растворе малоновой кислоты в выбранных условиях составляет d8/dt=30 мкм/ч, что превышает в два раза скорость роста АОА в растворе щавелевой кислоты. Согласно высокоупорядоченное анодирование А1 в растворе Н3РО4 позволяет сформировать оксиды с размерами пор вп 250 нм, что значительно расширяет спектр функциональности таких оксидов, создавая возможности их применения, например, в качестве фотонных кристаллов Однако попытка ВСР анодирования фольги в 10% Н3Р04 при Ua=160 В и Та=273К оказалась неудачной, поскольку при таком напряжении происходил неконтролируемый рост тока на начальном этапе формирования барьерного слоя. По этой причине далее в ГСР была сделана серия экспериментов для установления оптимального значения плотности тока анодирования, при котором напряжение стационарного роста достигло бы Uaст160 В. При анодировании химически очищенной алюминиевой фольги в ГСР в 1% Н3Р04 при jа=0.15 А/дм2 и 0.2 А/дм2 величина Гаст составляет 175В и 180В, соответственно (рис.3.14). Разброс в значениях напряжения Ua при jа=0.15 А/дм2 не превышает 3В, а при jа=0.2 А/дм2 доходит до 5В. Время выхода на стационарный режим при jа=0.15 А/дм2 составляет 3500 сек, а при jа=0.2 А/дм2 - 2400 сек. Отсюда следует, что наиболее оптимальными условиями для высокоупорядоченного роста АОА в фосфорнокислом электролите является концентрация электролита 1% Н3Р04, ja=0.15 А/дм2, использование которых позволяет проводить анодирование при Ua160 В. 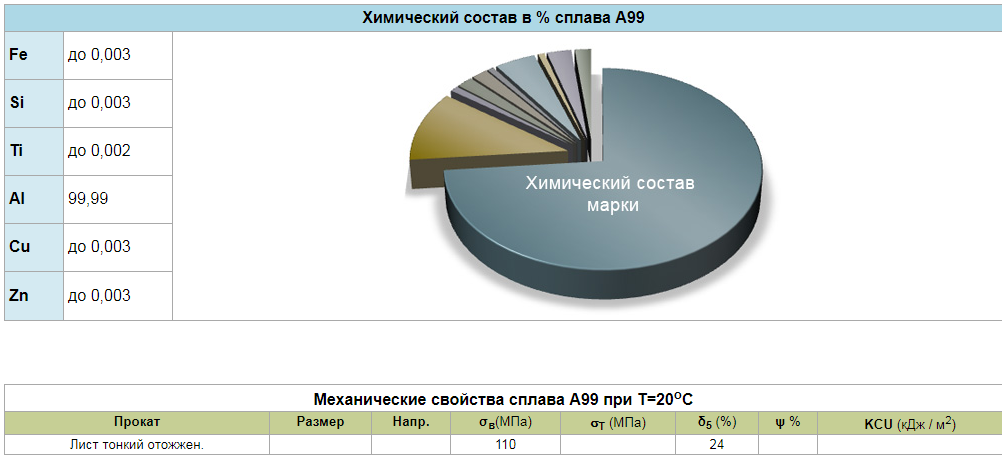 Листовой алюминий поставляется потребителям в листах мерной длины, кратной мерной в пределах длин, установленных ГОСТом 21631-76 (с интервалом 500 мм), немерной длины или в рулонах массой от одной до трех тонн. В зависимости от марки алюминия и технологии его обработки длина листа составляет от 2000 мм до 7000 мм. Ширина алюминиевого листа в мм, установленная ГОСТом: 600, 800, 900, 1000, 1200, 1400, 1600, 1800, 2000. По толщине листа листовой алюминий занимает промежуточное положение между алюминиевой фольгой (толщина 0,007–0,2 мм) и алюминиевыми плитами (толщина 11–200 мм). ГОСТ 21631-76 регламентирует как собственно толщину алюминиевого листа, так и предельно допустимые отклонения от нее. Согласно ГОСТу толщина алюминиевого листа должна составлять 0,3–10,5 мм. образцы алюминиевой фольги (А99) толщиной 100 мкм и более до 500 мкм В процессе электрохимического оксидирования алюминия в растворах электролитов (анодирования) часто имеет место конкуренция нескольких анодных процессов, таких как образование пленки, растворение пленки и растворение металла (питтинг) [1]. Это обеспечивает возможность формирования анодных оксидов алюминия (АОА) с широким спектром структурно-морфологических и электрофизических характеристик за счет изменения состава электролита и условий процесса анодирования. На алюминии (и целом ряде сплавов на его основе) могут быть получены как плотные, барьерного типа, так и пористые АОА, в том числе самоорганизованные пленки с регулярно расположенными цилиндрическими порами наноразмерного диаметра. Если толщина (δ) плотных пленок, как правило, не превышает 1 мкм, то для пористых АОА она может составлять сотни микрометров. Спектр функциональности пористых оксидных пленок (несмотря на более низкие по сравнению с барьерными диэлектрические характеристики) очень широк: они применяются как защитно-декоративные, электроизоляционные, износостойкие, антикоррозионные покрытия, используются в микроэлектронике, оптике, мембранной технике, различных датчиках. В ряде случаев формирование пористых оксидных пленок применяется для создания подслоев, обеспечивающих улучшенную адгезию при последующей обработке (нанесении лакокрасочных, некоторых гальванических покрытий и др.). Так, например, получение гальванических покрытий высокого качества на алюминии достигается при использовании предварительного анодирования алюминия в растворе фосфорной или азотной кислоты [2]. Следует отметить, что электрохимические процессы при формировании наноструктурированных анодно-оксидных пленок на алюминии и его сплавах осуществляются с использованием слабых, нетоксичных электролитов при более низких температурах и нормальном давлении, чем технологические процессы получения керамических покрытий, что определяет значительно меньшие значительно меньшие энергозатраты и более высокую степень экологичности. Пористые анодные оксиды алюминия (ПАОА) состоят из тонкого плотного или барьерного, примыкающего к поверхности металла, и пористого слоев. Согласно идеальной модели поры представляют собой одинаковые цилиндрические каналы с диаметром в зависимости от условий формирования от 10 до 250 нм, нормальные к поверхности металла и находящиеся в центрах гексагональных ячеек (рис. 1). Согласно многочисленным исследованиям [3—6], пористые АОА имеют явно гетерогенное строение, представленное областями условно чистого Al2O3 и оксида, «загрязненного» анионами электролита. Причем распределение анионов неоднородно: они сосредоточены в основном в стенках и у дна пор, где их концентрация может превышать более чем в два раза среднюю концентрацию в пленке. Приближенная оценка, проведенная на основе электронно-микроскопических данных, показывает, что анионо содержащая часть пористого оксида составляет примерно 60÷80% материала стенок ячеек для пленок, сформированных в водных растворах C2H2O4, 70% — H3PO4 и 30% — H2SO4 [7]. В соответствии с данными [7—11], формирование анионосодержащего слоя осуществляется в результате чередования процессов стимулированного полем растворения оксида с образованием оксоанионных комплексов и осаждения их на стенки пор. Соответственно, соотношение объемов чистого и загрязненного анионами оксида будет зависеть, прежде всего, от состава электролита, а также  Рис. 1. Фотографии реплик поверхности пористого (а) и барьерного (b) слоев оксидной пленки, сформированной при анодировании алюминия в 3% С2Н2О4. Схематическое изображение строения ПАОА (с) электрофизических условий анодирования. Анодирование алюминия и его сплавов в широком диапазоне условий (так называемое традиционное анодирование) [6, 12, 13] приводит к формированию ПАОА, строение которых заметно отличается от идеальной модели типа «пчелиных сот». Как видно из фотографий поверхности барьерного (рис. 1а) и пористого (рис. 1b) слоев ПАОА, сформированного таким способом в 3% С2Н2О4, ячейки имеют неправильную форму, а их взаимное расположение отклоняется от идеально гексагонального. Как правило, ПАОА, являются аморфными [6, 14—16]. Результаты исследования ближнего порядка в расположении атомов в аморфных пористых анодных оксидных пленках на алюминии с учетом их гетерогенности представлены в [6]. Показано, что расположение атомов в области ближнего порядка в барьерных АОА, а также ПАОА, сформированных в электролите на основе хромовой кислоты (не имеющих анионосодержащего слоя), соответствует искаженной γ'-Al2O3 со значением 1-го координационного числа NAl-O1 ≈ 5.4. Тогда как наличие в теле пористого оксида слоя, «обогащенного» частицами электролита, приводит к уменьшению интегрального значения первого координационного числа (КЧ), попадающего в диапазон NAl-O1 ≈ 4.6—5.1. При термических воздействиях происходит кристаллизация аморфного оксида [15, 17—19]. В процессе термической кристаллизации ПАОА образуются многофазные поликристаллические окисные пленки, что, по-видимому, обусловлено разными значениями скорости фазовых преобразований областей чистого аморфного Al2O3 и материала оксида, обогащенного анионами электролита [18]. При этом необходимо отметить, что вплоть до отжига при 1223 K морфологические изменения в ПАОА не происходят, и сохраняется регулярная ячеисто/пористая структура [18]. Нарушения в периодичности расположения отмечаются лишь при более высокой температуре отжига. Для описания строения ПАОА, в которых присутствуют регулярно расположенные поры наноразмерного диаметра, целесообразно использовать наряду с атомной структурой, описывающей взаимное расположение атомов, ионов или молекул, обусловленное их химической природой и характером сил взаимодействия между ними, понятие мезоскопической структуры [20], характеризующей взаимное расположение ячеек/пор на поверхности оксида. Тогда можно сказать, что традиционное анодирование обеспечивает формирование оксидов с «аморфной» мезоструктурой при сохранении близкого к гексагональному порядка в основном только для соседних ячеек. Анодирование алюминия в особых условиях самоорганизованного роста приводит к образованию ПАОА с «поликристаллической» мезоструктурой, которая характеризуется появлением хаотически разупорядоченных «зерен» или доменов (областей с идеальным гексагональным порядком в расположении ячеек/пор) с размером до нескольких десятков мкм2 [20—23]. Основным направлением исследований последних лет является разработка методик получения высоко упорядоченных, «самоорганизованных» ПАОА как с «поликристаллической», так и с практически «монокристаллической» макроструктурой [23]. Это продиктовано появлением новых функциональных назначений ПАОА, например, как основы для изготовления шаблонов для направленного выращивания и копирования наноструктур [21]. В настоящее время известен ряд специальных методик анодирования для получения АОА с высокой степенью порядка в расположении пор: длительное (или пролонгированное) анодирование [21, 22], анодирование с использованием метода нанолитографии [24—26], двухступенчатое анодирование (ДСА) [21, 27—29], анодирование при высоких напряжениях и плотностях тока («жесткое» анодирование) [30]. Методика Первую группу объектов исследования составили ПАОА с регулярно-пористой структурой, сформированные анодированием алюминия (А99, А0) (рис. 2) и алюминиевых сплавов (АМг, АД, А7Е и др.) в водных растворах различных кислот (С2Н2О4, H2SO4, H4C3O4 и H3РO4). Были получены оксидные пленки с различной степенью упорядочения ячеисто-пористого массива, т. е. как с аморфной, так и поликристаллической мезоструктурой. Вторую группу материалов образовали нанокомпозитные покрытия, созданные путем модификации самоорганизованной пористой оксидной матрицы наночастицами серебра или ультрадисперсного диоксида марганца. Анодирование выполнялось с помощью автоматизированного экспериментального комплекса, позволяющего в достаточно широких пределах изменять параметры процесса— плотность тока, напряжение, температуру. Поддержание заданной температуры электролита проводилось с помощью устройства на основе элементов Пельтье [49]. Анодирование проводилось в гальвано статическом режиме— ГСР (при постоянной плотности тока) и в вольт статическом режиме— ВСР (при постоянном напряжении). Перед анодированием образцы обезжиривают в растворе щелочи (3% KОН), тщательной промывались в дистиллированной воде и высушивались. Как правило, стадия электрохимической полировки исключалась. В процессе исследований регистрировалась кинетика роста оксидов, устанавливалось влияние параметров процесса на формирование оксидов. Анализ кинетических зависимостей позволил выявить оптимальные условия формирования само- организованных анодных оксидных покрытий на алюминии и сплавах. Для исследования структуры и морфологии объектов были использованы просвечивающая (ЭМ‐125) и сканирующая (JEОL JSM‐6480LV, FEI Nova NanoLab 600) электронная микроскопия, атомная силовая микроскопия (Solver Next), а также дифракция рентгеновских лучей. Особенности методики эксперимента и обработки данных описаны в работах [50—54]. Для установления антибактериального действия образцов серебросодержащих композиционных покрытий были использованы культуры факультативных анаэробных бактерий, относящихся к отделам Firmacutes и Gracilicutes, в исходной концентрации 5000 и 10000 кое/мл. Для приготовления данной концентрации микробных клеток использовались суточные тестовые культуры Staphylococcus еpidermidis (стафилококка эпидермального) и Escherihia coli (кишечной палочки). Технология получения нанопористого оксида алюминия электрохимическим способом На установке «Нано-ЭХ-09» был проведен ряд экспериментов по получению пористого анодного алюминиевого слоя и определены оптимальные параметры процесса, приводящего к возникно- вению регулярной нанопористой структуры. Предварительно был проведен отжиг алюминиевой пластины в муфельной печи при 500 °С в течение 1 часа, что способствовало снятию остаточного напряжения в структуре алюминия. Далее было проведено двухступенчатое анодирование: 1. Первое анодирование – в гальваностатическом режиме: плотность тока 25 мА/см 2 в 0,5 н. растворе (СООН)2 при комнатной температуре в течение 40 минут. После анодирования для снятия верхнего барьерного слояпластину кипятили в течение 5 минут в водном растворе CrO3 и H3PO4. 2. Второе анодирование – в вольтстатическом режиме: напряжение 40 В, температу а 2 °С, в течение 2 часов с последующей обработкой кипячением в течение 5 минут в водном растворе CrO3 и H3PO4 для снятия верхнего слоя и открытия пор. 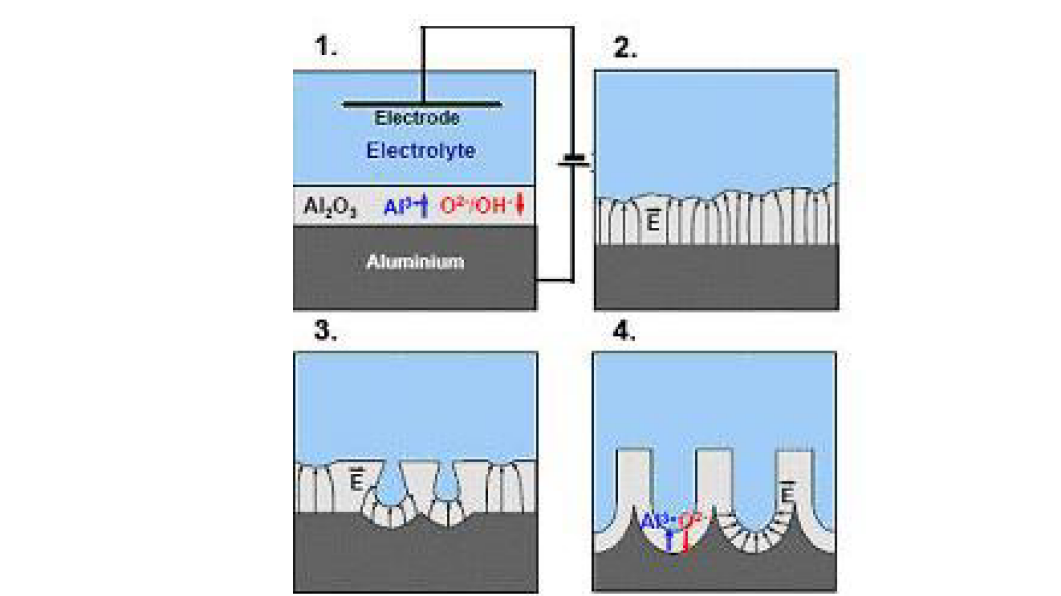 Рис. 3. Концепция формирования анодной пористой структуры оксида алюминия: концепция критической плотности тока В итоге получили поверхность плотноупакованных хорошо организованных пор анодного оксида алюминия. Топология поверхности была исследована помощью атомно-силового микроскопа (АСМ). Список литературы 1. Thompson G. E. Thin Solid Films, 1997, vol. 297, pp. 192—201. DOI: 10.1016/S0040—6090(96)09440—0 2. Yakovleva N. M., Anicai A., Yakovlev A. N., Dima L., Khanina E. Ya., Buda M., Chupakhina E. A. Thin Solid Films, 2002, vol. 416, no 1—2, pp. 16—23. DOI: 10.1016/S0040—6090(02)00625—9 3. Eftekhari A., Alkire R. C., Godotski Y., Simon P. Nanostructured materials in Electrochemistry. Weinheim: Willey-VCH Verlag GmbH and Co, 2008, 489 pp. DOI: 10.1002/9783527621507 4. Ono S., Masuko N. Corrosion Sci., 1992, vol. 33, no 6, pp. 841—850. DOI: 10.1016/0010—938X(92)90048—8 5. Сhoi J., Luo Y., Wehrspohn R. B., Hillerand R., Schilling J., Gösele U. J. Appl. Phys., 2003, vol. 94, pp. 4757—4762. DOI: 10.1063/1.1609033 6. Yakovleva N. M., Yakovlev A. N., Chupakhina E. A., Khanina E. Ya. Naukoemkie tekhnologii, 2004, vol. 5, pp. 3—11. 7. Thompson G. E., Furneaux R. C., Wood G. C., Richardson J. A., Goode J. S. Nature, 1978, vol. 272. pp. 433—435. DOI: 10.1038/272433a0 8. Wehrspohn R. B., Li A. P., Nieltsch K., Müller F., Erfurth W., Gösele U. Electrochemical Society Proceedings, 2000, vol. 4. pp. 271—282. 9. Choi J., Nielsch K., Reiche M., Wehrspohn R. B., Gösele U. J. Vac. Sci. Technol. B., 2003, vol. 21, no. 2, pp. 763—766. 10. Yao Z., Zheng M., Ma L., Shen W. Nanotechnology, 2008, vol. 19, pp. 1—7. DOI: 10.1088/0957—4484/19/46/465705 11. Shingubara S. Journal of Nanoparticle Research, 2003, vol. 5, pp. 17—30. 12. Thompson G. E., Xu Y., Skeldon P., Shimizu K., Han S. H., Wood G. C. Phil. Mag. B., 1987, vol. 55, no. 6, pp. 651—667. 13. Wood G. C. Oxide and oxide films, 1972, vol. 2, pp. 168—279. 14. Poinern G. E.J., Ali N., Fawcett D. Materials, 2011, vol. 4, pp. 487—526. DOI: 10.3390/ma4030487 15. M a rdilovich P. P., Govyadinov A . N . , Mukhurov N. I., Rzhevskii A. M., Paterson R. Journal of Membrane Science. 98, 1995, pp. 131—142. 16. Vasanthakumar K., Vanithakumari S. C., Kamachi Mudali U. J. Adv. Microsc. Res., 2011, vol. 6, pp. 207—214. DOI: 10.1007/s10853—010—4966—6 17. McQuaig Jr M. K., Toro A., Van Geertruyden W., Misiolek W. Z. J Mater Sci., 2011, vol. 46, pp. 243—253. DOI: 10.1007/s10853—010—4966—6 18. Yakovleva N. M., Yakovlev A. N., Chupakhina E. A. Kondensirovannye sredy i mezhfaznye granitsy, 2006, vol. 8, pp. 69—77. Available at: http://www.kcmf. vsu.ru/resources/t_08_1_2006_015.pdf 19. Marsal L. F., Vojkuvka L., Formentin P., Pallarés J., Ferré-Borrull J. Opt. Mater., 2009, vol. 31, pp. 860—864. DOI: 10.1016/j.optmat.2008.09.008 20. Nielsh K., Choi J., Schwirn K., Wehrspohn R., Gősele U. Nanoletters, 2002, vol. 2, no.7, pp. 676—680 21. Masuda H., Hasegwa F., Ono S. J. Electrochem. Soc., 1997, vol. 144, no. 5, pp. L127–L130. DOI: 10.1149/1.1837634 22. Jessensky O., Műller F., Gősele U. J. Electrochem. Soc., 1998, vol. 145, no. 11, pp. 3735—3740. DOI:10.1149/1.1838867 23. Choi J., Wehrspohn R., Gősele U. Electrochimica Acta, 2005, vol. 50, pp. 2591—2595. DOI: 10.1016/j.electacta.2004.11.004 24. Poznyak A. A. Modifitsirovannyi anodnyi oksid alyuminiya i kompozitnye materialy na ego osnove: monografiya. Minsk: Tsentr BGU Publ., 2007, 251 p. 25. Masuda H., Yamada H., Satoh M., Asoh H., Nakao M., Tamamura T. Appl. Phys. Lett., 1997, vol. 71(19), no. 10, pp. 2770—2772. DOI: 10.1063/1.120128 26. Asoh H., Nishio K., Nakao M., Tamamura T., Masuda H. // Journal of The Electrochemical Society, 2001, vol. 148, No 4, pp. B152–B156. 27. Yuan J. H., He F. Y., Sun D. C., Xia X. H. // Chem. Mater., 2004, vol. 16, pp. 1841—1844. 28. Razpet A., Possnert G., Johansson A., Hallén A., Hjort K. // Nuclear Instruments and Methods in Physics Research, 2004, vol. 222, pp. 593—600. 29. Li Y., Kanamori Y., Hane K. // Microsystem Technologies, 2004, vol. 10, pp. 272—274. 30. Lee W., Ji R., Gösele U., Nielsch K. // Nature materials, 2006, vol. 5, pp. 741—747. 31. Rauf A., Mehmood M., Rasheed M. A., Aslam M. // J. Solid State Electrochem., 2009, vol. 13, pp. 321—332. 32. http://www.dslib.net/kondensat/struktura-i-svojstva-kompozitnyh-pokrytij-na-osnove-poristyh-anodnyh-oksidov.html |
