ПРАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ ПО ТЕМЕ «РАСТВОРЫ. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ. ПРИГОТОВЛЕНИЕ РАСТВОРОВ С ИЗВЕСТНОЙ МАС. Отчет по решению задач занесите в рабочую тетрадь. Варианты определяет преподаватель на практическом занятии!
 Скачать 305.74 Kb. Скачать 305.74 Kb.
|
 Дисциплина «Химия», для студентов специальностей 31.05.01 Лечебное дело, 31.05.02 Педиатрия, 31.05.03 Стоматология  П  РАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ РАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ ПО ТЕМЕ «РАСТВОРЫ. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ. ПРИГОТОВЛЕНИЕ РАСТВОРОВ С ИЗВЕСТНОЙ МАССОВОЙ ДОЛЕЙ»  МНОГОВАРИАНТНЫЕ СИТАЦИОННЫЕ ЗАДАЧИ Используя выданное Вам лабораторное оборудование и реактивы осуществите: расчет массы навески вещества и объема воды, необходимые для приготовления раствора; приготовление раствора с определенной массовой долей; пересчет одного способа выражения концентрации раствора на другой; концентрирование и разбавление раствора; приготовление насыщенного раствора соли. Отчет по решению задач занесите в рабочую тетрадь. Варианты определяет преподаватель на практическом занятии!
РАБОЧАЯ ТЕТРАДЬ Ф.И. студента (студентки)Минзар Андрей Группа ДЛСД-111 П  РАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ РАКТИКУМ ПО РЕШЕНИЮ ЗАДАЧ ПО ТЕМЕ «РАСТВОРЫ. СПОСОБЫ ВЫРАЖЕНИЯ КОНЦЕНТРАЦИИ РАСТВОРОВ. ПРИГОТОВЛЕНИЕ РАСТВОРОВ С ИЗВЕСТНОЙ МАССОВОЙ ДОЛЕЙ» Цель: формирование умений готовить растворы с точной и приблизительной концентрацией. Задача 1. Расчет массы навески вещества и объема воды, необходимые для приготовления раствора а) Определение плотности раствора по графику зависимости плотности раствора от массовой доли растворенного вещества: 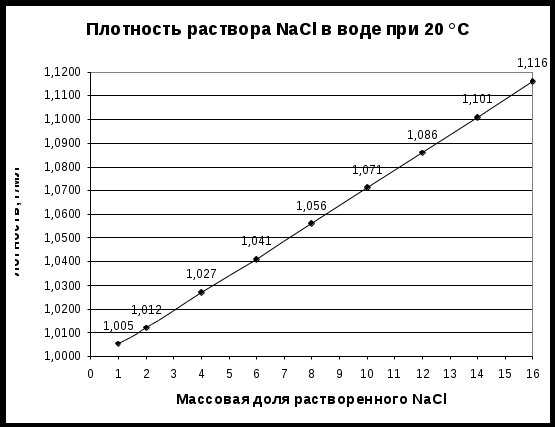 r(р-ра) = 300мл б) Расчет массы раствора: m (р-ра) = 0,03x300x1,2=9,18 в) Расчет массы навески соли: m (навески в-ва) = 300x1,02=306 г) Расчет массы воды, необходимой для приготовления раствора: m (Н2О) =306-9,18=297 д) Расчет объема воды необходимый для приготовления раствора: принимаем плотность воды при комнатной температуре 1,000 г/мл V (Н2О) = 297г/м Задача 2. Приготовление раствора с определенной массовой долей
Задача 3. Пересчет одного способа выражения концентрации раствора на другой. Использую формулы, рассчитайте мольную долю, молярную концентрацию, моляльность и титр полученного раствора.
Задача 4. Концентрирование и разбавление раствора. Рассчитайте массовую долю раствора: а) если в приготовленный Вами раствор прибавить 0,5 г соли. б) если в приготовленный Вами раствор прибавить 10 мл воды соли.
Задача 5. Приготовление насыщенного раствора соли Определите температуру в лаборатории. Т=36 оС Используя кривую растворимости, рассчитайте, какое количество соли нужно к приготовленному раствору для получения насыщенного раствора. 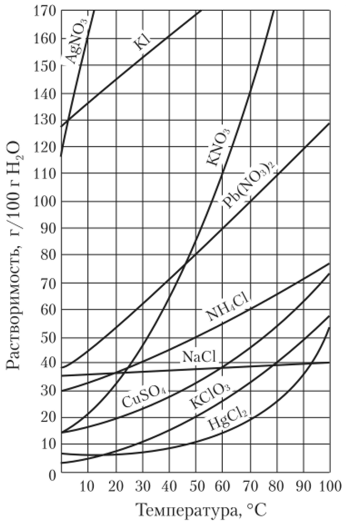
Самооценка Оцените эффективность формирования перечисленных умений у Вас лично по 10 бальной шкале (от 0 до 10)
|