Коллок. Коллок 1. Ответ а равновесное состояние
 Скачать 242.14 Kb. Скачать 242.14 Kb.
|
|
Дайте понятие равновесного и неравновесного состояние тел и систем. Напишите уравнение состояния гомогенного тела в явном и неявном виде. Дайте понятие изопотенциальной поверхности. Ответ: А) Равновесное состояние – состояние термодинамической системы, характеризующееся при постоянных внешних условиях неизменностью параметров во времени и отсутствием в системе потоков. Состояние термодинамической системы, не удовлетворяющее данному определению, называется неравновесной Б) 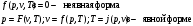 В) Изотермическую поверхность- геометрическое место точек в пространстве, занимаемом системой (телом), с одинаковыми температурами Дайте понятие энтропии и покажите ее связь с понятием обобщенной работы. Докажите принадлежность энтропии реальных веществ к параметрам состояния. Ответ: Энтропия – параметр состояния, соответствующий координате перемещения при действующей силе в виде абсолютной температуры, необходимый для расчета тепловой работы (теплоты). Природа теплоты та же, что и природа работы – мера энергетического взаимодействия. Следовательно, теплота может быть рассчитана по формуле обобщенной работы как произведение некоторой силы Fx на изменение некоторой координаты перемещения dx в направлении действия данной силы: 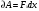 Используя понятие энтропии, можно получить расчетное выражение теплоты в виде 𝑄 = 𝑇𝑑𝑆. Это выражение отвечает требованиям к расчетному выражению теплоты как работы Дайте аналитические выражения для определения удельных теплоемкостей смеси газов: с, с', mс и коэффициента Пуассона смеси идеальных газов. Ответ: 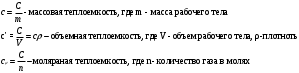  Поясните, чем обусловлены отличия свойств реальных газов от идеальных. Приведите изображение t=const для реальных веществ в р,v- диаграмме от области газа до области жидкости и поясните, чем обусловлен ее характер в каждом фазовом состоянии. Ответ: А) 1. Размеры молекул малы по сравнению с расстояниями между ними 2. Молекулы взаимодействуют друг с другом и со стенкой сосуда лишь в моментальных соударениях 3. Соударения частиц являются абсолютно упругими 4. Рассматривают любые газы, в которых число очень велико Б) 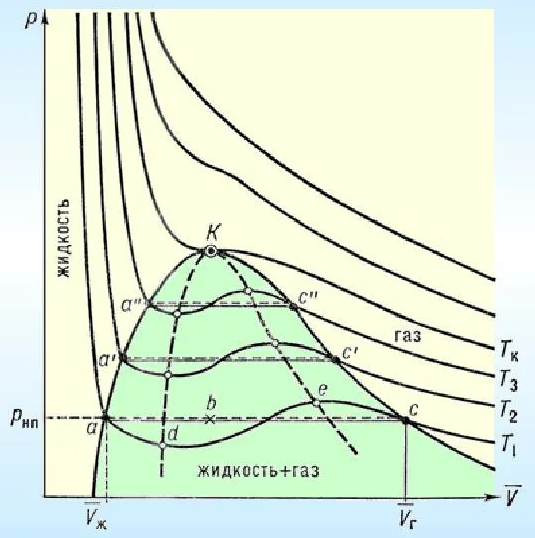 При T>Tкр вещество может существовать только в газообразном состоянии. При Т<Ткр вещество из газообразного состояния может быть переведено в жидкое состояние. При квазистатическом сжатии, начиная с точки а, система распадается на 2 фазы- жидкость+ газ, причем плотность жидкости и газа остается при сжатии неизменной и равными их значением в точка а и с соответственно. Понятие цикла. Какие термодинамические процессы называются циклом Ответ: А) Цикл- совокупность процессов, в результате которых рабочее тело периодически возвращается в исходное состояние Б) Термодинамические процессы, в которых рабочее тело претерпевает изменения и в результате возвращается в первоначальное состояние, называется циклом |
