Патологическая анатомия бешенства
 Скачать 2.48 Mb. Скачать 2.48 Mb.
|
|
Бешенство птиц. Домашние птицы, особенно куры, также восприимчивы к бешенству. Больные бывают, пугливы, беспокойны, беспрестанно бегают, прыгают, кричат. Они нападают на здоровых птиц, животных и даже людей, пуская в ход крылья, когти и клюв, пытаясь нанести удар животным в голову, людям в лицо. На второй день болезни развивается паралич и наступает смерть. У петухов нередко бывает паралитическая форма бешенства: крылья опущены (волочатся по земле), движения бесцельные, походка шаткая, голос хриплый, крик напоминает куриное кудахтанье; затем быстро наступает смерть от паралича. 5. Патогенез Локализация и выделение вируса. Многочисленные исследования патогенеза бешенства позволили условно разделить острую рабическую инфекцию на три основных фазы: I фаза — экстраневральная, без видимого размножения вируса в месте инокуляции; II фаза — интраневральное, центростремительное распространение инфекции; III фаза — диссеминация вируса по всему организму, сопровождаемая появлением симптомов болезни и, как правило, гибелью животного. Распространение вируса бешенства по нервным путям впервые доказали Пастер и Ру. Вирус проникает в организм животного со слюной в местах укуса, непродолжительное время сохраняется в месте внедрения (до 2 нед), а затем по центростремительным нервам продвигается к спинному и головному мозгу. Из мозга по центробежным нервам он попадает в слюнные железы, где репродуцируется в нервных узлах и после дегенерации нервных клеток выходит в протоки желез, инфицируя слюну. Из мозга вирус также нейрогенным путем попадает в слюну, роговицу, надпочечники. Выделение вируса со слюной начинается за 10 сут до проявления клинических признаков, поэтому французский регламент предусматривает 15-суточный срок наблюдения за покусавшим животным. У бешеной лисицы накапливается в слюнных железах столько вируса, что можно заразить 67 млн лисиц. Доказано нахождение вируса во всех внутренних органах и крови, кроме сальника, селезенки и желчного пузыря. Из центральной нервной системы по нервным волокнам вирус попадает во внутренние органы, а затем в кровь. Таким образом происходит генерализация инфекционного процесса. Вирус бешенства проникает в организм восприимчивого животного, продвигается по центральным нервным волокнам, головному и спинному мозгу, где размножается и вызывает негнойный полиэнцефалит. По центробежным нервным волокнам вирус попадает в слюнные железы, размножается в нервных ганглиях и после их дегенерации появляется в слюне. Наибольшее количество вируса содержится в аммоновых рогах, продолговатом мозге, мозжечке, в ядрах черепно-мозговых нервов и в поясничной части спинного мозга. Воздействие вируса вначале вызывает раздражение нервных клеток, а затем их дегенерацию, обусловливающую паралитическое явление. Синтез РНК. Первой стадией в инфекционном цикле любых РНК-содержащих вирусов с негативным геномом является синтез мРНК. В эукариотических клетках нет РНК-зависимой РНК-по-лимеразы, поэтому для экспрессии своего генома рабдовирусы должны иметь собственную полимеразу и упаковывать этот фермент в зрелые вирусные частицы. Сразу же после удаления оболочки инфекционный вирус с помощью фермента, привлеченного им в клетку, начинает транскрипцию. Репликация рабдовирусов осуществляется в две стадии. Минус-цепь в составе рибонуклеокапсида служит матрицей для синтеза комплементарной РНК, совпадающей по размеру с геномной. N-белок связывается с новосинтезированной РНК, образуя рибо-нуклеокапсид, создающий плюс-геномную РНК, после чего процесс повторяется и на плюс-РНК этого рибонуклеокапсида, как на Матрице, образуются новые минус-цепи. Синтез и созревание вирусных белков. МРНК рабдовирусов эффективно транслируется рибосомами клетки-хозяина. Для регуляции количества каждого белка используется не трансляционный, а транскрипционный контроль. Количество синтезируемых вирусных белков пропорционально количеству соответствующих мРНК. Поскольку транскрипция рабдовирусов последовательна и полярна, ее наиболее высокий уровень достигается для N-мРНК и, следовательно, для N-белка, а наименьший — для L-мРНК и L-белка. Фракционирование клеточных экстрактов и опыты с импульсной меткой показали, что каждый вирусный белок проходит свой путь созревания, который завершается переносом на клеточную мембрану, где происходят сборка и почкование зрелых вирионов. Рабдовирусы состоят из двух отдельных морфологических единиц — оболочки и рибонуклеопротеина (РНП). РНП, состоящий из РНК и белков N, NS и L, собирается как отдельная структура в цитоплазме координировано с репликацией вирусной РНК. Основным белком РНП является N-белок, который включается в РНП, не подвергаясь постгрансляционным модификациям. Новосинтезированный N-белок перед сборкой в РНК входит в пул растворимых цитоплазматических белков. При этом он избирательно инкапсидирует только решшкативные РНК, хотя более 90 % последовательностей, входящих в состав репликативной плюс-геномной РНК, представлено и в мРНК. Добавление N-белка приводит к накоплению в цитоплазме РНП, содержащих как плюс-, так и минус-геномные РНК. РНП, содержащие плюс-РНК, остаются в цитоплазме; их единственная функция — служить матрицей для синтеза минус-цепей. Новосинтезированные минус-РНП могут использоваться им как матрицы для синтеза мРНК (вторичная транскрипция), или для реплика-тивного синтеза плюс-цепей РНК, или для включения в почкующиеся вирионы. С цитоплазматическими РНП ассоциированы также два белка с полимеразной активностью (NS и L), но пути их созревания различны, причем эти пути отличаются и от пути созревания N-белка. NS-белок интенсивно фосфорилируется по сериновым и трео-ниновым остаткам, что приводит к гетерогенности популяции его молекул. Сборка оболочки вириона начинается с включения вирусного гликопротеина в плазматическую мембрану клетки. Гликопротеин претерпевает сложный путь созревания, включающий протеолитическое нарезание, присоединение и процессинг олигосахаридов, присоединение жирных кислот. Эти модификации осуществляются одна за другой в ходе синтеза и последующего транспорта G-белка к поверхности клетки. Изучение кинетики этого процес-са показало, что для достижения клеточной мембраны новосинтезированному G-белку требуется по меньшей мере 15 мин. В отличие от четырех других вирусных белков G-белок всегда связан с мембраной; его мРНК обнаруживается в рибосомах, связанных с мембранами. М-белок имеет относительно простой механизм созревания. Хотя он является белком наружной мембраны, его мРНК транслируется на свободных полисомах, а сам белок проходит через небольшой пул растворимых цитоплазматических белков. Поскольку М-белок выстилает внутреннюю поверхность липидной оболочки вириона, а также связывается с нуклеокапсидом, оказалось неожиданным, что он, не накапливаясь ни на клеточной мембране, ни в цитоплазматических РНП, непосредственно включается в состав вирионов из растворимой фракции. Опыты по кинетике позволяют предложить следующее объяснение: М-белок образует центр нуклеации при почковании, и стоит ему начать взаимодействие с мембраной или РНП, как дальнейшие стадии этого взаимодействия произойдут с такой быстротой, что их невозможно зарегистрировать. Сборка вирионов. Почкование зрелых вирионов — сложный процесс, для которого необходимы ассоциированный с мембраной G-белок, растворимый М-белок и РНП-частицы. Все эти компоненты собираются на определенном участке мембраны. М-белок обеспечивает почкование благодаря образованию локальных кластеров с G-белком, после чего происходят быстрое присоединение РНП и почкование. Хотя липидный состав оболочки вириона близок к аналогичному составу клеточной плазматической мембраны, часто он с ним не совпадает, т. е. включение липидов в мембрану вириона носит в какой-то степени избирательный характер. В ходе почкования из вирусной мембраны практически полностью исключаются вирусные белки. Влияние на метаболизм клетки-хозяина. Рабдовирусы представляют собой цитолитические вирусы, быстро убивающие зараженные клетки. Гибели клетки предшествует эффективное выключение синтеза хозяйских белков, ДНК и РНК. До сих пор до конца неизвестно, что служит причиной гибели клетки: кумуляторное действие вируса на клеточный метаболизм или его действие на специфическую мишень. Почему клетка гибнет так быстро? Чтобы понять это, нужно иметь в виду, что при заражении затрагиваются, три основные пути биосинтеза и различные клеточные линии обладают разной чувствительностью. Хотя общая картина того, как вирус убивает клетку, еще не сложилась, уже частично изучены факторы, включающие отдельные биосинтетические пути. Для гибели зараженной клетки необходима не репликация вируса, а транскрипция вирусного генома, так же как для включения всех трех биосинтетических путей. Поскольку репликация рабдовирусов происходит в цитоплазме зараженных клеток и может осуществляться даже в клетках, лишенных ядра, столь сильное влияние вируса на процессы, протекающие в ядре, вызывает удивление. Например, существенно снижают уровень синтеза РНК всеми тремя клеточными РНК-поли-меразами: Pol 1, 2, 3. Опыты в реконструированных системах in vitro показали, что блокирование синтеза РНК обусловлено необратимой инактивацией не хозяйских транскриптаз, а скорее частоты инициации in vitro. Эксперименты с 15-мутантами свидетельствуют о том, что для подавления синтеза клеточных РНК необходима транскрипция вирусного генома. Но по данным опытов с УФ-инактивацией, транскрипции должна подвергнуться лишь малая часть генома, возможно, только лидерная последовательность. Появление надежных систем для эукариотической транскрипции in vitro дало возможность изучать непосредственно влияние продуктов вирусов бешенства на транскрипцию, обусловленную Pol 2. Вирусная персистенция. Несмотря на то, что в целом рабдовирусы относятся к высоковирулентным цитопатическим вирусам, оказалось возможным получить несколько персистентно зараженных линий, или линий—носителей вируса бешенства. Для них характерны слабый цитопатический эффект и непрерывный, но низкий уровень продукции вируса. Некоторые зараженные культуры клеток поддерживаются более 5 лет. Чтобы установить и поддерживать персистентную инфекцию, следует нейтрализовать нормальное цитопатическое действие вируса; при этом резко снижается его способность реплицироваться. Персистентная инфекция может запускаться стандартным вирулентным вирусом, если его репликацию подавить предварительной обработкой клеток интерфероном или заражать им совместно с большим количеством дефектных интерферирующих частиц (ДИЧ). Поддержание персистентной инфекции коррелирует со многими факторами, которые варьируют в разных линиях, но все без исключения снижают уровень репликации вируса. ДИЧ и интерферон важны не только для установления, но и для поддержания персистенции. Тем не менее оказалось, что главную роль в поддержании персистенции играет отбор мутантов. Вирусы, выделенные из персистентно зараженных клеток, существенно отличаются от тех, которые использовали для заражения: как правило, они образуют мелкие бляшки, реплицируются хуже, чем родительский штамм. Принимая во внимание сложный механизм гибели клетки при рабдовирусной инфекции, кажется вероятным, что персистентная инфекция отражает не нарушение специальной летальной функции вируса, а угнетение вирусных функций ниже уровня, необходимого для гибели клетки. Изучение персистентно зараженных клеточных линий показало, что in vitro стандартный цитопатический характер взаимодействия между рабдовирусом и клеткой может быть изменен, однако все еще неясно, справедливо ли это для природных условий in vivo. За последние годы описаны казуистические случаи неоднократного выделения вируса бешенства из слюны здоровых собак на протяжении почти 2 лет после их инфицирования. Аналогичная картина наблюдалась и у некоторых экспериментально зараженных кошек. В 1981 г. представлены результаты 4-летнего изучения вируса бешенства мангустов, выловленных в ряде районов Гренады. С помощью ИФ вирус бешенства обнаружен в срезах мозга 100 (2,1 %) из 4754 обследованных мангустов. Среди 1675 обследованных животных обнаружены ВНА в пробах 498 сывороток (30 %). При сопоставлении результатов обнаружения вируса бешенства и соответствующих антител (АТ) оказалось, что число больных животных в течение 1971—1974 гг. ежегодно снижалось (с 3,5 до 0,6 %), а число мангустов с определяемыми АТ увеличилось с 20,8 до 43,2 %. АТ к вирусу бешенства, как отмечено в опытах с отловленными в природе мангустами (20 особей), циркулировали в крови еще 35 мес. У животных с наиболее высокими титрами АТ (1:1400) наблюдалась и наибольшая скорость их снижения. Одно из свойств вируса бешенства — способность к персистенции in vivo и in vitro. Хроническая инфекция клеток Нер-2/2 и ВНК-21/13 фиксированным вирусом бешенства сопровождается определенными изменениями клеточного метаболизма. Антиген (АГ) вируса бешенства образуется в цитоплазме клеток независимо от включений. Персистенцию вируса бешенства удается наблюдать при хронической инфекции в клеточных культурах, причем по морфологии и скорости размножения клеток хронически инфицированные культуры не отличались от незараженных. Вирусный АГ передавался при делении клеток. После того как была показана возможность образования ДИЧ вируса бешенства при первичной инфекции in vivo, ДИЧ были выделены и охарактеризованы при хронической инфекции вируса бешенства клеток ВНК. Генерация ДИЧ в нейронах ЦНС может не только определять окончательный исход инфекции, но и объяснять ее латентный характер. В настоящее время данные о роли интерферона и ДИЧ в механизме хронической инфекции вируса бешенства в клеточных культурах противоречивы. Показано, что ts-мутанты, представляющие собой условно дефектные вирусы, могут интерферировать с размножением вируса дикого типа. Роль ts-мутантов при хронической инфекции изучена недостаточно. Современные представления о мутации этого вируса подтверждаются рядом примеров. Так, с помощью моноклониальных АТ из популяции вирулентного вируса бешенства удавалось селекционировать варианты с измененным поверхностным гликопротеином и признаками аттенуации для ЦНС. Мутант вируса бешенства, имеющий две аминокислотные замены (лейцин-132 на фенилаланин и аргинин-333 на глютамин), утратил нейровирулентность для взрослых мышей. Вирулентность штаммов ЕКА и СУ5 вируса бешенства для мышей зависела от наличия аргинина или лизина в положении 333 вирусного гликопротеина. Замена аргинина в положении 333 на лейцин, изолейцин, метионин, цистин или серии обеспечивала полную авирулентность. Такие варианты характеризовались минимальным количеством точечных мутаций. Особенности репродукции вируса бешенства. При связывании с тканью вирус бешенства концентрируется в неврологических контактах. Этот процесс ингибируется d-бунгаротоксином и d-тубакурарином, каждый из которых способен связываться с ацетилхолиновыми рецепторами. Следовательно, последние служат высокоэффективными рецепторами для вируса бешенства. Этот вывод помогает понять природу нейротропности вируса, но поскольку в условиях in vitro он поражает не только нервные клетки, должны существовать также и другие рецепторы. Хотя рабдовирусы имеют липидную оболочку, в клетки они проникают в основном с помощью эндоцитоза, а не путем прямого слияния с мембраной. Этот процесс удается наблюдать только при кислых значениях рН или после осаждения вирионов на клетки с помощью центрифугирования. 6. Патоморфология Патоморфологические изменения при бешенстве животных немногочисленны и неспецифичны, приобретают диагностическое значение лишь при учете клинических признаков болезни. При внешнем осмотре трупа отмечают истощение, следы укусов и расчесов, часто шерсть на шее и груди пропитана слюной.  Рисунок 13. Повреждение тканей конечности собаки при самопогрызании  Рисунок 14. Инородное тело (ветка ели) в желудке собаки7 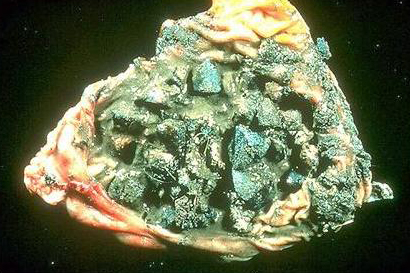 Рисунок 15. Вскрытый желудок собаки с большим количеством заглоченных камней. На вскрытии устанавливают цианоз слизистых оболочек. В желудке отсутствуют кормовые массы, но часто находят различные инородные предметы (волосы, тряпки, камни, кусочки дерева, почва и др.) (рисунок 13, 14, 15). Слизистая оболочка желудка отечна, гиперемирована с петехиальными кровоизлияниями (рисунок 16). Воспалительные явления по всему желудочно-кишечному тракту.8 По данным Г. Боля, «кровоизлияния» представляют собой геморрагические инфаркты, возникающие в следствии спазма сосудов. У крупных животных наблюдаются кровоизлияния в подкожной клетчатке, мускулатуре, плевре, под эпикардом (рисунок 17). При бешенстве так же отмечается гиперемия и отечность слизистых оболочек глотки и гортани.  Рисунок 16. Пятнистые кровоизлияния в слизистой оболочке желудка собаки  Рисунок 17. Кровоизлияния под эпикардом коровы.9 В головном и спинном мозге, в их оболочках гиперемия, отечность и кровоизлияния; точечные кровоизлияния в мозжечке, продолговатом мозге и на дне четвертого желудочка (рисунок 18).  Рисунок 18. Геморрагический энцефалит серого вещества спинного мозга. Ярко выраженное кровоизлияние не является характерным, однако может наблюдаться при длительном тяжелом течении. Гистологические изменения при бешенстве выражены в головном и спинном мозге, нервных ганглиях и периферических нервах. Поражение головного мозга характеризуется наличием диссеминированного негнойного полиэнцефалита, наиболее выраженного в аммоновых рогах и продолговатом мозге (рисунок 19). 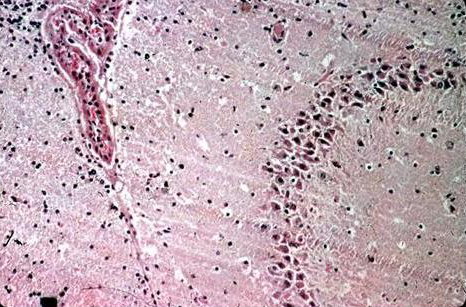 Рисунок 19. Гистологическая картина энцефалита при бешенстве, минимальная реакция (рассеянные красные тельца в ткани). В белом веществе обычно димиелинизация и распад осевых цилиндров. В коре головного мозга и мозжечка также наблюдают картину острого разрушения нейронов. Частый признак бешенства — поражения, проявляющиеся вакуолизацией клеток, особенно в таламусе и в коре головного мозга. В цитоплазме ганглиозных клеток обнаруживают специфические тельца-включения Бабеша—Негри, имеющие резко очерченные базофильные структуры овальной или удлиненной формы диаметром от 2 до 10 мкм; в настоящее время их обнаруживают только у 24,5...73 % инфицированных животных (Рисунок 20, 21). В периферических нервах отмечают воспалительно-дистрофические процессы и лимфоидные инфильтраты по ходу нервных волокон (Рисунок 22, 23, 24).10 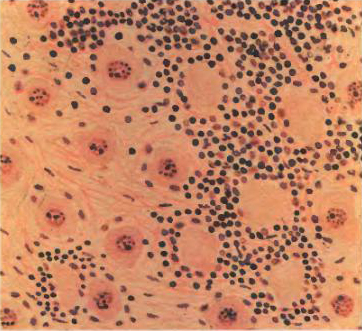 Рисунок 20. Замещение ганглиозных клеток клетками-стеллитами в ганглии переферической нервной системе собаки (окраска гемотоксилин-эозином).  Рисунок 21. Тельца Бабеша-Негри в ганглиозных клетках амонова рога головного мозга собаки (окраска по Туревичу).11 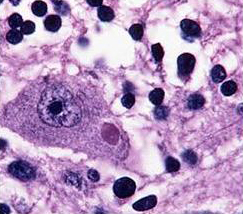 Рисунок 22. Тельца Бабеши-Негри различимые в световой микроскоп. Разрез через волокна Пуркинье мозжечка. (тельца в цитоплазме).  Рисунок 23. Тельца Бабеши-Негри в крупных нервных клетках аммоновых рогов (окраска по Ленцу). 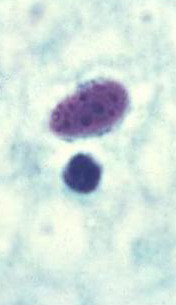 Рисунок 24. Тельца Бабеши-Негри – отчетливо видны внутренние базофильные структуры (окраска по Муромцеву). |
