Технология переработки природного газа. Практическая работа Технология подготвки и переработки природно. Практическая работа по дисциплине технология подготовки и переработки природного газа
 Скачать 20.61 Kb. Скачать 20.61 Kb.
|
|
МИНИСТЕРСТВО НАУКИ И ВЫСШЕГО ОБРАЗОВАНИЯ РОССИЙСКОЙ ФЕДЕРАЦИИ Федеральное государственное бюджетное образовательное учреждение высшего образования «ТЮМЕНСКИЙ ИНДУСТРИАЛЬНЫЙ УНИВЕРСИТЕТ» ИНСТИТУТ ДОПОЛНИТЕЛЬНОГО И ДИСТАНЦИОННОГО ОБРАЗОВАНИЯ Практическая работа по дисциплине: ««ТЕХНОЛОГИЯ ПОДГОТОВКИ И ПЕРЕРАБОТКИ ПРИРОДНОГО ГАЗА» Преподаватель: Е. Н. Скворцова кандидат технических наук, доцент Слушатель направления «Химическая технология природных энергоносителей и углеродных материалов": Пуронен Н.А. Тюмень 2023 Вариант 1. Задача 1. Смесь газов состоит из 800 м3 H2 (водорода), 370 м3 N2 (азота), 50 м3 CH4 (метана). Определить: а) объемные доли компонентов в смеси; б) состав газовой смеси в массовых долях. Решение: определяю суммарный объем газов смеси: V = 800+370+50=1220 м3 Далее, нахожу объемные доли компонентов смеси: Х(Н2) = 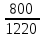 = 0,665 или 65,5 = 0,665 или 65,5 Х(N2) = 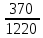 = 0,303 или 30,3 = 0,303 или 30,3 Х(CH4) = 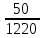 = 0,041 или 0,4 = 0,041 или 0,4 Теперь, определю массовые доли компонентов смеси 1 моль любого газа при нормальных условиях занимает объем = 22,4 л Определяю массу компонентов по формуле m= 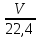 · M, · M, где М – молярная масса компонента; V – объем компонента М(Н2) = 2·1= 2 М(N2) = 2·14= 28 М(CH4) = 12+4·1=16 m(H2) = 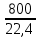 ·2=71 кг ·2=71 кгm(N2) = 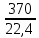 ·28=463 кг ·28=463 кгm(CH4) = 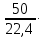 16=35 кг 16=35 кгm общая = 89+425+7 = 569 кг Массовые доли компонентов равны: х(Н2) = 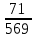 = 0,13 или 13% = 0,13 или 13% х(N2) = 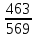 = 0,81 или 81% = 0,81 или 81%х(CH4) = 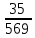 = 0,06 или 6% = 0,06 или 6%Задача 2. Газовая смесь получена из 64 м3этилена и 28 м3 пентана. Плотность этилена 1,2605 кг/м3, плотность пентана 3,4570 кг/м3. Выразить состав смеси в объемных и массовых процентах. Решение: определим суммарный объем газов смеси V = 64+28 = 92 м3 Далее нахожу объемные доли компонентов смеси Xv= 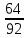 = 0,70 или 70% = 0,70 или 70%Xv= 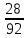 = 0,30 или 30% = 0,30 или 30%Пересчитаем объемные доли в массовые по формуле: Хi= 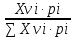 Х1= 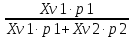 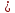 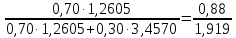 = 0,459 или 45,9 % = 0,459 или 45,9 %Х2= 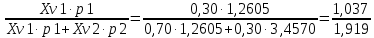 = 0,540 или 54 % = 0,540 или 54 % |
