лабораторная работа. Лабораторная работа Юрьевой. Практикум для студентов заочного обучения машиностроительных специальностей Красноярск 2002 удк 669. 01(07)
 Скачать 1.28 Mb. Скачать 1.28 Mb.
|
Рис. 2.5 Диаграмма состояния V рода с устойчивыми химическими соединениямиЛинии МЕ1СЕ2N – линия ликвидус, линия mnop – линия солидус. Точки М и N – температуры плавления компонентов А и В. Точка С – температура плавления химического соединения Аm Bn. Точки Е1 и Е2 – эвтектические точки. Состав эвтектики Е1 будет А+АmBn, эвтектики Е2 – B+AmBn. При кристаллизации эвтектических сплавов система будет нонвариантной в обоих случаях (С = 2 – 3 + 1 = 0). Диаграмма состояния с устойчивым химическим соединением может быть представлена и в других видах, где наряду с чистыми компонентами и одним химическим соединением могут быть и твердые растворы (ограниченные и неограниченные) и другие химические соединения. 2.4. Правило отрезков В любой точке диаграммы равновесия, когда в сплаве одновременно существуют две фазы, можно определить концентрацию и количество обеих фаз. Этому служит правило отрезков или правило рычага. Первое положение правило отрезков: чтобы определить концентрацию компонентов в фазах, через данную точку, характеризующую состояние сплава, проводят горизонтальную линию до пересечения с линиями, ограничивающими данную область; проекции точек пересечения на ось концентраций показывают состав фаз. Для примера рассмотрим сплав Х при температуре t1 на диаграмме 1 рода (рис. 2.6). 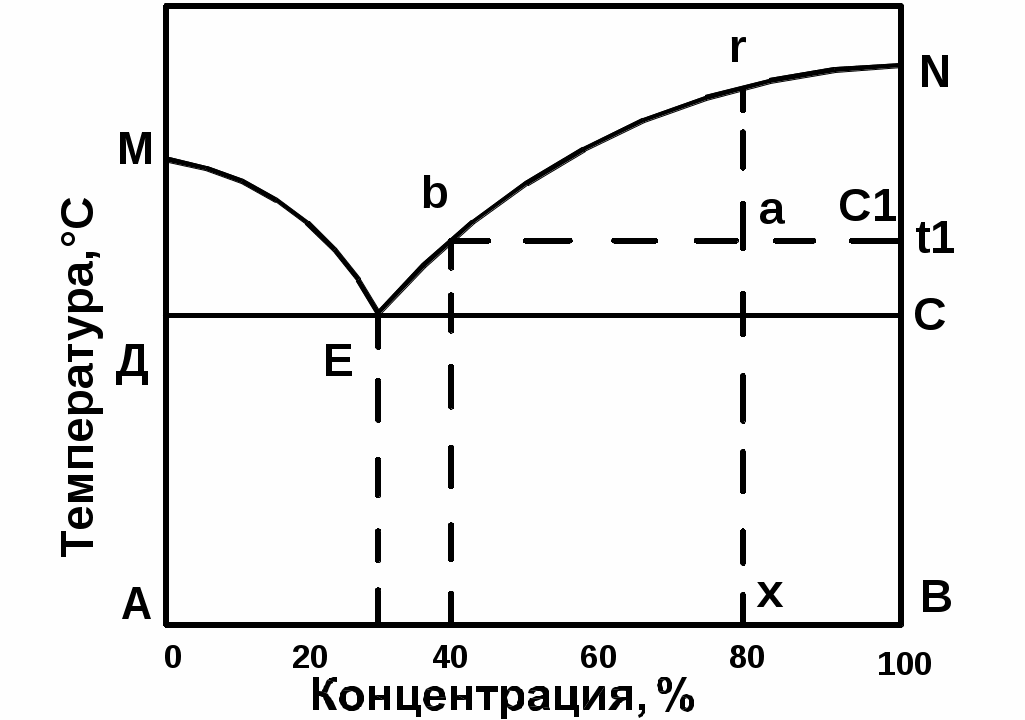 Рис 2.6 Диаграмма состояния I рода (с применением к ней правила отрезков) Следовательно, для сплава Х при температуре t1 составы фаз определяются проекциями соответствующих точек. Состав жидкой фазы будет соответствовать точке В, а твердой фазы – точке С1. Второе положение правила отрезков: для того чтобы определить количественное соотношение фаз при данной температуре, через заданную точку проводят горизонтальную линию. Отрезки этой линии между заданной точкой и точками, определяющими состав фаз, обратно пропорциональны количествам этих фаз. Для сплава Х при температуре t1 это соотношение будет где QЖ – количество жидкой фазы; QВ – количество кристаллов компонента В; Q – общее количество сплава. Отсюда количество жидкой фазы в процентах будет Тогда т.е. при температуре t1 сплав Х будет состоять из 66,7% кристаллов компонента В и 33,3% жидкого раствора компонентов А и В. По правилу отрезков подобным же образом можно определить объем эвтектики и объем кристаллов В после затвердевания. Для сплава Х Правило отрезков применимо для всех двухфазных областей любых диаграмм состояний. ИЗУЧЕНИЕ СЛОЖНЫХ ДИАГРАММ СОСТОЯНИЙ ДВОЙНЫХ СИСТЕМ Большая часть двойных сплавов имеет более сложные (комбинированные) диаграммы состояния. Зная основные типы диаграмм состояний, каждую сложную диаграмму можно мысленно разбить на составляющие части, соответствующие основным типам, и в зависимости от состава сплава, рассматривать соответствующую часть диаграммы. В качестве примера разберем диаграмму состояния сплавов «алюминий-кальций». На рис. Представлена фазовая диаграмма состояния и кривая охлаждения сплава с 25% кальция, на рис. – структурная диаграмма состояния сплавов «алюминий- кальций». 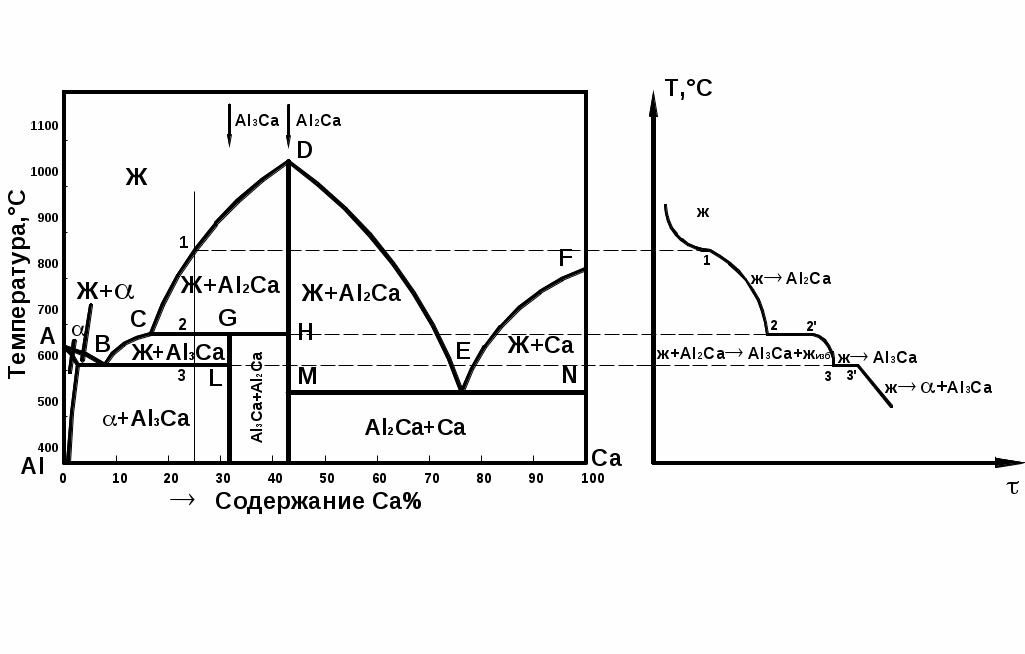 Рис 2.7 Фазовая диаграмма состояния системы Al-Ca и кривая охлаждения При общем рассмотрении диаграммы необходимо выделить ее части, соответствующие типовым диаграммам состояния; область существования жидкой фазы, твердой и жидкой фаз, области твердых растворов; найти эвтектические, эвтектоидные и перитектические точки и линии; линии ликвидус и солидус, выяснить, какие фазы существуют в данной системе. Фазами могут быть: твердые растворы, химические соединения, чистые компоненты и жидкость. Для нашего примера область жидкой фазы лежит выше линии ABCDEF, а область одновременного существования жидкой и твердой фаз – между линиями ликвидус ABCDEF и солидус AKBLGHMEN. 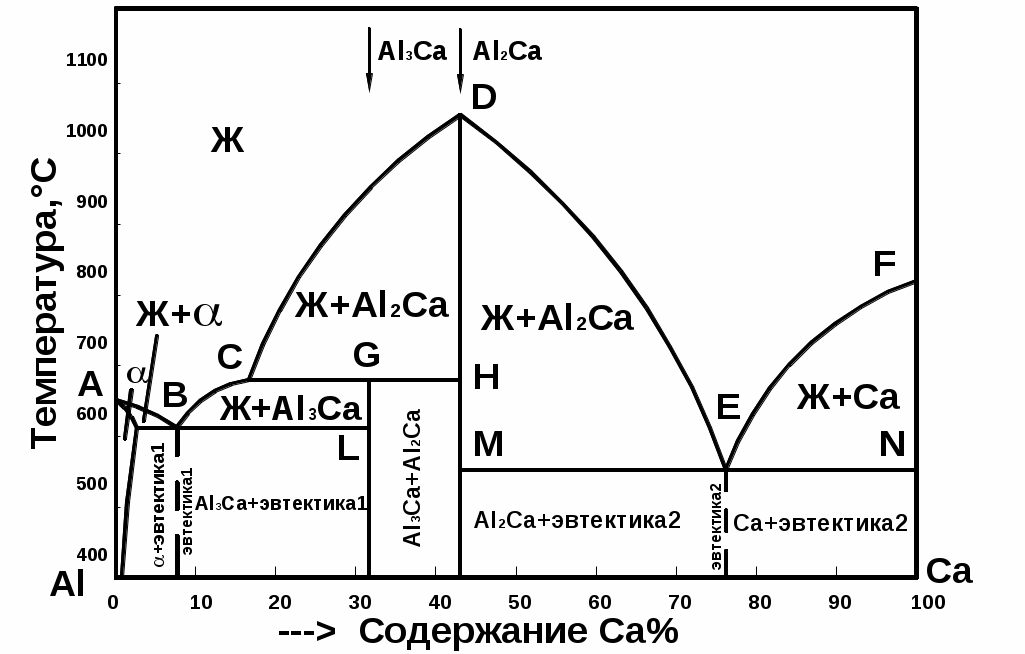 Рис 2.8 Структурная диаграмма состояния системы Al-Ca В рассматриваемой системе существует один твердый раствор α, соответствующий области AKS. Это твердый раствор кальция в алюминии. Точка К – точка максимальной растворимости, KS – линия предельной растворимости кальция в алюминии. Алюминий в кальции не растворяется. Таким образом, фазами в данной системе являются: жидкость, Для диаграммы алюминий-кальций характерно следующее: 1. Линия KBL – линия эвтектического превращения, тогда В - эвтектическая точка. Эвтектика представляет собой механическую смесь кристаллов α-твердого раствора и химического соединения Al3Ca. Эвтектическое превращение протекает по уравнению Жв αк + Al3Ca В соответствии с правилом фаз эвтектическое превращение протекает при постоянной температуре, т.к. сплав находится в трехфазном равновесном состоянии. В этих условиях число степеней свободы будет равно нулю: С = К - Сплавы, в структуре которых есть эвтектика, делятся на доэвтектические, эвтектические и заэвтектические. У сплавов, расположенных ниже линии КВ структура будет состоять из α-твердого раствора и эвтектики, у сплавов ниже линии BL – из хим.соединения Al3Ca и эвтектики; эвтектический сплав в т. В состоит из одной эвтектики. 2. Линия CGH – линия образования неустойчивого химического соединения Al3Ca. Точка G – перитектическая точка. Реакция перитектического превращения: Жс + Al2Ca Al3Ca. Перитектическое превращение заключается в образовании кристаллов Al3Ca при взаимодействии жидкой и твердой фазы определенных химических составов. Для сплава в точке G в результате завершения перитектического превращения весь сплав будет состоять из химического соединения Al3Ca. Для сплавов, расположенных левее т. G (т. G до т. С) в избытке будет оставаться жидкая фаза; для сплавов, расположенных правее т. G (от т. G до т. Н) в избытке будет оставаться соединение Al2Ca. В соответствии с правилом фаз перитектическое превращение так же протекает при постоянной температуре. 3. Линия MEN – линия второго эвтектического превращения: ЖЕ Al2Ca + Ca Эвтектика будет состоять из мелкодисперсных кристаллов Ca и хим. соединения Al2Ca. Сплавы, расположенные ниже линии МЕ являются доэвтектическими, структура их состоит из эвтектики и Al2Ca; сплавы, расположенные ниже линии EN являются заэвтектическими, структура состоит из Ca и эвтектики. 1. ПОСТРОЕНИЕ КРИВОЙ ОХЛАЖДЕНИЯ Кривая охлаждения строится в координатах «температура – время». Процесс рассматривается при охлаждении сплава из жидкого состояния до комнатной температуры. Рассмотрим кристаллизацию сплава с 25% кальция. Для этого необходимо провести вертикальную линию сплава и обозначить критические точки индексами 1, 2, 3. До т. 1 жидкость охлаждается без фазовых превращений, кривая имеет вогнутый вид. От т. 1 до т. 2 из жидкости выделяются кристаллы Al2Ca, на кривой охлаждения образуется перегиб. В т. 2 происходит перитектическое превращение: Же + Al2Ca Al3Ca + Жизб На кривой охлаждения образуется площадка. От т.2 до т. 3 кристаллизация продолжается, т.е. из жидкости выделяются кристаллы Al3Ca, при этом химический состав жидкости изменяется от т. С до т. В. В т. 3 кристаллизация заканчивается образованием эвтектики: Жв αк + Al3Ca. На кривой охлаждения образуется горизонтальная площадка. Таким образом, ниже т. 3 структура сплава состоит из химического соединения Al3Ca и эвтектики. Вопросы для проверки 1.Что такое диаграмма состояния сплава? Для чего она используется? 2. В каких координатах строится диаграмма состояния? 3. Что позволяет определить диаграмма состояния? 4. Что такое линия ликвидус и линия солидус? 5. Начертите и проанализируйте диаграмму состояния для случая полной нерастворимости компонентов в твердом состоянии. 6. Начертите и проанализируйте диаграмму состояния для случая образования непрерывного ряда твердых растворов. 7. Начертите и проанализируйте диаграмму состояния для случая образования эвтектики, состоящей из ограниченных твердых растворов. 8. В чем различие между эвтектической и перитектической кристаллизациями? |
