подготовка к экз фх. Экзамен ФХ (автовосстановление). Простая реакция
 Скачать 1.2 Mb. Скачать 1.2 Mb.
|
|
Билет 10 Понятие простой и сложной реакции. Основные принципы к описанию кинетики сложных реакций. Принцип независимости отдельных стадий. Для некоторой реакции А + В C получено следующее выражение для скорости r = kCA1/2CB3/2 . Определите общий порядок реакции и сделайте вывод о типе реакции (простая или сложная). элементарная (простая) реакция ― химическая реакция, происходящая в одну стадию. Сложная реакция ― включает несколько различных стадии, приводящих к конечным продуктам.  2. Кинетика сложных реакций. Обратимые реакции. Превращение роданида аммония (NH4SCN) в тиомочевину (NH4)2C=S обратимая реакция первого порядка. Рассчитайте константы скорости прямой и обратной реакции и константу равновесия на основании следующих данных по степени превращения NH4SCN
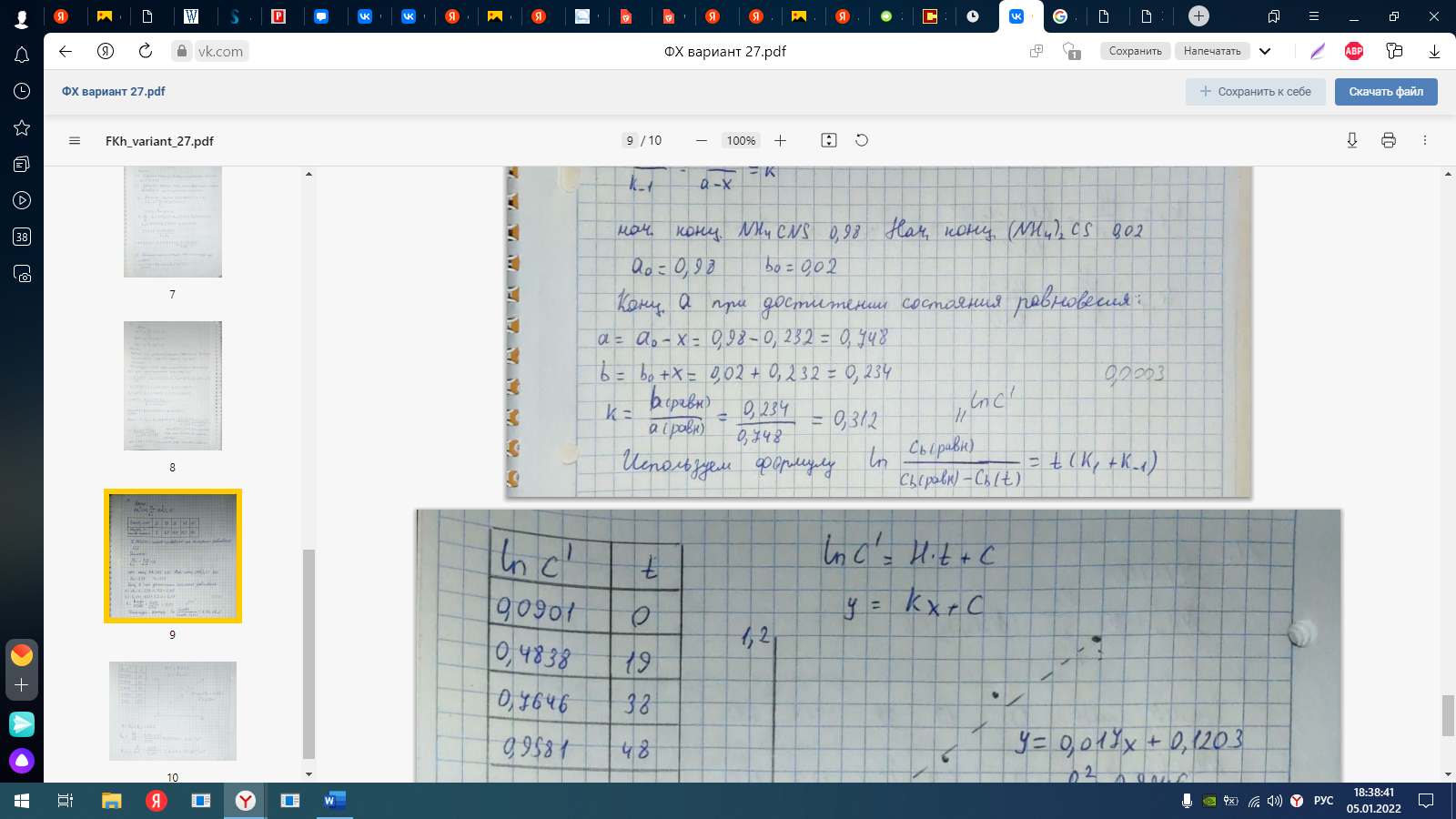    Основные положения теории активного комплекса (ТАК). Запишите выражение для скорости бимолекулярной реакции в ТАК. Задача. Определите энергию активации реакции и предэкспоненциальный множитель A, энтальпию и энтропию активации реакции омыления этилацетата щелочью, если константа скорости изменяется с ростом температуры следующим образом:
|
