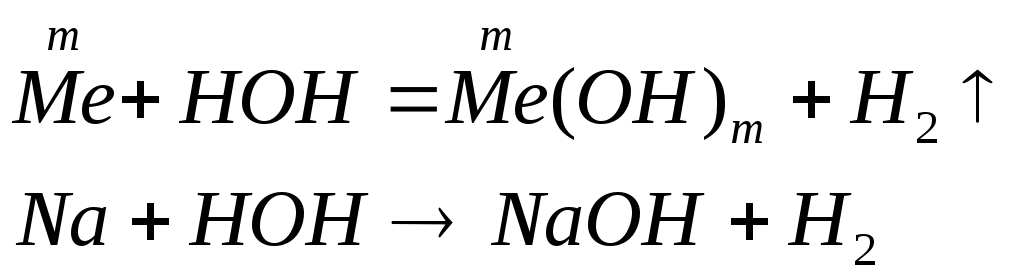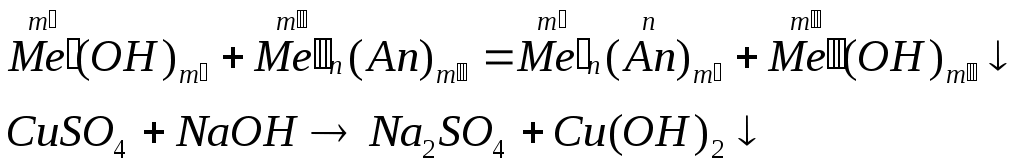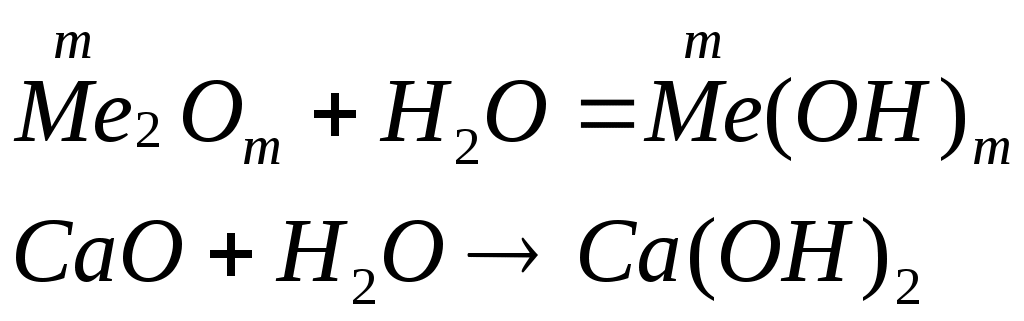Растворимые или щелочи нерастворимые
 Скачать 69 Kb. Скачать 69 Kb.
|
|
Гидроксиды металлов

Классификация оснований по кислотности – однокислотные (содержат одну гидроксильную группу), многокислотные (содержат несколько гидроксильных групп) по растворимости в воде – растворимые или щелочи и нерастворимые. Номенклатура оснований и амфотерных гидроксидов: гидроксид + русское название металла + (валентность металла) Физические свойства: все неорганические основания – твердые вещества, большинство оснований белого цвета, однако, есть окрашенные, например Cu(OH)2 – голубого, CuOH – желтого, Fe(OH)3 – красно-бурого цвета. По отношению к воде растворимые и нерастворимые (выпишите растворимые и нерастворимые основания по таблице). Химические свойства Химические свойства щелочей. растворяются в воде действуют на индикаторы взаимодействуют с кислотными оксидами: 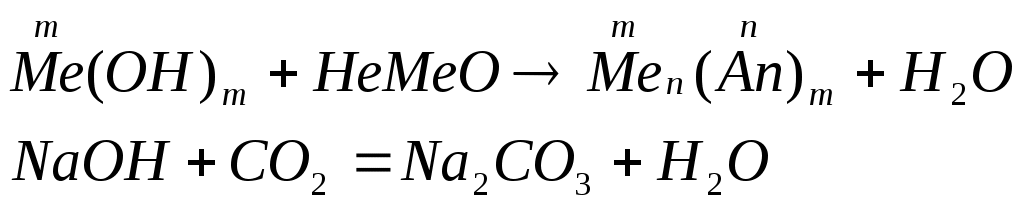 взаимодействуют с кислотами (реакция нейтрализации) 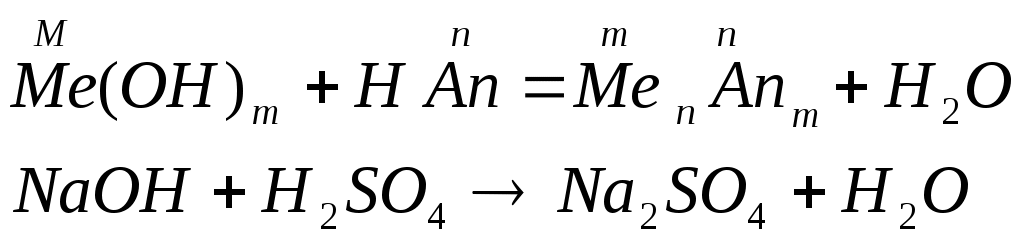 взаимодействуют с солями, если выпадает осадок 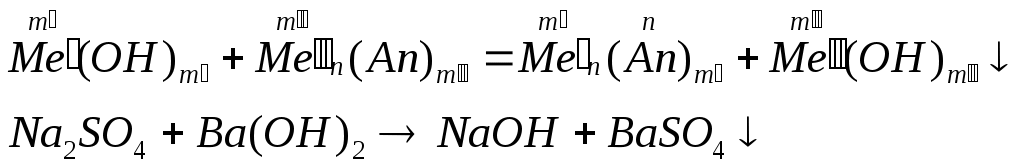 взаимодействуют с амфотерными оксидами 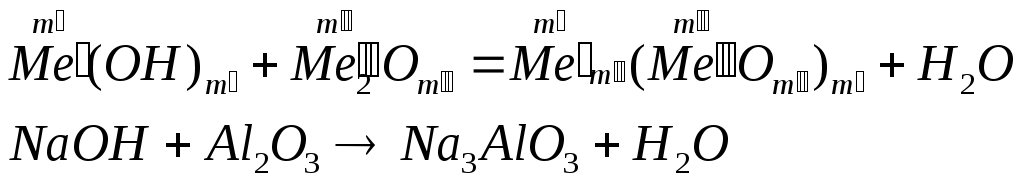 взаимодействуют с амфотерными гидроксидами. 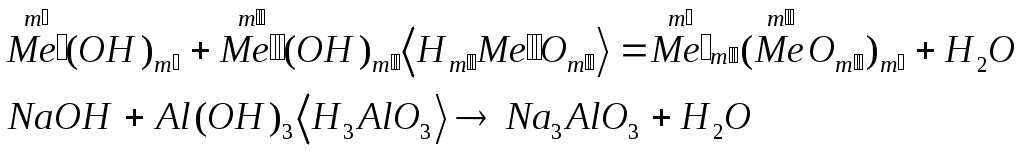 Химические свойства нерастворимых оснований взаимодействуют с кислотами 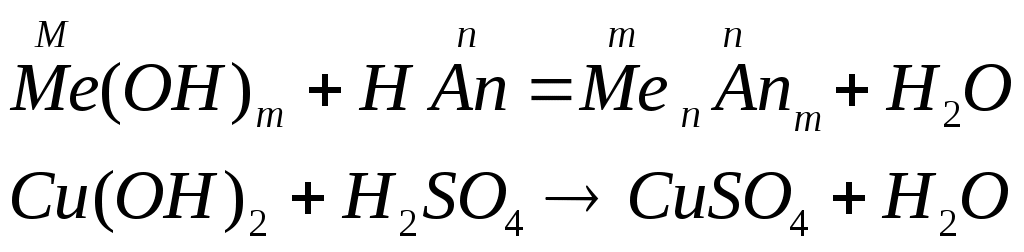 разлагаются при нагревании 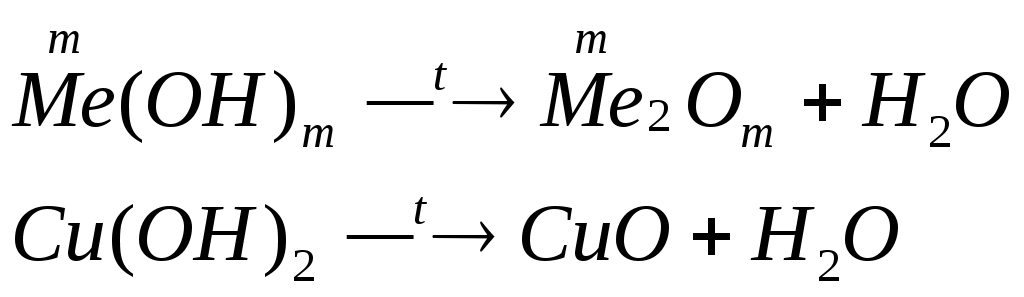 Химические свойства амфотерных гидроксидов. взаимодействуют с кислотами 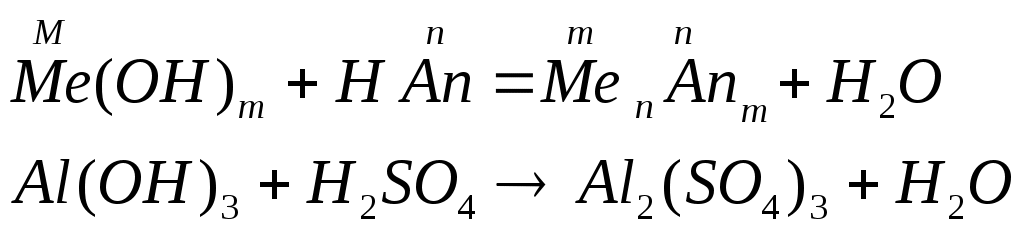 разлагаются при нагревании  взаимодействуют с основаниями 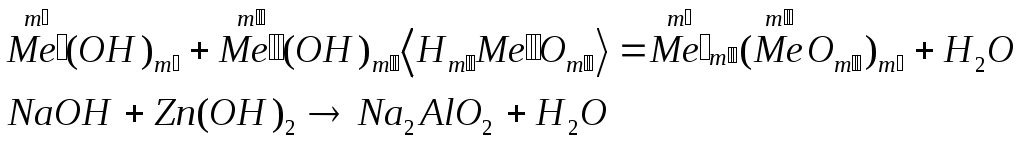 ПОЛУЧЕНИЕ ОСНОВАНИЙ
|


 ИДРОКСИДЫ Ме
ИДРОКСИДЫ Ме
 СНОВАНИЯ
СНОВАНИЯ