Реферат На тему адсорбция Студент Преподаватель Екатеринбург 2006г
 Скачать 1.06 Mb. Скачать 1.06 Mb.
|
1 2 * Предельно высокодисперсные системы (золи) иногда трудно классифицировать по агрегатному состоянию дисперсной фазы. Мицелла (новолат. micella, уменьшительное от лат. mica — крошка, крупинка), отдельная частица дисперсной фазы золя, т. е. высокодисперсной коллоидной системы с жидкой дисперсионной средой. М. состоит из ядра кристаллической или аморфной структуры и поверхностного слоя, включающего сольватно связанные (см. Сольватация) молекулы окружающей жидкости. Поверхностный слой М. лиофобного золя (см. Лиофильные и лиофобные коллоиды) образован адсорбированными молекулами или ионами стабилизирующего вещества. В случае лиофобных гидрозолей, стабилизованных электролитами, ядро М. окружено двумя слоями противоположно заряженных ионов, т. н. двойным электрическим слоем. Число положительных и отрицательных зарядов в нём одинаково, и поэтому М. в целом электронейтральна. Непосредственно у поверхности ядра расположены ионы адсорбционного слоя. В него входят все ионы одного знака и часть ионов другого знака (противоионы). Остальные противоионы образуют диффузный слой; он окружает М. в виде ионного «облака», плотность которого падает по мере удаления от ядра. Диффузный слой препятствует сближению и агрегированию (сцеплению) частиц в процессе броуновского движения. В лиофильных золях, коллоидных дисперсиях типа гидрозолей мыл, например олеата натрия или лаурилсульфата калия, М. представляет собой ассоциат (объединение) молекул. В каждой такой молекуле длинный углеводородный (гидрофобный) радикал связан с полярной (гидрофильной) группой. При образовании М. несколько десятков или сотен молекул объединяются так, что гидрофобные радикалы образуют ядро (внутреннюю область), а гидрофильные группы — поверхностный слой М. Если дисперсионной средой является органическая жидкость, ориентация молекул в М. может быть обратной: в ядре сосредоточатся полярные группы, тогда как гидрофобные радикалы будут обращены во внешнюю фазу. Изобразив молекулу мицеллообразующего вещества в виде волнистой линии (гидрофобный радикал) с кружочком на конце (гидрофильная группа), можно представить простейшие структурные типы М. схемами: Мицеллярные структуры 1 и 2 относятся к гидрофильным золям, а 3 и 4 — к органофильным. Сферические М. (1 и 3) при разбавлении системы ниже критической концентрации мицеллообразования обратимо распадаются на отдельные молекулы или димеры (подробнее см. Полуколлоидные системы). При более высоких концентрациях сферические М. превращаются в пластинчатые (2 и 4). Последние, взаимодействуя между собой, способны создавать в объёме системы структурную сетку геля (см. Гели, Дисперсная структура). Наличием М. объясняется моющее действие водных растворов (точнее, коллоидных дисперсий) мыл, а также некоторые явления в биологических системах и при технологических процессах (см. также Солюбилизация). Коагуляция (от лат. Coagulatio — свёртывание, сгущение), слипание частиц коллоидной системы при их столкновениях в процессе теплового (броуновского) движения, перемешивания или направленного перемещения во внешнем силовом поле. В результате К. образуются агрегаты — более крупные (вторичные) частицы, состоящие из скопления более мелких (первичных). Первичные частицы в таких скоплениях соединены силами межмолекулярного взаимодействия непосредственно или через прослойку окружающей (дисперсионной) среды. К. сопровождается прогрессирующим укрупнением частиц (увеличением размера и массы агрегатов) и уменьшением их числа в объёме дисперсионной среды — жидкости или газа. Различают быструю и медленную К. При быстрой К. почти каждое соударение частиц эффективно, т. е. приводит к их соединению; при медленной К. соединяется часть сталкивающихся частиц. В жидкой среде, например при К. золей, укрупнение частиц до известного предела (приблизительно до размера 10-4 см) не сопровождается их оседанием или всплыванием. Это скрытая К., при которой система сохраняет седиментационную устойчивость. Дальнейший рост частиц приводит к образованию сгустков или хлопьев (флокул), выпадающих в осадок (коагулят, коагель) или скапливающихся в виде сливок у поверхности; это явная К. В некоторых случаях при К. во всём объёме дисперсионной среды возникает рыхлая пространственная сетка (коагуляционная структура) и расслоения системы не происходит (см. Гели). Если коллоидные частицы — капельки жидкости или пузырьки газа, то К. может завершиться их слиянием, коалесценцией. К. — самопроизвольный процесс, который, в соответствии с законами термодинамики, является следствием стремления системы перейти в состояние с более низкой свободной энергией. Однако такой переход затруднен, а иногда практически невозможен, если система агрегативно устойчива, т. е. способна противостоять укрупнению (агрегированию) частиц. Защитой от К. при этом может быть электрический заряд и (или) адсорбционно-сольватный слой на поверхности частиц, препятствующий их сближению (подробнее см. Коллоидные системы). Нарушить агрегативную устойчивость можно, например, повышением температуры (термокоагуляция), перемешиванием или встряхиванием, введением коагулирующих веществ (коагулянтов) и др. видами внешнего воздействия на систему. Минимальная концентрация введенного вещества, электролита или неэлектролита, вызывающая К. в системе с жидкой дисперсионной средой, называется порогом коагуляции. В полидисперсных системах, где частицы имеют разную величину, можно наблюдать ортокинетическую К. — налипание мелких частиц на более крупные при их оседании или всплывании. Слипание однородных частиц называется гомокоагуляцией, а разнородных — гетерокоагуляцией или адагуляцией. Гетерокоагуляция часто происходит при смешении дисперсных систем различного состава. К. может наступить без какого-либо внешнего воздействия на коллоидную систему (автокоагуляция) как результат физических или химических изменений, происходящих при её старении. Иногда К. обратима; в благоприятных условиях, особенно при введении поверхностно-активных веществ, понижающих поверхностную межфазную энергию и облегчающих диспергирование, возможен распад агрегатов на первичные частицы (пептизация) и переход коагеля в золь. К. играет важную роль во многих технологических, биологических, атмосферных и геологических процессах. Так, при нагревании биополимеров (белков, нуклеиновых кислот) и при некоторых др. воздействиях на них, например изменении pH, наблюдается их К. Явления К. во многих биологических дисперсных системах (например, крови, лимфе) важны в связи с вопросами их агрегативной устойчивости. Очистка природных и сточных вод от высокодисперсных механических примесей, борьба с загрязнением воздушного пространства аэрозолями,выделение каучука из латекса, получение сливочного масла и др. пищевых продуктов — характерные примеры использования К. в практических целях. Нежелательна К. при получении и хранении суспензий,эмульсий, порошков и др. дисперсных систем промышленного или бытового назначения. Топохимические реакции, реакции химические, происходящие на границе раздела твёрдых фаз. Примеры Т. р.: дегидратация кристаллогидратов, восстановление окислов, термический распад азидов тяжёлых металлов и т.д. Особенности Т. р.: 1) они начинаются не во всём объёме, а с отдельных, наиболее реакционноспособных мест твёрдого тела (локализация процесса); 2) возникнув в каком-то месте, реакция продолжается в соседних областях кристалла (автолокализация процесса). Причины локализации процесса при Т. р. обычно связаны с наличием дефектов в кристаллах и малой подвижностью ионов, атомов или молекул, образующих кристаллическую решётку. Автолокализация процесса обусловлена каталитическим влиянием твёрдого или газообразного продукта реакции, а также кристаллохимическими особенностями развития реакции в кристалле. Межфазовая поверхность, в пределах которой локализованы Т. р., возникает вследствие образования и роста реакционных ядер; скорость процесса обычно пропорциональна величине этой поверхности в каждый данный момент времени. Поэтому кинетический анализ Т. р. включает не только учёт развития процесса во времени, но и в пространстве. Значит, влияние на скорость Т. р. оказывают дефекты в кристаллах. Оно проявляется в изменении как числа потенциальных центров реакции на поверхности, так и условий для явлений переноса в твёрдом теле. С существенной ролью дефектов в развитии Т. р. связаны также широко известный эффект влияния «предыстории» препарата (реагента) на его реакционную способность, многообразие факторов, воздействующих на их скорость, и т.д. Характер влияния дефектов в кристаллах на скорости Т. р. в каждом конкретном случае зависит как от вида и концентрации дефектов, так и от механизма элементарных стадий. Т. р. широко используются на практике. К числу наиболее важных Т. р. относятся процессы обжига, восстановления, хлорирования руд многих металлов, цементация стали, производство керамики и огнеупоров, приготовление катализаторов, получение ферритов, некоторые стадии фотографического процесса, газовая коррозия металлов и сплавов. Во многих случаях разложение взрывчатых веществ при нагревании, процессы синтеза и очистки полупроводниковых материалов также относятся к Т. р. Катализ (от греч. katálysis — разрушение), изменение скорости химических реакций в присутствии веществ (катализаторов),вступающих в промежуточное химическое взаимодействие с реагирующими веществами, но восстанавливающих после каждого цикла промежуточных взаимодействий свой химический состав. Реакции с участием катализаторов называются каталитическими. Количество реагирующего вещества, которое может испытать превращение в присутствии определённого количества катализатора, не ограничивается какими-либо стехиометрическими соотношениями и может быть очень большим. Этим каталитические реакции отличаются от индуцируемых, или сопряжённых реакций, когда одна реакция вызывается или ускоряется (индуцируется) другой и происходит необратимое превращение вещества-индуктора. Возможные изменения катализатора при каталитических реакциях являются результатом побочных процессов, ни в коей мере не обусловливающих каталитическое действие. Воздействие катализатора открывает новый реакционный путь, обычно с большим числом стадий, на котором катализатор входит в состав активного комплекса (активированного комплекса) по крайней мере одной из стадий. Если при этом скорость реакции становится больше, чем в отсутствие катализатора, то К. называется положительным (его нередко отождествляют с общим понятием К.). Возможен и обратный случай, когда происходит отрицательный К.: в присутствии катализатора исключается один из возможных путей реакции и остаются лишь более медленные, в результате чего реакция замедляется или даже практически полностью подавляется (см. Антиокислители, Ингибиторы химические). Особый случай К. — ускорение реакции при воздействии продукта реакции или одного из промежуточных веществ, образующихся при реакции (см. Автокатализ). К. не связан с изменением свободной энергии катализатора, и воздействие катализатора не может поэтому смещать положение равновесия химической реакции. Вблизи состояния равновесия катализаторы в равной степени ускоряют как прямую, так и обратную реакцию. Основным фактором, определяющим скорость химического превращения, является энергия активации (Е) — разность энергий активного комплекса и исходных реагирующих молекул. Если предположить, что реакция не нарушает равновесного распределения энергии между молекулами, то вероятность образования активного комплекса, а следовательно, и скорость реакции в первом приближении пропорциональна exp (—E/RT), где R — газовая постоянная, Т — абсолютная температура. Отсюда следует, что скорость реакции тем больше, чем меньше Е, и вследствие экспоненциальной зависимости возрастает значительно даже при небольшом снижении Е. 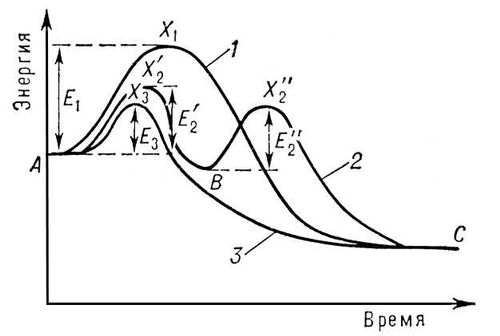 На рис. представлено изменение энергии при реакции без катализатора (кривая 1) и при участии катализатора (кривые 2 и 3). Кривая 2 с двумя максимумами соответствует образованию одного промежуточного продукта. Число стадий и промежуточных продуктов часто бывает значительно большим. Взаимодействие реагирующих веществ с катализатором может и не приводить к образованию стабильной формы промежуточного соединения (кривая 3). Но и в этом случае катализатор входит в состав активного комплекса и взаимодействие реагирующих веществ с катализатором определяет реакционный путь. Если энергии активных комплексов всех стадий реакционного пути с участием катализатора ниже энергии активного комплекса реакции без катализатора (т. е. Характер промежуточного химического взаимодействия при К. весьма разнообразен. Обычно различают две группы каталитических процессов: кислотно-основной (гетеролитический) и окислительно-восстановительный (гомолитический). В процессах первой группы происходит промежуточное кислотно-основное взаимодействие реагирующих веществ с катализатором, например переход протона от катализатора к реагирующим веществам или наоборот. На последующих стадиях протон перемещается в обратном направлении, и катализатор восстанавливает свой состав. При К. апротонными кислотами взаимодействие осуществляется через свободную пару электронов реагирующего вещества. Примерами кислотно-основного К. могут служить гидролиз сложных эфиров, ускоряемый кислотами; гидратация олефинов в присутствии фосфорно-кислотных катализаторов; изомеризация и крекинг углеводородов на алюмосиликатных катализаторах; алкилирование; полимеризация и многие другие реакции. При реакциях окислительно-восстановительного К. промежуточное взаимодействие связано с электронными переходами между катализатором и реагирующими веществами. К этой группе относятся окисление двуокиси серы в трёхокись в производстве серной кислоты; окисление аммиака до окиси азота при получении азотной кислоты; многочисленные процессы парциального окисления органических соединений, например этилена в окись этилена, нафталина во фталевый ангидрид; гидрогенизация; дегидрогенизация; циклизация и ароматизация углеводородов; разложение перекиси водорода и многие др. Каталитической активностью в отношении окислительно-восстановительных реакций обладают преимущественно металлы 4-, 5- и 6-го периодов системы Д. И. Менделеева, имеющие недостроенную d-оболочку электронов, их соединения и в меньшей мере соединения элементов с достраивающейся f-оболочкой (лантаноиды и актиноиды). Рассмотренные группы далеко не охватывают всё разнообразие каталитических реакций. Характер промежуточного взаимодействия при К. гораздо более сложен и зависит от всех деталей электронной структуры как реагирующих веществ, так и катализатора. Конкретные механизмы каталитических реакций многообразны и пока лишь в немногих случаях твёрдо установлены. В зависимости от фазового состояния реагирующих веществ и катализатора различают гомогенный и гетерогенный К. Промежуточное положение занимает микрогетерогенный К. в коллоидных системах (например, К. ферментами). При гомогенном К. катализатор и реагирующие вещества образуют одну однородную систему, границы раздела между катализатором и реагирующими веществами отсутствуют. При гетерогенном К. катализатор и реагирующие вещества находятся в разных фазах и отделены друг от друга границей раздела. Наиболее важны случаи, когда катализатор является твёрдым телом, а реакционная система образует жидкую или газообразную фазу. Промежуточное взаимодействие происходит при этом преимущественно на поверхности твёрдого катализатора. Выбор состава катализатора для определённой реакции является очень сложной проблемой, решаемой пока главным образом эмпирическим путём. В СССР предложен и развит ряд теоретических подходов, основанных на корреляции отдельных частных свойств катализаторов с их активностью. Так, мультиплетная теория К. (первые публикации 1929) предполагает промежуточное взаимодействие реагирующих веществ с несколькими атомами на поверхности твёрдых катализаторов и придаёт решающее значение соответствию расстояний между атомами в молекулах реактантов и параметров кристаллической структуры катализатора. В дальнейшем теория была дополнена представлением о необходимости определённого соответствия энергий связей, разрывающихся и образующихся в результате реакции, и энергий связей реактантов с катализатором при промежуточном взаимодействии. Значительное распространение в 50-х гг. получило представление о зависимости каталитической активности твёрдых катализаторов, обладающих полупроводниковыми свойствами, от их электрических характеристик, — так называемая электронная теория К. По этой теории предполагается, что промежуточное взаимодействие реактантов с катализатором осуществляется при участии электронов проводимости твёрдого катализатора и поэтому зависит от его коллективных электронных свойств — расположения энергетических зон и локальных уровней электронов, работы выхода электрона, концентрации носителей тока и др. В гетерогенном К. широко использовалось предположение (выдвинутое в 1939) о существовании на поверхности твёрдых катализаторов особых активных центров, представляющих собой ребра, углы или различные структурные нарушения (дислокации) нормальной кристаллической структуры. Предполагалось также, что при нанесении каталитически активного вещества на инертный носитель особые каталитические свойства проявляют отдельно расположенные атомы или совокупности небольшого числа атомов — ансамбли. Появление точных методов определения поверхности катализаторов позволило установить, что активность, отнесённая к единице поверхности (удельная каталитическая активность), определяется химическим составом и очень мало зависит от структурных дислокаций. Удельная каталитическая активность различных граней кристаллов иногда различается в несколько раз. Большое влияние на активность оказывают нарушения химического состава (отклонение от стехиометрии, внедрение примесей, локальные химические образования и т.п.). В 60-е годы промежуточное химическое взаимодействие в гетерогенном К. рассматривается преимущественно как локальное, определяемое электронной структурой отдельных атомов или ионов каталитически активного компонента на поверхности катализатора с учётом влияния ближайшего окружения. Значительную помощь в развитии этого подхода оказала обнаруженная экспериментально аналогия в действии твёрдых катализаторов, содержащих определённый металл, при гетерогенном К. и растворимых комплексов, компонентом которых является тот же металл, при гомогенном К. в растворах. При этом используются теории кристаллического поля и поля лигандов, ещё ранее успешно применявшиеся в химии комплексных соединений. Для ряда классов катализаторов и каталитических реакций установлены корреляции между каталитической активностью и энергиями связей реактантов с катализатором при промежуточном взаимодействии, облегчающие в отдельных случаях подбор катализаторов. Первые научные сведения о К. относятся к началу 19 в. В 1806 французские химики Н. Клеман и Ш. Дезорм открыли каталитическое действие окислов азота на окисление сернистого газа в камерном процессе получения серной кислоты, В 1811 русский химик К. С. Кирхгоф открыл, что разбавленные кислоты способны вызывать превращение крахмала в сахар (глюкозу); в 1814 им же было установлено, что эту реакцию может катализировать диастаза из ячменного солода, — так было положено начало изучению биологических катализаторов — ферментов. В 1818 французский химик Л. Тенар установил, что большое число твёрдых тел оказывает ускоряющее действие на разложение растворов перекиси водорода, а английский химик Г. Дэви открыл способность паров спирта и эфира окисляться кислородом на платине. В 1822 нем. химик И. Дёберейнер установил, что водород и кислород соединяются на платине при обычной температуре. За этим последовало открытие и ряда др. примеров резкого положительного действия веществ на скорость или возникновение химических реакций. Это привело к выделению особой группы явлений, названных нем. химиком Э. Мичерлихом контактными (1833) и швед. химиком И. Берцелиусом каталитическими (1835). В дальнейшем было открыто большое число каталитических реакций, и за последние 50 лет К. стал ведущим методом осуществления химических реакций в промышленности. Применение катализаторов позволяет проводить химические превращения с высокими скоростями при небольших температурах — большинство промышленных каталитических процессов без катализаторов вообще не могло бы быть реализовано. Подбирая катализаторы, можно направлять химические превращение в сторону образования определённого продукта из ряда возможных. Применение стереоспецифичных катализаторов позволяет регулировать и строение конечных продуктов, например полимеров. С помощью К. в начале 20 в. была решена проблема фиксации азота воздуха. Промотированные железные и другие катализаторы позволили преодолеть химическую инертность элементарного азота и осуществить синтез аммиака. Одновременно был разработан каталитический метод получения азотной кислоты путём окисления аммиака на платиновых сетках. На каталитических реакциях основываются современные методы получения водорода из природного газа. Каталитические методы занимают господствующее положение и в технологии нефтепереработки. Сотни миллионов тонн высококачественного моторного топлива производятся с помощью каталитических реакций крекинга, гидрокрекинга, риформинга, циклизации и изомеризации углеводородов нефти. Особенно большую роль играют каталитические методы в осуществлении процессов органического синтеза. В нашей стране впервые в мире было разработано и реализовано производство синтетического каучука, основанное на превращении этилового спирта в дивинил с помощью многокомпонентного окисного катализатора Лебедева. Каталитические методы используются для получения подавляющего большинства продуктов нефтехимического синтеза: растворителей, ароматических углеводородов, мономеров для производства синтетических каучуков, синтетических волокон и др. полимерных материалов. Катализаторы широко используются и для полимеризации. К. играет ведущую роль в химических превращениях в живой природе. Вся сложная система управления жизненными процессами в организмах основана на каталитических реакциях. Биологические катализаторы, называемые ферментами или энзимами, представляют собой вещества белковой природы с химически активными группами, часто включающими в свой состав атомы переходных элементов. По некоторым свойствам ферменты превосходят промышленные катализаторы. В СССР и за рубежом широко ведутся исследования новых типов сложных синтетических катализаторов — комплексных соединений, органических полупроводников, полимеров, характеризующихся более простым составом по сравнению с ферментами, но моделирующих в известной степени их действие. Науке о К. принадлежит существенная роль как в прогрессе химической промышленности, так и в раскрытии важнейших биологических закономерностей. Список литературы Лит.: Курс физической химии, т. 1, М., 1964; Бур Я.Х., Динамический характер адсорбции, пер. с англ., М., 1962; Трепнел Б., Хемосорбция, пер. с англ., М., 1958; Бладергрен В., Физ. химия в медицине и биологии, пер. с нем., М., 1951. 1 2 |
